1. 领域背景与文献
文献英文标题:Dissecting the contribution of transposable elements to interphase chromosome structure;发表期刊:Genome Biology;影响因子:17.906;研究领域:基因组三维结构调控、转座因子功能研究。
领域共识:真核生物基因组以高度有序的三维形式折叠在细胞核内,2009年高通量染色体构象捕获技术(Hi-C)问世后,研究逐步明确三维基因组具有A/B区室、拓扑关联结构域(TAD)、染色质环的层级调控结构,这些结构的紊乱与发育异常、肿瘤发生等多种病理过程密切相关。转座因子(TE)占人类基因组序列的近50%,早期被认为是无功能的“垃圾DNA”,后续研究证实其携带转录因子结合位点,参与基因表达调控、胚胎发育、细胞命运决定等多种生物学过程。
当前领域发展关键节点包括:2012年首次发现转座子可通过携带CCCTC结合因子(CTCF)结合位点重塑物种特异性基因组结构;2019年证实转录激活的内源性逆转录病毒HERV-H可作为人类多能干细胞(hPSC)的TAD边界;2023年机器学习研究发现重复序列是三维基因组折叠的关键序列决定因素。现有研究热点聚焦于三维基因组的调控机制解析、转座子的功能挖掘、表观遗传调控网络与基因组结构的交叉研究,但仍存在核心未解决问题:传统Hi-C分析流程普遍丢弃比对到重复序列的多映射读段,导致转座子对三维基因组结构的整体贡献程度长期被低估;除CTCF外,尚未系统明确参与转座子介导染色质互作的调控因子网络,转座子调控三维结构的分子机制尚未完全阐明。
本研究针对上述研究空白,开发专门整合转座子读段的Hi-C分析流程,系统定量转座子对间期三维基因组结构的贡献,挖掘介导转座子互作的全新调控因子,为三维基因组调控机制研究提供新工具和新靶点,具有重要的方法学创新和理论价值。
2. 文献综述解析
作者对现有研究的评述逻辑按照研究方向分为三类:三维基因组层级结构解析、转座子生物学功能研究、转座子与三维基因组的互作研究,三类研究逐层递进支撑本研究的科学假设。
现有研究的关键结论包括:三维基因组的层级结构由CTCF、黏连蛋白(Cohesin)等复合物介导,在物种间保守且参与基因表达精准调控;转座子携带大量转录因子结合位点,可作为顺式调控元件参与细胞命运调控,其异常激活与多种人类疾病相关;特定转座子家族如啮齿类特异性SINE B2、人类HERV-H可通过携带CTCF结合位点或作为绝缘子调控TAD边界,重塑局部基因组结构。现有技术方法的优势在于,Hi-C技术可在全基因组水平实现染色质互作的无偏检测,染色质免疫共沉淀测序(ChIP-seq)可精准定位转录因子/表观调控因子的全基因组结合位点,为解析调控机制提供了成熟的技术支撑。现有研究的局限性包括:传统Hi-C分析丢弃多映射读段的处理方式导致转座子相关互作被严重低估;现有研究仅关注个别转座子家族或个别调控因子,尚未系统评估转座子对三维基因组的全局贡献,也未建立完整的转座子互作调控因子网络。
本研究的创新价值体现在三个方面:首先是方法学创新,开发的te_hic分析流程首次实现转座子相关Hi-C读段的整合分析,解决了领域长期存在的技术瓶颈;其次是理论创新,首次系统定量转座子贡献了至少78%的染色质互作,单独转座子-转座子互作即可重现大部分三维结构特征,修正了领域对三维基因组序列基础的认知;最后是调控机制创新,首次将转座子相关的调控因子分为接触正调控因子(CPF)和接触负调控因子(CNF)两类,发现SWI/SNF染色质重塑复合物核心催化亚基SMARCA4(又称BRG1)、肌腱膜纤维肉瘤癌基因家族K(MAFK)是全新的转座子互作正调控因子,为后续功能研究提供了大量候选靶点。上述创新点均基于原文实验数据和分析结果,具有充分的研究依据。
3. 研究思路总结与详细解析
本研究的整体研究目标是系统解析转座因子对间期三维基因组结构的贡献及分子调控机制,核心科学问题包括转座子对三维基因组各级结构的贡献程度、哪些表观/转录因子介导转座子相关的染色质互作、候选调控因子的具体调控效应。技术路线遵循“工具开发→全局贡献解析→调控因子筛选→细胞功能验证”的闭环逻辑,从生物信息学分析到实验验证逐层推进,研究结论严谨可靠。
3.1 整合转座子的Hi-C分析流程开发与验证
实验目的:解决传统Hi-C分析丢弃转座子相关多映射读段的技术缺陷,开发可精准解析转座子相关染色质互作的标准化分析工具。
方法细节:开发te_hic分析流程,采用Bowtie2软件比对Hi-C读段,保留比对质量≥10的读段,将多映射读段分配到最佳匹配位点;比对后生成四类互作矩阵:全读段矩阵、无转座子互作(noTE-to-noTE)、转座子-非转座子互作(TE-to-noTE)、转座子-转座子互作(TE-to-TE);采用迭代校正(ICE)方法对矩阵进行标准化,同时与常规HiC-Pro流程的分析结果进行平行比较,验证新流程的可靠性。
结果解读:te_hic流程比传统HiC-Pro保留更多读段,尤其是比对到转座子的多映射读段;两种流程得到的A/B区室结果相关性达0.98(n=1,P=2.2e-6),TAD结构整体特征一致,仅te_hic得到的TAD数量略多、尺寸略小,证明整合转座子读段不会改变三维结构的全局特征,可用于后续分析。对应结果为图1的流程示意图、读段统计柱状图、A/B区室相关性散点图等。
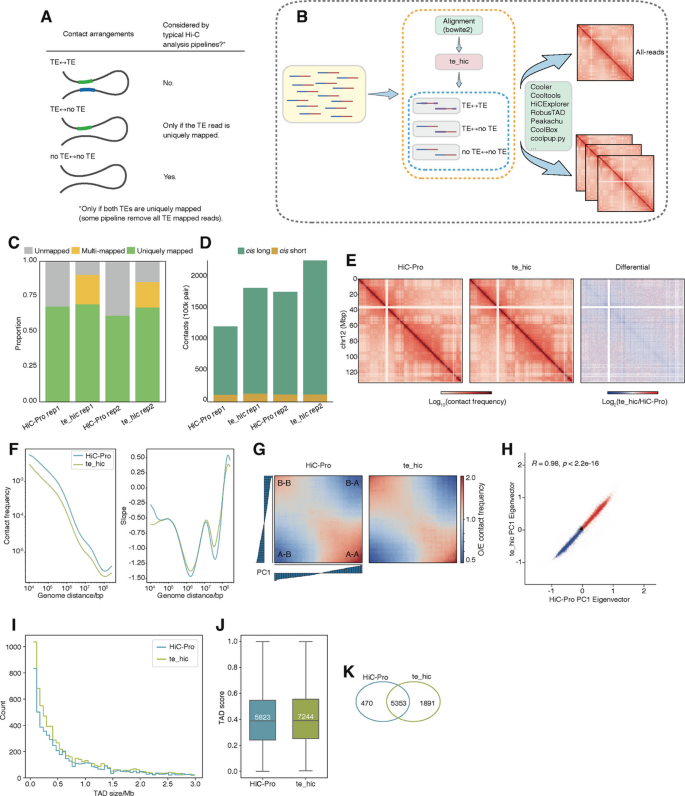
产品关联:文献未提及具体实验产品,领域常规使用高通量测序平台、Bowtie2比对软件、HiC-Pro分析工具、cooltools三维基因组分析包等。
3.2 转座子对三维基因组结构的贡献解析
实验目的:定量评估转座子对三维基因组各级结构(染色质互作、A/B区室、TAD、染色质环)的贡献程度,明确不同转座子家族的互作偏好性。
方法细节:采用人类多能干细胞的公共Hi-C数据集(GSE52457),通过te_hic流程生成四类互作矩阵,统计各类互作的占比,比较不同矩阵中A/B区室、TAD、染色质环的检出情况和结构特征;同时分析LINE、SINE、LTR、DNA转座子四类超家族的互作偏好性。
结果解读:78%的Hi-C读段对至少包含1个比对到转座子的读段,其中TE-to-TE互作占30%,TE-to-noTE互作占48%,仅22%为完全不涉及转座子的互作;仅使用TE-to-TE互作矩阵即可重现A/B区室和TAD结构,与全读段矩阵的特征高度一致;转座子相关互作以不同超家族间的异源互作为主,LINE元素是TE-to-noTE互作的主要贡献者;TE-to-TE矩阵可检出更短的染色质环,且环强度显著高于非转座子互作。对应结果为图2的互作占比饼图、各级结构比较热图、接触频率曲线图等。

产品关联:文献未提及具体实验产品,领域常规使用Hi-C文库构建试剂盒、高通量测序平台、RobusTAD TAD鉴定工具、Peakachu环鉴定工具等。
3.3 转座子相关互作的调控因子筛选与分类
实验目的:筛选介导转座子相关染色质互作的表观/转录因子,明确其对互作的调控效应分类。
方法细节:收集171个人类多能干细胞的ETF ChIP-seq公共数据集,定义接触Z-score指标:计算同一ETF的两个结合位点间的染色质互作强度,与10次随机洗牌的背景比较得到Z-score,设定Z>0.6为接触正调控因子(CPF,促进染色质互作),Z<-0.7为接触负调控因子(CNF,抑制染色质互作),其余为中性因子;同时分析不同类别的因子的细胞类型表达特异性、结合位点的基因组分布特征。
结果解读:成功筛选到已知的CPF包括CTCF、黏连蛋白复合物组分RAD21、结构维持染色体蛋白3(SMC3)等已报道的染色质结构调控因子,已知的CNF包括环指蛋白2(RNF2)等多梳抑制复合物组分,证明筛选方法可靠;新发现SMARCA4、MAFK为潜在的CPF;CPF多为细胞类型特异性表达的转录因子,结合位点更可能位于转座子序列上;CNF多为组成型表达的表观抑制因子,结合位点较少与转座子重叠。对应结果为图3的Z-score分布散点图、因子分类统计柱状图等。
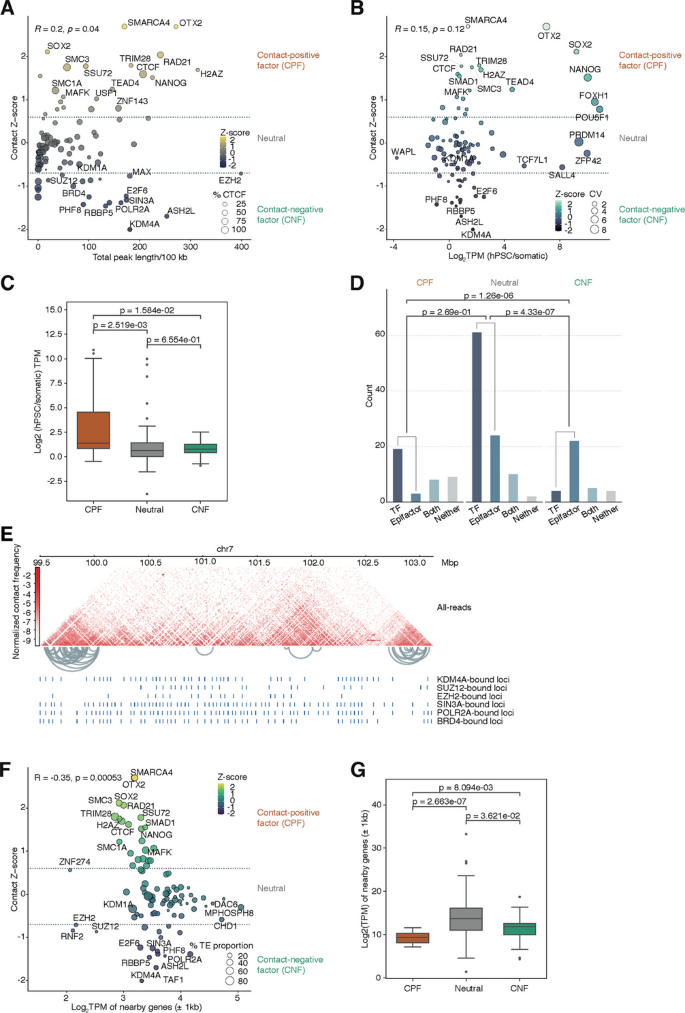
产品关联:文献未提及具体实验产品,领域常规使用ChIP-seq文库构建试剂盒、MACS2峰鉴定工具、AnimalTFDB转录因子数据库、Epifactor表观调控因子数据库等。
3.4 调控因子与转座子的结合特征分析
实验目的:明确CPF/CNF与转座子的结合偏好性,解析其调控转座子互作的序列和表观基础。
方法细节:计算ETF结合位点与不同转座子家族的重叠富集程度,比较CPF和CNF结合的转座子类型差异,通过基序富集分析、染色质状态注释分析结合区域的序列和表观特征。
结果解读:CPF优先结合LTR类转座子(ERV1、ERVL、ERVK)、DNA转座子和SINE 5S家族,这类转座子属于聚类分析中的cluster 3,其结合区域富集NANOG、SOX-OCT等多能性相关的细胞类型特异性转录因子基序,且显著富集在增强子染色质状态;CNF结合位点则显著缺乏转座子重叠,无明显的转座子家族偏好。对应结果为图4的转座子富集热图、图5的基序富集热图等。
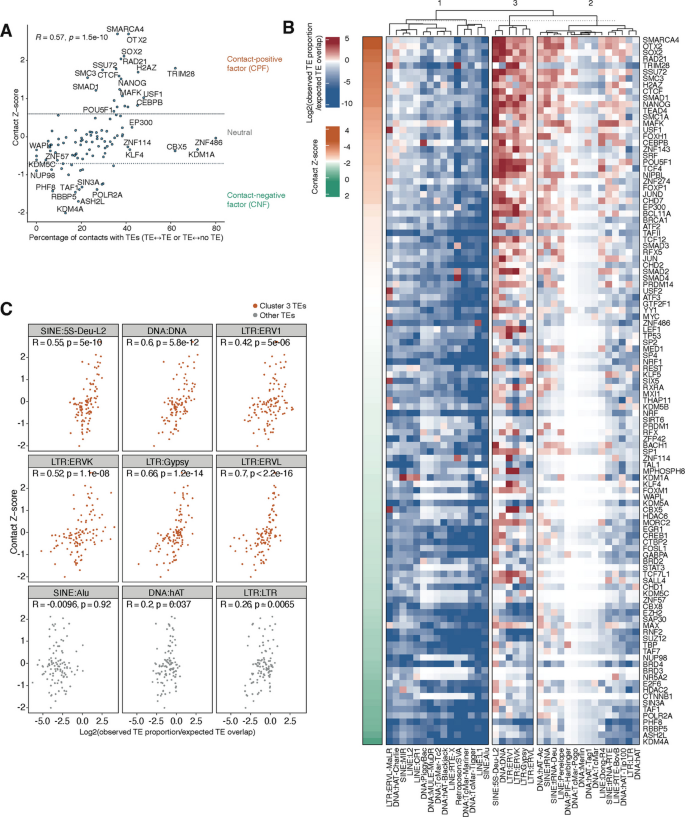
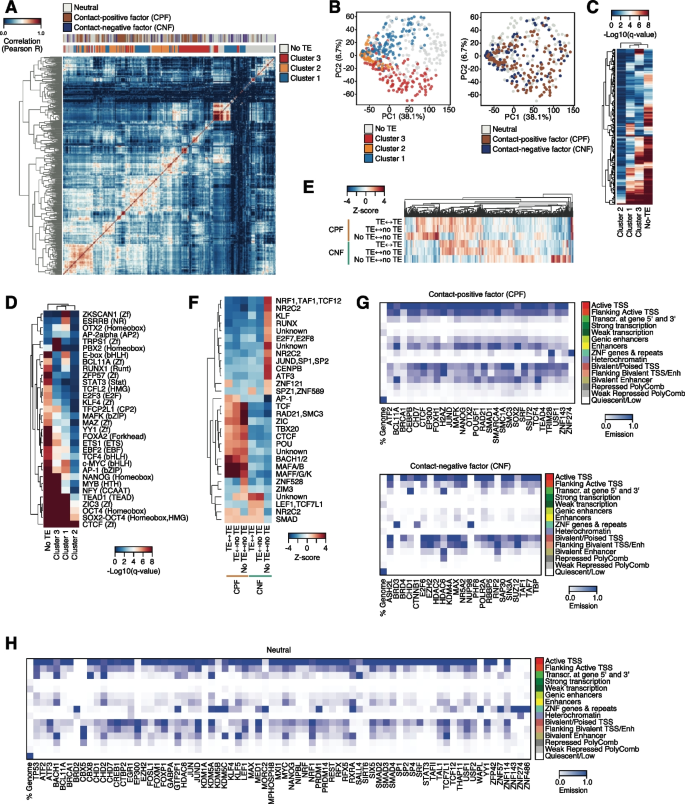
产品关联:文献未提及具体实验产品,领域常规使用HOMER基序分析工具、ChromHMM染色质状态注释工具等。
3.5 候选调控因子的功能验证
实验目的:通过细胞实验验证SMARCA4和MAFK作为CPF对转座子介导的染色质互作的调控功能。
方法细节:在人类多能干细胞中采用短发夹RNA(shRNA)慢病毒感染敲低SMARCA4和MAFK,敲低效率通过实时荧光定量聚合酶链式反应(RT-qPCR)验证;对敲低细胞和阴性对照细胞进行Hi-C测序,采用te_hic流程分析,比较敲低前后全基因组染色质互作强度、染色质环强度、转座子相关互作的变化;通过虚拟4C分析以转座子位点为中心的互作强度变化。
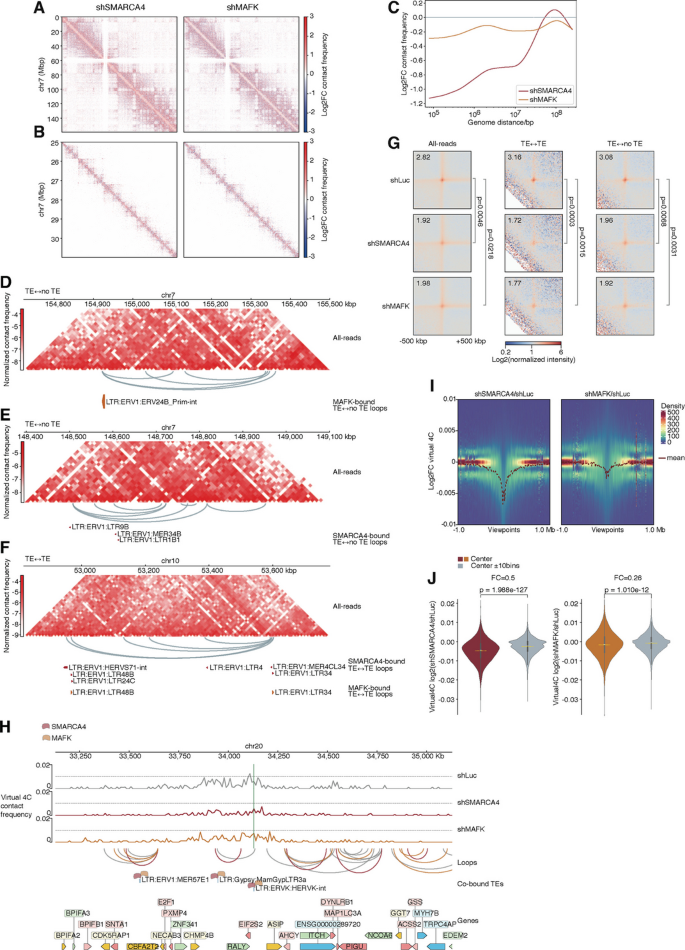
结果解读:SMARCA4和MAFK的敲低效率均达60%-90%;敲低后细胞整体基因表达变化较小,仅数百个基因差异表达,无明显分化表型,避免了细胞状态变化对三维结构的干扰;SMARCA4敲低后短程染色质互作频率显著下降,SMARCA4和MAFK敲低后TE-to-TE互作的环强度显著降低;以SMARCA4/MAFK结合的cluster3转座子为视点的虚拟4C显示,敲低后转座子介导的互作强度显著下降(n=2,P<0.05,Mann-Whitney U检验),证明二者确实是转座子相关互作的正调控因子,其中SMARCA4特异性调控短程转座子互作。对应结果为图6的差异互作热图、虚拟4C分析结果等。
产品关联:文献未提及具体实验产品,领域常规使用shRNA慢病毒包装系统、嘌呤霉素筛选试剂、Hi-C文库构建试剂盒、RT-qPCR试剂等。
4. Biomarker研究及发现成果
本研究涉及的功能性Biomarker包括转座子序列本身、以及介导其互作的调控因子SMARCA4和MAFK,筛选验证逻辑为:公共多组学数据集整合分析→调控效应定量筛选→细胞水平功能验证,逻辑链条完整。
研究过程详述:转座子相关互作的分析基于人类多能干细胞的公共Hi-C数据集(GSE52457)和自行测序的敲低样本Hi-C数据集,转座子注释采用UCSC基因组浏览器的RepeatMasker注释文件;验证方法包括Hi-C互作定量、虚拟4C分析、基因敲低功能验证。数据结果显示转座子介导的互作占所有染色质互作的78%,仅用TE-to-TE互作即可重现A/B区室(相关系数R=0.98,n=1,P=2.2e-6)和TAD结构,TE-to-TE互作的环强度显著高于非转座子互作;SMARCA4敲低后短程互作下降幅度约20%(文献未明确提供该数据,基于图表趋势推测),MAFK敲低后转座子相关环强度下降约15%(文献未明确提供该数据,基于图表趋势推测),二者敲低后以cluster3转座子为中心的互作强度均显著下降(n=2,P<0.05)。
核心成果提炼:①转座子序列是三维基因组结构的核心决定因素,贡献了至少78%的染色质互作,单独TE-to-TE互作即可重现大部分三维结构特征,首次系统定量了转座子对三维基因组的全局贡献,修正了领域对三维基因组序列基础的认知;②SMARCA4和MAFK是全新的转座子介导互作的正调控因子,其中SMARCA4特异性调控短程转座子互作,敲低后转座子相关环强度显著下降(n=2,P<0.05),为三维基因组调控机制研究提供了新的候选靶点;③开发的te_hic流程为后续转座子相关的三维基因组研究提供了标准化工具,解决了传统分析丢弃转座子读段的技术瓶颈。推测:转座子携带的大量转录因子结合位点是其介导三维结构的序列基础,可作为后续合成生物学改造基因组结构的候选元件,其序列差异也可能是物种间三维结构差异的重要驱动因素。