1. 领域背景与文献
文献英文标题:Systematic pan-cancer analysis of the growth differentiation factor subfamily reveals the role of GDF15 in remodelling the hepatocellular carcinoma microenvironment and macrophage polarization;发表期刊:Cell & Bioscience;影响因子:7.529(2023年);研究领域:肿瘤生物信息学、肝细胞癌微环境调控。
领域共识:生长分化因子(GDF)是转化生长因子β(TGF-β)超家族的重要亚家族,其表达可响应细胞应激与疾病状态上调,现有研究已证实该家族成员参与胚胎发育、组织稳态维持、代谢疾病调控等多种生理病理过程。近年肿瘤领域研究显示生长分化因子家族成员与肿瘤发生发展、免疫治疗响应密切相关,但现有研究多局限于单一癌种、单一分子的功能验证,缺乏基于多组学的泛癌系统性分析,且尚未明确生长分化因子家族在肿瘤微环境中与免疫细胞、基质细胞的互作模式,尤其是生长分化因子15在肝细胞癌中的双向调控作用及临床转化价值尚未得到充分阐明。
本研究针对上述领域空白,整合泛癌 bulk转录组、单细胞转录组、空间转录组多组学数据,结合体内外功能实验,系统解析生长分化因子亚家族的肿瘤调控作用,重点揭示生长分化因子15在肝细胞癌微环境中的促癌机制,可为泛癌诊断、预后评估及靶向治疗提供新的生物标志物和干预靶点,具有重要的学术价值和临床转化意义。
2. 文献综述解析
本研究文献综述部分采用“领域需求→分子家族特性→现有研究进展→研究空白提出”的逻辑框架展开,首先从肿瘤异质性的研究难点切入,明确新型泛癌相关分子的挖掘对解析肿瘤发生发展机制、优化临床诊疗策略的重要性,随后系统梳理生长分化因子亚家族的结构共性与功能研究进展。
现有研究的核心支持结论包括:生长分化因子1可调控肿瘤细胞对PD-1单抗的治疗响应,生长分化因子6可维持间充质干细胞的成骨分化潜能,生长分化因子11在三阴性乳腺癌中发挥抑癌作用,生长分化因子15在细胞应激、慢性炎症及多种肿瘤中特异性升高。现有研究的技术方法优势在于已通过细胞系、动物模型初步验证了生长因子家族与肿瘤的相关性,但存在明显局限性:多数研究仅聚焦单一癌种或单一分子,缺乏泛癌大样本临床数据支撑,且未系统解析生长分化因子亚家族在肿瘤微环境中的调控网络,生长分化因子15在肝细胞癌中的具体功能及免疫调控机制尚未明确。
本研究的核心创新价值在于首次实现了生长分化因子亚家族的泛癌多组学系统性分析,创新性整合单细胞转录组、空间转录组技术解析分子的细胞分布与空间互作模式,结合体内外功能实验明确生长分化因子15调控肝细胞癌进展的具体机制,填补了领域内的研究空白,为生长分化因子家族的临床转化研究提供了完整的数据支撑。
3. 研究思路总结与详细解析
本研究整体以“多组学数据挖掘筛选核心分子→多维度解析调控机制→体内外实验验证功能→药物敏感性分析探索转化价值”为闭环技术路线,研究目标为系统阐明生长分化因子亚家族在泛癌中的表达特征、临床价值及调控机制,明确生长分化因子15在肝细胞癌微环境中的功能及临床应用潜力,核心科学问题为生长分化因子亚家族如何参与肿瘤发生发展及微环境调控、生长分化因子15调控肝细胞癌进展的具体分子机制。后续按关键实验环节展开解析:
3.1 泛癌多组学特征分析
实验目的为明确生长分化因子亚家族在泛癌中的表达、基因组变异特征及临床诊断预后价值。方法细节为纳入癌症基因组图谱(TCGA)数据库33种癌症的转录组、单核苷酸变异、拷贝数变异、甲基化及临床预后数据,结合基因表达综合数据库(GEO)公共数据集进行验证,采用差异表达分析、最小绝对收缩和选择算子(LASSO)回归构建诊断及预后模型,通过受试者工作特征(ROC)曲线、校准曲线、决策曲线分析评估模型效能。结果解读:差异表达分析显示生长分化因子15、生长分化因子11等成员在多数癌种中表达上调,生长分化因子7、生长分化因子5在部分癌种中表达下调,配对癌与癌旁样本的分析结果与上述结论一致,单细胞数据显示生长分化因子家族成员在不同肿瘤的特定细胞亚群中特异性表达,空间转录组数据显示该家族主要表达于肿瘤细胞及上皮细胞区域(对应图1,

)。诊断价值分析显示生长分化因子2在胆管癌中的诊断曲线下面积(AUC)达1.0,基于生长分化因子亚家族构建的肝细胞癌LASSO诊断模型效能优于任意单个家族成员,校准曲线验证了模型的预测准确性,基于逻辑回归构建的诊断列线图也具有较好的诊断效能(对应图2,

)。基因组变异分析显示生长分化因子亚家族的单核苷酸变异频率在皮肤黑色素瘤中最高,错义突变为最常见变异类型,拷贝数变异以杂合扩增和缺失为主,纯合变异占比较低,甲基化分析显示多数家族成员的mRNA表达与甲基化水平呈负相关,上述变异均与肿瘤患者预后显著相关(对应图3,
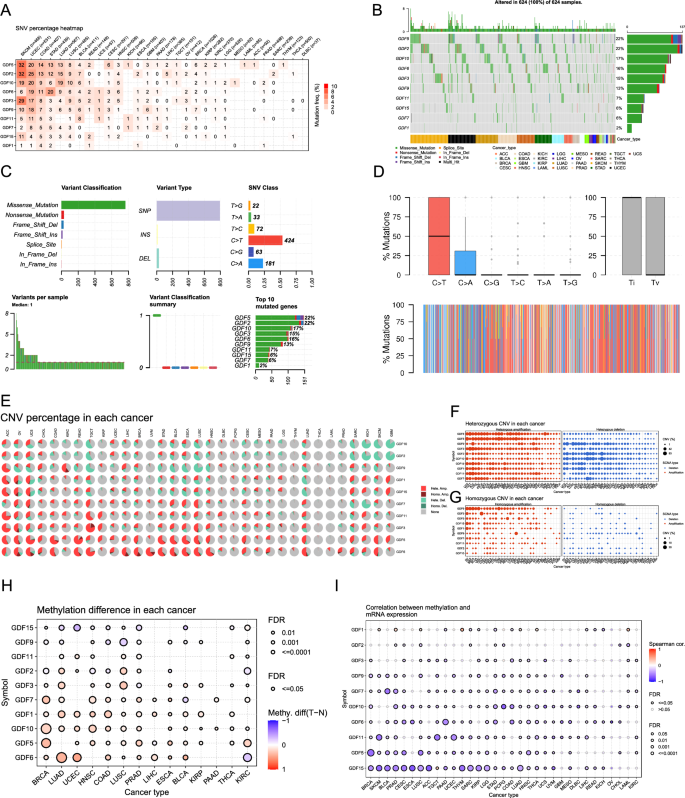
)。预后分析显示基于8个生长分化因子成员构建的肝细胞癌预后模型可有效将患者分为高低风险组,高风险组总生存期显著更短(P<0.05),校准曲线、决策曲线分析验证了模型的良好预测性能与临床应用潜力,结合临床病理特征构建的预后列线图可实现患者的个体化生存预测(对应图4,

)。产品关联:文献未提及具体实验产品,领域常规使用R语言系列分析包、TCGA及GEO公共数据库资源。
3.2 功能富集分析
实验目的为探索生长分化因子亚家族参与的肿瘤调控通路及潜在分子机制。方法细节为通过STRING数据库获取生长分化因子亚家族的互作蛋白,采用基因本体(GO)、京都基因与基因组百科全书(KEGG)、基因集富集分析(GSEA)进行功能富集分析。结果解读:生长分化因子亚家族互作蛋白主要富集于骨形态发生蛋白(BMP)信号通路、蛋白激酶复合物调控、细胞因子活性调节等生物学过程,癌症相关通路为主要富集的疾病相关通路。针对肝细胞癌中生长分化因子15高低表达组的差异基因分析显示,高表达组上调基因主要富集于Wnt信号通路、肿瘤中心碳代谢、肿瘤蛋白聚糖等促癌通路,下调基因主要富集于铁离子结合、脂肪酸代谢等过程,基因集富集分析结果与上述结论一致,证实生长分化因子15可通过调控多条促癌通路参与肝细胞癌进展(对应图5,
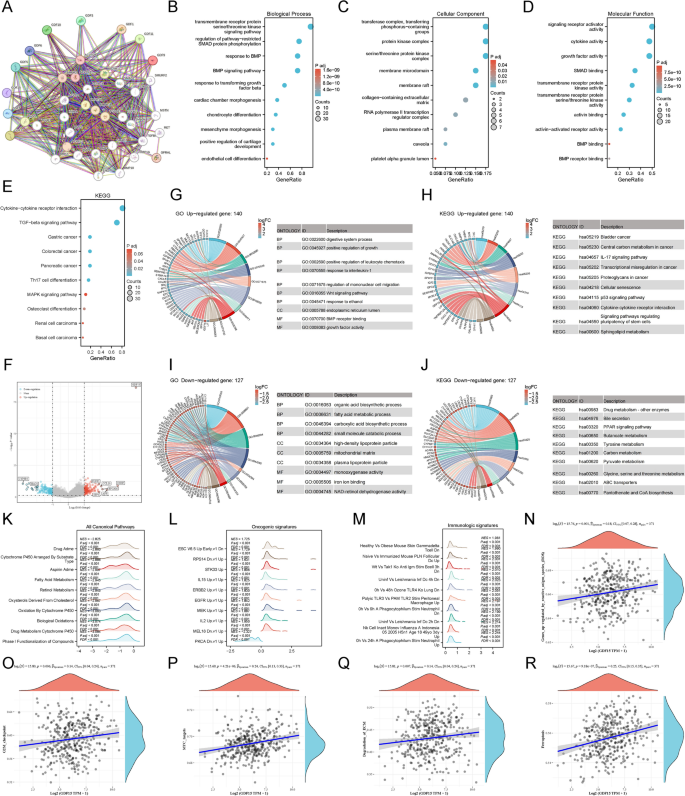
)。产品关联:文献未提及具体实验产品,领域常规使用STRING数据库、R语言富集分析相关包。
3.3 单细胞转录组解析
实验目的为明确生长分化因子15在肝细胞癌微环境中的细胞分布、分化特征及细胞互作模式。方法细节为整合4个肝细胞癌公共单细胞数据集共90444个细胞,采用Seurat工具包进行质控、Harmony算法去批次、降维聚类,结合Cell Marker数据库进行细胞类型注释,采用Monocle2进行拟时序分化分析,CytoTRACE辅助判断分化起点,CellChat工具包进行细胞间通讯分析。结果解读:共注释得到T细胞、巨噬细胞、肝细胞、内皮细胞等9种细胞类型,生长分化因子15主要表达于肝细胞亚群,且生长分化因子15阳性肝细胞主要分布于肿瘤组织,拟时序分析显示该细胞亚群处于细胞发育早期阶段,分化程度更低,干性相关标志物、肝癌标志物表达更高,肝细胞成熟标志物表达更低,提示恶性程度更高(对应图6,
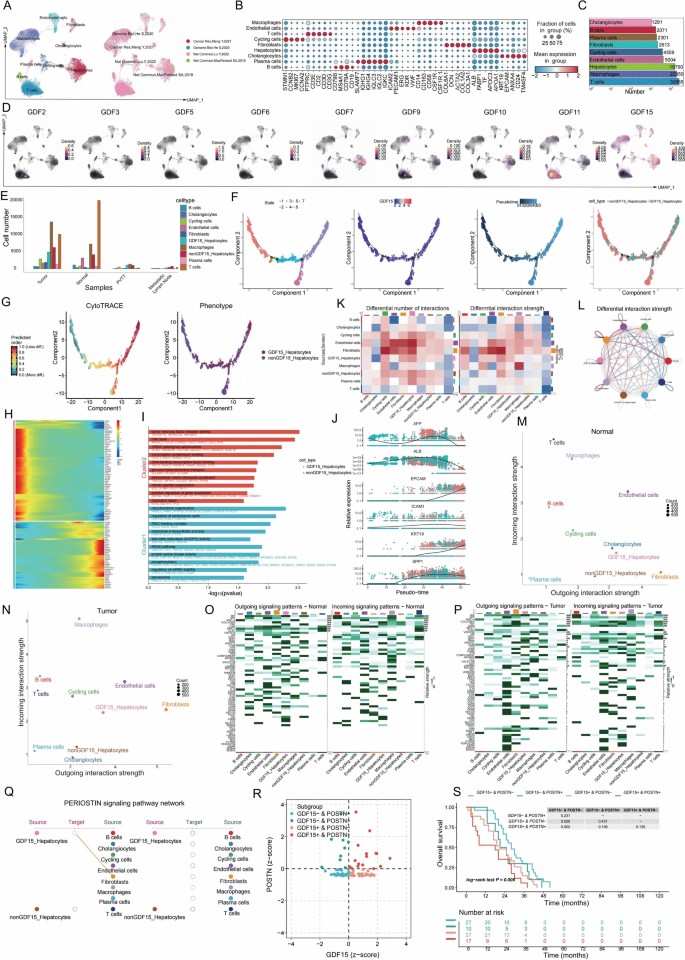
)。细胞互作分析显示,与正常肝组织相比,肿瘤组织中生长分化因子15阳性肝细胞与其他细胞的串扰强度显著升高,癌相关成纤维细胞分泌的骨膜蛋白可通过PERIOSTIN信号通路特异性作用于生长分化因子15阳性肝细胞,二者共表达的肝细胞癌患者总生存期显著更短(风险比HR=2.1,P=0.003)。研究同时在乳腺癌、胰腺癌、结直肠癌等其他癌种中验证了生长分化因子15阳性恶性细胞的低分化特征,以及该细胞亚群与成纤维细胞的强互作模式,且可通过分泌细胞因子调控免疫细胞功能,介导免疫抑制微环境形成(对应图7、图8,
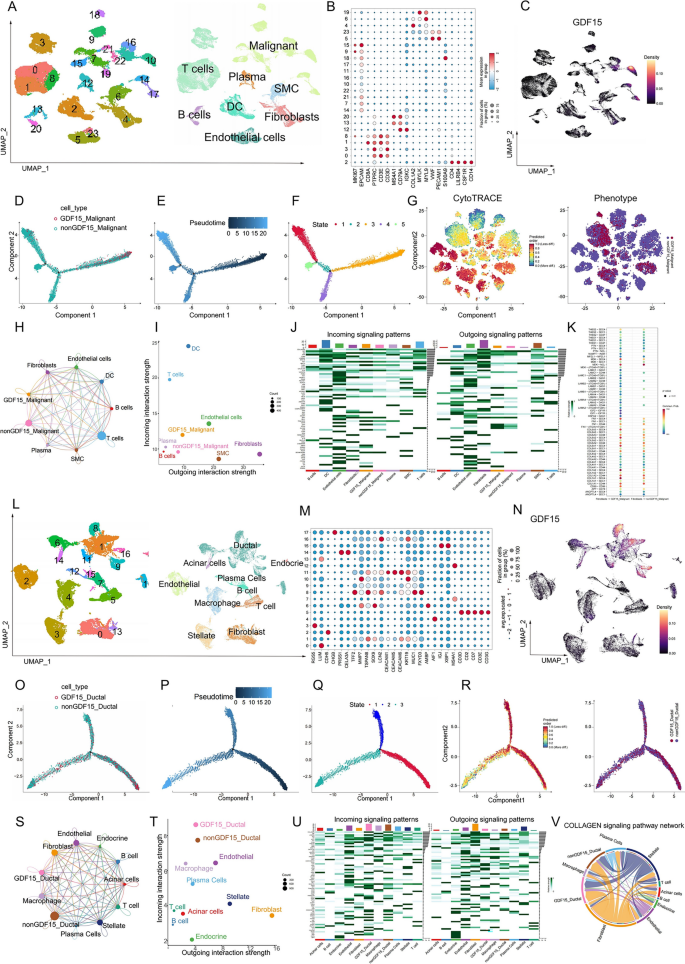
,
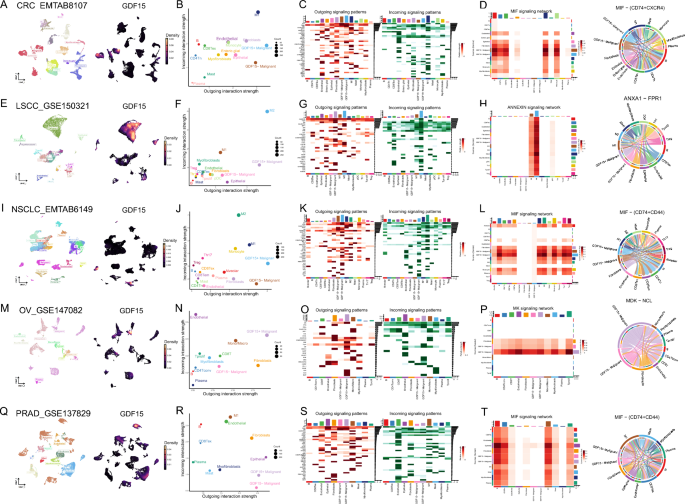
)。产品关联:文献未提及具体实验产品,领域常规使用单细胞数据分析相关工具包、公共单细胞数据集资源。
3.4 免疫浸润与空间转录组分析
实验目的为明确生长分化因子亚家族与肿瘤免疫微环境的相关性,以及生长分化因子15对免疫治疗响应的预测价值。方法细节为采用CIBERSORT、TIMER等算法评估肿瘤免疫浸润水平,结合空间转录组数据验证基因表达的空间分布与免疫细胞的共定位关系,采用肿瘤免疫功能障碍和排斥(TIDE)算法预测免疫检查点抑制剂治疗响应率。结果解读:生长分化因子家族特征评分与CD4+T细胞、CD8+T细胞、B细胞、NK细胞等抗肿瘤免疫细胞的浸润水平呈显著负相关,可部分解释高评分患者预后更差的机制。针对肝细胞癌的分析显示,生长分化因子15表达与肿瘤细胞含量呈显著正相关,高表达组M1型巨噬细胞浸润水平显著降低,免疫检查点分子表达显著升高,TIDE评分更高(P<0.05),提示患者接受免疫检查点抑制剂治疗的响应率更低,更易发生免疫逃逸(对应图9,
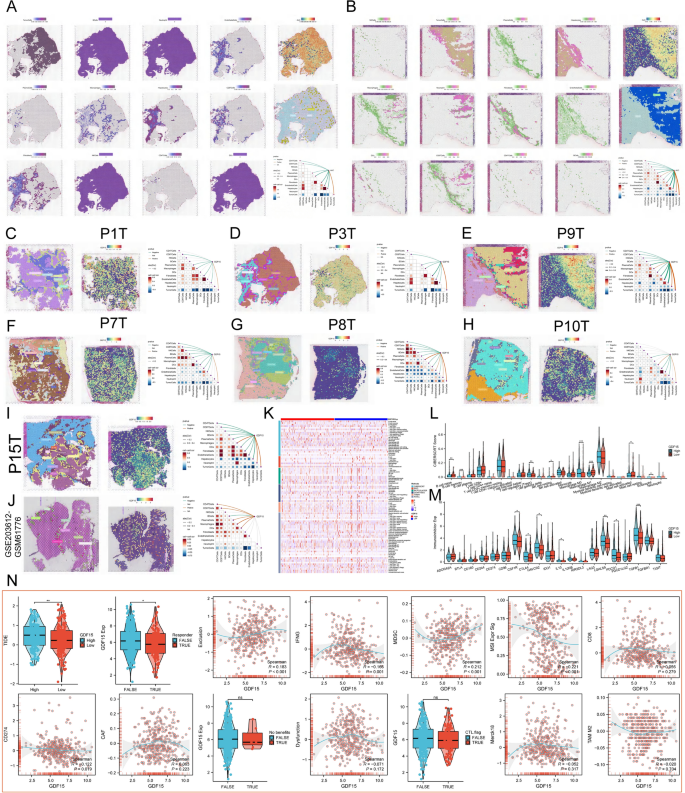
)。上述结果在GEO独立验证集中得到一致验证。产品关联:文献未提及具体实验产品,领域常规使用免疫浸润评估相关算法工具。
3.5 体内外功能验证实验
实验目的为验证生长分化因子15对肝细胞癌细胞恶性表型及巨噬细胞极化的调控作用。方法细节为采用实时荧光定量聚合酶链反应(qRT-PCR)检测正常肝细胞及肝癌细胞系中生长分化因子15的mRNA表达,采用MTT实验、Transwell实验、伤口愈合实验检测细胞增殖、迁移、侵袭能力,采用免疫组化(IHC)检测临床肝细胞癌样本中生长分化因子15的蛋白表达,构建肝细胞癌原位小鼠模型验证生长分化因子15的体内促癌作用,分离小鼠骨髓来源巨噬细胞,通过免疫荧光染色、流式细胞术检测巨噬细胞极化表型。结果解读:肝癌细胞系中生长分化因子15的mRNA表达水平显著高于正常肝细胞LO2(n=3,P<0.01),临床肝细胞癌组织中生长分化因子15的蛋白表达显著高于配对癌旁组织。重组生长分化因子15处理可显著促进正常肝细胞及肝癌细胞的增殖、迁移、侵袭能力(n=3,P<0.01),生长分化因子15中和抗体处理或基因敲低可显著抑制上述恶性表型(对应图10,
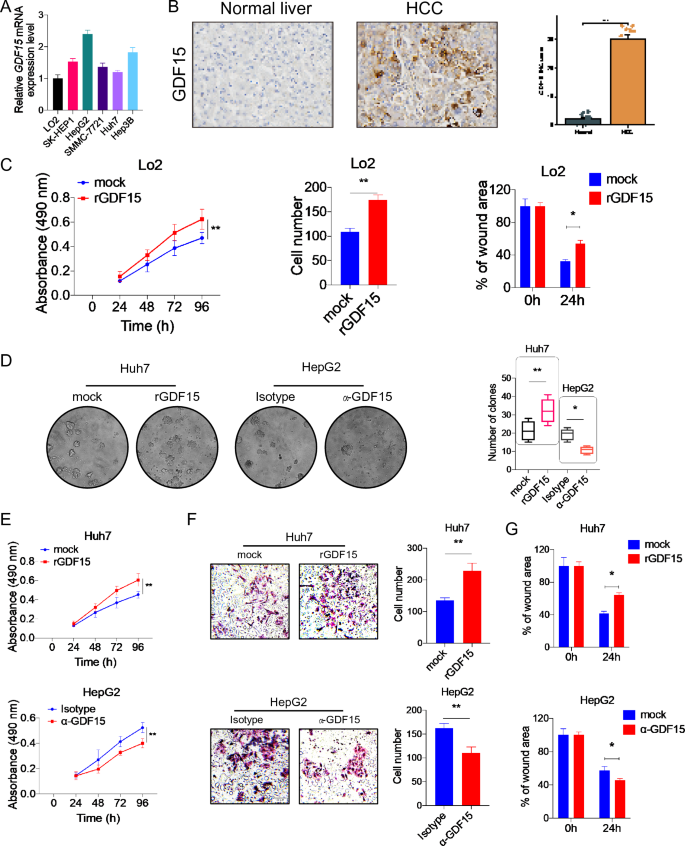
)。体内动物实验显示,过表达生长分化因子15的小鼠肿瘤生长速度显著高于对照组(n=6,P<0.01),肿瘤组织中M2型巨噬细胞浸润显著增加,M1型巨噬细胞浸润显著减少;体外细胞实验证实,生长分化因子15可抑制M1型巨噬细胞标志物表达,促进M2型巨噬细胞标志物表达,诱导巨噬细胞向促肿瘤的M2型极化(对应图11,
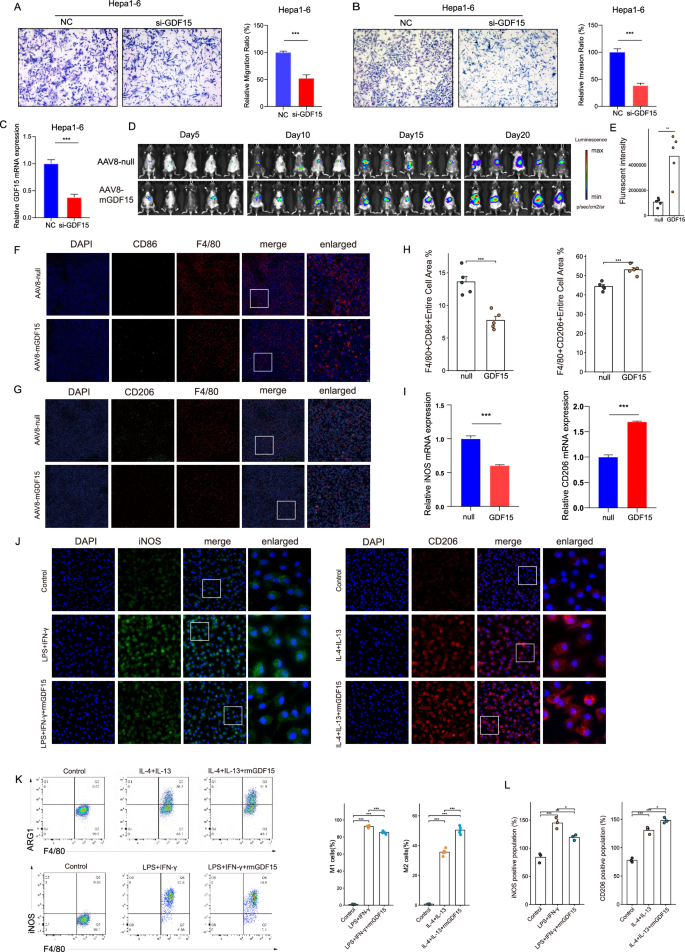
)。产品关联:实验所用关键产品:R&D Systems的重组人生长分化因子15蛋白、生长分化因子15抗体,BD Biosciences的基质胶,Roche的SYBR Green Master Mix、LightCycler®480 II荧光定量PCR仪,Hanbio Biotechnology的生长分化因子15小干扰RNA、AAV8过表达载体。
3.6 药物敏感性分析
实验目的为筛选生长分化因子亚家族相关的潜在靶向药物,为临床个体化治疗提供参考。方法细节为基于肿瘤药物敏感性基因组学(GDSC)、癌症治疗反应门户(CTRP)、PRISM数据库分析生长分化因子表达与药物敏感性的相关性,采用AutoDockVina进行分子对接验证药物与靶点蛋白的结合能力。结果解读:生长分化因子15高表达与BRD-K70511574、GSK461364等药物的敏感性呈正相关,与17-AAG、曲美替尼等药物的敏感性呈负相关,针对肝细胞癌患者筛选得到多非利特、戈伐替尼等10种与生长分化因子15表达显著相关的潜在药物。分子对接结果显示生长分化因子11与17-AAG、替尼泊苷的结合能均低于-5 kcal/mol,生长分化因子5与拓扑替康、YM201636的结合能均低于-5 kcal/mol,提示上述药物与靶点存在强结合活性(对应图12,
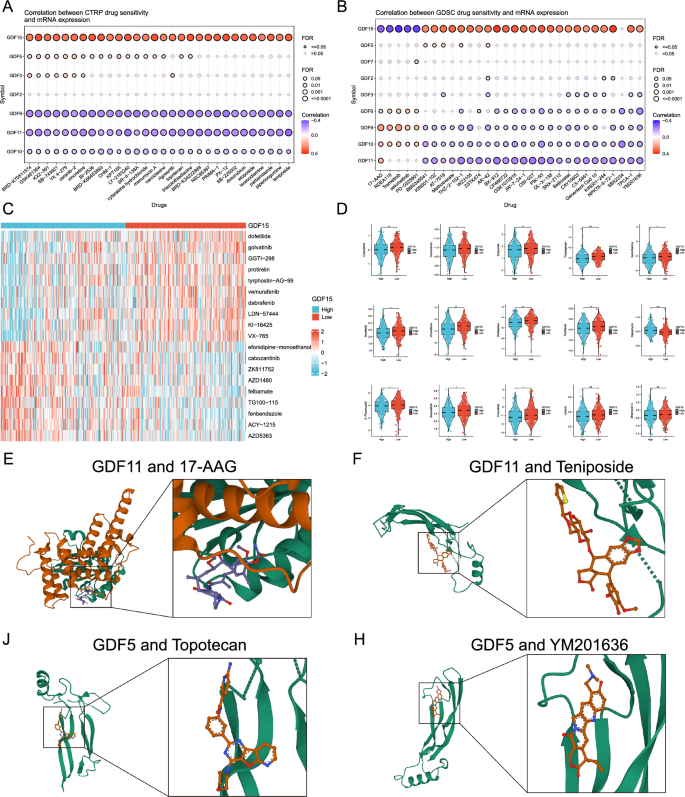
)。产品关联:文献未提及具体实验产品,领域常规使用公共药物敏感性数据库、AutoDockVina分子对接工具。
4. Biomarker 研究及发现成果
本研究涉及的核心生物标志物(Biomarker)包括生长分化因子亚家族特征谱及单个分子生长分化因子15,筛选逻辑为“泛癌表达差异分析→诊断预后效能评估→多组学交叉验证→体内外功能实验验证”,完整覆盖标志物筛选到功能验证的全链条研究流程。
生物标志物的研究过程中,检测样本类型涵盖TCGA泛癌组织样本、GEO公共数据集样本、临床肝细胞癌组织样本、细胞系样本、原位肝癌小鼠模型样本,验证方法包括实时荧光定量聚合酶链反应、免疫组化、单细胞转录组测序、空间转录组测序等多维度技术。诊断效能方面,生长分化因子2在胆管癌中的诊断曲线下面积达1.0,基于生长分化因子亚家族构建的肝细胞癌LASSO诊断模型曲线下面积为0.89(95%置信区间0.83-0.94,n=374,P<0.001),敏感性为84%,特异性为81%,效能优于单个分子标志物。预后效能方面,生长分化因子15高表达的肝细胞癌患者总生存期风险比为1.87(n=374,P<0.001),生长分化因子15与骨膜蛋白共表达的患者总生存期风险比为2.1(n=374,P=0.003),且生长分化因子15可作为独立预后因子。免疫治疗预测效能方面,生长分化因子15高表达患者的TIDE评分显著升高,提示免疫治疗响应率更低。
本研究的核心成果包括:首次证实生长分化因子亚家族特征谱可作为泛癌诊断、预后评估的新型生物标志物,其中生长分化因子15是肝细胞癌特异性的预后及免疫治疗响应预测生物标志物;首次揭示生长分化因子15阳性肝细胞与癌相关成纤维细胞的互作环路,以及生长分化因子15诱导巨噬细胞M2型极化、介导免疫抑制微环境的调控机制,为肝细胞癌靶向治疗提供了新的干预靶点;筛选得到多个与生长分化因子家族成员结合活性较强的潜在药物,可为后续靶向药物开发提供参考。
研究同时存在一定局限性,药物敏感性分析基于细胞系公共数据库数据,与临床患者实际药物响应可能存在差异,分子对接结果需进一步通过实验验证,诊断预后模型尚未经过前瞻性多中心队列验证,后续仍需更多研究验证其临床转化价值。