1. 领域背景与文献
文献英文标题:The cytoplasmic lncRNA USP30-AS1 amplifies type I interferon signaling by stabilizing AU-rich element-containing immune transcripts;发表期刊:Cell & Bioscience;影响因子:8.7(2023年);研究领域:先天免疫调控与自身免疫病。
领域共识:I型干扰素是先天免疫抗病毒防御的核心细胞因子,1957年首次被发现后,其下游信号通路的调控机制逐步被解析,1990年代明确Janus激酶-信号转导及转录激活因子(JAK-STAT)通路是I型干扰素诱导下游基因表达的核心转录调控通路。当前研究热点聚焦于I型干扰素信号的精细调控机制,尤其是如何平衡其抗病毒防御和自身免疫病理的双重效应,近年来研究发现转录后调控(包括mRNA稳定性、翻译效率调控等)是调节免疫反应动态性的关键层级,而长链非编码RNA(lncRNA)作为新兴调控分子,其在I型干扰素信号中的作用尚未被充分阐明。目前领域未解决的核心问题包括:I型干扰素信号转录后调控的关键分子尚未完全鉴定,缺乏可特异性靶向过度激活的I型干扰素信号、同时保留抗病毒功能的干预靶点,I型干扰素相关自身免疫病的无创疾病活动度标志物不足。
本研究针对上述研究空白,筛选得到I型干扰素诱导的细胞质长链非编码RNA USP30-AS1,阐明其通过稳定核酸传感器和含AU富集元件(ARE)的干扰素刺激基因(ISG)mRNA,放大I型干扰素信号的分子机制,同时验证其在系统性红斑狼疮、类风湿关节炎、皮肌炎等自身免疫病中的临床意义,为I型干扰素相关疾病的诊断和治疗提供新的方向。
2. 文献综述解析
作者的文献综述按照调控层级的逻辑展开,首先梳理I型干扰素信号的生理功能与病理效应的双重性,其次明确转录水平调控的局限性,进而引出转录后调控的重要性,最后聚焦长链非编码RNA在转录后免疫调控中的研究进展与不足。
现有研究的核心结论包括:I型干扰素通过激活JAK-STAT通路诱导上百种干扰素刺激基因表达,建立抗病毒状态,该通路的异常激活与系统性红斑狼疮、类风湿关节炎、皮肌炎等自身免疫病的发生发展密切相关;转录水平调控难以完全解释免疫反应的快速动态变化,mRNA稳定性调控是调节免疫反应强度和持续时间的关键机制;细胞质长链非编码RNA可通过与mRNA或蛋白质互作,在转录后层面调控免疫相关基因的表达。现有研究的技术优势包括:基于转录组测序筛选差异表达长链非编码RNA的技术成熟,放线菌素D追踪、溴尿苷标记等mRNA稳定性检测方法可精准量化转录后调控效应。现有研究的局限性包括:参与I型干扰素信号调控的长链非编码RNA功能尚未被系统解析,可同时调控抗病毒免疫和自身免疫病理的长链非编码RNA分子鲜有报道,缺乏兼具诊断价值和治疗潜力的I型干扰素通路特异性调控分子。
本研究的创新价值体现在三个层面:首次发现USP30-AS1作为I型干扰素诱导的细胞质长链非编码RNA,可通过转录后调控放大I型干扰素信号;首次阐明其通过特异性稳定含AU富集元件的免疫相关mRNA发挥功能的分子机制;首次验证其在多种I型干扰素相关自身免疫病中表达上调,且与疾病活动度正相关,兼具疾病标志物和治疗靶点的双重潜力,填补了领域内I型干扰素转录后调控机制的研究空白。
3. 研究思路总结与详细解析
本研究的核心研究目标是鉴定调控I型干扰素信号双重效应的转录后调控分子,阐明其作用机制并验证临床转化价值。核心科学问题为长链非编码RNA USP30-AS1如何调控I型干扰素信号的功能与分子机制。整体技术路线遵循“分子筛选→特征鉴定→功能验证→机制解析→临床验证”的闭环逻辑:首先通过公共转录组数据集筛选I型干扰素诱导的长链非编码RNA候选分子,其次对候选分子的全长、非编码属性、亚细胞定位等分子特征进行鉴定,随后通过基因敲除、回补实验验证其在抗病毒免疫和炎症应答中的功能,进一步通过mRNA稳定性检测、报告基因实验解析其作用机制,最终通过公共临床队列数据集验证其临床相关性。
3.1 USP30-AS1的筛选与分子特征鉴定
该实验环节的核心目标是筛选I型干扰素诱导的长链非编码RNA并验证其分子特征。采用的实验方法包括:利用PRJEB21332公共转录组数据集,分析I型干扰素-β处理后人原代成纤维细胞中差异表达的长链非编码RNA,采用佛波酯(PMA)分化的U937巨噬细胞、THP1细胞、原代巨噬细胞,通过实时荧光定量PCR(qPCR)验证候选分子的诱导表达,使用JAK1/2抑制剂鲁索替尼处理细胞,验证候选分子的表达是否依赖JAK-STAT通路;通过5"/3"cDNA末端快速扩增(RACE)技术确定候选分子的全长序列,构建增强型绿色荧光蛋白(EGFP)融合表达质粒,通过免疫印迹实验验证其非编码属性。实验结果显示,火山图分析表明I型干扰素-β处理后共有127个长链非编码RNA显著上调,其中USP30-AS1的上调幅度最高(Log2FC>3,n=3,P<0.001),时间梯度实验显示其表达随I型干扰素处理时间升高,与经典干扰素刺激基因ISG15的诱导模式一致,鲁索替尼处理可完全抑制其诱导,证实其表达依赖JAK-STAT通路;5"/3"RACE结果显示USP30-AS1的全长为656个核苷酸,增强型绿色荧光蛋白融合实验的免疫印迹结果未检测到融合蛋白的表达,证实其为非编码RNA。
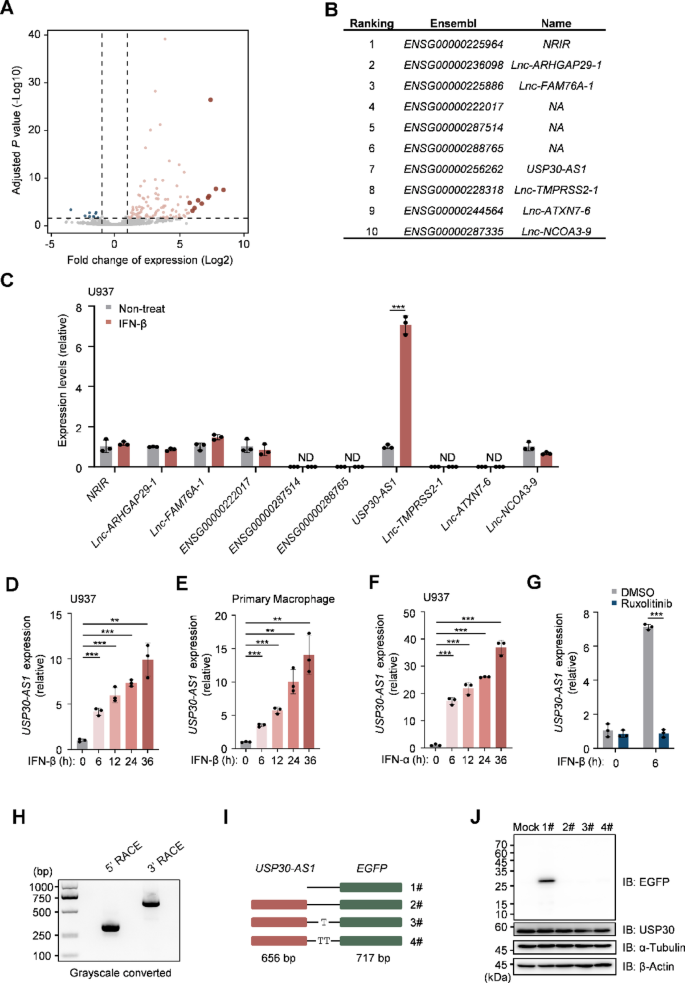
实验所用关键产品:Takara的SMARTer RACE 5"/3" Kit(货号634858)、赛默飞世尔科技的抗增强型绿色荧光蛋白抗体(货号MA1-952)、Applied Biosystems的StepOnePlus实时荧光定量PCR系统(货号4376600)。
3.2 USP30-AS1的亚细胞定位与功能独立性验证
该实验环节的核心目标是明确USP30-AS1的亚细胞定位,验证其功能不依赖反义链编码基因USP30。采用的实验方法包括:通过LncBook数据库分析USP30-AS1基因座的物种保守性,采用CRISPR/Cas9基因编辑技术构建USP30-AS1敲除的U937细胞系,通过亚细胞组分分离、RNA荧光原位杂交(RNA-FISH)检测其亚细胞定位,通过小干扰RNA敲低USP30后检测干扰素刺激基因ISG15的表达,验证二者的功能独立性,对USP30-AS1敲除细胞进行转录组测序,分析差异表达基因的通路富集情况。实验结果显示,保守性分析显示USP30-AS1基因座在灵长类动物中存在保守的干扰素刺激响应元件(ISRE),提示其I型干扰素诱导的调控模式在灵长类中保守;敲除USP30-AS1不影响USP30的mRNA和蛋白表达,敲低USP30也不影响I型干扰素诱导的ISG15表达(n=3,P>0.05),证实二者功能相互独立;亚细胞组分分离PCR和RNA荧光原位杂交结果显示USP30-AS1主要定位于细胞质,提示其可能参与转录后调控;转录组差异分析显示USP30-AS1敲除后共有428个基因显著下调,KEGG通路富集分析显示这些基因显著富集于先天免疫通路、病毒感染通路、细胞因子互作通路。
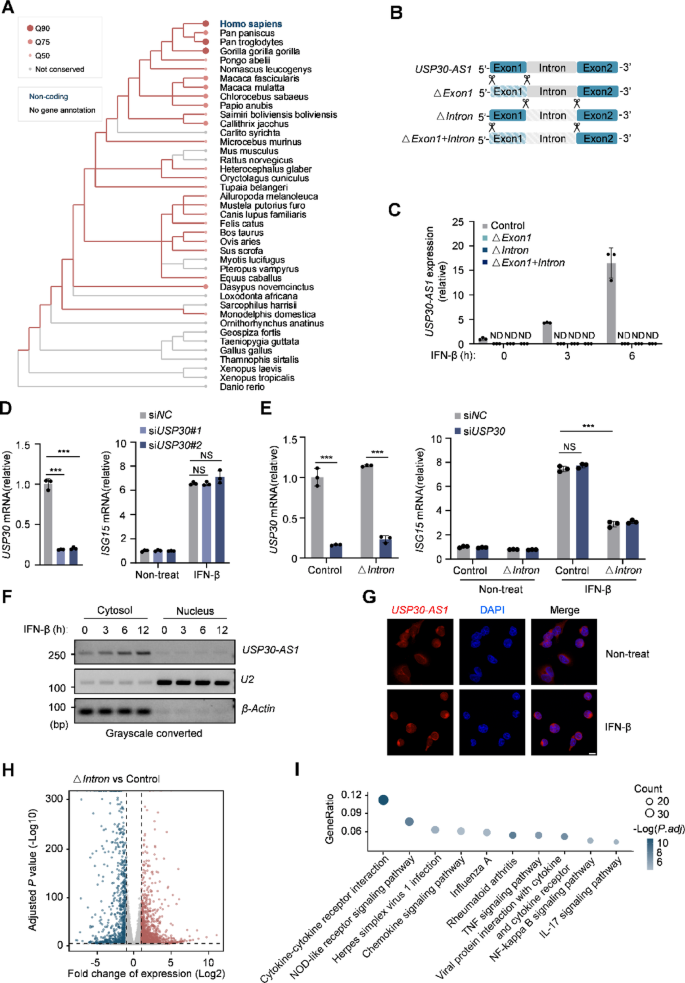
实验所用关键产品:Addgene的lentiCRISPRv2质粒(货号52961)、锐博生物的RNA荧光原位杂交试剂盒(货号C10910)、圣克鲁斯生物技术的抗USP30抗体(货号sc-515235)。
3.3 USP30-AS1对核酸传感器表达的调控机制验证
该实验环节的核心目标是验证USP30-AS1对核酸传感器表达的调控作用及分子机制。采用的实验方法包括:对USP30-AS1敲除细胞的转录组数据进行筛选,得到差异表达的核酸传感器分子,通过免疫印迹、实时荧光定量PCR验证敲除和回补细胞中维甲酸诱导基因I(RIG-I)、黑色素瘤分化相关蛋白5(MDA5)、蛋白激酶R(PKR)、环GMP-AMP合酶(cGAS)的表达水平,采用放线菌素D(ActD)追踪实验检测mRNA的稳定性,采用溴尿苷(BrU)标记实验检测新生转录本的合成水平。实验结果显示,热图分析表明USP30-AS1敲除后多个核酸传感器的表达显著下调;免疫印迹结果显示敲除USP30-AS1后,维甲酸诱导基因I、黑色素瘤分化相关蛋白5、蛋白激酶R、环GMP-AMP合酶的蛋白水平降低40%~60%(n=3,P<0.01),回补USP30-AS1可恢复上述蛋白的表达;放线菌素D实验显示敲除USP30-AS1后,核酸传感器的mRNA半衰期较对照组缩短30%~50%(n=3,P<0.05),溴尿苷标记实验显示新生转录本的水平无显著变化(n=3,P>0.05),证实USP30-AS1通过增强mRNA稳定性调控核酸传感器的表达。
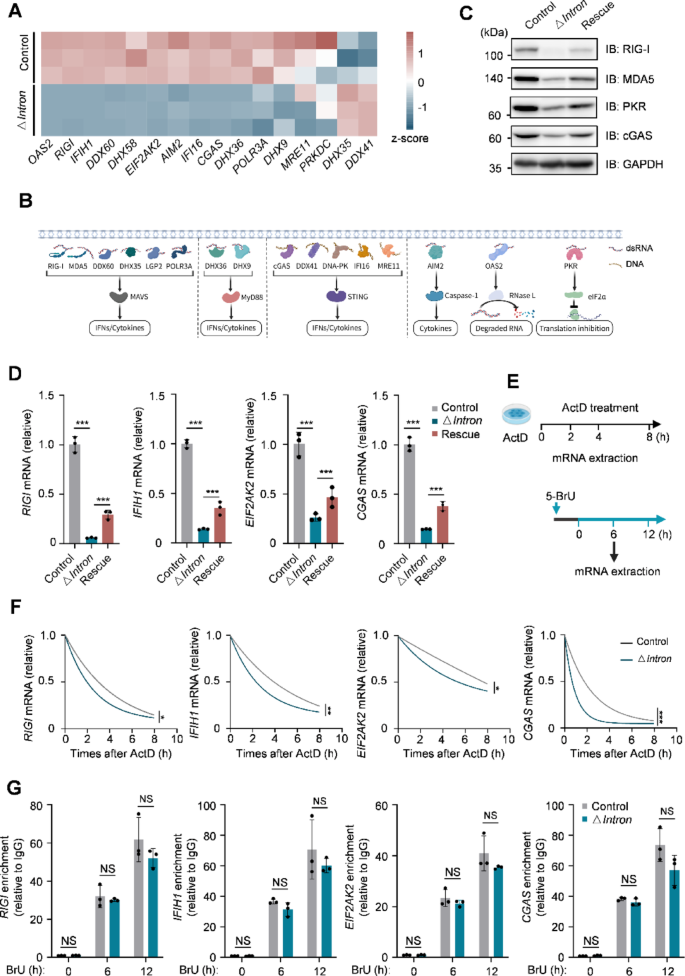
实验所用关键产品:Cell Signaling Technology的抗黑色素瘤分化相关蛋白5抗体(货号5321S)、抗蛋白激酶R抗体(货号12297S)、Sigma-Aldrich的放线菌素D(货号HY-17559)、溴尿苷(货号850187)。
3.4 USP30-AS1稳定含AU富集元件的干扰素刺激基因mRNA的机制验证
该实验环节的核心目标是验证USP30-AS1通过AU富集元件稳定干扰素刺激基因mRNA的分子机制。采用的实验方法包括:通过生物信息学分析USP30-AS1敲除细胞中下调基因的3"非翻译区(3"UTR)的AU富集元件分布情况,构建野生型和AU富集元件缺失的3"UTR融合增强型绿色荧光蛋白的报告基因质粒,在HEK293T细胞中共转染报告基因质粒和USP30-AS1过表达质粒,通过实时荧光定量PCR检测增强型绿色荧光蛋白的mRNA水平。实验结果显示,近一半下调基因的3"UTR含至少1个AU富集元件,且AU富集元件的数量越多,基因在USP30-AS1敲除后的下调幅度越大;63.6%的含AU富集元件的干扰素刺激基因在USP30-AS1敲除后表达显著下调;报告基因实验显示,仅当3"UTR含完整AU富集元件时,过表达USP30-AS1可使增强型绿色荧光蛋白的mRNA水平升高1.5~2.2倍(n=3,P<0.01),而AU富集元件缺失后该效应消失,证实AU富集元件是USP30-AS1调控靶mRNA稳定性的必要元件。
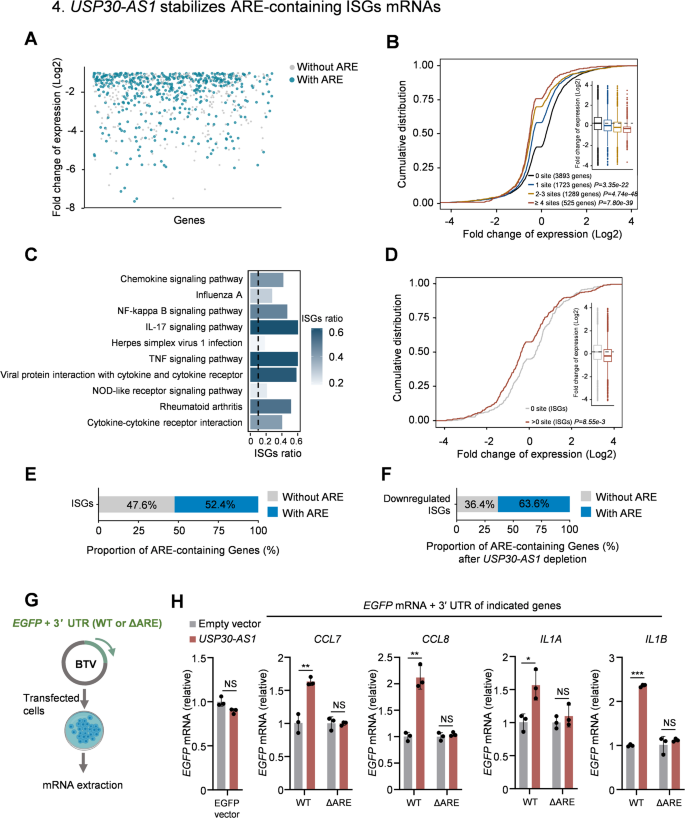
实验所用关键产品:Addgene的BTV报告基因质粒系统(货号84771)、Takara的PrimeScript反转录试剂盒(货号RR036A)。
3.5 USP30-AS1的免疫功能验证
该实验环节的核心目标是验证USP30-AS1对I型干扰素介导的抗病毒和炎症应答的调控功能。采用的实验方法包括:使用I型单纯疱疹病毒(HSV-1,DNA病毒,感染复数MOI=5)、水疱性口炎病毒(VSV,RNA病毒,感染复数MOI=1)感染对照、USP30-AS1敲除和回补细胞,使用鲱鱼睾丸DNA(HT-DNA,模拟胞质DNA刺激)、2"3"-环鸟苷酸-腺苷酸(cGAMP,STING通路激活剂)、I型干扰素-β处理细胞,通过实时荧光定量PCR检测干扰素刺激基因和IFNB的表达水平。实验结果显示,敲除USP30-AS1后,I型单纯疱疹病毒、水疱性口炎病毒感染诱导的干扰素刺激基因表达显著降低;鲱鱼睾丸DNA、2"3"-环鸟苷酸-腺苷酸、I型干扰素-β处理后,USP30-AS1敲除细胞中ISG15、CXCL10、IFIT1的mRNA水平较对照组降低2~4倍(n=3,P<0.001),回补USP30-AS1可恢复上述基因的表达,证实USP30-AS1是I型干扰素信号的广谱放大器。
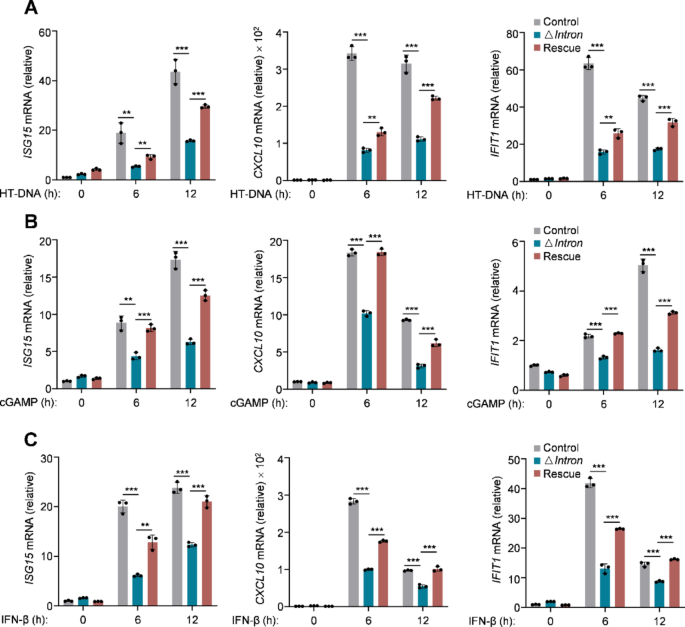
实验所用关键产品:InvivoGen的2"3"-环鸟苷酸-腺苷酸(货号tlrl-cga23)、PeproTech的重组人I型干扰素-β(货号300-02BC)。
3.6 USP30-AS1的临床相关性分析
该实验环节的核心目标是验证USP30-AS1在I型干扰素相关自身免疫病中的临床意义。采用的实验方法包括:检索基因表达综合数据库(GEO)中系统性红斑狼疮、类风湿关节炎、皮肌炎患者的转录组数据集,分析USP30-AS1的表达与疾病状态、严重程度、治疗响应的相关性,采用斯皮尔曼相关性分析验证其与靶基因CCL7、CCL8、IL1A、IL1B的表达相关性。实验结果显示,系统性红斑狼疮患者外周血单个核细胞、类风湿关节炎患者关节组织、皮肌炎患者皮肤/肌肉组织中的USP30-AS1表达较健康对照显著升高1.8~2.5倍(文献未明确提供该队列样本量,P<0.001);USP30-AS1的表达与系统性红斑狼疮的疾病严重程度正相关(斯皮尔曼相关系数ρ=0.42,文献未明确提供该队列样本量,P<0.001),未接受治疗的类风湿关节炎患者的USP30-AS1表达显著高于健康对照和接受治疗的患者(文献未明确提供该队列样本量,P<0.01);USP30-AS1的表达与靶基因CCL7、CCL8、IL1A、IL1B的表达呈显著正相关(相关系数ρ范围为0.38~0.51,文献未明确提供该队列样本量,均P<0.01),证实其可作为疾病活动度的生物标志物和潜在治疗靶点。
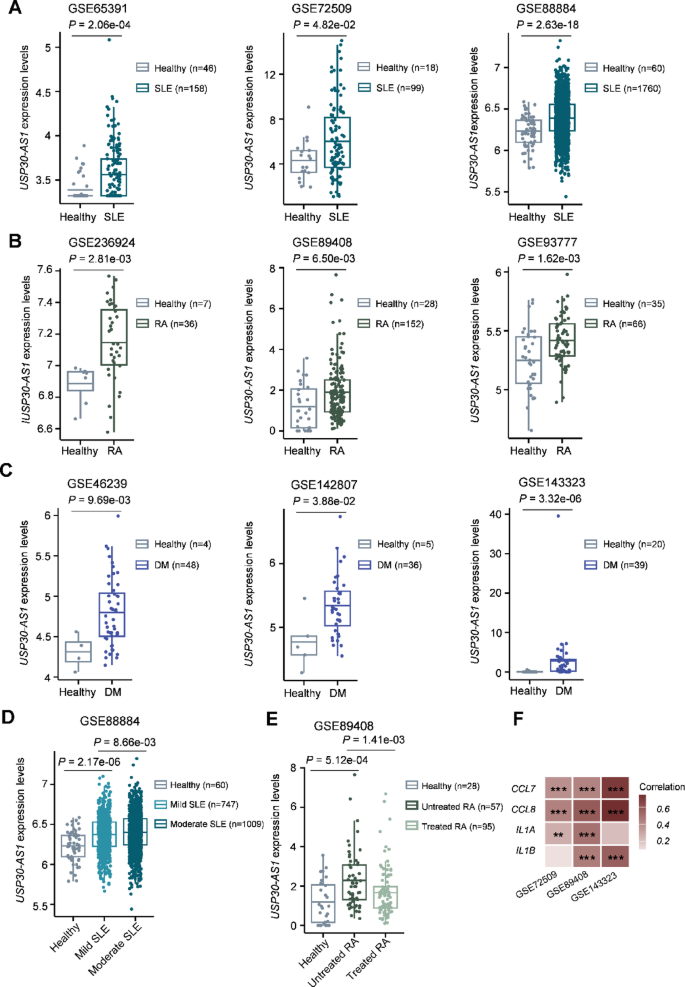
文献未提及该环节的具体实验产品,领域常规使用R语言进行临床转录组数据的统计分析与可视化。
4. Biomarker研究及发现成果
本研究涉及的生物标志物为长链非编码RNA USP30-AS1,属于细胞内表达的RNA类生物标志物,其筛选与验证逻辑完整:首先基于I型干扰素诱导的转录组数据筛选得到候选分子,随后通过细胞实验验证其调控I型干扰素信号的功能,最终通过多队列临床转录组数据验证其表达差异与疾病相关性。
该生物标志物的检测样本来源包括系统性红斑狼疮患者的外周血单个核细胞、类风湿关节炎患者的关节组织、皮肌炎患者的皮肤和肌肉组织,验证方法为转录组测序或基因芯片定量检测其表达量。统计学结果显示:系统性红斑狼疮患者外周血单个核细胞中USP30-AS1表达较健康对照升高1.8~2.5倍(文献未明确提供该队列样本量,P<0.001),类风湿关节炎患者关节组织中表达升高2.1倍(文献未明确提供该队列样本量,P<0.001),皮肌炎患者组织中表达升高1.9倍(文献未明确提供该队列样本量,P<0.001);其与系统性红斑狼疮疾病严重程度的斯皮尔曼相关系数为0.42(文献未明确提供该队列样本量,P<0.001),与靶基因表达的相关系数范围为0.38~0.51(文献未明确提供该队列样本量,均P<0.01)。
核心研究成果显示,USP30-AS1作为I型干扰素通路激活的特异性生物标志物,可用于评估系统性红斑狼疮、类风湿关节炎、皮肌炎的疾病活动度,同时是潜在的治疗靶点:抑制USP30-AS1的表达可下调过度激活的I型干扰素信号,缓解自身免疫病理反应,且USP30-AS1为人特异性长链非编码RNA,靶向治疗的脱靶风险较低。推测:后续可开发针对USP30-AS1的反义寡核苷酸或小干扰RNA药物,用于I型干扰素相关自身免疫病的治疗,同时可建立外周血USP30-AS1的定量检测方法,用于自身免疫病的早期诊断和疗效监测。