1. 领域背景与文献
文献英文标题:PINK1 regulates meiotic progression and mitochondrial homeostasis in murine oocytes;发表期刊:Cell & Bioscience;影响因子:8.7(2023年);研究领域:生殖生物学/卵母细胞衰老与质量调控。
生殖生物学领域中,卵母细胞质量是决定受精结局、妊娠成功率及子代健康的核心因素,高龄女性卵母细胞质量下降是当前辅助生殖临床面临的核心未解决难题。领域共识:卵母细胞成熟过程中核质同步成熟、线粒体稳态维持是保证减数分裂正常进行的必要前提,线粒体功能异常、氧化应激积累、纺锤体组装缺陷是高龄卵母细胞发育潜能降低的主要诱因。线粒体自噬作为线粒体质量控制的核心机制,既往研究已证实PTEN诱导激酶1(PINK1)-帕金蛋白(PRKN)通路是介导线粒体自噬的经典通路,但该通路在卵母细胞中的调控机制长期不明确,尤其是生理及衰老状态下卵母细胞线粒体自噬的激活调控及功能效应仍存在较大研究空白,现有研究尚未明确PINK1在卵母细胞减数分裂进程中的具体作用,也缺乏靶向调控线粒体自噬改善高龄卵母细胞质量的有效靶点。本研究针对这一核心问题展开,为卵母细胞质量调控及高龄生殖干预提供新的理论依据与潜在靶点。
2. 文献综述解析
本研究的文献综述按线粒体功能调控、线粒体自噬通路、RAB GTP酶功能三个维度展开梳理,系统总结了领域内现有研究的核心结论与局限性。
现有研究已证实卵母细胞线粒体数量、分布及膜电位状态与卵母细胞成熟质量高度相关,线粒体功能障碍会导致三磷酸腺苷(ATP)生成不足、活性氧(ROS)积累,进而引发纺锤体组装异常、减数分裂阻滞,该类研究已在多种模式生物中得到验证,为卵母细胞质量评估提供了多个潜在功能指标,但针对线粒体功能异常的上游调控机制解析不足。在线粒体自噬研究层面,现有研究明确了PINK1-PRKN通路是介导线粒体损伤后自噬激活的核心通路,该通路功能异常与帕金森病、神经退行性疾病等多种衰老相关疾病密切相关,研究方法体系成熟,结论可靠性高,但现有研究大多聚焦于体细胞层面,针对卵母细胞这一特殊生殖细胞的研究十分匮乏,且现有报道指出正常生理状态下卵母细胞无法有效激活线粒体自噬清除损伤线粒体,其背后的调控机制尚未明确。在RAB GTP酶研究层面,现有研究证实RAB8A作为小GTP酶家族成员,参与晚期内体-溶酶体融合、自噬体成熟等多个生物学过程,且已证实RAB8A敲低会导致小鼠卵母细胞纺锤体迁移缺陷、极体排出失败,但其是否参与卵母细胞中线粒体自噬的调控尚未见报道。本研究的创新点在于首次系统解析了PINK1在小鼠卵母细胞减数分裂进程中的功能,明确了RAB8A活性是PINK1介导线粒体自噬的关键调控因子,填补了领域内关于卵母细胞线粒体自噬调控机制的研究空白。
3. 研究思路总结与详细解析
本研究的核心目标是解析PINK1在小鼠卵母细胞减数分裂及线粒体稳态调控中的功能,明确高龄卵母细胞质量下降的分子机制,核心科学问题包括PINK1表达异常对卵母细胞减数分裂进程的影响、PINK1调控卵母细胞线粒体功能的下游机制、RAB8A在PINK1介导的线粒体自噬中的作用,整体技术路线遵循“表型发现-功能验证-机制解析-干预验证”的闭环逻辑。
3.1 衰老卵母细胞PINK1表达特征分析
实验目的:明确衰老与年轻小鼠卵母细胞中PINK1的表达差异,确定PINK1与卵母细胞衰老的相关性。方法细节:采用6-8周龄年轻小鼠、42-45周龄高龄小鼠的生发泡(GV)期卵母细胞为研究模型,分别采用蛋白免疫印迹、免疫荧光染色结合激光共聚焦显微镜检测PINK1的表达水平与定位特征,同时检测不同减数分裂阶段(GV、生发泡破裂、第一次减数分裂中期、第二次减数分裂中期)卵母细胞的PINK1表达水平。结果解读:蛋白免疫印迹结果显示高龄小鼠GV期卵母细胞PINK1蛋白表达水平显著高于年轻小鼠(对应图1A、1B),免疫荧光定量结果显示高龄卵母细胞PINK1荧光强度显著升高(n=32年轻卵母细胞,n=37高龄卵母细胞,P<0.05,对应图1C、1D),且PINK1在卵母细胞减数分裂各阶段表达水平稳定(对应图1E),证实PINK1表达上调与卵母细胞衰老显著相关。
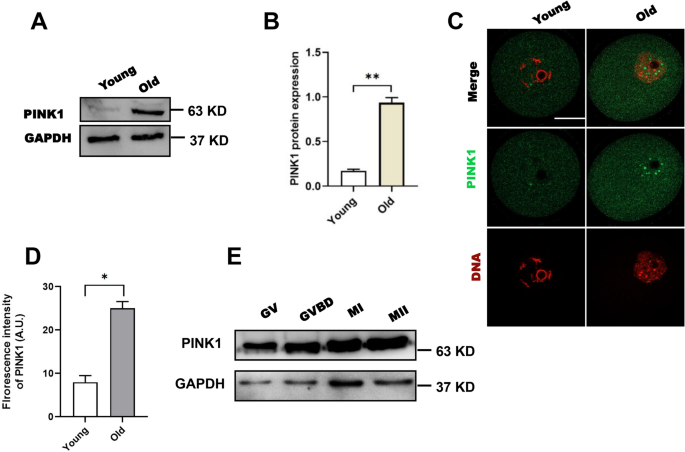
产品关联:实验所用关键产品包括Abcam的相关一抗、Proteintech的内参抗体,激光共聚焦显微镜为卡尔蔡司LSM 710型号。
3.2 PINK1过表达对卵母细胞减数分裂进程的影响分析
实验目的:验证PINK1表达上调是否会导致卵母细胞减数分裂异常。方法细节:构建Pink1过表达载体,体外转录获得mRNA后显微注射入年轻小鼠GV期卵母细胞,设立等体积磷酸盐缓冲液(PBS)注射的对照组,培养3h检测生发泡破裂率,培养14h检测第一极体排出率,采用蛋白免疫印迹验证过表达效率。结果解读:蛋白免疫印迹结果证实PINK1过表达效率良好(对应图2A),培养3h后对照组与Pink1过表达组生发泡破裂率无显著差异(对照组82.6±1.32%,n=144;过表达组81.6±0.74%,n=149,P>0.05,对应图2B、2C),培养14h后过表达组第一极体排出率仅为30.1±1.13%,显著低于对照组的80.9±1.13%(n=149,P<0.05,对应图2D),证实PINK1过表达会阻滞卵母细胞减数分裂进程。
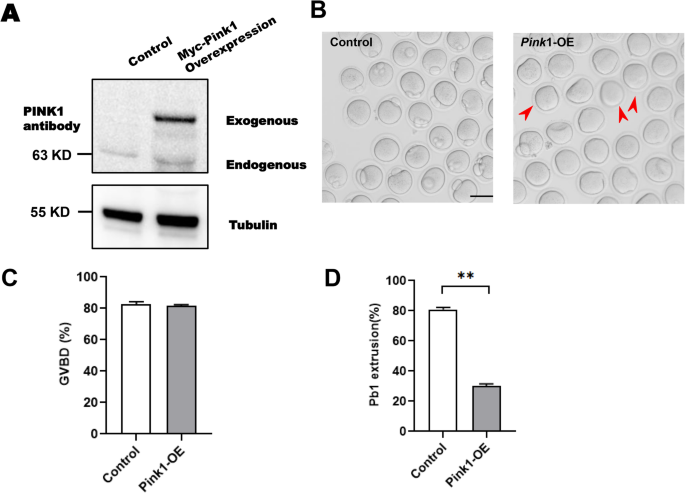
产品关联:体外转录采用Ambion的SP6 mMESSAGE mMACHINE试剂盒,卵母细胞培养采用Sigma的M16培养基。
3.3 PINK1过表达对卵母细胞线粒体功能的影响分析
实验目的:解析PINK1过表达导致减数分裂阻滞的下游机制,明确其对线粒体分布、膜电位及能量生成的影响。方法细节:采用MitoTracker Red标记线粒体,激光共聚焦显微镜观察线粒体分布模式;采用JC-1荧光探针检测线粒体膜电位;采用ATP检测试剂盒检测卵母细胞ATP含量。结果解读:正常GV期卵母细胞线粒体主要呈核周分布模式,Pink1过表达组线粒体聚集分布比例显著升高,核周分布比例显著降低(极化分布比例对照组82.6±1.32%,n=54;过表达组30.0±1.57%,n=49,P<0.05;聚集分布比例对照组9.53±1.02%,过表达组39.1±2.22%,P<0.05,对应图3A、3B);JC-1检测显示过表达组红/绿荧光比值为0.68±0.05,显著低于对照组的1.37±0.04(n=52,P<0.05,对应图3C、3D);过表达组ATP含量较对照组降低32%(对照组0.50±0.11,n=42;过表达组0.34±0.07,n=45,P<0.05,对应图3E),证实PINK1过表达会破坏线粒体分布、降低线粒体膜电位与能量生成能力。

产品关联:MitoTracker Red购自Molecular Probes,JC-1探针、ATP检测试剂盒购自碧云天生物技术有限公司。
3.4 PINK1过表达对卵母细胞氧化还原稳态与基因组稳定性的影响分析
实验目的:明确PINK1过表达是否会引发氧化应激与DNA损伤,进一步解析其导致卵母细胞质量下降的机制。方法细节:采用CM-H2DCFDA荧光探针检测细胞内ROS水平;采用γH2AX免疫荧光染色检测DNA损伤水平。结果解读:过表达组ROS荧光强度为23.0±3.04,显著高于对照组的7.14±2.12(n=65,P<0.05,对应图4A、4B);过表达组γH2AX荧光强度为29.9±2.04,显著高于对照组的12.4±2.07(n=35,P<0.05,对应图4C、4D),证实PINK1过表达会导致卵母细胞氧化应激积累、DNA损伤水平升高。

产品关联:CM-H2DCFDA探针购自Invitrogen,γH2AX抗体购自Abcam。
3.5 PINK1过表达对卵母细胞纺锤体组装与染色体排列的影响分析
实验目的:验证PINK1过表达是否会破坏减数分裂过程中纺锤体与染色体的正常结构。方法细节:采用异硫氰酸荧光素(FITC)标记的α-微管蛋白抗体染色显示纺锤体结构,碘化丙啶(PI)染色显示染色体,激光共聚焦显微镜观察第一次减数分裂中期卵母细胞的纺锤体形态与染色体排列情况。结果解读:对照组卵母细胞大多呈现典型的桶状纺锤体与排列整齐的染色体,纺锤体/染色体缺陷发生率仅为9.4±0.75%(n=86),而过表达组缺陷发生率为45.3±1.10%(n=74,P<0.05,对应图5A、5B),证实PINK1过表达会显著破坏纺锤体组装与染色体排列的稳定性。
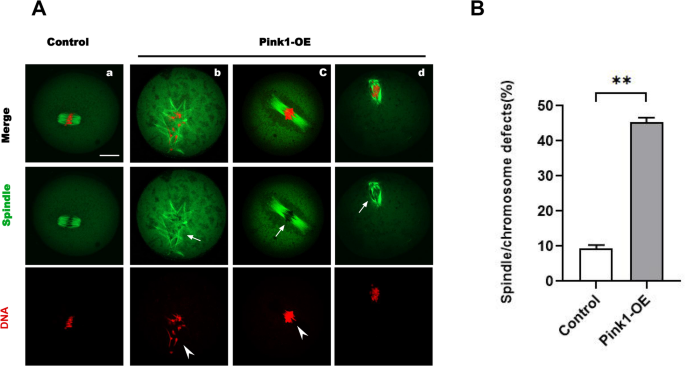
产品关联:FITC标记的α-微管蛋白抗体购自Sigma。
3.6 PINK1过表达对早期胚胎发育潜能的影响分析
实验目的:明确PINK1表达上调是否会影响后续早期胚胎的发育能力。方法细节:将Pink1 mRNA显微注射入小鼠受精卵,体外培养3.5天,检测2细胞期与囊胚期发育率;分别采用CM-H2DCFDA、γH2AX染色检测2细胞期胚胎的ROS水平与DNA损伤水平;采用末端脱氧核苷酸转移酶介导的dUTP缺口末端标记(TUNEL)试剂盒检测囊胚期细胞凋亡水平。结果解读:过表达组与对照组2细胞期发育率无显著差异(对照组81.2±0.33%,n=106;过表达组80.5±1.80%,n=94,P>0.05),但过表达组囊胚发育率仅为16.3±0.78%,显著低于对照组的40.2±1.17%(P<0.05,对应图6A、6B);过表达组2细胞期胚胎ROS水平、γH2AX荧光强度均显著高于对照组(ROS:对照组6.7±2.74%,n=15;过表达组19.5±3.17%,n=21,P<0.05;γH2AX:对照组19.6±1.80%,n=35;过表达组40.1±1.93%,n=41,P<0.05,对应图6C-6F);过表达组囊胚TUNEL阳性凋亡细胞比例为35.9±1.60%,显著高于对照组的8.6±0.71%(n=37,P<0.05,对应图6G、6H),证实PINK1过表达会显著降低早期胚胎的发育潜能。
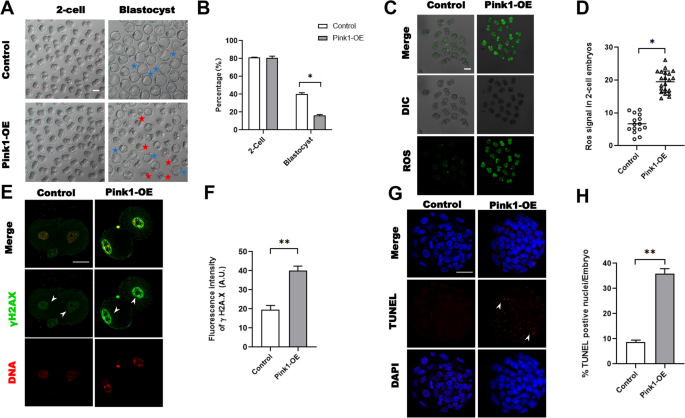
产品关联:TUNEL凋亡检测试剂盒购自碧云天生物技术有限公司。
3.7 PINK1介导线粒体自噬的机制解析
实验目的:明确PINK1过表达是否会激活卵母细胞线粒体自噬,以及下游的调控分子。方法细节:采用微管相关蛋白1轻链3(LC3)免疫荧光染色与蛋白免疫印迹检测自噬水平;采用实时荧光定量聚合酶链式反应(qRT-PCR)检测线粒体DNA(mtDNA)拷贝数;检测PINK1过表达及羰基氰化物间氯苯腙(CCCP)诱导线粒体损伤模型中PRKN、RAB8A的表达水平;分别将野生型、激活型(Q67L)、失活型(T22N)RAB8A mRNA注射入高龄卵母细胞,检测减数分裂表型、线粒体自噬水平的变化,采用透射电镜观察自噬体结构,采用MitoTracker与LysoTracker共定位检测线粒体与溶酶体的融合情况。结果解读:Pink1过表达组LC3聚集的自噬阳性细胞比例为31.7±2.24%,显著高于对照组的9.6±1.60%(n=36,P<0.05,对应图7A、7B),LC3II蛋白表达水平显著升高,mtDNA拷贝数较对照组降低30.5%(对照组88175.2±5645.62,n=27;过表达组61280±9338.36,n=35,P<0.05,对应图7C-7E),证实PINK1过表达会激活线粒体自噬。PINK1过表达组及CCCP损伤组的PRKN、RAB8A蛋白表达水平均显著升高(对应图8A-8G),证实RAB8A参与PINK1-PRKN介导的线粒体自噬通路。高龄卵母细胞中RAB8A蛋白表达水平显著低于年轻卵母细胞,仅激活型RAB8A-Q67L注射可显著恢复高龄卵母细胞的减数分裂能力,提高线粒体自噬体数量(高龄+Q67L组每细胞切片自噬体数量为2.13±0.21,显著高于高龄组的1.13±0.17,P<0.05,对应图9A-9E),促进线粒体与溶酶体的融合,证实RAB8A的三磷酸鸟苷(GTP)结合活性是PINK1介导的线粒体自噬正常进行的必要条件。
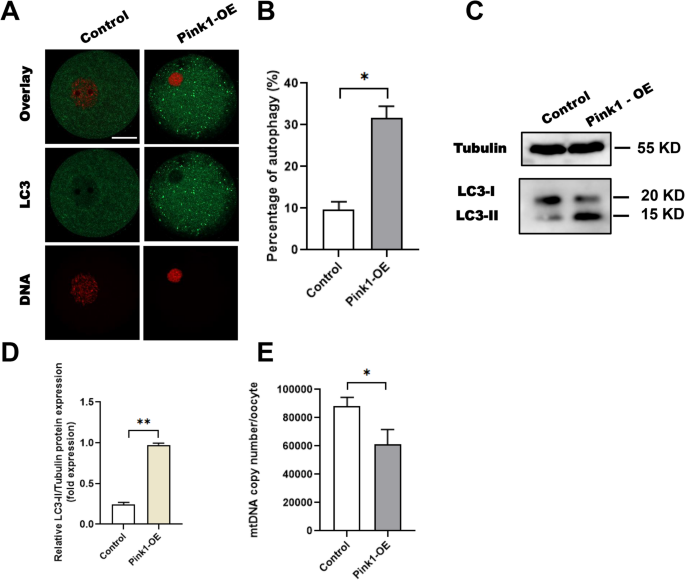

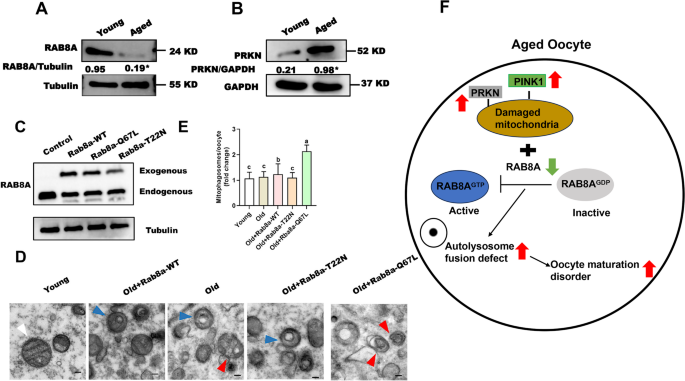
产品关联:RAB8A抗体购自Abcam,透射电子显微镜为日立H-7800型号。
4. Biomarker研究及发现成果
本研究共鉴定得到2个与卵母细胞质量及衰老相关的潜在生物标志物,分别为PINK1蛋白与激活型RAB8A,筛选与验证逻辑遵循“差异表达筛选→功能验证→机制解析→干预验证”的完整链条。
PINK1蛋白属于胞内蛋白类生物标志物,来源为卵母细胞胞质,验证方法包括蛋白免疫印迹、免疫荧光染色,研究显示高龄小鼠GV期卵母细胞PINK1表达水平较年轻小鼠显著升高,PINK1过表达可直接导致卵母细胞减数分裂阻滞、早期胚胎发育潜能下降,其表达水平与卵母细胞质量呈显著负相关,可作为卵母细胞衰老的潜在评估标志物。激活型RAB8A属于胞内功能蛋白类生物标志物,来源为卵母细胞胞质,验证方法包括蛋白免疫印迹、突变体功能回补实验,研究显示高龄卵母细胞中RAB8A蛋白表达水平显著降低,仅激活型(GTP结合态)RAB8A可有效恢复高龄卵母细胞的线粒体自噬功能与减数分裂能力,其活性水平是决定卵母细胞线粒体自噬正常进行的关键因素,可作为高龄卵母细胞质量改善的潜在干预靶点。
核心成果方面,本研究首次明确了PINK1在卵母细胞减数分裂进程中的负调控作用,首次证实RAB8A活性是PINK1-PRKN介导线粒体自噬的必要条件,为卵母细胞衰老的机制解析提供了新的理论依据,也为辅助生殖领域卵母细胞质量改善提供了新的潜在靶点。所有相关实验均重复3次以上,组间差异P<0.05,结果可靠性高。