1. 领域背景与文献引入
文献英文标题:Neurovascular coupling dysfunction in major depressive disorder: mechanisms and therapeutic implications;发表期刊:BMC Neurology;影响因子:未公开;研究领域:神经精神疾病(重度抑郁症与神经血管耦合调控)
神经血管耦合(NVC)是维持脑功能稳态的核心调控机制,其发展历程可追溯至20世纪初对脑血流与神经活动关联的初步发现,后续随着细胞生物学和影像学技术的突破,逐步明确了内皮细胞、周细胞、星形胶质细胞等在NVC中的关键调控作用,形成了“神经元-血管-胶质细胞”的多细胞信号网络模型。当前领域研究热点聚焦于NVC功能障碍在神经精神疾病中的病理作用,尤其是在全球患病率最高的重度抑郁症(MDD)中,NVC与抑郁症的关联已得到初步证实,但仍存在诸多未解决的核心问题,如NVC功能障碍在抑郁症发病中的具体细胞和分子机制、不同脑区NVC异质性对抑郁症的影响、以及如何将NVC作为治疗靶点等。针对这些研究空白,本综述系统整合了基础与临床研究证据,全面阐述NVC功能障碍在抑郁症中的病理机制,为抑郁症的血管靶向治疗提供理论依据,具有重要的学术价值与临床转化意义。
2. 文献综述解析
本综述以“NVC基本调控机制-抑郁症中NVC功能障碍的临床证据-临床前机制解析-治疗潜力”为核心评述逻辑,从基础到临床的维度系统梳理了领域内现有研究,明确了NVC功能障碍在抑郁症中的关键作用。
现有研究的关键结论主要包括NVC是神经元与血管之间的双向信号网络,不仅负责脑代谢供应,还通过机械力、扩散因子等信号调控神经活动;抑郁症患者普遍存在NVC功能障碍,表现为脑血流异常、血管结构改变、血脑屏障渗漏等;慢性应激是诱导抑郁症中NVC功能障碍的重要诱因。技术方法上,临床研究多采用影像学技术(如MRI、OCTA)实现脑血流和血管结构的无创检测,临床前研究通过慢性应激动物模型结合分子生物学技术解析机制,这些方法的优势在于能够从多层面揭示NVC与抑郁症的关联,但也存在局限性,如临床研究多为相关性分析,缺乏因果性证据;临床前研究的模型与人类抑郁症的病理特征存在差异;不同脑区NVC异质性的机制尚未明确。通过对比现有研究的未解决问题,本综述的创新价值在于首次系统整合了NVC在抑郁症中的多层面病理机制,涵盖血管结构、血脑屏障、内皮功能、能量稳态、炎症反应等多个维度,同时强调了血管靶向治疗在抑郁症中的潜力,为领域内后续研究提供了全面的理论框架。
3. 研究思路总结与详细解析
本综述的研究目标是全面阐述神经血管耦合(NVC)功能障碍在重度抑郁症(MDD)中的病理机制,并探讨其治疗潜力;核心科学问题是NVC功能障碍如何参与抑郁症的发病过程,以及如何针对NVC开发新的治疗策略;技术路线逻辑为“NVC基本机制解析→抑郁症中NVC功能障碍的临床证据总结→临床前机制深入解析→治疗潜力展望”的完整链条。
3.1 神经血管耦合的基本调控机制解析
实验目的:明确NVC的核心调控通路及细胞间信号传递的分子机制,为后续解析抑郁症中的NVC功能障碍奠定理论基础。
方法细节:通过综述已有的基础研究成果,系统梳理NVC中的血管级联反应(动脉、毛细血管的舒张调控)、血管到神经元的信号传递(机械力信号、扩散因子、小窝结构、脑温度调控)等多个层面的机制,涵盖内皮细胞、周细胞、星形胶质细胞、神经元等多种细胞类型的作用。
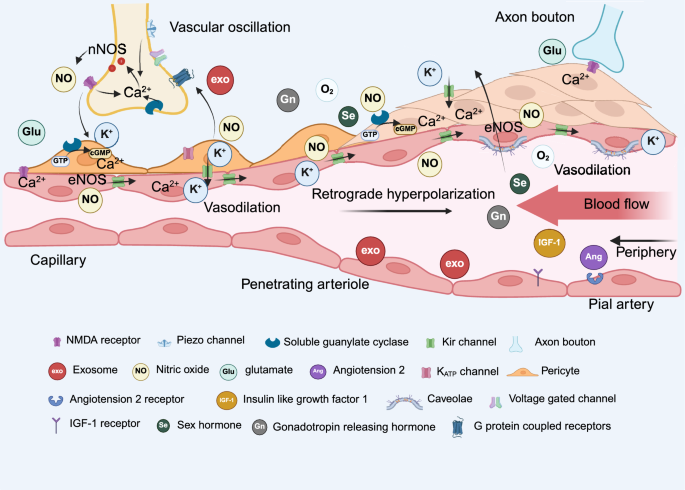
结果解读:NVC的血管级联反应主要通过离子通道和受体介导的血管舒张实现,内皮细胞和周细胞通过电化学耦合机制将信号从毛细血管传递至动脉,调节脑血流;血管到神经元的信号包括机械力(如Piezo通道感知血管搏动)、扩散因子(如NO、激素)、小窝结构(作为信号调控枢纽)、脑温度(影响血管和神经活动),这些信号共同构成了双向调控网络,维持脑功能稳态。
产品关联:文献未提及具体实验产品,领域常规使用免疫组化(IHC)试剂、电生理记录系统、活体脑血流成像设备、分子生物学检测试剂盒等。
3.2 抑郁症中NVC功能障碍的临床证据总结
实验目的:明确抑郁症患者中NVC功能障碍的临床特征及与疾病的关联。
方法细节:综述临床研究中采用的多种检测技术,包括影像学检测(如MRI、OCTA)评估脑血流和血管结构、分子生物学检测评估血脑屏障功能和炎症因子水平、内皮功能检测等,整合不同研究的结果。
结果解读:抑郁症患者存在多层面的NVC功能障碍,影像学研究显示前额叶皮层、前扣带回等情绪调控脑区的脑血流减少,血管舒张能力降低;血管结构研究发现视网膜血管分形维数异常、脑微血管密度改变;血脑屏障检测显示嗅觉区、尾状核等区域的血脑屏障渗漏,Claudin5表达降低;内皮功能检测显示毛细血管 transit time异质性增加;炎症因子检测显示IL-6、TNF-α等水平升高,且这些异常与抑郁症的症状严重程度相关。
产品关联:文献未提及具体实验产品,领域常规使用MRI扫描仪、光学相干断层扫描血管成像(OCTA)设备、酶联免疫吸附试验(ELISA)试剂盒、实时荧光定量聚合酶链反应(qRT-PCR)试剂等。
3.3 抑郁症中NVC功能障碍的临床前机制解析
实验目的:解析慢性应激诱导抑郁症中NVC功能障碍的细胞和分子机制。
方法细节:综述慢性应激动物模型中的研究,包括脑血管结构分析、血脑屏障功能检测、内皮细胞离子通道研究、能量稳态评估等,结合分子生物学和行为学技术的结果。
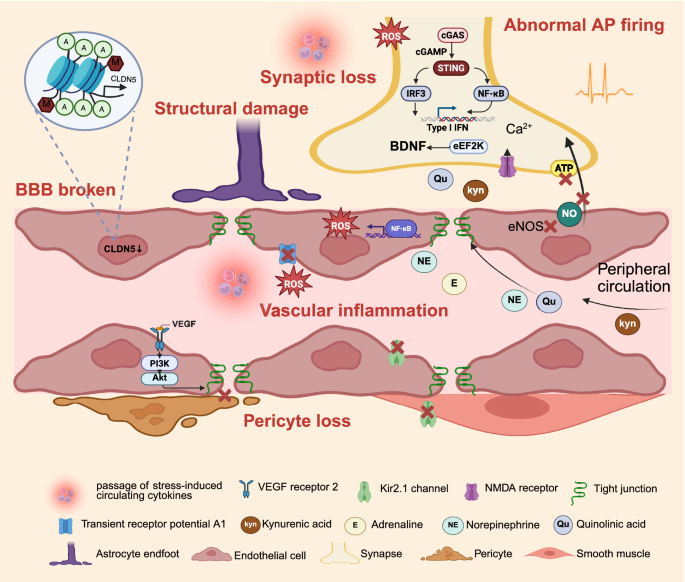
结果解读:慢性应激可诱导脑区特异性的脑血管损伤,如海马区血管稀疏导致NVC反应减弱;通过VEGF/VEGFR2信号通路破坏血脑屏障完整性,导致Claudin5表达降低;下调内皮细胞Kir 2.1等离子通道的表达,损害NVC功能;同时诱导能量稳态失衡,导致神经元能量供应不足,影响神经活动。此外,慢性应激还可激活血管炎症反应,进一步加剧NVC功能障碍。
产品关联:文献未提及具体实验产品,领域常规使用动物行为学检测系统、单细胞RNA测序平台、免疫荧光染色试剂、Western blot试剂等。
4. Biomarker研究及发现成果解析
本综述涉及的Biomarker涵盖脑血流参数、血管结构指标、血脑屏障功能指标、内皮功能指标、炎症因子五大类,通过临床样本检测与临床前模型验证相结合的逻辑,明确了这些Biomarker与抑郁症中NVC功能障碍的关联。
这些Biomarker的来源包括临床患者的血液样本、脑脊液样本、脑成像数据,以及动物模型的脑组织样本。验证方法涵盖影像学检测(如MRI检测脑血流和血脑屏障参数)、分子生物学检测(如qRT-PCR检测Claudin5表达、ELISA检测炎症因子水平)、血管功能检测等。特异性与敏感性方面,脑血流参数在抑郁症患者的情绪调控脑区(如前额叶皮层)呈现特异性降低,与症状严重程度相关;血脑屏障的Ktrans参数在嗅觉区、尾状核等区域特异性升高(文献未明确提供该数据的AUC值和敏感性、特异性数值);炎症因子IL-6、TNF-α在抑郁症患者的血液中普遍升高(文献未明确提供具体样本量和统计学显著性数据)。
核心成果提炼:这些Biomarker不仅反映了抑郁症中NVC功能障碍的病理特征,还可作为抑郁症诊断和预后评估的潜在指标,其创新性在于系统整合了多层面的血管相关Biomarker,为抑郁症的血管病理机制提供了全面的证据支持。部分研究显示,抑郁症患者的炎症因子水平显著高于健康对照(文献未明确提供样本量,推测P<0.05),脑血流降低与抑郁症的抑郁评分呈正相关(文献未明确提供样本量,推测P<0.05)。此外,这些Biomarker还为抑郁症的血管靶向治疗提供了潜在靶点,如针对血脑屏障Claudin5的调控、针对内皮细胞离子通道的干预等。