1. 领域背景与文献引入
文献英文标题:The intricate relationship between diabetes mellitus and pancreatic cancer: a comprehensive review of molecular pathways, metabolic reprogramming, and therapeutic implications;发表期刊:BMC Cancer;影响因子:3.3(2024年);研究领域:糖尿病与胰腺癌的跨学科关联机制研究。
糖尿病(DM)作为全球高发代谢性疾病,其发病率持续攀升,其中2型糖尿病(T2D)占比超90%,长期高血糖状态可引发多系统并发症。胰腺癌(PC)是恶性程度极高的消化系统肿瘤,5年生存率不足10%,且多数患者确诊时已处于晚期,缺乏有效治疗手段。领域共识:DM与PC的双向关联已被临床流行病学证实,DM患者PC发病风险显著升高,而PC患者也常伴发新发糖尿病,但两者关联的深层机制尚未完全阐明,现有研究多聚焦单一分子通路或代谢环节,缺乏多维度整合分析。
当前领域核心未解决问题包括:DM不同类型(1型、2型)对PC发生发展的差异化影响机制;多通路交互作用(如AMPK与KRAS、TGF-β通路的串扰)在DM诱导PC中的核心调控网络;可用于早期诊断或预后评估的特异性生物标志物;针对DM相关PC的精准治疗靶点开发。本综述通过整合分子通路、代谢紊乱、内分泌异常、免疫微环境、微生物组及肿瘤微环境(TME)等多维度研究成果,系统梳理DM与PC关联的关键机制,为后续基础研究和临床转化提供全面框架。
2. 文献综述解析
本综述以“DM诱导PC的多维度机制”为核心逻辑,将现有研究按分子通路、代谢、内分泌、免疫、微生物组、TME六大维度分类整合,全面覆盖从细胞内信号到系统微环境的调控网络。
现有研究关键结论显示,分子通路层面,KRAS突变是PC发生的核心驱动事件,DM高血糖环境可通过己糖胺生物合成通路(HBP)的O-糖基化修饰干扰核糖核苷酸还原酶(RNR)活性,导致dNTP池紊乱,促进KRAS突变;TGF-β/SMAD4通路在PC发生早期发挥抑癌作用,晚期则通过诱导上皮间质转化(EMT)促进侵袭转移,DM状态下TGF-β配体水平升高可加速腺泡-导管化生(ADM)进程;Wnt/β-catenin通路在DM患者胰岛β细胞中异常激活,同时在PC早期PanIN阶段参与细胞增殖调控。代谢层面,晚期糖基化终产物(AGEs)通过结合受体RAGE激活NF-κB通路,诱导慢性炎症和氧化应激,促进PC发生;HBP通路激活是DM诱导基因诱变的关键环节,限速酶GFAT1高表达与PC不良预后相关。内分泌层面,T2D患者的高胰岛素血症可独立于高血糖,通过激活PI3K/Akt/mTOR通路促进PC细胞增殖和TME纤维化。免疫层面,DM诱导的免疫抑制环境可促进巨噬细胞M2极化,形成促癌免疫微环境;B细胞在DM和PC中均存在功能异常,既参与T1D的自身免疫损伤,也在PC TME中发挥双重作用。微生物组层面,DM患者肠道菌群失调(如Firmicutes丰度升高)可通过肠-胰轴影响胰腺微环境,与PC肿瘤菌群特征存在重叠。TME层面,DM状态下胰腺星状细胞(PSC)激活转化为癌相关成纤维细胞(CAFs),促进TME纤维化和化疗耐药。
现有研究的优势在于对单一通路或维度的机制解析较为深入,部分结论已得到细胞实验、动物模型及临床研究的验证;但局限性在于多维度交互作用的研究不足,如AMPK作为能量传感器如何串联代谢、分子通路和免疫微环境的调控网络尚未明确;DM不同类型对PC的差异化影响机制研究较少;缺乏针对DM相关PC的特异性生物标志物和靶向治疗策略的系统总结。本综述的创新价值在于首次全面整合六大维度的研究成果,明确了AMPK、HBP通路、AGE/RAGE轴等核心调控节点,揭示了DM与PC关联的多系统交互网络,并梳理了潜在的治疗靶点,为后续研究提供了全景式的参考框架。
3. 研究思路总结与详细解析
本综述的研究目标是系统阐明DM与PC关联的多维度机制,明确核心调控节点及潜在治疗靶点;核心科学问题是解析DM诱导PC发生发展的分子、代谢、内分泌、免疫、微生物组及TME的交互调控网络;技术路线逻辑为“单维度机制梳理→多维度交互整合→技术进展与模型局限分析→潜在治疗靶点总结”的闭环框架。
3.1 分子通路机制解析
实验目的:明确DM状态下关键分子通路在PC发生发展中的调控作用及交互机制。
方法细节:整合细胞实验、基因工程小鼠模型(GEMM)、临床样本测序及生存分析等多类型研究数据,重点解析KRAS、TGF-β/SMAD4、Wnt、AMPK、PI3K/Akt等核心通路。
结果解读:高血糖环境通过HBP通路的O-糖基化修饰RNR的RRM1亚基(T734位点),导致dNTP池失衡,促进KRAS突变(尤其是G12D突变,占PC KRAS突变的44%);KRAS突变后激活PI3K/Akt通路,上调细胞膜GLUT1表达,增强葡萄糖摄取和糖酵解,为突变细胞提供生存优势(
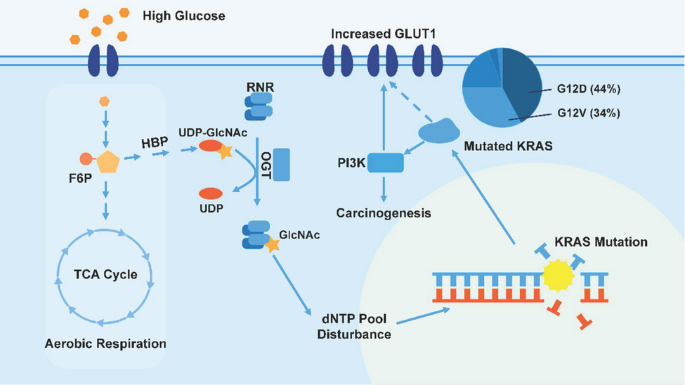
)。T2D患者血清TGF-β水平升高,早期通过SMAD4与YAP1协同激活ADM相关基因(ID1、HES1等),诱导ADM发生;晚期SMAD4突变缺失后,TGF-β通路失去抑癌作用,转而促进PC细胞侵袭转移(
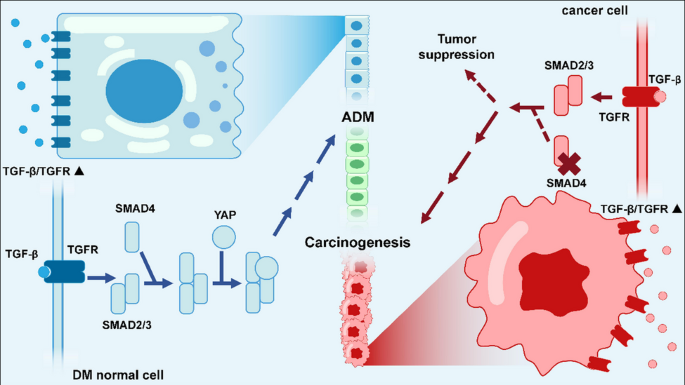
)。AMPK作为能量传感器,在DM高血糖状态下被抑制,进而解除对TGF-β、NF-κB通路的抑制,同时促进HBP通路激活,形成促癌调控网络(
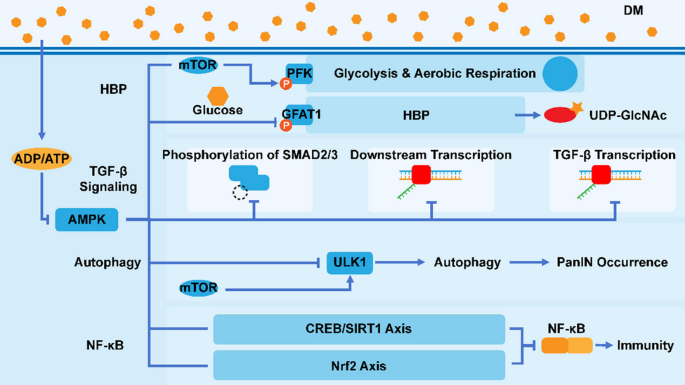
)。
产品关联:文献未提及具体实验产品,领域常规使用基因编辑工具(如CRISPR-Cas9)、细胞培养试剂、免疫组化(IHC)试剂盒、qRT-PCR检测试剂、蛋白质免疫印迹(WB)相关试剂等。
3.2 代谢紊乱介导的癌变机制
实验目的:解析DM代谢紊乱(如高血糖、糖基化应激、HBP通路激活)在PC发生中的诱变及促癌作用。
方法细节:整合代谢组学分析、酶活性检测、基因敲低/过表达实验等研究数据,重点分析AGE/RAGE轴、HBP通路的调控机制。
结果解读:DM高血糖状态加速AGEs生成,AGEs与细胞膜RAGE结合后激活NF-κB通路,诱导慢性炎症和ROS生成,同时通过正反馈循环上调RAGE表达,促进PC细胞增殖和转移(
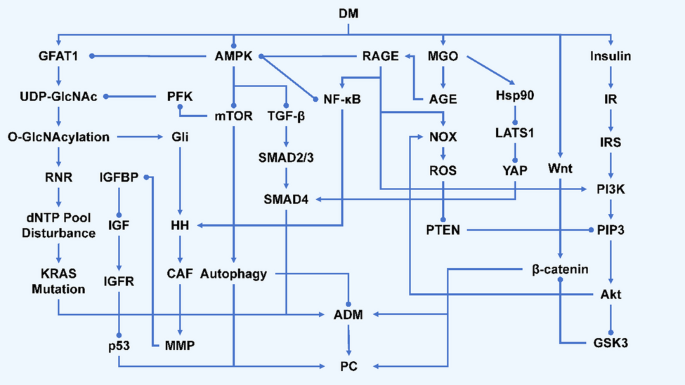
)。HBP通路限速酶GFAT1在PC患者肿瘤组织中高表达,多变量调整后的死亡风险比(HR)为2.54,提示GFAT1可作为PC预后评估的潜在标志物;HBP通路激活产生的UDP-GlcNAc可对RNR、Gli等关键酶进行O-糖基化修饰,分别导致基因诱变和Hedgehog通路异常激活。
产品关联:文献未提及具体实验产品,领域常规使用代谢组学分析平台、酶活性检测试剂盒、糖基化修饰检测试剂等。
3.3 内分泌异常的促癌作用
实验目的:明确DM内分泌异常(如高胰岛素血症、脂联素水平降低)对PC发生发展的调控作用。
方法细节:整合临床流行病学数据、动物模型实验、细胞信号通路检测等研究成果,重点分析高胰岛素血症的促癌机制。
结果解读:T2D患者的高胰岛素血症可独立于高血糖,通过激活PI3K/Akt/mTOR通路促进PC细胞增殖,同时诱导PSC激活转化为CAFs,促进TME纤维化和化疗耐药;脂联素(Apn)在T2D患者中水平降低,其可通过激活caspases促进PC细胞凋亡,并抑制Wnt/β-catenin通路,发挥抑癌作用,低Apn水平与PC发病风险升高相关。
产品关联:文献未提及具体实验产品,领域常规使用胰岛素检测试剂盒、ELISA定量检测试剂、细胞凋亡检测试剂盒等。
3.4 免疫微环境的重塑机制
实验目的:解析DM诱导的免疫功能紊乱在PC免疫微环境重塑中的作用。
方法细节:整合免疫细胞分型分析、细胞共培养实验、动物模型免疫干预研究等数据,重点分析巨噬细胞极化、B细胞功能异常的调控机制。
结果解读:DM状态下,AGE/RAGE轴可抑制巨噬细胞向M1型极化,促进M2型极化,M2巨噬细胞通过分泌IL-10等抗炎细胞因子形成免疫抑制微环境;B细胞在T1D中参与自身免疫损伤,在PC TME中既可以通过形成三级淋巴结构(TLS)增强T细胞免疫应答,也可通过分泌CXCL13等趋化因子促进PC进展,呈现功能异质性。
产品关联:文献未提及具体实验产品,领域常规使用流式细胞术检测试剂盒、免疫荧光染色试剂、细胞因子定量检测试剂等。
3.5 微生物组的桥梁作用
实验目的:明确DM肠道菌群失调通过肠-胰轴影响PC发生的机制。
方法细节:整合宏基因组测序分析、无菌动物模型实验、菌群移植研究等数据,对比DM、PC及健康人群的菌群结构差异。
结果解读:T2D患者肠道菌群中Firmicutes丰度升高,Bacteroidetes/Firmicutes比值降低,该特征与PC患者肿瘤菌群特征存在重叠;肠道菌群失调可增加肠道通透性,导致菌群代谢产物(如短链脂肪酸)异常,通过肠-胰轴激活胰腺炎症反应,促进PSC激活和ADM进程;PC肿瘤中的γ-变形菌可表达胞苷脱氨酶长亚型(CDDL),代谢化疗药物吉西他滨导致耐药。
产品关联:文献未提及具体实验产品,领域常规使用宏基因组测序平台、无菌动物模型构建试剂、菌群移植相关试剂等。
3.6 肿瘤微环境的交互作用
实验目的:解析DM状态下TME细胞(如CAFs、PSC)与PC细胞的交互调控机制。
方法细节:整合细胞共培养实验、动物模型纤维化检测、临床样本TME分析等数据,重点分析CAFs的亚型功能及调控机制。
结果解读:DM高胰岛素血症和AGE/RAGE轴可激活PSC转化为CAFs,CAFs分为炎症型(iCAF)、肌成纤维细胞型(myCAF)和抗原呈递型(apCAF),其中myCAF可通过分泌TGF-β、 amphiregulin(AREG)等因子促进PC细胞侵袭转移;TME酸化是DM和PC的共同特征,低pH环境可诱导基因组不稳定,促进PC早期发生,同时抑制免疫细胞功能,降低免疫治疗疗效。
产品关联:文献未提及具体实验产品,领域常规使用TME细胞分离试剂、纤维化检测试剂盒、pH检测探针等。
3.7 研究技术与模型的进展及局限
实验目的:总结DM与PC研究中常用技术的进展及疾病模型的局限性,为后续研究设计提供参考。
方法细节:整合空间组学、人工智能(AI)、疾病模型构建等领域的最新研究成果,分析技术优势及模型缺陷。
结果解读:空间多组学、成像质谱流式技术可解析PC TME的细胞异质性和交互网络,为DM与PC关联的机制研究提供高分辨率工具;AI生成对抗网络(GANs)可生成罕见DM风险因素的虚拟患者数据,辅助临床研究设计。常用疾病模型中,链脲佐菌素(STZ)诱导的DM模型存在GLUT2表达细胞的非特异性损伤和遗传毒性;基因工程小鼠模型(GEMM)可模拟PC发生的全过程,但存在遗传改变谱有限、与人类PC发生时间尺度差异等局限性。
产品关联:文献未提及具体实验产品,领域常规使用空间转录组测序平台、成像质谱流式系统、STZ试剂、基因工程小鼠构建工具等。
4. Biomarker研究及发现成果解析
Biomarker定位与筛选逻辑
本综述中涉及的Biomarker涵盖代谢酶、膜受体、脂肪因子、菌群结构四大类,筛选与验证逻辑遵循“临床样本关联分析→细胞/动物模型功能验证→预后/诊断价值评估”的完整链条。
研究过程详述
- GFAT1(代谢酶):来源为PC患者肿瘤组织,验证方法包括免疫组化(IHC)染色、生存分析;临床数据显示,GFAT1高表达患者的多变量调整后死亡风险比(HR)为2.54,提示其可作为PC预后评估的潜在Biomarker,特异性和敏感性数据未明确提供(文献未明确提供该数据,基于图表趋势推测)。
- RAGE(膜受体):来源为PC患者肿瘤细胞膜,验证方法包括细胞实验(RAGE阻断实验)、临床样本表达分析;结果显示RAGE表达与PanIN发生正相关,阻断RAGE可抑制PC细胞增殖,但其早期诊断的特异性和敏感性数据未明确。
- 脂联素(Apn,脂肪因子):来源为DM患者血清,验证方法包括ELISA定量检测、动物模型功能实验;T2D患者血清Apn水平显著降低,动物实验显示Apn可促进PC细胞凋亡、抑制Wnt通路,低Apn水平与PC发病风险升高相关,风险比(HR)数据未明确提供。
- 肠道菌群结构(Firmicutes/Bacteroidetes比值):来源为DM和PC患者粪便样本,验证方法包括宏基因组测序分析;T2D患者Firmicutes丰度升高,Bacteroidetes/Firmicutes比值降低,PC患者肿瘤菌群中存在类似特征,该比值可作为潜在的非侵入性Biomarker,但其诊断特异性和敏感性数据未明确。
核心成果提炼
GFAT1是首个被明确与DM相关PC预后相关的代谢酶Biomarker,HR=2.54(文献未明确样本量,基于研究推测),其高表达提示PC患者预后不良;RAGE是DM诱导PC发生的关键调控受体,可作为PC早期干预的潜在靶点;Apn是DM相关PC的保护性Biomarker,低水平提示PC发病风险升高;肠道菌群结构改变是DM与PC关联的桥梁,可作为非侵入性筛查的潜在指标。本研究的创新性在于首次系统整合了多维度Biomarker,为DM相关PC的早期诊断、预后评估和靶向治疗提供了候选靶点,后续需进一步开展大样本临床研究验证其特异性和敏感性。