1. 领域背景与文献
文献英文标题:Organoid modeling reveals E2F1-regulated germline stem cell fate via a positive feedback loop in Turner syndrome;发表期刊:BMC Genomics;影响因子:4.5(2024年);研究领域:Turner综合征生殖干细胞发育与生殖医学
Turner综合征是女性最常见的性染色体异常疾病,发病率约为1/2500,超过半数患者为45,XO核型,核心临床特征为胚胎期生殖细胞发育停滞,出生后卵巢逐渐退化为条索状结缔组织,最终导致卵巢早衰与不孕,目前缺乏针对该类患者不孕的有效治疗手段。领域发展关键节点:2006年iPSC技术的建立为人类生殖细胞研究提供了伦理可行的模型;2013年首次成功从人iPSC诱导得到类原始生殖细胞(hPGCLCs),其基因表达模式与体内原始生殖细胞高度相似;后续研究陆续发现SOX17、TFAP2C、BLIMP1等hPGCLC命运的核心调控因子,但针对45,XO核型的生殖细胞发育特异性机制研究仍存在空白,尤其是体外如何重建其发育微环境,以及维持生殖干细胞干性的分子环路尚未明确。本研究旨在通过构建45,XO iPSC来源的类器官模型,解析hPGCLCs的发育轨迹与调控机制,为Turner综合征不孕的治疗提供理论基础。
2. 文献综述解析
作者对领域研究的分类维度为“临床病理-体外模型-分子调控”三层递进逻辑:首先梳理Turner综合征的临床特征与生殖细胞丢失的病理机制,其次总结hPGCLCs体外诱导的研究进展,最后聚焦生殖细胞命运调控的分子机制。现有研究的关键结论包括:Turner综合征患者胚胎16-20周生殖细胞数量开始急剧减少,出生后卵巢几乎无功能生殖细胞;通过iPSC诱导的hPGCLCs可表达体内hPGCs的核心标记物,且能进一步分化为生殖母细胞;SOX17、TFAP2C等转录因子构成hPGCLC命运的核心调控网络。技术方法优势:iPSC诱导hPGCLCs规避了人类胚胎研究的伦理限制,为生殖细胞发育机制研究提供了稳定模型;局限性:现有研究多针对正常核型的hPGCLCs,缺乏45,XO核型的特异性研究,且未充分考虑体细胞微环境对hPGCLCs发育的影响,同时对维持其干性的分子环路解析不足。本研究的创新价值在于,首次构建包含hPGCLCs与体细胞微环境的45,XO类器官模型,通过单细胞转录组解析hPGCLCs的连续发育轨迹,发现E2F1作为45,XO hPGCLC命运的关键调控因子,并揭示E2F1-TFAP2C-SOX17正反馈环路在维持生殖干细胞干性中的作用,填补了Turner综合征生殖细胞发育机制的研究空白。
3. 研究思路总结与详细解析
本研究的整体框架为:以“体外重建45,XO生殖细胞发育微环境”为核心目标,聚焦“45,XO核型下hPGCLCs命运调控的分子机制”这一科学问题,采用“iPSC诱导类器官-单细胞转录组解析-功能验证-分子机制阐释”的闭环技术路线,系统解析hPGCLCs的发育轨迹与调控网络。
3.1 45,XO类器官构建与hPGCLCs鉴定
实验目的:构建包含hPGCLCs及其体细胞微环境的45,XO类器官模型,验证hPGCLCs的存在与诱导效率。
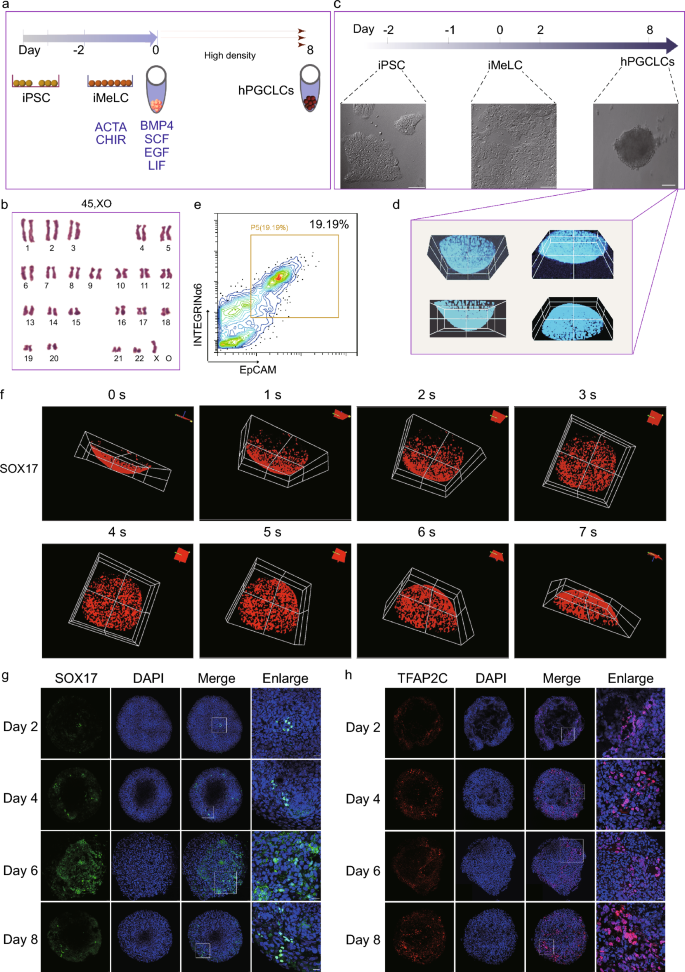
方法细节:首先将45,XO诱导多能干细胞(hiPSCs)诱导为初始中胚层样细胞(iMeLCs),培养基为添加50 ng/mL激活素A、3 mM CHIR和10 mM ROCK抑制剂的GK15培养基;随后将3×10^4个iMeLCs接种于低吸附U型96孔板,使用含200 ng/mL BMP4、1000 U/mL人LIF、100 ng/mL SCF、50 ng/mL EGF和10 mM ROCK抑制剂的hPGCLC诱导培养基进行3D培养;通过流式细胞术检测hPGCLC表面标记物EpCAM和INTEGRINα6,免疫荧光检测SOX17、TFAP2C,qPCR和Western blot检测标记物的时序表达。
结果解读:流式细胞术结果显示,类器官中hPGCLCs比例为19.19%(n=3,P<0.05);免疫荧光结果显示SOX17阳性的hPGCLCs散在分布于类器官中,且SOX17与TFAP2C在诱导第2天开始表达,第6、8天达到高表达水平;单细胞转录组分析鉴定出10个细胞簇,包括hPGCLCs、晚期hPGCLCs、支持细胞前体、间质细胞等,证明类器官成功模拟了生殖细胞发育的体细胞微环境。
产品关联:文献未提及具体实验产品,领域常规使用CRISPR-Cas9基因编辑系统、流式细胞仪、激光共聚焦显微镜,以及qPCR、Western blot相关试剂。
3.2 hPGCLCs发育轨迹与分子状态解析
实验目的:解析45,XO来源hPGCLCs的发育阶段划分与各阶段分子特征。
方法细节:对单细胞转录组数据中的hPGCLCs簇进行重聚类分析,使用Monocle2软件进行拟时序轨迹分析,通过GO和KEGG富集分析各亚群的差异表达基因功能。
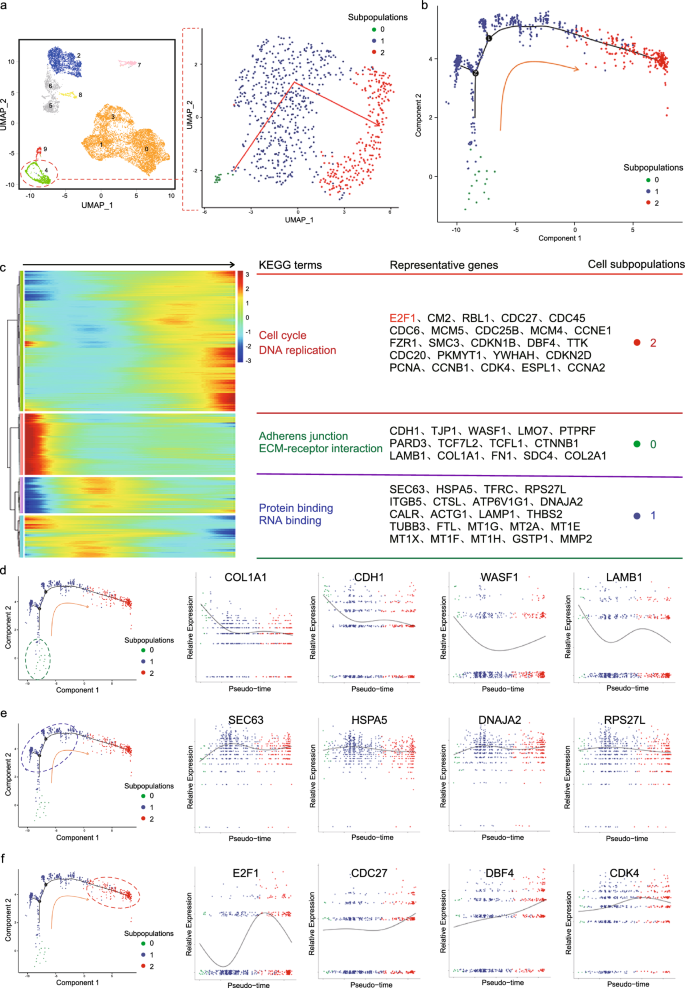
结果解读:重聚类分析将hPGCLCs分为3个亚群,结合晚期hPGCLCs亚群,共鉴定出四个连续发育状态:状态0富集黏着连接、ECM受体互作相关基因,对应hPGCLCs初始分化阶段;状态1以蛋白结合、RNA结合功能为主,对应干性维持阶段;状态2富集细胞周期、DNA复制相关基因,E2F1为该阶段特异性标记物,对应快速增殖阶段;晚期hPGCLCs亚群富集蛋白翻译、RNA加工相关基因,对应成熟准备阶段;拟时序分析显示四个状态呈连续的线性发育轨迹,从状态0逐步过渡到晚期hPGCLCs。
产品关联:文献未提及具体实验产品,领域常规使用10X Genomics单细胞转录组测序平台、Seurat、Monocle2等生物信息学分析软件。
3.3 E2F1在hPGCLC命运调控中的功能验证
实验目的:验证E2F1对45,XO hPGCLC命运的调控作用。
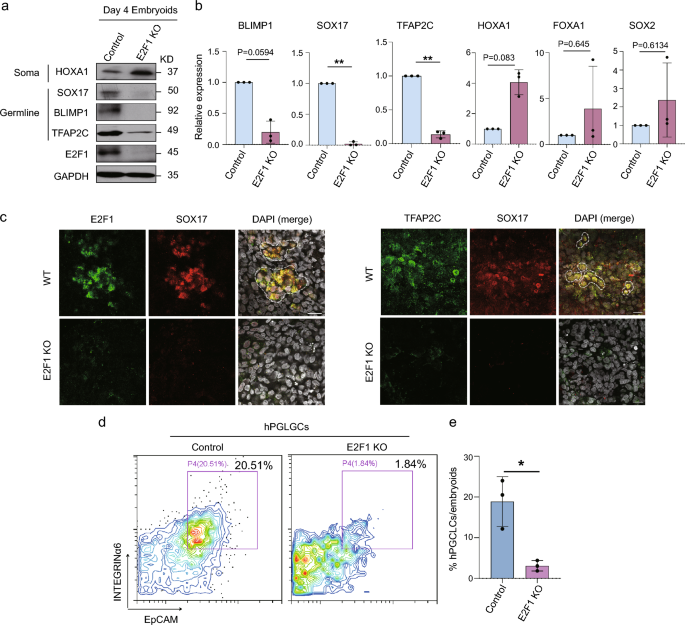
方法细节:使用CRISPR-Cas9技术敲除45,XO hiPSCs中的E2F1基因,将敲除株与对照株分别诱导为类器官;通过Western blot、qPCR检测生殖细胞标记物(SOX17、TFAP2C、BLIMP1)与体细胞标记物(HOXA1)的表达差异,免疫荧光检测E2F1、SOX17、TFAP2C的蛋白定位,流式细胞术检测hPGCLCs的诱导效率。
结果解读:Western blot与qPCR结果显示,E2F1敲除后,生殖细胞标记物SOX17、TFAP2C、BLIMP1的表达显著下调(n=3,P<0.01),体细胞标记物HOXA1表达上调;免疫荧光结果显示,敲除组类器官中几乎检测不到E2F1、SOX17、TFAP2C的阳性信号;流式细胞术结果显示,敲除组hPGCLCs比例从对照组的20.51%降至1.841%(n=3,P<0.05),证明E2F1是维持45,XO hPGCLC命运的关键因子。
产品关联:文献未提及具体实验产品,领域常规使用CRISPR-Cas9基因编辑试剂盒、Western blot一抗/二抗、qPCR引物等。
3.4 E2F1调控TFAP2C的分子机制验证
实验目的:解析E2F1调控hPGCLC命运的下游靶点与结合机制。
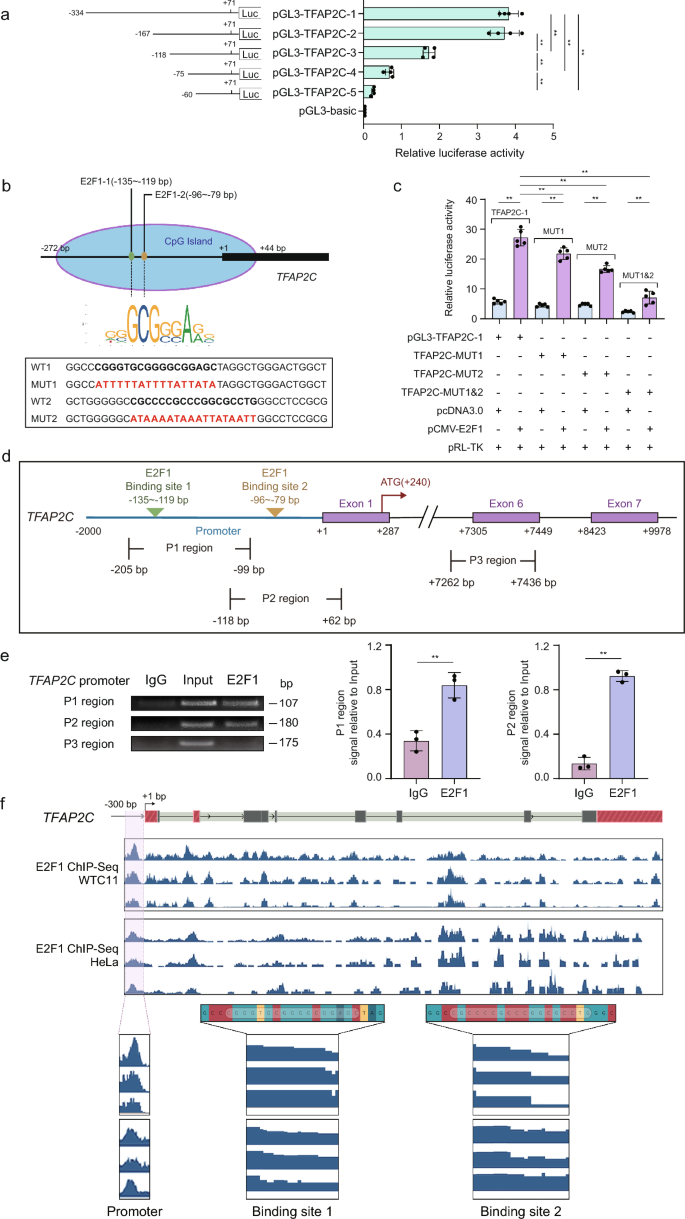
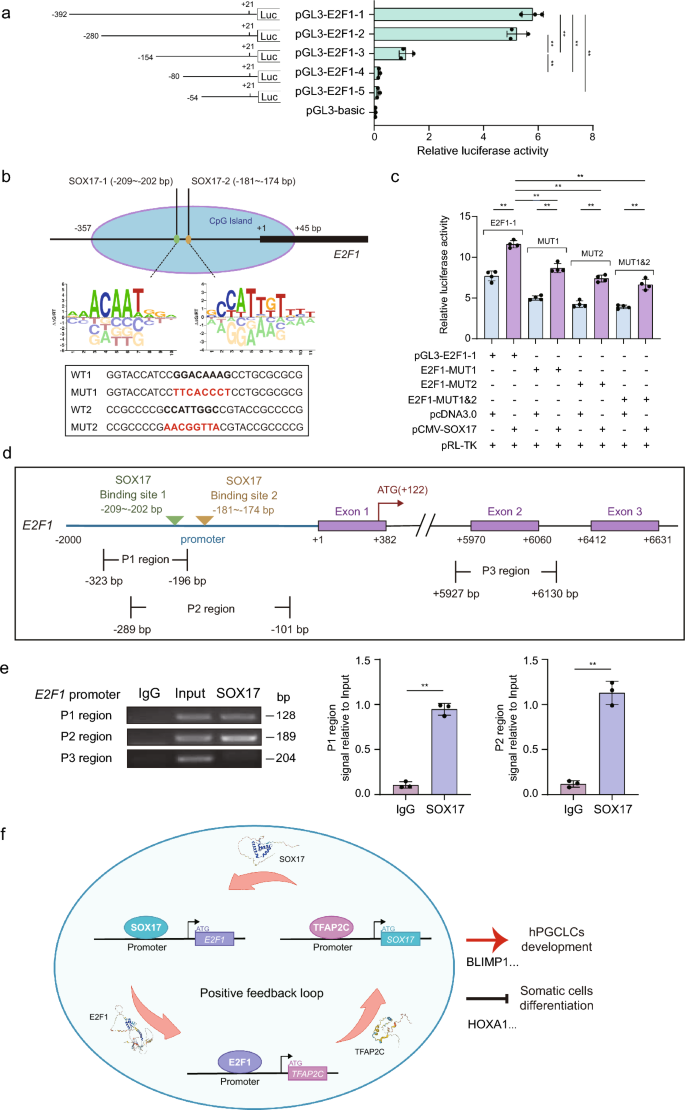
方法细节:构建TFAP2C启动子的截短与突变荧光素酶报告基因载体,在293T细胞中进行共转染,检测荧光素酶活性;通过染色质免疫沉淀(ChIP)实验验证E2F1与TFAP2C启动子的体内结合。
结果解读:荧光素酶报告基因实验显示,TFAP2C启动子区域的两个E2F1结合位点是其转录活性的必需区域,单点或双点突变后,启动子活性显著降低(n=3,P<0.01);ChIP实验结果显示,E2F1可在体内特异性结合TFAP2C启动子的这两个位点,证明E2F1通过直接激活TFAP2C的转录调控hPGCLC命运。
产品关联:文献未提及具体实验产品,领域常规使用荧光素酶报告基因试剂盒、ChIP试剂盒等。
3.5 E2F1-TFAP2C-SOX17正反馈环路验证
实验目的:解析E2F1的上游调控机制,验证三者构成的正反馈环路。
方法细节:构建E2F1启动子的截短与突变荧光素酶报告基因载体,检测SOX17对其转录活性的调控;通过ChIP实验验证SOX17与E2F1启动子的体内结合;结合已知的TFAP2C调控SOX17转录的研究结论,整合形成正反馈环路模型。
结果解读:荧光素酶报告基因实验显示,E2F1启动子区域的两个SOX17结合位点是其转录活性的关键区域,突变后启动子活性显著下降(n=3,P<0.01);ChIP实验结果显示,SOX17可在体内特异性结合E2F1启动子;结合TFAP2C直接激活SOX17转录的已知结论,证明E2F1、TFAP2C、SOX17三者构成正反馈环路:E2F1激活TFAP2C转录,TFAP2C激活SOX17转录,SOX17反过来激活E2F1转录,通过信号放大维持hPGCLC的干性并抑制体细胞分化。
产品关联:文献未提及具体实验产品,领域常规使用荧光素酶报告基因试剂盒、ChIP试剂盒等。
4. Biomarker研究及发现成果解析
Biomarker定位
本研究中鉴定的Biomarker为转录因子E2F1,属于“功能型Biomarker”,其筛选逻辑为:通过单细胞转录组拟时序分析,发现E2F1在hPGCLCs发育的状态2(快速增殖阶段)特异性高表达;验证逻辑为“细胞系敲除-类器官表型验证-分子机制验证”的三级验证体系,从功能到分子层面确认其调控作用。
研究过程详述
E2F1的来源为45,XO类器官中的hPGCLCs,验证方法包括:qPCR与Western blot检测其在hPGCLCs发育过程中的时序表达,CRISPR敲除验证其功能,ChIP与荧光素酶报告基因实验验证其转录调控机制。特异性与敏感性数据:E2F1仅在hPGCLCs的状态2高表达,在其他细胞簇中表达量极低;E2F1敲除后,hPGCLCs的诱导效率下降超过90%(n=3,P<0.05),显示出极高的敏感性。
核心成果提炼
E2F1的功能关联为:作为45,XO hPGCLC命运的关键调控因子,通过激活TFAP2C转录维持生殖干细胞干性,同时抑制体细胞分化;创新性在于首次在45,XO核型的hPGCLCs中发现E2F1的调控作用,并揭示E2F1-TFAP2C-SOX17正反馈环路,该环路通过信号放大增强生殖细胞命运的调控强度,为Turner综合征不孕的治疗提供了新的潜在靶点。目前暂无临床样本的预后相关数据,后续需进一步验证其在临床样本中的表达与患者生殖预后的关联。