1. 领域背景与文献引入
文献英文标题:Porcine rotavirus hijacks host METTL3-mediated m6A methylation to regulate its replication and host immune response;发表期刊:BMC Veterinary Research;影响因子:2.8(2023年JCR);研究领域:动物病毒学(猪轮状病毒感染与表观遗传调控)
N6-甲基腺嘌呤(m⁶A)是真核生物mRNA中最丰富的内部修饰,其动态调控由甲基转移酶(如METTL3、METTL14)、去甲基化酶(如FTO、ALKBH5)及识别蛋白(如YTHDF1/2/3)共同介导,参与免疫应答、细胞分化等多种核心生物学过程,是当前表观遗传学与病毒学交叉领域的研究热点。领域共识:病毒已进化出多种策略劫持宿主m⁶A修饰系统,通过调控自身RNA的稳定性、翻译效率实现免疫逃逸与复制增强,而宿主也可通过调节m⁶A水平调控免疫相关基因表达,建立抗病毒防御机制。目前,多种人类病毒(如肠道病毒71型、寨卡病毒)与m⁶A的相互作用机制已被阐明,但作为仔猪病毒性腹泻主要病原体的猪轮状病毒(PoRV),其与宿主m⁶A修饰系统的双向调控机制尚未明确,缺乏针对猪肠道上皮细胞中m⁶A修饰调控病毒复制与免疫应答的系统性研究,这一空白限制了猪轮状病毒新型防控策略的开发。本文针对该核心问题,通过多组学与分子生物学技术,首次揭示了PoRV与宿主m⁶A系统的相互作用机制,为猪病毒性腹泻的防控提供了新靶点。
2. 文献综述解析
本文综述部分以“病毒-宿主m⁶A修饰双向调控”为核心逻辑,按“病毒利用宿主m⁶A系统促进自身复制”“宿主通过m⁶A修饰调控免疫应答抵抗感染”两个维度对现有研究进行分类梳理。现有研究表明,多种病毒的基因组存在m⁶A修饰,其调控作用具有双向性:肠道病毒71型感染可上调宿主m⁶A甲基转移酶表达,促进自身复制;而寨卡病毒的m⁶A修饰则被YTHDF2识别并介导RNA降解,抑制病毒复制。同时,部分病毒可通过劫持宿主m⁶A系统实现免疫逃逸,如人巨细胞病毒通过自身RNA的m⁶A修饰模拟宿主RNA,逃避RIG-I的识别。宿主层面,研究发现降低m⁶A修饰水平可稳定干扰素调节因子7(IRF7)的mRNA,增强I型干扰素表达以抑制轮状病毒感染。现有研究的局限性在于,针对猪源病毒与宿主m⁶A相互作用的研究较为匮乏,尤其是PoRV感染猪肠道上皮细胞过程中,m⁶A修饰对病毒复制与宿主免疫应答的调控机制尚未阐明。本文的创新点在于首次揭示PoRV通过结构蛋白VP6劫持宿主METTL3介导自身基因组m⁶A甲基化,并阐明宿主通过降低m⁶A水平稳定IFI44L和IRF2 mRNA以抑制病毒复制的双向调控机制,填补了猪轮状病毒表观遗传调控领域的研究空白。
3. 研究思路总结与详细解析
本研究的整体目标是阐明PoRV与宿主m⁶A修饰系统的相互作用机制,核心科学问题包括PoRV如何利用宿主m⁶A系统促进自身复制,以及宿主如何通过m⁶A调控免疫应答抵抗感染,技术路线遵循“病毒感染模型构建→m⁶A修饰谱分析→关键分子互作验证→功能机制验证→免疫调控通路解析”的闭环逻辑,通过多组学技术与分子生物学实验的结合,系统解析了双向调控的分子机制。
3.1 细胞模型构建与病毒感染验证
实验目的是建立PoRV感染的猪肠道上皮细胞模型并验证感染效率。方法细节为使用IPEC-J2猪肠道上皮细胞,以感染复数(MOI)=0.1的PoRV NJ2012株(G9P[7]亚型)感染细胞,感染后6小时通过实时荧光定量聚合酶链反应(qRT-PCR)检测病毒Nsp5基因拷贝数,通过免疫印迹(WB)检测不同时间点病毒结构蛋白VP6的表达水平。结果解读显示,感染6小时后病毒Nsp5基因拷贝数显著升高(n=3,P<0.001),VP6蛋白表达随感染时间延长逐渐上调,证明PoRV感染细胞模型构建成功。实验所用关键产品:Gibco的DMEM/F12培养基(货号11320033)、胎牛血清(货号A3160801),Accurate Biotechnology的RNA提取试剂(货号AG21102)。
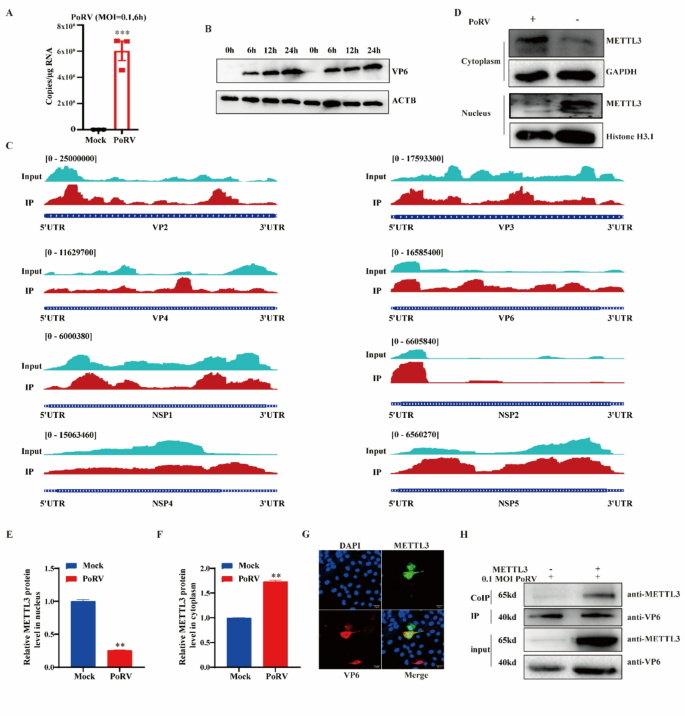
3.2 猪轮状病毒基因组m⁶A修饰谱分析
实验目的是鉴定PoRV基因组上的m⁶A修饰位点。方法细节为通过蔗糖密度梯度离心纯化PoRV颗粒,采用m⁶A甲基化RNA免疫沉淀结合高通量测序(MeRIP-seq)技术分析病毒基因组的m⁶A修饰谱,每个实验组设置3个生物学重复。结果解读显示,在PoRV基因组上共鉴定到17个m⁶A修饰峰,主要分布于VP2、VP3、VP4、VP6等结构蛋白基因及NSP1、NSP2、NSP5等非结构蛋白基因的5’-UTR和3’-UTR区域,提示PoRV基因组存在特异性m⁶A修饰。实验所用关键产品:NEB的m⁶A抗体(货号E1610S),Illumina HiSeq4000测序平台。

3.3 METTL3与VP6的互作验证
实验目的是验证PoRV是否通过结构蛋白VP6劫持宿主METTL3介导自身m⁶A甲基化。方法细节为通过核质分离试剂盒提取感染后IPEC-J2细胞的核蛋白与胞质蛋白,采用WB检测METTL3的亚细胞定位;通过免疫荧光(IF)染色观察VP6与METTL3的共定位情况;通过免疫共沉淀(Co-IP)实验验证两者的直接相互作用。结果解读显示,PoRV感染后,细胞核内METTL3表达显著降低,细胞质内METTL3表达显著升高(n=3,P<0.01);免疫荧光染色显示VP6与METTL3在细胞质中大量共定位;Co-IP实验证实VP6可与METTL3直接结合,提示PoRV通过VP6劫持METTL3至细胞质以介导自身基因组的m⁶A修饰。实验所用关键产品:Beyotime的核质分离试剂盒(货号P0027)、RIPA裂解液(货号P0013B)。

3.4 m⁶A修饰对PoRV复制的功能验证
实验目的是验证METTL3和YTHDF2对PoRV复制的调控作用。方法细节为构建靶向Mettl3和Ythdf2的小干扰RNA(siRNA)及过表达质粒,转染IPEC-J2细胞24小时后感染PoRV,感染12小时后通过WB检测VP6蛋白表达,通过TCID₅₀法检测病毒滴度,通过qRT-PCR检测Nsp5基因拷贝数。结果解读显示,沉默Mettl3或Ythdf2后,VP6蛋白表达显著降低(n=3,P<0.01),病毒滴度和Nsp5基因拷贝数显著减少;过表达Mettl3或Ythdf2后,VP6蛋白表达显著上调(n=3,P<0.001),病毒滴度显著升高,证明METTL3和YTHDF2可促进PoRV复制。文献未提及具体实验产品,领域常规使用siRNA转染试剂、qRT-PCR引物等。
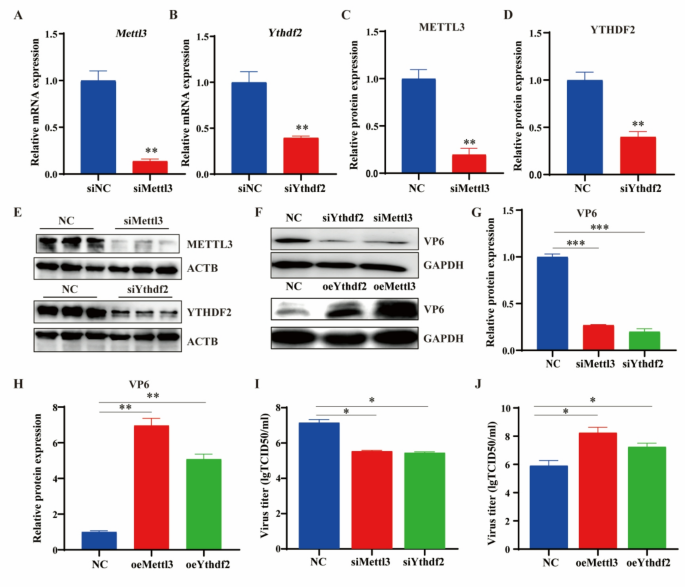
3.5 宿主免疫应答与m⁶A修饰的关联分析
实验目的是解析PoRV感染对宿主免疫应答和m⁶A修饰的影响。方法细节为通过RNA-seq分析感染后IPEC-J2细胞的基因表达变化,通过MeRIP-seq分析宿主m⁶A修饰谱变化,通过qRT-PCR和ELISA检测IFN-β、TNF-α等免疫因子的表达水平。结果解读显示,PoRV感染后239个基因上调、113个基因下调,差异基因富集于病毒防御应答、I型干扰素分泌等生物学通路;感染12小时后,IFN-β、TNF-α的表达显著升高(n=3,P<0.05);宿主总m⁶A水平显著降低(n=3,P<0.001),m⁶A修饰峰数量从33858个减少至30843个,且约8.76%的峰为感染后新增的去 novo修饰位点。实验所用关键产品:Epigentek的m⁶A RNA甲基化定量试剂盒(货号P-9005),Accurate Biotechnology的PrimeScript @ RT试剂盒(货号AG11728)。
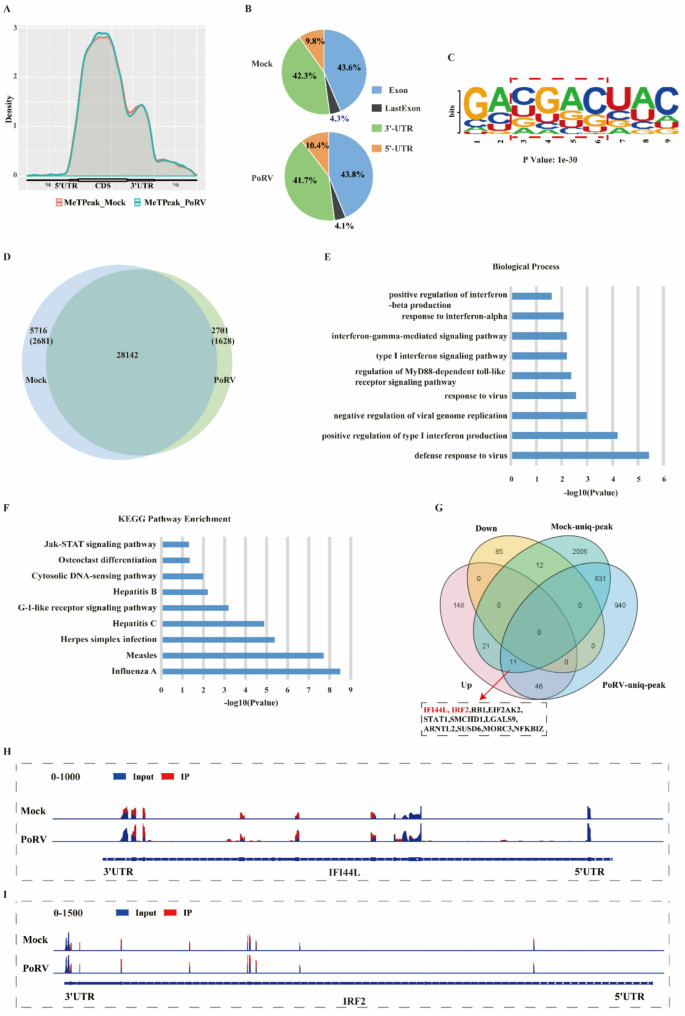
3.6 IFI44L和IRF2的功能机制验证
实验目的是阐明m⁶A修饰调控IFI44L和IRF2的分子机制及对病毒复制的影响。方法细节为沉默Mettl3或Ythdf2后,通过qRT-PCR和WB检测IFI44L和IRF2的表达水平;通过放线菌素D处理抑制转录,检测IFI44L和IRF2的mRNA稳定性;通过RNA免疫沉淀(RIP)-qPCR验证YTHDF2与IFI44L、IRF2 mRNA的结合;同时沉默或过表达IFI44L和IRF2,检测PoRV的复制情况。结果解读显示,沉默Mettl3或Ythdf2后,IFI44L和IRF2的mRNA表达分别上调约2.5倍和2.2倍(n=3,P<0.01),蛋白表达显著升高;mRNA稳定性实验显示,沉默Mettl3或Ythdf2可显著延长IFI44L和IRF2的mRNA半衰期;RIP-qPCR证实YTHDF2可直接结合IFI44L和IRF2的mRNA;沉默IFI44L或IRF2后,VP6蛋白表达显著上调(n=3,P<0.001),病毒滴度升高约3倍;过表达则相反,抑制病毒复制。实验所用关键产品:Beyotime的BCA蛋白定量试剂盒(货号P0010)。
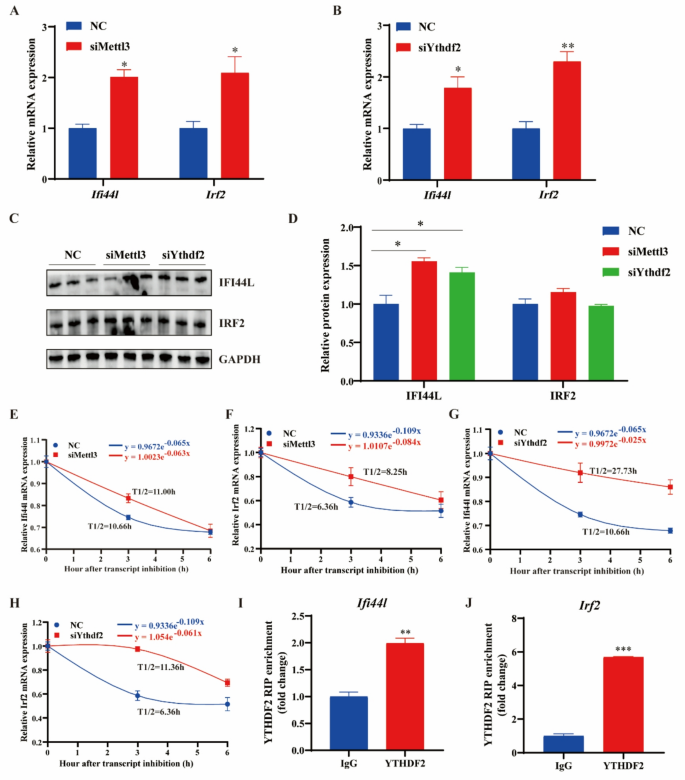
4. Biomarker研究及发现成果解析
Biomarker定位与筛选逻辑
本文涉及两类Biomarker:一是病毒层面的PoRV基因组m⁶A修饰位点,二是宿主层面的IFI44L和IRF2蛋白。病毒m⁶A修饰位点的筛选逻辑为“MeRIP-seq全基因组扫描→亚细胞定位验证→分子互作验证”;宿主IFI44L和IRF2的筛选逻辑为“RNA-seq与MeRIP-seq联合分析筛选差异表达且受m⁶A调控的基因→mRNA稳定性实验验证→功能实验验证抗病毒作用”,形成完整的筛选与验证链条。
研究过程详述
病毒m⁶A修饰位点来源于蔗糖密度梯度离心纯化的PoRV颗粒,通过MeRIP-seq鉴定得到17个修饰峰,验证方法包括免疫印迹检测METTL3的亚细胞定位、免疫荧光观察VP6与METTL3的共定位、免疫共沉淀验证两者的相互作用,未提及特异性与敏感性数据。宿主IFI44L和IRF2来源于IPEC-J2细胞的mRNA,验证方法包括qRT-PCR和WB检测表达水平、mRNA稳定性实验检测半衰期、RIP-qPCR验证YTHDF2的结合;特异性与敏感性数据显示,沉默Mettl3后,IFI44L mRNA表达上调约2.5倍(n=3,P<0.01),IRF2 mRNA表达上调约2.2倍(n=3,P<0.01);沉默IFI44L后,病毒滴度升高约3倍(n=3,P<0.001)。
核心成果提炼
IFI44L和IRF2作为宿主抗病毒Biomarker,其功能与m⁶A修饰直接相关:m⁶A甲基转移酶METTL3和识别蛋白YTHDF2可介导IFI44L和IRF2的mRNA降解,降低其表达水平;而宿主通过降低m⁶A修饰水平,可稳定IFI44L和IRF2的mRNA,增强其表达以抑制PoRV复制。创新性在于首次揭示IFI44L和IRF2作为m⁶A调控的抗病毒效应分子,在猪轮状病毒感染中的作用机制;统计学结果显示,所有实验数据均设置3个生物学重复,差异具有统计学显著性(P<0.05、P<0.01或P<0.001)。该成果为猪轮状病毒的防控提供了新的潜在靶点,同时拓展了m⁶A修饰在宿主抗病毒免疫应答中的调控机制研究。