1. 领域背景与文献
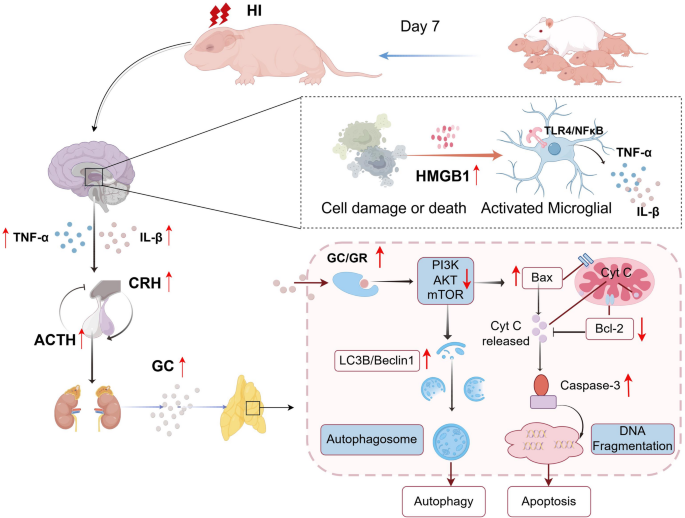
文献英文标题:Hypoxic–ischemic encephalopathy induces thymic atrophy via HMGB1/TLR4/NF-κB-mediated HPA axis activation in neonatal rats;发表期刊:BMC Pediatrics;影响因子:3.1(2023年);研究领域:新生儿神经免疫学、缺氧缺血性脑病(HIE)。
缺氧缺血性脑病是新生儿急性死亡和慢性神经系统疾病的首要原因,传统研究长期聚焦于神经元损伤机制与神经保护策略的开发,而HIE对新生儿免疫系统发育的调控作用及潜在机制尚未得到系统阐明。领域共识:中枢神经系统与免疫系统存在精密的双向调控网络,成人缺血性脑损伤可通过下丘脑-垂体-肾上腺(HPA)轴诱导脾脏、胸腺等外周免疫器官的淋巴细胞丢失,进而引发全身免疫抑制,但新生儿期中枢神经系统与免疫系统均未发育成熟,其脑损伤与免疫调控的相互作用机制与成人存在显著差异,这是当前领域未解决的核心问题。针对这一研究空白,本研究以新生大鼠HIE模型为研究对象,旨在揭示HIE诱导胸腺萎缩的神经-内分泌-免疫调控机制,为HIE患儿的综合治疗策略提供理论基础与潜在靶点。
2. 文献综述解析
作者对领域现有研究的分类维度涵盖成人与新生儿缺血性脑损伤的免疫调控差异、HPA轴在脑损伤后免疫抑制中的作用、神经炎症与HPA轴激活的关联三个核心方向。现有研究显示,成人缺血性脑损伤可通过HPA轴激活诱导外周免疫器官的淋巴细胞凋亡,导致免疫功能抑制;临床研究发现新生儿HIE患儿存在淋巴细胞亚群分布异常,且免疫功能紊乱会进一步加重脑损伤,但HIE影响新生儿胸腺发育的具体细胞与分子机制尚未被阐明。现有研究的局限性在于,缺乏针对新生儿期脑损伤-免疫调控轴的机制研究,尤其是神经炎症如何通过HPA轴调控胸腺细胞凋亡与自噬的关键通路未被揭示。本研究的创新点在于,首次在新生大鼠HIE模型中证实高迁移率族蛋白B1(HMGB1)/ Toll样受体4(TLR4)/核因子κB(NF-κB)信号通路介导的下丘脑神经炎症可激活HPA轴,进而诱导胸腺细胞凋亡与自噬,最终导致胸腺萎缩,填补了新生儿HIE免疫损伤机制的研究空白,为HIE的多靶点干预提供了新的思路。
3. 研究思路总结与详细解析
本研究的核心目标是明确HIE诱导新生大鼠胸腺萎缩的分子机制,核心科学问题是HIE如何通过神经-内分泌-免疫轴调控胸腺细胞的存活与功能,技术路线遵循“模型构建→表型观察→机制探索→干预验证”的闭环逻辑:首先构建稳定的新生大鼠HIE模型,观察脑损伤与胸腺萎缩的关联;随后检测胸腺细胞凋亡与自噬的变化及相关信号通路的激活状态;接着分析HPA轴的功能变化及上游神经炎症机制;最后通过特异性抑制剂干预验证调控通路的因果关系。
3.1 新生大鼠HIE模型构建与脑-胸腺关联验证
实验目的:构建稳定的新生大鼠HIE模型,明确脑损伤与胸腺萎缩的时序性关联及调控趋势。
方法细节:采用经典Rice-Vannucci法,选取7日龄SPF级Sprague Dawley(SD)大鼠,经异氟烷麻醉后分离并结扎右侧颈总动脉,恢复1.5小时后置于氧浓度为7%的低氧箱中处理1小时,假手术组仅分离颈总动脉不进行结扎。在造模后1、3、7、14、21天五个时间点,分别检测大鼠脑指数、胸腺指数及胸腺CD3+T细胞比例,并进行相关性分析。
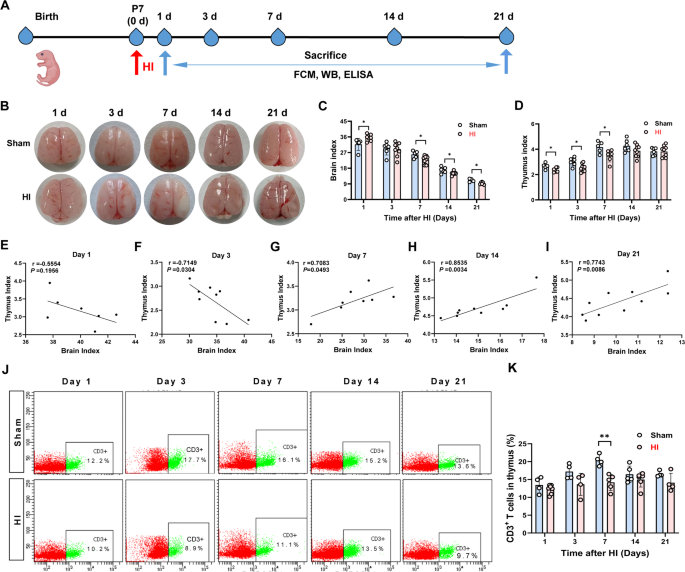
结果解读:HI组大鼠造模后第1天出现明显脑水肿,脑指数显著升高(n=7-10,P<0.05),第7天起出现脑萎缩液化,脑指数逐渐降低;胸腺指数在造模后1、3、7天显著降低(n=7-10,P<0.05),第7天CD3+T细胞比例较假手术组显著下降(n=4-6,P<0.05);相关性分析显示,脑指数与胸腺指数在造模后1、3天呈负相关,7、14、21天呈正相关,提示脑损伤与胸腺萎缩存在动态双向调控关系。
产品关联:实验所用关键产品:异氟烷(Beikang,No.21042801)、PerCP/Cyanine 5.5抗大鼠CD3抗体(Elabscience,中国)、BD FACS Canto II流式细胞仪。
3.2 胸腺细胞凋亡与自噬的分子机制检测
实验目的:明确HIE诱导胸腺萎缩的细胞机制,解析胸腺细胞凋亡与自噬的调控通路。
方法细节:采用Annexin V/PI双染流式细胞术检测造模后不同时间点胸腺细胞的凋亡比例;通过蛋白质免疫印迹(Western blot)检测凋亡相关蛋白(Cleaved-半胱天冬酶3、B细胞淋巴瘤-2(Bcl-2)、Bcl-2相关X蛋白(Bax))、自噬相关蛋白(Beclin-1、微管相关蛋白1轻链3 II/I(LC3 II/I))及磷脂酰肌醇3-激酶(PI3K)/蛋白激酶B(Akt)/雷帕霉素靶蛋白(mTOR)通路蛋白的磷酸化水平。
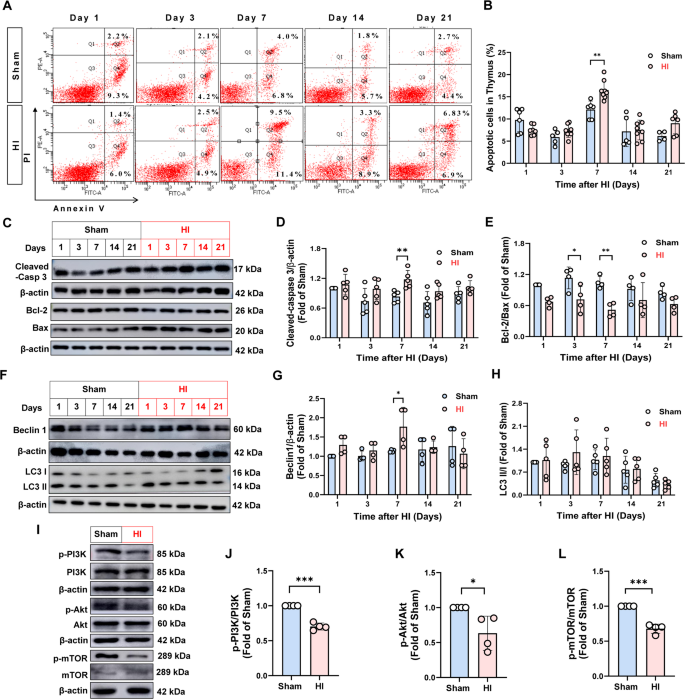
结果解读:HI组胸腺细胞凋亡比例在造模后3、7、14、21天持续升高,第7天达到峰值(n=5-8,P<0.05);第7天Cleaved-半胱天冬酶3蛋白表达显著上调(n=4-5,P<0.05),Bcl-2/Bax比值在3、7天显著降低(n=4-5,P<0.05),提示凋亡通路被激活;自噬相关蛋白Beclin-1、LC3 II/I在第7天表达显著升高,同时PI3K、Akt、mTOR的磷酸化水平显著降低(n=4,P<0.01),表明HIE通过抑制PI3K/Akt/mTOR通路诱导胸腺细胞自噬。
产品关联:实验所用关键产品:Annexin V/PI凋亡检测试剂盒(BD,美国)、Cleaved-半胱天冬酶3抗体(WL02117,Wanleibio)、Bcl-2抗体(WL01556,Wanleibio)、Bax抗体(WL01637,Wanleibio)、Amersham Imager 600蛋白成像系统(美国)。
3.3 HPA轴激活状态与胸腺糖皮质激素信号检测
实验目的:明确HIE诱导HPA轴激活的时序性变化,解析糖皮质激素信号对胸腺细胞的调控作用。
方法细节:检测造模后不同时间点下丘脑、垂体、肾上腺的器官指数;采用酶联免疫吸附试验(ELISA)检测下丘脑促肾上腺皮质激素释放激素(CRH)、血清促肾上腺皮质激素(ACTH)、皮质醇(CORT)水平;通过核浆蛋白提取试剂盒分离胸腺细胞的胞浆与核蛋白,检测糖皮质激素受体(GR)的核转位情况。
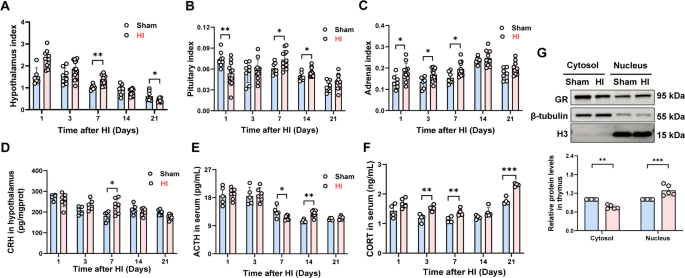
结果解读:HI组下丘脑指数在第7天显著升高(n=7-12,P<0.05),垂体指数在第1天降低、7和14天显著升高(n=7-12,P<0.05),肾上腺指数在1、3、7天显著升高(n=7-12,P<0.05);下丘脑CRH水平在第7天显著升高(n=5-8,P<0.05),血清CORT水平在3、7、21天显著升高(n=4-8,P<0.05);第7天胸腺细胞GR核转位显著增加(n=5,P<0.01),提示HIE诱导HPA轴过度激活,糖皮质激素信号在胸腺细胞中显著增强。
产品关联:实验所用关键产品:CRH、ACTH、CORT ELISA试剂盒(Omnimabs,美国)、核浆蛋白提取试剂盒(Wanleibio,中国)、GR抗体(WL02695,Wanleibio)。
3.4 下丘脑神经炎症与HMGB1/TLR4/NF-κB通路验证
实验目的:明确HIE诱导HPA轴激活的上游神经炎症机制,验证HMGB1/TLR4/NF-κB通路的调控作用。
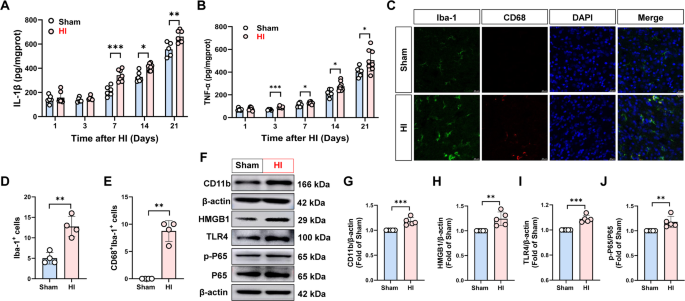
方法细节:采用ELISA检测下丘脑肿瘤坏死因子-α(TNF-α)、白细胞介素-1β(IL-1β)水平;通过免疫荧光染色检测小胶质细胞激活标记物离子钙结合衔接分子1(Iba-1)和CD68的表达;Western blot检测HMGB1、TLR4、磷酸化NF-κB(p-P65)的蛋白水平。
结果解读:HI组下丘脑IL-1β水平在7、14、21天显著升高(n=5-8,P<0.05),TNF-α水平在3、7、14、21天显著升高(n=5-8,P<0.05);免疫荧光显示HI组小胶质细胞呈典型激活形态,Iba-1荧光强度和CD68+细胞比例显著升高(n=4,P<0.001);第7天下丘脑HMGB1、TLR4、p-P65蛋白水平显著升高(n=5,P<0.01),提示HIE通过激活HMGB1/TLR4/NF-κB通路诱导下丘脑小胶质细胞活化和持续神经炎症。
产品关联:实验所用关键产品:TNF-α、IL-1β ELISA试剂盒(Proteintech,中国)、Iba-1/CD68免疫荧光试剂、HMGB1抗体(ab18256,Abcam)、TLR4抗体(sc-293072,Santa Cruz)。
3.5 特异性抑制剂干预的机制验证
实验目的:验证HMGB1/TLR4/NF-κB通路与HPA轴在HIE诱导胸腺萎缩中的因果关系。
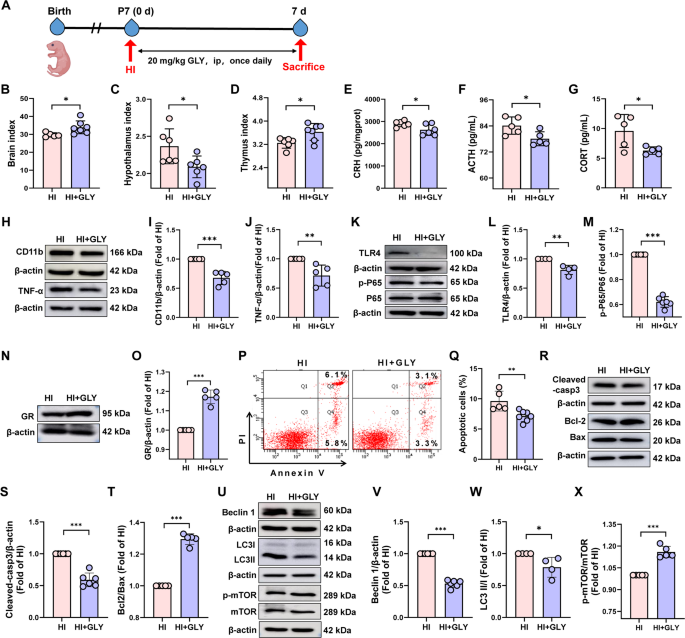
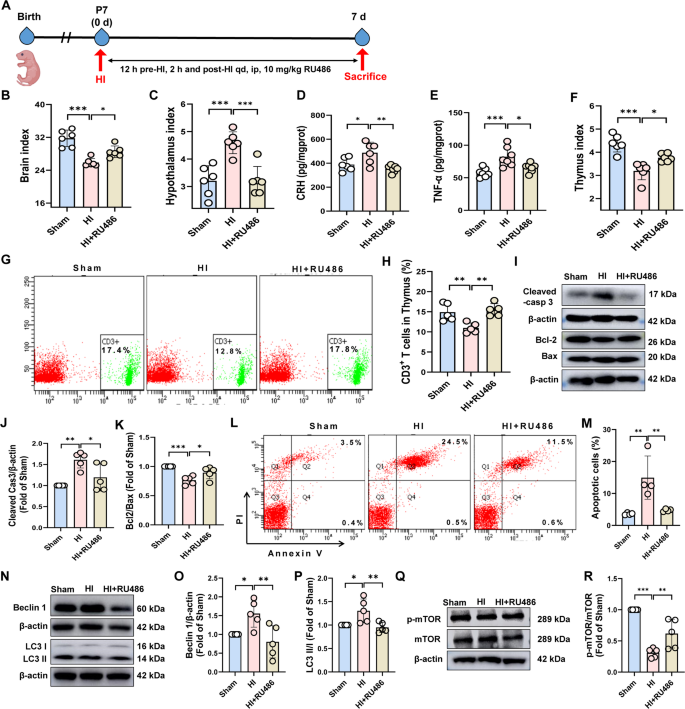
方法细节:设置HMGB1抑制剂甘草酸(GLY)干预组和GR拮抗剂米非司酮(RU486)干预组,GLY在造模后立即腹腔注射(20mg/kg),每日1次;RU486在造模前12h和造模后2h腹腔注射(10mg/kg),每日1次。在造模后第7天检测HPA轴功能、神经炎症指标及胸腺损伤相关指标。
结果解读:GLY干预显著降低下丘脑CRH、血清ACTH和CORT水平(n=5-6,P<0.05),抑制下丘脑小胶质细胞活化和HMGB1/TLR4/NF-κB通路激活,同时减少胸腺细胞凋亡和自噬,恢复胸腺指数(n=5-7,P<0.05);RU486干预显著抑制HPA轴激活,降低胸腺细胞凋亡比例(n=4,P<0.01),上调Bcl-2/Bax比值,抑制自噬相关蛋白表达,恢复CD3+T细胞比例(n=5,P<0.05),证实HPA轴激活是HIE诱导胸腺萎缩的关键环节,而HMGB1是上游调控因子。
产品关联:实验所用关键产品:HMGB1抑制剂GLY(Selleck chem,美国)、GR拮抗剂RU486(MedChemExpress,美国)。
4. Biomarker研究及发现成果解析
本研究涉及的Biomarker涵盖神经炎症标志物、HPA轴功能标志物、胸腺损伤标志物三类,筛选与验证逻辑遵循“时序性变化→功能关联→干预验证”的链条:首先基于HIE模型的时序性变化筛选差异表达的标志物,随后通过分子实验验证其与胸腺损伤的功能关联,最后通过抑制剂干预验证其调控作用。
神经炎症标志物HMGB1、TLR4、p-P65来源于下丘脑组织,通过Western blot验证其在HIE后第7天表达显著升高(n=5,P<0.01),其表达水平与HPA轴激活指标(CRH、CORT)及胸腺损伤指标(Cleaved-半胱天冬酶3、Beclin-1)显著正相关;HPA轴功能标志物CRH、ACTH、CORT分别来源于下丘脑、垂体和血清,通过ELISA验证其在HIE后不同时间点的异常表达,其中CORT水平与胸腺细胞凋亡比例正相关(P<0.05);胸腺损伤标志物Cleaved-半胱天冬酶3、Beclin-1、CD3+T细胞比例分别通过Western blot和流式细胞术检测,Cleaved-半胱天冬酶3和Beclin-1的表达升高与胸腺萎缩显著相关,CD3+T细胞比例在HIE后第7天显著降低(n=4-6,P<0.05),可反映胸腺功能损伤程度。
本研究的核心成果在于,证实HMGB1可作为HIE诱导神经炎症的关键Biomarker,其表达升高可预测HPA轴激活和胸腺萎缩的发生;CRH、CORT可作为HPA轴过度激活的Biomarker,为HIE的免疫功能评估提供参考;CD3+T细胞比例可作为胸腺功能损伤的Biomarker,提示HIE患儿的免疫抑制状态。本研究首次揭示了HMGB1/TLR4/NF-κB通路介导的神经炎症- HPA轴-胸腺损伤轴在新生儿HIE中的作用,为HIE的早期免疫评估和靶向治疗提供了潜在的Biomarker与干预靶点。