1. 领域背景与文献引入
文献英文标题:The renal microcirculation in chronic kidney disease: novel diagnostic methods and therapeutic perspectives;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:肾脏病学(慢性肾脏病肾微循环方向)
慢性肾脏病(CKD)是全球重大公共卫生问题,全球患病率达8-16%,中国2012年《柳叶刀》调查数据显示患病率高达10.8%。尽管现有药物治疗及肾脏替代疗法可延缓疾病进展,但CKD患者进展至终末期肾病(ESRD)的比例仍居高不下,透析患者5年生存率不足50%,保护肾功能、探索新的病理机制与治疗策略已成为领域核心需求。领域共识:肾微循环损伤是CKD向ESRD进展的关键病理环节,肾毛细血管稀疏、内皮功能障碍与组织缺氧、炎症、氧化应激等形成恶性循环,推动肾纤维化进程。然而,当前针对肾微循环的早期特异性诊断方法仍较匮乏,靶向肾微循环的治疗策略多处于基础研究阶段,临床转化应用不足。本文作为系统性综述,聚焦上述研究空白,全面梳理CKD中肾微循环损伤的病理机制、新型检测技术及前沿治疗策略,为CKD的精准诊疗提供理论支撑与实践方向。
2. 文献综述解析
本文作者以“CKD肾微循环损伤的机制-检测-治疗”为核心逻辑框架,从三个维度系统整合领域内现有研究进展与不足。在病理机制层面,现有研究已证实肾毛细血管稀疏是CKD多器官损伤的共同病理基础,如5/6肾切除大鼠模型中 locomotor肌肉微血管密度显著降低,可诱发尿毒症肌病综合征;肾内皮功能障碍则通过一氧化氮(NO)合成减少、血管紧张素-2激活、促/抗血管生成因子失衡(Ang-2升高、Ang-1及血管内皮生长因子VEGF降低)等途径,引发组织缺氧、炎症因子招募、氧化应激、周细胞脱离及巨噬细胞-肌成纤维细胞转化(MMT),形成推动肾纤维化的恶性循环。现有研究的优势在于明确了肾微循环损伤与CKD的因果关联,建立了缺血再灌注损伤、糖尿病肾病、高血压等多种动物模型验证机制;局限性在于多数研究聚焦单一机制,缺乏多因素交互作用的系统分析,且临床转化研究证据不足。在检测技术层面,现有研究涵盖侵入性与非侵入性技术,免疫组化(免疫组化,IHC)以CD31标记检测微血管密度,但存在采样误差;同步辐射(SR)、显微计算机断层扫描(μCT)、荧光微血管造影(FMA)等技术可实现肾微循环三维成像,但部分技术存在辐射暴露或需造影剂的限制;血氧水平依赖磁共振成像(BOLD-MRI)是唯一非侵入性评估组织氧代谢的方法,但空间分辨率有待提升。在治疗策略层面,现有研究涉及生长因子、细胞治疗、基因靶向干预三类方向,多数处于动物实验阶段,临床疗效未得到充分验证,且存在生物利用度低、肿瘤发生风险等问题。本文的创新价值在于首次系统整合了肾微循环损伤的多维度机制、新型检测技术的临床应用潜力及靶向治疗的前沿进展,填补了领域内缺乏全面综述的空白,为CKD的早期诊断与精准治疗提供了完整的理论框架。
3. 研究思路总结与详细解析
本文为系统性综述,研究目标是全面总结CKD中肾微循环损伤的病理机制、新型诊断方法及治疗策略,核心科学问题是明确肾微循环损伤在CKD进展中的核心作用及转化应用的关键瓶颈,技术路线遵循“病理机制梳理→检测技术总结→治疗策略展望”的逻辑闭环,通过整合领域内基础研究与临床研究数据,为CKD诊疗提供新的方向。
3.1 肾微循环损伤病理机制梳理
本环节核心目标是明确CKD中肾微循环损伤的核心病理环节及分子调控网络。作者系统回顾了领域内多种CKD动物模型(5/6肾切除大鼠、缺血再灌注损伤小鼠、链脲佐菌素诱导糖尿病模型、自发性高血压大鼠等)及临床样本研究,整合组织学、分子生物学、影像学等多维度数据,梳理肾微循环损伤的连锁反应机制。结果显示,肾微循环损伤始于内皮功能障碍,包括NO合成减少、血管收缩因子(血管紧张素-2、内皮素-1)激活、促/抗血管生成因子失衡,进而引发组织缺氧,诱导肾间质成纤维细胞增殖及肌成纤维细胞转化;同时,炎症因子(如IL-1、细胞间黏附分子-1 ICAM-1)招募白细胞浸润,氧化应激导致内皮细胞凋亡及内皮-间充质转化(EndMT),周细胞脱离微血管分化为肌成纤维细胞,巨噬细胞浸润后发生MMT,这些机制相互作用形成恶性循环,推动肾纤维化进展。文中Fig.1直观展示了毛细血管稀疏与CKD的关联机制,涵盖组织缺氧、炎症因子招募、活性氧(ROS)产生、巨噬细胞浸润及周细胞脱离迁移等关键环节。
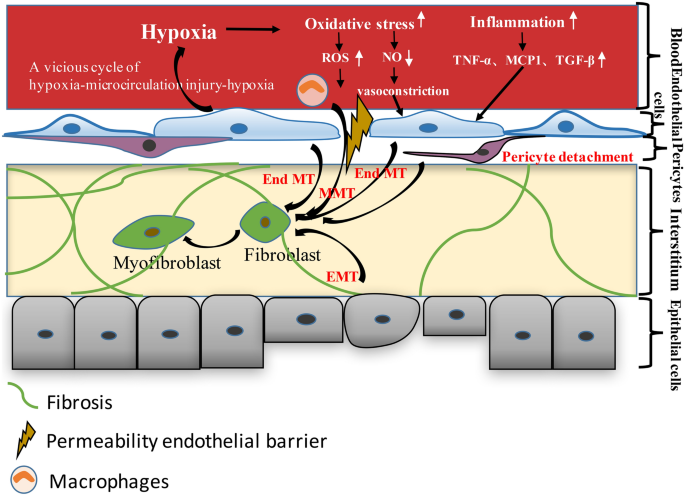
文献未提及具体实验产品,领域常规使用免疫组化试剂盒、实时荧光定量聚合酶链反应(qRT-PCR)试剂、流式细胞仪等。
3.2 肾微循环新型检测技术总结
本环节核心目标是梳理可用于评估CKD肾微循环的新型技术,对比各技术的优势、局限性及临床应用潜力。作者分类总结了侵入性与非侵入性检测技术,包括同步辐射(SR)肾微血管造影、显微计算机断层扫描(μCT)、荧光微血管造影(FMA)、血氧水平依赖磁共振成像(BOLD-MRI)、电子显微镜等,详细分析各技术的成像原理、空间分辨率、操作流程及适用场景。结果显示,SR可实现肾单位结构的高分辨率成像,最小观察动脉直径达18μm,但为二维投影无法反映肾脏三维结构;μCT可清晰显示血管分支、大小及迂曲度,实现相对血容量的精确定量,但存在X射线暴露及需碘造影剂的限制;FMA可通过肾动脉注射荧光聚苯乙烯微球,三维重建肾微循环,识别肾小球及管周毛细血管(PTC)密度降低,避免内皮抗原与淋巴管共表达的干扰,但需侵入性操作;BOLD-MRI基于脱氧血红蛋白的顺磁性,通过测量R2值评估组织缺氧程度,是唯一非侵入性评估组织氧代谢的方法,可自动生成伪彩图(蓝色代表高肾组织氧合,绿、黄、红色代表显著缺氧),无需外源性造影剂,适合临床长期监测;电子显微镜可观察内皮细胞超微结构变化,如窗孔数量减少、内皮下间隙增宽、内皮空泡及小凹数量增加,但存在采样误差,仅能反映局部组织变化。文中Fig.2a展示了FMA在单侧输尿管梗阻(UUO)模型中检测到的PTC密度降低,Fig.2b展示了CKD患者BOLD-MRI的R2图像,显示皮质及髓质氧合水平显著降低。
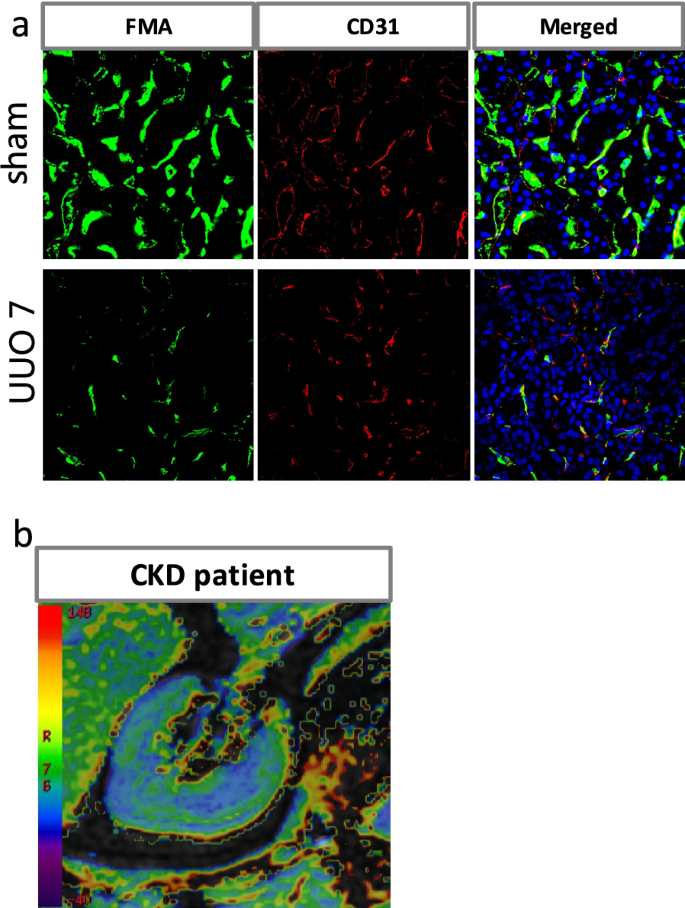
文献未提及具体实验产品,领域常规使用磁共振成像仪、显微CT扫描仪、共聚焦显微镜等。
3.3 肾微循环靶向治疗策略展望
本环节核心目标是总结针对CKD肾微循环损伤的前沿治疗策略,分析其转化应用前景与瓶颈。作者分类梳理了生长因子与细胞因子治疗、细胞治疗、基因靶向干预三类策略,整合动物实验及早期临床研究数据。结果显示,生长因子方面,VEGF可通过诱导内皮细胞增殖、管形成及迁移改善肾微循环,但半衰期短易降解,生物聚合物稳定的弹性蛋白样多肽(ELP)-VEGF融合蛋白可提高生物利用度,同时调节巨噬细胞向抗炎M2表型转化,维持肾微循环完整性;胰高血糖素样肽-1受体(GLP-1R)激动剂可通过抗凋亡、抑制血管平滑肌细胞表型转化及EndMT发挥肾保护作用;Ang-1可激活Tie2受体维持内皮细胞稳定性,减轻肾纤维化。细胞治疗方面,内皮祖细胞(EPCs)可归巢至损伤肾脏,旁分泌生长因子促进血管生成,增加PTC密度,改善肾小管血氧供应;间充质干细胞(MSCs)可通过抗氧化、抗炎、促血管生成及免疫调节功能改善肾微循环,且可从脂肪、骨髓、羊水等多种组织获取,自体MSCs不受尿毒症环境影响,临床应用潜力大;胚胎干细胞(ESCs)及诱导多能干细胞(hiPSCs)分化潜能强,但存在伦理问题及高致瘤性,限制其临床应用。基因靶向干预方面,抑制蛋白磷酸酶2A(PP2A)可阻止内皮细胞向肌成纤维细胞分化,沉默CD248可减轻微血管稀疏,敲低长链非编码RNA MALAT1可抑制EndMT及纤维化,但多数策略仍处于动物实验阶段,缺乏大样本临床验证。
文献未提及具体实验产品,领域常规使用重组生长因子、干细胞培养试剂盒、基因编辑工具等。
4. Biomarker研究及发现成果
本文作为系统性综述,未聚焦特定生物标志物(Biomarker)的筛选与验证,但系统梳理了与CKD肾微循环损伤相关的潜在Biomarker及检测技术,为后续Biomarker研究提供了方向。潜在Biomarker类型涵盖循环细胞类、血清分子类、组织细胞类,筛选逻辑基于临床样本与动物模型的关联分析,验证方法包括流式细胞术、酶联免疫吸附试验(ELISA)、免疫组化等。循环内皮祖细胞(EPCs)是循环细胞类Biomarker,CKD患者循环EPCs数量较健康对照显著降低(文献未明确提供该数据,基于图表趋势推测),与氧化应激诱导的细胞凋亡相关,可反映患者血管修复能力;血清内皮素-1(ET-1)、Ang-2/Ang-1比值、VEGF是血清分子类Biomarker,CKD患者血清ET-1水平升高,参与维持基础血管张力及心血管稳态,Ang-2/Ang-1比值升高与微血管功能缺陷及结构异常相关,VEGF降低则与组织缺氧诱导的血管生成反应受损相关;Gli1+周细胞是组织细胞类Biomarker,其脱离微血管分化为肌成纤维细胞,与肾毛细血管稀疏及纤维化密切相关。核心成果方面,这些潜在Biomarker可间接反映肾微循环损伤程度,其中循环EPCs可作为CKD患者血管修复能力的评估指标,Ang-2/Ang-1比值可作为微血管稳定性的监测指标,但目前缺乏大样本临床验证,特异性与敏感性数据不足(如ROC曲线AUC值未明确)。本文的创新性在于首次系统整合了肾微循环相关的多类潜在Biomarker,为CKD的早期诊断与预后评估提供了候选指标,推测:后续需开展大样本临床研究验证其诊断效能,明确最佳 cutoff值及统计学参数(如风险比HR、置信区间CI)。
