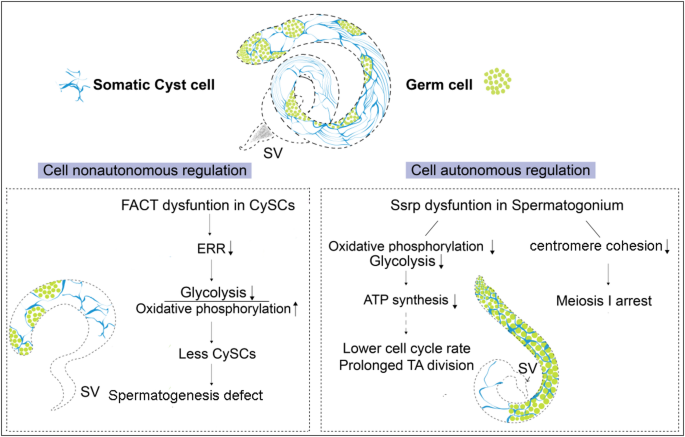
1. 领域背景与文献引入
文献英文标题:Ssrp governs germline development independent of the FACT complex in Drosophila spermatogenesis;发表期刊:Cell & Bioscience;影响因子:未明确提供;研究领域:果蝇生殖生物学、染色质调控与精子发生机制
FACT(染色质转录促进)复合物是由SSRP1/Ssrp和SUPT16H/Dre4组成的经典组蛋白伴侣,在DNA复制、修复及RNA转录过程中发挥核心调控作用,其突变与人类智力障碍密切相关,且在胚胎干细胞、神经干细胞及肿瘤细胞的干性维持中已被证实具有关键功能。领域共识:精子发生是从精原干细胞到成熟精子的高度保守过程,涉及精原细胞扩增、减数分裂及精子形成三个核心阶段,代谢稳态与染色质动态平衡是维持该过程的关键调控节点。当前研究热点聚焦于生殖细胞特异性染色质调控因子及代谢重编程机制,但FACT复合物在精子发生中的具体功能,尤其是亚基是否存在独立于复合物的非经典作用,尚未被系统探究。尽管人类蛋白质组学数据显示SSRP1和SUPT16H在睾丸生殖细胞中高表达,且脑与睾丸组织存在转录组相似性,但二者在生殖系统中的功能关联仍属空白。本研究以果蝇为经典模型,旨在填补这一领域空白,明确FACT复合物在精子发生中的细胞特异性功能,为人类生殖障碍的机制研究提供参考。
2. 文献综述解析
作者以FACT复合物的经典功能为切入点,先梳理其在干细胞维持中的代谢调控机制,再结合人类睾丸组织的表达数据,提出FACT复合物在精子发生中功能未知的科学问题,综述逻辑遵循“经典功能→已知延伸→领域空白”的递进式结构。
现有研究证实FACT复合物作为异二聚体,在胚胎干细胞、神经干细胞及肿瘤细胞中通过调控染色质动态维持细胞干性,其中在果蝇神经干细胞中,FACT通过结合雌激素相关受体(ERR)的启动子区域,促进糖酵解代谢,维持干细胞增殖能力;技术方法上,多采用细胞系敲低、免疫染色及转录组分析,优势在于能明确复合物的整体功能,但局限性在于未涉及生殖系统的研究,也未探讨亚基是否存在独立于复合物的功能,且缺乏体内模型的验证。本研究的创新价值在于,首次在体内模型中揭示FACT复合物亚基的上下文依赖功能,即Ssrp在果蝇睾丸体细胞中与Dre4形成复合物发挥作用,而在生殖细胞中独立于Dre4调控精子发生,突破了FACT复合物作为固定异二聚体的传统认知,为生殖领域的染色质调控研究提供了新的范式。
3. 研究思路总结与详细解析
本研究的整体研究目标是探究FACT复合物在果蝇精子发生中的细胞特异性功能,核心科学问题为Ssrp与Dre4是否始终以异二聚体形式发挥作用,以及Ssrp调控生殖系发育的分子机制,技术路线遵循“细胞特异性敲低→表型鉴定→组学分析→机制验证→结论整合”的闭环逻辑。
3.1 睾丸体细胞中FACT复合物功能验证
实验目的:明确Ssrp与Dre4在睾丸体细胞(cyst干细胞,CySCs)中的功能及调控机制。方法细节:采用UAS/Gal4系统,以Tj-Gal4驱动Ssrp和Dre4的RNAi(至少2条RNAi线,经BLAST验证无脱靶),通过免疫染色验证蛋白敲低效率;检测不同基因型果蝇的睾丸形态、雄性育性;采用ATP-SPARK方法检测体细胞中ATP水平;通过过表达ERR进行表型挽救实验。结果解读:免疫染色结果显示,Tj-Gal4驱动的RNAi可有效降低Ssrp或Dre4的蛋白表达;与对照组相比,Ssrp或Dre4敲低的果蝇睾丸显著缩小,seminal vesicle几乎无成熟精子,雄性育性分别降至5.4%和0%(n=3,P<0.0001);ATP-SPARK检测显示体细胞敲低Ssrp后ATP水平升高;过表达ERR可恢复睾丸大小、Zfh1阳性细胞数量及育性(n=3,P<0.0001),说明体细胞中Ssrp与Dre4形成FACT复合物,通过ERR调控糖酵解维持CySCs的稳态,进而非细胞自主影响生殖细胞分化。产品关联:文献提及实验所用关键产品包括Abcam的GFP抗体、ATP5A抗体,DSHB的Eya抗体、Bam抗体、DE-cadherin抗体,Millipore的Phospho-Histone H3抗体,Sigma-Aldrich的γ-tubulin抗体,以及课题组自制的Ssrp、Dre4多克隆抗体。
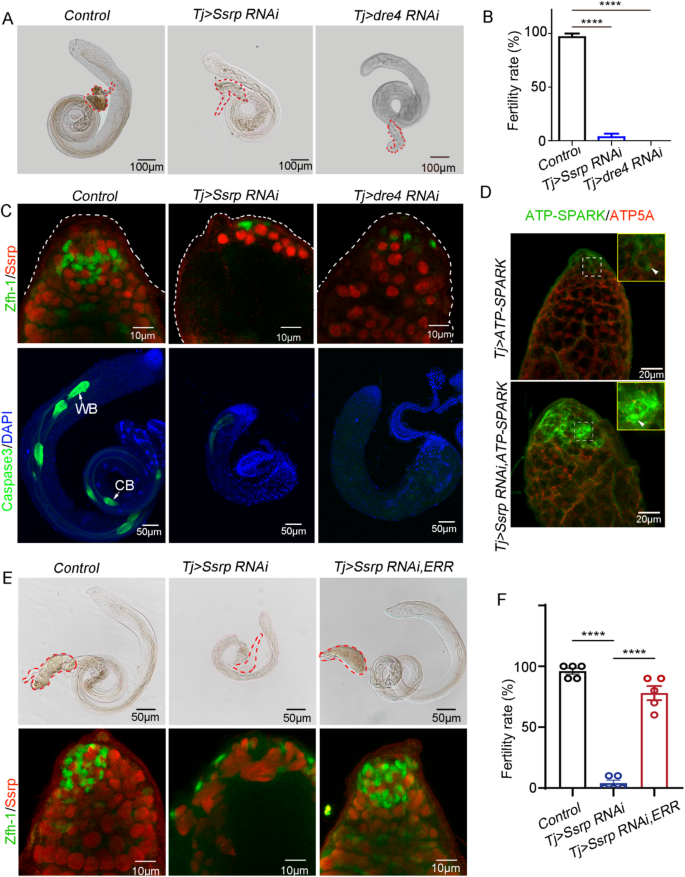
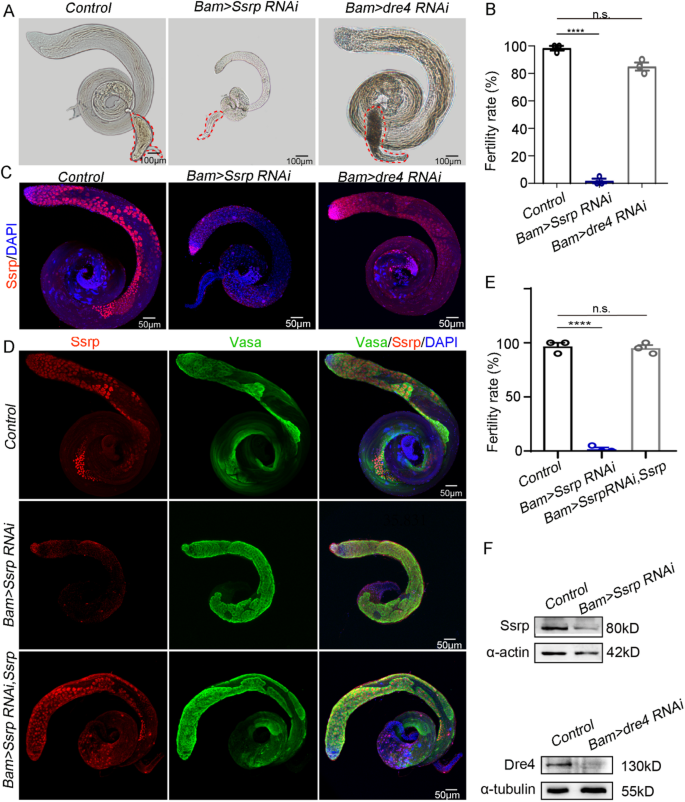
3.2 生殖细胞中Ssrp的独立功能验证
实验目的:探究Ssrp在生殖细胞中的功能是否依赖Dre4。方法细节:采用nos-Gal4(表达于精原干细胞和早期精原细胞)和bam-Gal4(表达于精原细胞)分别驱动Ssrp和Dre4的RNAi,检测雄性育性、睾丸形态;通过免疫染色、Western blot验证蛋白敲低效率;构建Bam > Ssrp RNAi/UAS-Ssrp进行遗传挽救实验。结果解读:nos-Gal4或bam-Gal4驱动的Ssrp敲低均导致雄性完全不育,睾丸萎缩且seminal vesicle无成熟精子,而Dre4敲低无此表型;免疫染色显示Ssrp敲低后生殖细胞中Ssrp信号显著降低,Western blot证实Ssrp和Dre4的蛋白水平分别在对应RNAi组中下降,且生殖细胞敲低Ssrp不影响Dre4的表达;遗传挽救实验显示过表达Ssrp可恢复睾丸形态及育性(n=3,P<0.0001),说明生殖细胞中Ssrp的功能独立于Dre4,是维持雄性育性的必需因子。
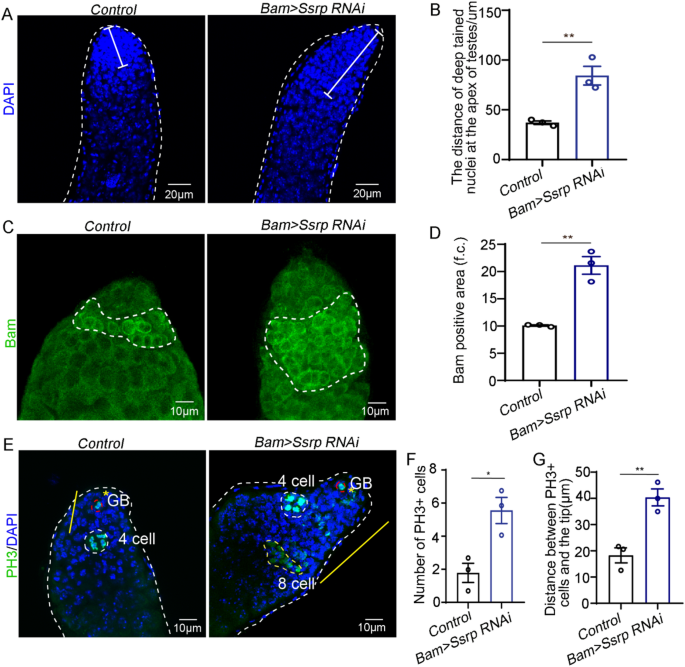
3.3 精原细胞增殖与减数分裂停滞表型分析
实验目的:解析Ssrp敲低后生殖细胞发育的具体缺陷阶段。方法细节:采用DAPI染色标记细胞核,Bam抗体标记精原细胞,Phospho-Histone H3(PH3)标记分裂细胞,γ-tubulin标记中心体,ATP5A标记线粒体形态;统计精原细胞区域长度、Bam阳性区域比例、PH3阳性细胞数量及距离,分析减数分裂阶段的细胞形态。结果解读:DAPI染色显示Ssrp敲低后睾丸顶端的精原细胞区域显著扩大(n=3,P<0.01);Bam阳性区域比例升高(n=3,P<0.05);PH3阳性细胞数量增加且距离顶端更远(n=3,P<0.05),提示精原细胞有丝分裂延迟,transit-amplifying(TA)分裂延长;γ-tubulin染色显示16细胞期精原细胞的中心体形态异常,无32细胞期出现;ATP5A染色显示无减数分裂I后期的蝴蝶状线粒体,说明减数分裂停滞在减数分裂I阶段。
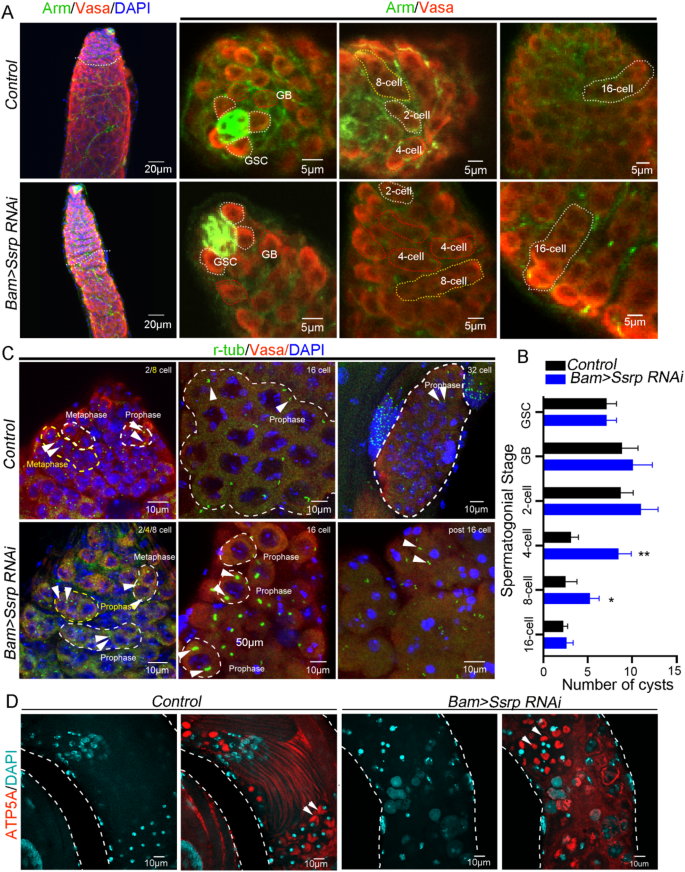
3.4 代谢通路调控机制分析
实验目的:探究Ssrp调控生殖细胞发育的代谢机制。方法细节:对Bam > Ssrp RNAi和对照组睾丸进行bulk RNA-seq和单细胞RNA-seq(scRNA-seq)分析;采用ATP-SPARK检测生殖细胞中的ATP水平;通过bam-Gal4敲低Opa1(线粒体融合基因)模拟氧化磷酸化缺陷,检测表型。结果解读:bulk RNA-seq分析显示,Ssrp敲低后共有4608个差异表达基因,其中糖酵解和氧化磷酸化通路显著下调(P<0.05);scRNA-seq分析显示精原细胞中代谢通路相关基因表达下调;ATP-SPARK检测显示生殖细胞中ATP水平显著降低(n=3,P<0.001);敲低Opa1导致ATP水平下降、TA分裂延长及育性降低,部分模拟Ssrp敲低的表型,说明代谢缺陷是Ssrp敲低导致生殖细胞发育异常的重要原因。
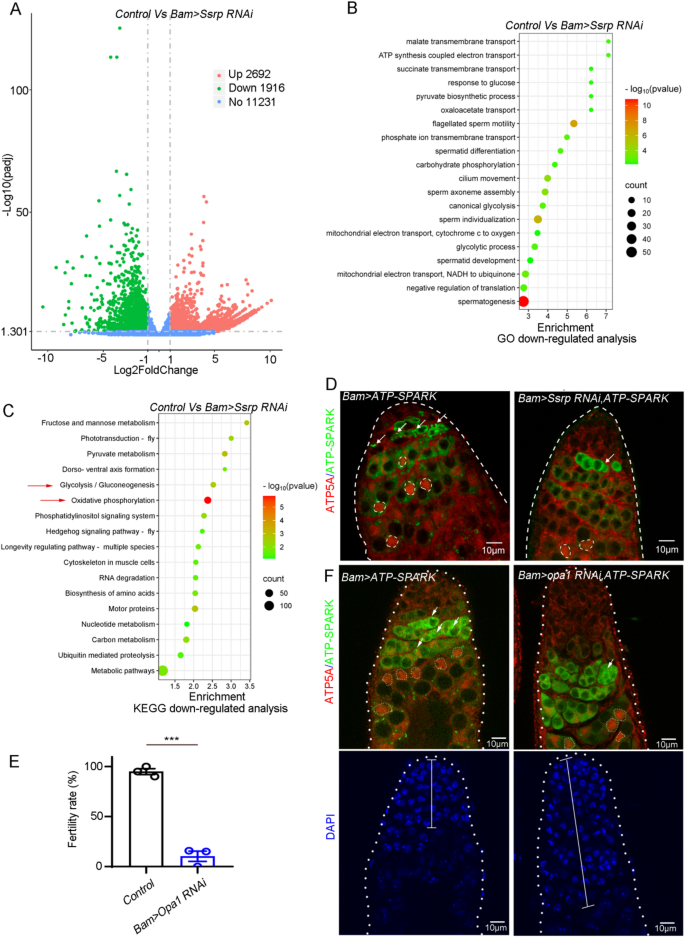
3.5 着丝粒 cohesion缺陷机制验证
实验目的:探究Ssrp对减数分裂染色体稳定性的影响。方法细节:通过scRNA-seq分析CENP-A的表达;采用Western blot和免疫染色检测CENP-A的蛋白水平;统计减数分裂I后期(S5/6阶段)的着丝粒焦点数量。结果解读:scRNA-seq显示精原细胞中CENP-A的mRNA表达升高(P<0.0001);Western blot证实CENP-A蛋白水平升高;免疫染色显示Ssrp敲低后减数分裂I后期的着丝粒焦点数量从对照组的6.7个增加到8.3个(n=3,P<0.001),说明姐妹着丝粒 cohesion缺陷,导致减数分裂停滞。
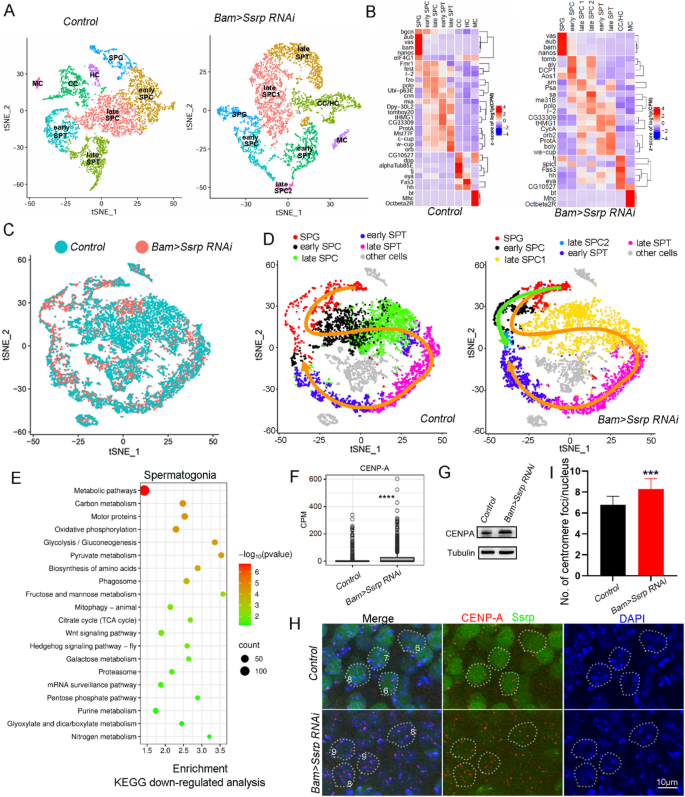
4. Biomarker研究及发现成果
本研究中鉴定的核心功能Biomarker为Ssrp,其作为FACT复合物的亚基,在果蝇精子发生中具有细胞特异性的调控功能,为生殖系发育的染色质调控研究提供了新的靶点。
Biomarker定位:Ssrp属于染色质调控类功能Biomarker,筛选逻辑基于FACT复合物在干细胞中的已知功能,结合人类睾丸组织的表达数据,通过果蝇体内细胞特异性敲低实验验证其在精子发生中的功能;验证逻辑为“体细胞敲低→表型分析→生殖细胞敲低→表型差异→组学分析→机制验证”。研究过程详述:Ssrp的来源为果蝇睾丸的体细胞和生殖细胞,验证方法包括RNAi敲低、免疫染色、Western blot、bulk及scRNA-seq分析、遗传挽救实验;特异性表现为,体细胞中Ssrp与Dre4共同作用维持CySCs稳态,而生殖细胞中Ssrp独立于Dre4调控精原细胞增殖和减数分裂;敏感性数据显示,生殖细胞特异性敲低Ssrp后雄性育性降至0%(n=3,P<0.0001),表型完全外显。核心成果提炼:Ssrp是果蝇精子发生中的多功能调控因子,其在体细胞中通过FACT复合物调控ERR依赖的糖酵解,在生殖细胞中独立调控代谢通路(糖酵解和氧化磷酸化)和着丝粒 cohesion,首次揭示了FACT复合物亚基的上下文依赖功能;该成果的创新性在于突破了FACT复合物作为固定异二聚体的传统认知,为人类生殖障碍中SSRP1突变的机制研究提供了体内模型的参考;统计学结果显示,各项表型数据均具有显著的统计学差异(P<0.05至P<0.0001),样本量均为3次生物学重复。