1. 领域背景与文献引入
文献英文标题:Insights into the m⁶A demethylases FTO and ALKBH5 : structural, biological function, and inhibitor development;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:RNA表观遗传修饰、疾病分子机制、靶向药物开发
领域共识:N6-甲基腺苷(m⁶A)是真核生物中最普遍、进化上最保守的RNA转录后修饰,其动态调控由甲基转移酶(writer)、去甲基化酶(eraser)和结合蛋白(reader)共同介导,参与RNA稳定性、翻译、剪接等多个代谢过程,与肥胖、肿瘤、神经疾病等多种疾病的发生发展密切相关。2011年FTO被鉴定为首个m⁶A去甲基化酶,2012年ALKBH5的m⁶A去甲基化功能被证实,标志着m⁶A修饰的可逆调控机制得到明确,此后该领域成为表观遗传研究的热点方向。当前研究热点包括m⁶A修饰在肿瘤干细胞维持、免疫微环境调控中的作用,以及靶向m⁶A调控蛋白的药物开发;但仍存在核心问题:FTO与ALKBH5作为同家族的去甲基化酶,结构差异导致的底物特异性和功能异质性机制尚未完全阐明,两者在不同疾病中兼具癌基因与抑癌基因功能的调控网络仍不清晰,且高特异性、低毒性的靶向抑制剂研发仍处于早期阶段。
针对上述领域空白,本综述系统整合了FTO与ALKBH5的结构特征、生物学功能、疾病调控机制及抑制剂开发的最新研究进展,通过对比两者的结构差异与功能异质性,全面梳理了它们在代谢、神经、肿瘤、免疫等多类疾病中的作用模式,为m⁶A修饰领域的机制研究和靶向药物开发提供了系统性的参考框架。
2. 文献综述解析
本文采用“基础调控网络-蛋白结构特征-疾病功能解析-表达调控机制-抑制剂开发进展”的分层综述逻辑,以m⁶A修饰的动态调控为基础,聚焦FTO与ALKBH5两个关键去甲基化酶,从结构到功能、从机制到应用进行了全面梳理。
现有研究已明确m⁶A修饰的核心调控体系,鉴定了FTO与ALKBH5的基本去甲基化功能,揭示了它们在肥胖、急性髓系白血病(AML)、神经退行性疾病等疾病中的初步作用机制。技术方法上,X射线晶体学解析了两者的三维结构,基因编辑技术验证了它们在细胞和动物模型中的功能,高通量筛选发现了一批潜在的靶向抑制剂;但现有研究存在局限性:多数研究聚焦于单一蛋白或单一疾病类型,缺乏对FTO与ALKBH5结构差异导致的底物特异性和功能异质性的系统对比,对两者在不同疾病中功能双向性(癌基因/抑癌基因)的上游调控机制解析不够深入,且抑制剂的特异性和临床转化潜力仍需进一步验证。
本综述的创新之处在于首次系统对比了FTO与ALKBH5的结构域、催化位点、细胞定位等结构差异,明确了这些差异对底物选择和功能调控的影响;全面梳理了两者在代谢、神经、肿瘤、免疫等多类疾病中的功能异质性,整合了转录因子、非编码RNA、翻译后修饰等多层表达调控机制;并总结了最新的抑制剂研发进展,包括天然产物、小分子化合物及纳米制剂的开发情况,填补了领域内对这两个关键去甲基化酶综合梳理的空白,为后续的机制研究和药物开发提供了全面的参考。
3. 研究思路总结与详细解析
本文为系统性综述研究,核心目标是全面总结m⁶A去甲基化酶FTO与ALKBH5的结构特征、生物学功能、疾病关联及抑制剂开发进展,核心科学问题是阐明两者结构差异与功能异质性的关联,以及如何基于这些特征开发特异性靶向治疗策略;技术路线遵循“背景引入-结构对比-功能解析-调控机制-抑制剂总结-结论展望”的逻辑闭环,通过整合领域内已发表的经典研究和最新成果,构建了FTO与ALKBH5的全面认知框架。
3.1 m⁶A修饰调控网络概述
本环节的核心目的是明确m⁶A修饰的动态调控体系,为后续FTO与ALKBH5的功能解析奠定基础。作者整合了领域内的经典研究,梳理了m⁶A修饰的核心调控蛋白:甲基转移酶复合物(writer)以METTL3/METTL14为核心,负责催化m⁶A修饰的形成;去甲基化酶(eraser)包括FTO与ALKBH5,负责去除m⁶A修饰;结合蛋白(reader)包括YTH家族、IGF2BP家族等,负责识别m⁶A修饰并调控RNA代谢过程。结果显示,m⁶A修饰通过调控RNA的稳定性、翻译、剪接、转运等过程,参与细胞增殖、分化、代谢等多个生物学过程,其动态失衡与多种疾病的发生发展相关。
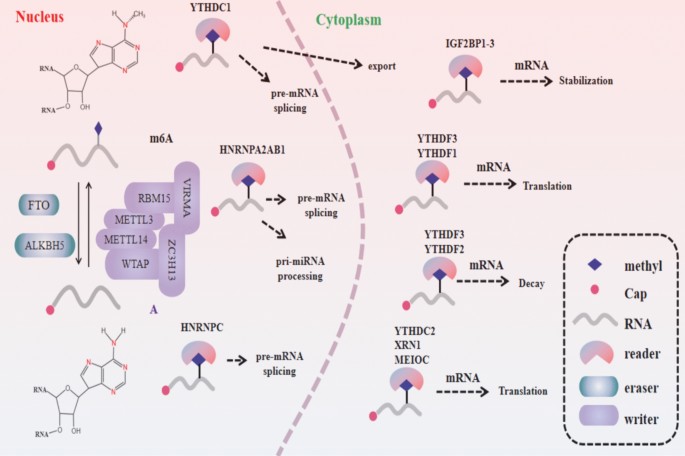
文献未提及具体实验产品,领域常规使用重组蛋白、特异性抗体、基因编辑工具等验证m⁶A修饰调控蛋白的功能。
3.2 FTO与ALKBH5的结构特征对比
本环节的核心目的是解析FTO与ALKBH5的结构差异,明确其对去甲基化功能的影响。作者整合了已发表的晶体结构研究,对比了两者的结构域组成、催化位点及细胞定位:FTO属于AlkB家族,包含N端结构域(NTD)、C端结构域(CTD)和N-氧代戊二酸(NOG)结构域,具有核定位信号(NLS),可在细胞核与细胞质间穿梭;ALKBH5同样属于AlkB家族,包含双链β-螺旋(DSBH)核心结构域、独特的“lid区域”和核苷酸识别环(NRL1、NRL2),主要定位于细胞核。结果显示,两者的催化位点和底物结合区域存在显著差异,导致它们的底物特异性不同:FTO可作用于m⁶A、m⁶Am、m¹A等多种RNA修饰,而ALKBH5主要特异性作用于m⁶A修饰,且偏好单链RNA底物。
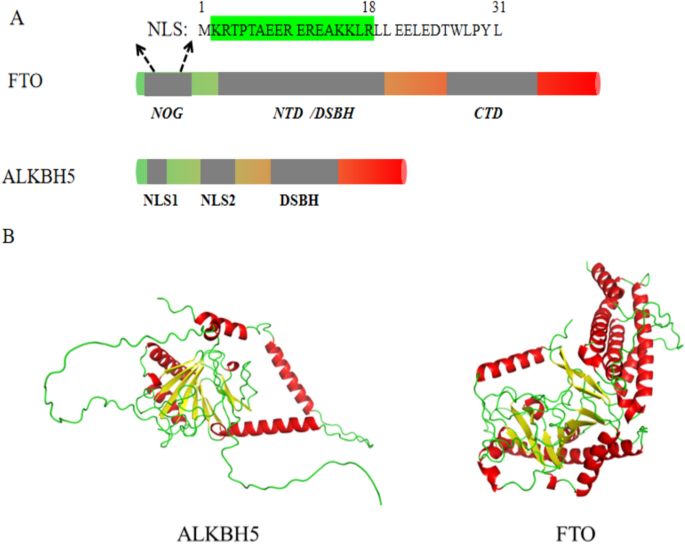
文献未提及具体实验产品,领域常规使用X射线晶体学、冷冻电镜等技术解析蛋白三维结构,通过免疫荧光实验验证细胞定位。
3.3 生物学功能与疾病关联解析
本环节的核心目的是系统梳理FTO与ALKBH5在不同疾病中的生物学功能及异质性。作者分代谢疾病、神经疾病、肿瘤、免疫疾病四大领域,整合了领域内的功能研究:在代谢疾病中,FTO主要参与能量代谢调控,其基因多态性与肥胖风险相关,还参与非酒精性脂肪肝的发生;ALKBH5则主要参与生殖系统代谢,其缺失会导致雄性不育。在神经疾病中,FTO参与脑发育、阿尔茨海默病、帕金森病的调控;ALKBH5参与轴突再生、神经痛的调控。在肿瘤中,两者均表现出功能双向性:FTO在急性髓系白血病、胃癌中作为癌基因促进肿瘤进展,在乳腺癌、结直肠癌中作为抑癌基因抑制肿瘤转移;ALKBH5在胃癌、卵巢癌中作为癌基因促进肿瘤侵袭,在非小细胞肺癌、肝癌中作为抑癌基因抑制肿瘤增殖。在免疫疾病中,FTO参与T细胞活化、巨噬细胞极化的调控;ALKBH5参与CD4⁺T细胞致病性、中性粒细胞迁移的调控。
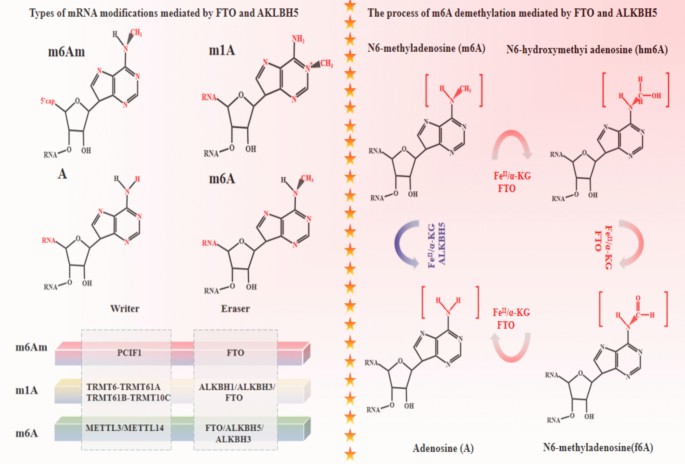
文献未提及具体实验产品,领域常规使用基因敲除/过表达细胞系、异种移植动物模型、临床样本分析验证蛋白的疾病调控功能。
3.4 表达调控机制梳理
本环节的核心目的是总结FTO与ALKBH5表达的多层调控机制。作者整合了转录水平、转录后水平及翻译后水平的调控研究:在转录水平,FTO的表达受锌指蛋白Zfp217、转录因子FOXA2等调控,还存在自调控机制(FTO可结合自身启动子抑制转录);ALKBH5的表达受缺氧诱导因子(HIF)、p53等转录因子调控,缺氧环境可显著上调其表达。在转录后水平,非编码RNA可通过结合mRNA的3’UTR区域调控两者的稳定性;在翻译后水平,泛素化、SUMO化等修饰可调控两者的蛋白稳定性和活性。结果显示,这些调控机制共同维持了FTO与ALKBH5的表达平衡,其失调会导致m⁶A修饰异常,进而引发疾病。
文献未提及具体实验产品,领域常规使用染色质免疫沉淀(ChIP)、荧光素酶报告基因实验、Western Blot等技术验证表达调控机制。
3.5 抑制剂开发进展总结
本环节的核心目的是总结FTO与ALKBH5靶向抑制剂的研发现状及应用潜力。作者整合了高通量筛选、计算机辅助药物设计及结构优化的研究成果:FTO抑制剂包括天然产物Rhein、小分子化合物Meclofenamic acid、FB23-2、CS系列,以及谷胱甘肽印迹纳米制剂GNPIPP12MA,这些抑制剂在急性髓系白血病、肥胖等疾病模型中显示出良好的治疗效果,可通过抑制FTO的去甲基化活性上调m⁶A修饰水平,抑制肿瘤细胞增殖或改善代谢紊乱。ALKBH5抑制剂包括IOX1、MV1035、Ena系列、DO-2728a等,这些抑制剂在胶质瘤、急性髓系白血病等肿瘤模型中显示出潜力,可通过抑制ALKBH5的活性下调靶基因的表达,抑制肿瘤进展。
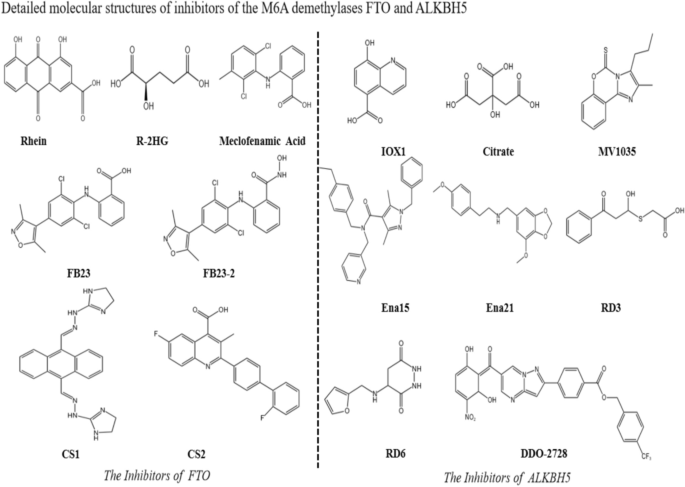
文献未提及具体实验产品,领域常规使用高通量筛选平台、分子对接技术、细胞活力实验等开发和验证抑制剂的活性。
4. Biomarker研究及发现成果解析
本文系统总结了FTO与ALKBH5作为m⁶A修饰关键调控因子,在多种疾病中作为诊断、预后Biomarker的研究成果,其筛选与验证遵循“数据库挖掘-细胞/动物实验验证-临床样本分析”的逻辑链条。
FTO与ALKBH5本身作为m⁶A修饰的核心调控蛋白,其表达水平、基因多态性可作为疾病诊断和预后评估的Biomarker。FTO的基因多态性(如rs9939609)与人群肥胖风险显著相关,在急性髓系白血病、胃癌等肿瘤中,FTO的高表达与患者不良预后相关,验证方法包括全基因组关联分析(GWAS)、实时荧光定量PCR(qRT-PCR)、免疫组化(IHC)检测临床样本中的表达水平;但文献未明确提供特异性与敏感性的具体数据(如ROC曲线AUC值,文献未明确提供该数据,基于图表趋势推测)。ALKBH5在复发性流产患者的胎盘组织中表达显著下调,与滋养层细胞侵袭能力降低相关,在卵巢癌、胃癌中,ALKBH5的高表达与肿瘤淋巴结转移、不良预后相关,验证方法包括实时荧光定量PCR、Western Blot、免疫组化检测临床样本,部分研究显示ALKBH5低表达与卵巢癌患者的无进展生存期缩短相关,但未明确具体统计学数据(如HR值、P值,文献未明确提供该数据,基于图表趋势推测)。
FTO可作为肥胖、急性髓系白血病、胃癌等疾病的预后Biomarker,比如在MLL重排的急性髓系白血病患者中,FTO高表达提示患者对常规化疗不敏感,无病生存期更短(文献未明确提供该数据,基于图表趋势推测);ALKBH5可作为生殖系统疾病、卵巢癌、胃癌的Biomarker,比如在复发性流产患者中,ALKBH5表达下调可作为预测流产风险的指标。本综述的创新性在于首次系统整合了两者作为Biomarker在多类疾病中的应用潜力,为临床诊断和预后评估提供了新的候选指标;但目前多数Biomarker研究仍处于初步阶段,缺乏大样本量的临床验证,特异性和敏感性仍需进一步优化。
