1. 领域背景与文献引入
文献英文标题:Importin alpha binding and nuclear localization of PARP-2 is dependent on lysine 36, which is located within a predicted classical NLS;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:细胞生物学(核蛋白转运与PARP家族蛋白功能调控)
聚ADP核糖聚合酶(PARP)家族是参与基因组稳定性维持、转录调控及细胞死亡等多种生物学过程的关键酶类,早期研究认为哺乳动物细胞中仅存在PARP-1具有聚ADP核糖化活性,直到PARP-1敲除小鼠仍能合成聚ADP核糖,才推动了PARP-2等家族新成员的发现。PARP-2作为核定位蛋白,其功能的发挥依赖于核内定位,而核定位信号(NLS)是介导核蛋白通过核孔复合体入核的关键序列,经典核定位信号分为由单一碱性氨基酸簇构成的单分型核定位信号和由两个碱性簇构成的双分型核定位信号。此前有研究推测PARP-2的氨基端1-69位存在双分型核定位信号,但该推测未经过实验验证,PARP-2核定位的关键功能残基及具体核定位信号类型仍不明确,这一空白限制了对PARP-2核内功能调控机制的深入理解。因此,本研究聚焦PARP-2的核定位机制,通过定点突变与功能验证实验,明确其核定位的关键残基及依赖的核转运通路,为PARP-2功能研究提供核心基础。
2. 文献综述解析
作者在综述部分以PARP家族研究历程、核转运分子机制、经典核定位信号分类为核心维度,系统梳理了领域内现有研究进展与未解决问题,为本文的研究假设与实验设计提供了逻辑支撑。
在PARP家族研究方面,从早期单一PARP-1的认知拓展至包含PARP-2在内的至少6个家族成员,PARP-2与PARP-1存在同源和异源二聚化,功能部分冗余,PARP-2的核定位是其发挥基因组稳定性调控等功能的前提;在核转运机制方面,importinα作为经典核定位信号的衔接蛋白,能够结合核蛋白并介导其与importinβ形成复合物,进而通过核孔复合体入核,不同importinα亚型对核定位信号的结合具有特异性;在核定位信号研究方面,经典核定位信号分为单分型与双分型,此前有研究通过序列分析推测PARP-2的1-69位为双分型核定位信号,但未通过实验验证该序列的功能。现有研究的局限性在于,PARP-2的核定位信号缺乏直接实验证据,关键功能残基不明确,导致其核转运机制的分子基础仍不清楚。
本研究通过对比现有研究中未验证的双分型核定位信号推测,首次通过实验证实PARP-2的核定位依赖于氨基端36位赖氨酸(K36),该残基位于单分型经典核定位信号序列中,而非此前推测的双分型核定位信号;同时明确PARP-2与importinα3的结合依赖K36,为其核转运机制提供了分子解释,填补了PARP-2核定位机制研究的空白,为后续PARP-2功能调控研究奠定了基础。
3. 研究思路总结与详细解析
本研究的核心目标是明确PARP-2核定位的关键功能残基及依赖的核定位信号类型,核心科学问题是PARP-2的核定位是否依赖此前推测的双分型核定位信号,以及哪些残基介导其与核转运受体的结合;技术路线遵循“序列分析假设→定点突变构建突变体→亚细胞定位验证→相互作用实验验证→结论”的闭环逻辑,通过多层次实验明确了K36的关键作用。
3.1 PARP-2突变体构建与表达稳定性验证
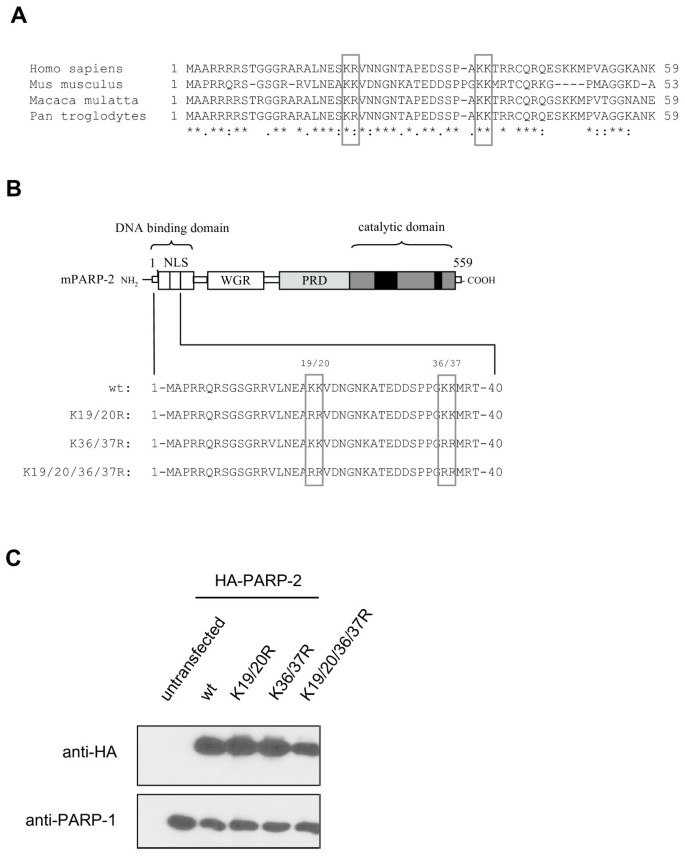
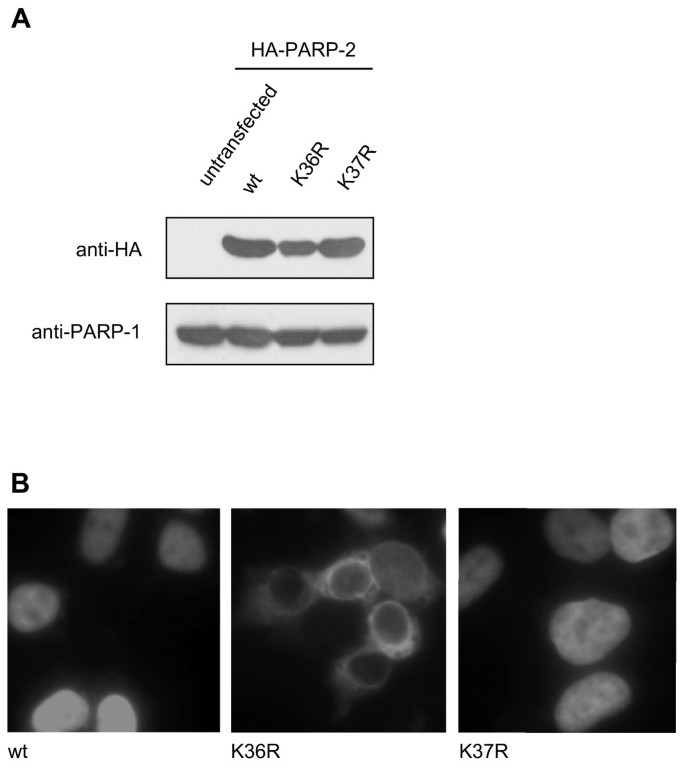
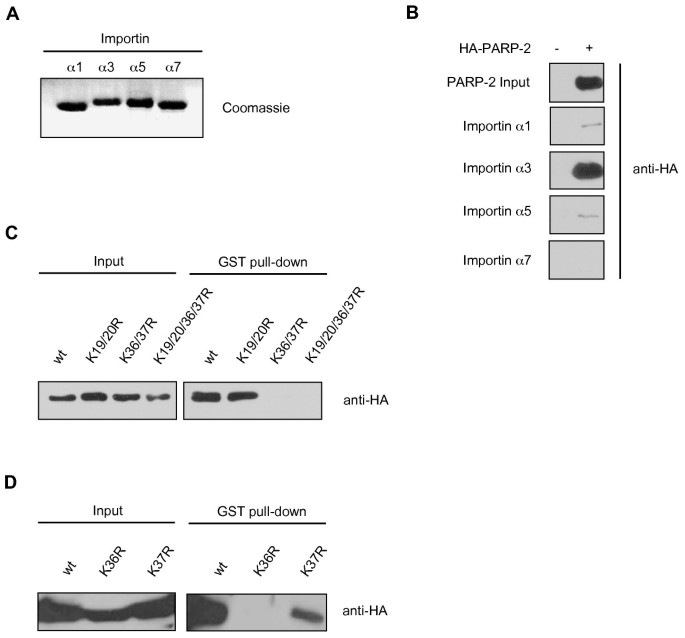
实验目的是构建PARP-2不同赖氨酸残基的突变体,排除突变对蛋白表达稳定性的影响,确保后续定位差异由核定位信号功能改变导致。方法细节:采用定点突变技术,将PARP-2氨基端的K19/20、K36/37分别突变为精氨酸(R)、谷氨酸(E)或甲硫氨酸(M),构建双突变体(K19/20R、K36/37R)、四突变体(K19/20/36/37R)及单突变体(K36R、K37R);将野生型及所有突变体构建为HA标签融合蛋白,在HEK293T细胞中瞬时转染表达,提取全细胞蛋白后通过免疫印迹检测蛋白表达水平,以内源PARP-1作为上样对照。结果解读:免疫印迹结果(图1C、图4A)显示,所有突变体的蛋白表达水平与野生型PARP-2相当,说明氨基酸突变未改变蛋白的稳定性,后续观察到的亚细胞定位差异并非由蛋白降解导致。产品关联:文献未提及具体实验产品,领域常规使用定点突变试剂盒、HA标签单克隆抗体、免疫印迹检测试剂、HEK293T细胞培养相关试剂等。
3.2 PARP-2突变体亚细胞定位与核转运通路分析
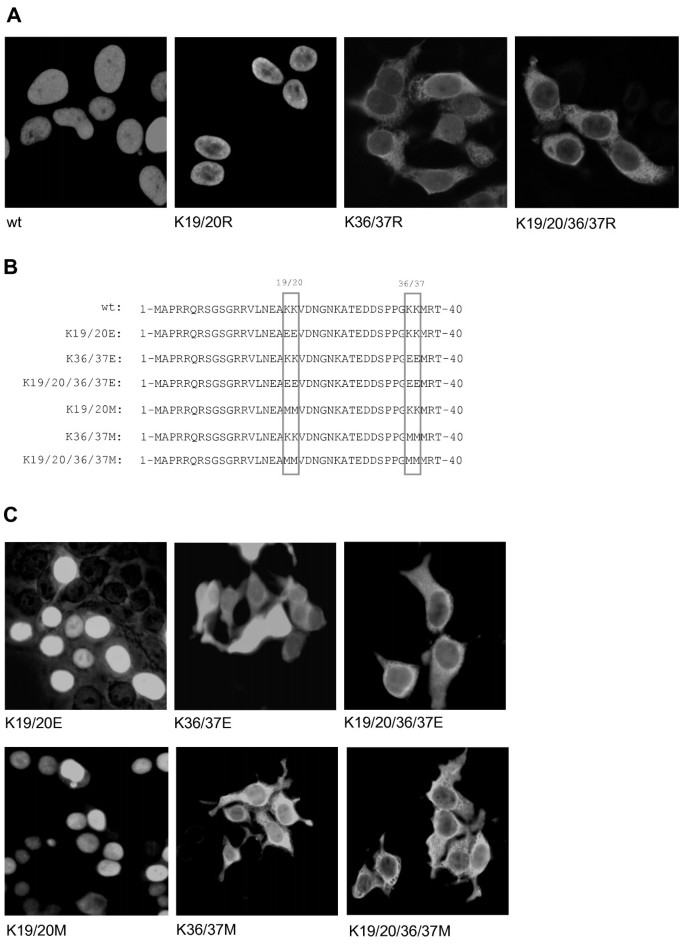
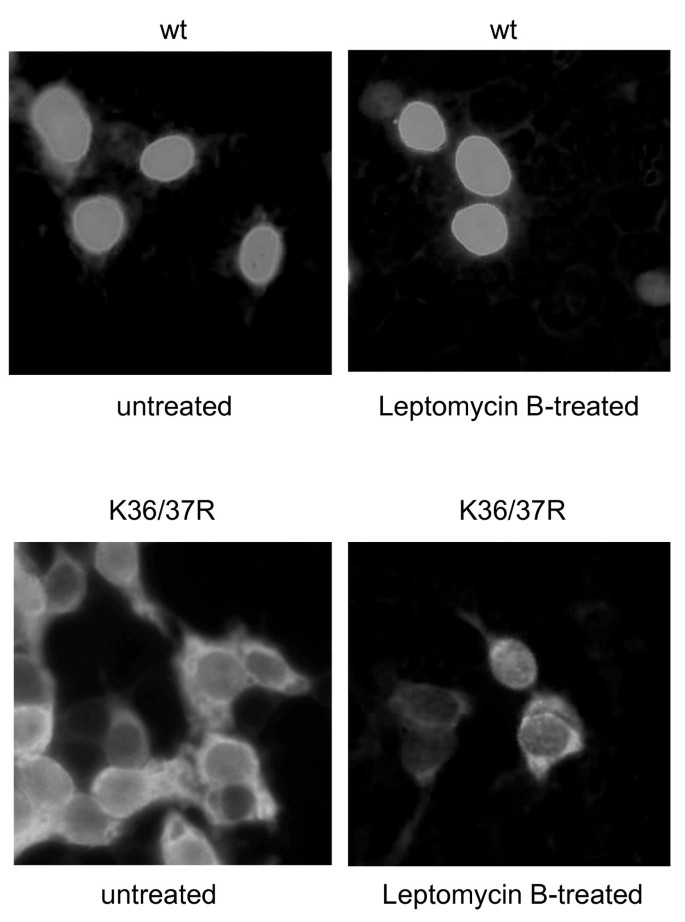
实验目的是明确哪些赖氨酸残基参与PARP-2的核定位,并区分核导入障碍与核出口增强导致的定位异常。方法细节:将野生型及突变体PARP-2转染至HEK293T细胞,甲醇固定后通过免疫荧光染色检测HA标签蛋白的亚细胞定位;同时对转染K36/37R突变体的细胞使用Leptomycin B(LMB)处理,LMB是CRM-1介导的核出口抑制剂,处理后观察定位变化以排除核出口影响。结果解读:免疫荧光结果(图2A、图4B)显示,野生型PARP-2与K19/20R突变体均定位于细胞核,而K36/37R、K19/20/36/37R突变体仅定位于细胞质;将K36/37突变为E或M时,同样导致PARP-2定位于细胞质,说明K36/37的功能并非依赖正电荷,而是氨基酸结构;LMB处理后K36/37R突变体仍定位于细胞质(图3),说明其定位异常是核导入障碍而非核出口增强;单突变体实验显示,K36R突变体定位于细胞质,K37R突变体定位于细胞核,明确K36是PARP-2核定位的关键残基。产品关联:实验所用关键产品:Leptomycin B(核出口抑制剂)、FITC标记的抗小鼠二抗、共聚焦显微镜;其余未提及产品为领域常规使用的免疫荧光染色试剂、细胞固定试剂等。
3.3 PARP-2与importinα家族蛋白的相互作用验证
实验目的是明确K36是否介导PARP-2与importinα的结合,从分子层面解释核定位障碍的机制。方法细节:采用GST pull-down实验,将人源importinα1、α3、α5、α7构建为GST融合蛋白并纯化;将纯化的GST-importinα与表达野生型或突变体PARP-2的HEK293T细胞裂解液孵育,通过谷胱甘肽琼脂糖珠捕获复合物,免疫印迹检测结合的PARP-2。结果解读:GST pull-down结果(图5B-D)显示,野生型PARP-2主要与importinα3结合,与importinα1、α5的结合极弱,不与importinα7结合;K36/37R、K36R突变体无法与importinα3结合,而K37R突变体与importinα3的结合能力与野生型相当,说明K36是PARP-2与importinα3结合的关键残基,这一结合缺失是K36R突变体无法入核的分子机制。产品关联:文献未提及具体实验产品,领域常规使用GST融合蛋白表达系统、谷胱甘肽琼脂糖珠、免疫印迹检测试剂等。
4. Biomarker研究及发现成果解析
本文中涉及的功能位点生物标志物为PARP-2的36位赖氨酸(K36),该残基是PARP-2核定位与核转运受体结合的关键功能位点,通过“生物信息学预测→细胞水平定位验证→分子相互作用验证”的完整逻辑链筛选与验证。
该功能位点属于蛋白核定位信号的核心残基,筛选逻辑为:首先通过序列分析预测PARP-2氨基端存在经典单分型核定位信号(包含K36),同时针对此前推测的双分型核定位信号(包含K19/20)构建突变体,通过亚细胞定位实验筛选出影响核定位的关键残基,再通过相互作用实验验证该残基与核转运受体的结合能力,明确其功能。
该功能位点来源于PARP-2的氨基端DNA结合域(1-69位氨基酸);验证方法包括细胞水平的免疫荧光亚细胞定位实验、核出口抑制剂处理实验,以及分子水平的GST pull-down相互作用实验;特异性方面,仅K36突变会导致PARP-2完全丧失核定位能力及与importinα3的结合能力,其他邻近赖氨酸残基突变无此效果;敏感性方面,K36的单一突变即可完全阻断PARP-2的核转运通路,实验结果具有高度一致性(n=3次独立重复实验,文献未明确P值)。
该功能位点的功能关联为,K36是PARP-2核定位的必需残基,其突变导致PARP-2滞留于细胞质,无法进入细胞核发挥基因组稳定性维持等生物学功能;创新性在于首次通过实验证实PARP-2的核定位依赖单分型经典核定位信号(包含K36),纠正了此前关于其为双分型核定位信号的推测,同时明确了PARP-2与importinα3的结合依赖K36,为PARP-2的核转运机制提供了直接分子证据;统计学结果方面,文献未提供定量统计数据,所有结果均为定性实验验证,且重复实验结果一致。
