1. 领域背景与文献引入
文献英文标题:A computational model of mutual antagonism in the mechano-signaling network of RhoA and nitric oxide;发表期刊:BMC Molecular and Cell Biology;影响因子:未公开;研究领域:细胞力学信号转导、细胞骨架调控
领域共识:Rho家族GTPases是细胞骨架收缩性的核心调控因子,一氧化氮(NO)是细胞松弛的关键信号分子,二者的信号通路在血管内皮细胞、成纤维细胞等多种细胞类型中存在拮抗作用。领域发展关键节点包括:1990年代RhoA的细胞骨架调控功能被明确,1998年NO作为信号分子的研究获诺贝尔生理学或医学奖,2010年代后系统生物学方法开始应用于信号通路的网络调控研究。当前研究热点聚焦于信号通路的高阶调控基序(如相互拮抗、正反馈)与细胞行为(如迁移、极性建立)的关联,未解决的核心问题是RhoA与NO的双向拮抗是否在同一细胞系统中共存,以及这种相互作用的系统级功能意义,现有研究多聚焦单个方向的拮抗机制,缺乏系统级的整合分析。
针对上述空白,本研究首先在非高NO、非高收缩性的上皮细胞系中验证RhoA与NO的双向拮抗,进而构建包含力学张力反馈的计算模型,分析其双稳态潜力,为细胞骨架重塑和迁移过程中的信号域自组织提供理论基础。
2. 文献综述解析
作者从信号通路相互作用的方向、系统级调控的研究现状两个维度梳理领域内研究,明确现有研究的局限性与本研究的创新定位。
现有研究的关键结论显示,RhoA/ROCK通路通过多种机制抑制内皮型一氧化氮合酶(eNOS)/NO通路,包括降低eNOS mRNA稳定性、抑制Akt磷酸化从而减少eNOS激活;而NO/cGMP/蛋白激酶G(PKG)通路则通过磷酸化RhoA的Ser188位点,阻止其向膜转运并促进与RhoGDI结合,从而抑制RhoA活性。技术方法上,单个分子机制的验证实验(如基因敲低、抑制剂处理)具有明确的靶向性,能精准定位单个作用节点,但局限性在于多数研究仅聚焦单一方向的拮抗,且分别在高NO的血管内皮细胞或高收缩性的成纤维细胞中开展,缺乏同一细胞系中双向拮抗的验证,同时未从系统层面分析这种相互作用的动态行为(如双稳态)。
本研究的创新价值在于,首次在同一上皮细胞系中验证RhoA与NO的双向拮抗,填补了不同细胞系研究的割裂空白;并构建包含力学张力反馈的计算模型,首次从系统层面证明该相互拮抗网络具有鲁棒的双稳态特性,为细胞行为的系统级调控提供新的理论视角。
3. 研究思路总结与详细解析
本研究采用“实验验证→理论建模→扩展分析”的闭环逻辑,先通过细胞实验确认上皮细胞中RhoA与NO的双向拮抗,再构建无张力的计算模型分析双稳态潜力,最后加入力学张力反馈扩展模型,验证双稳态的鲁棒性,最终得出该双稳态系统值得进一步实验验证的结论。
3.1 上皮细胞中RhoA与NO双向拮抗的实验验证
实验目的是确认同一非特殊细胞系中存在RhoA与NO的双向拮抗作用,避免之前研究的细胞类型特异性局限。方法细节为选用Madin-Darby犬肾(MDCK)上皮细胞系,分别采用两种抑制剂处理:用L-NG-硝基精氨酸甲酯(L-NAME)抑制组成型一氧化氮合酶(cNOS)以减少内源性NO生成,用Y-27632抑制ROCK以阻断RhoA下游信号;通过免疫印迹(Western blot)检测关键蛋白的磷酸化水平,实验重复三次(n=3)。
结果解读:如图1所示,
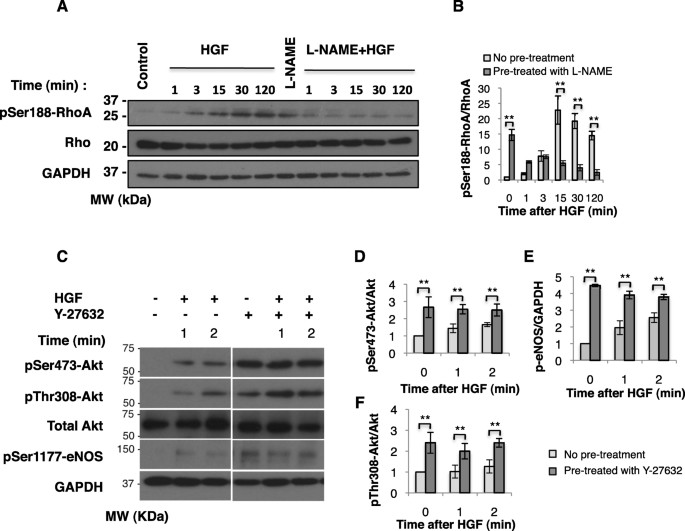
,L-NAME预处理后,肝细胞生长因子(HGF)无法诱导RhoA Ser188位点的磷酸化,说明NO是HGF诱导RhoA磷酸化的必要条件,即NO通路参与抑制RhoA;Y-27632处理后,Akt Ser473、Thr308位点及eNOS的磷酸化水平显著升高(P<0.005,n=3),说明ROCK通路抑制Akt/eNOS的激活,即RhoA通路参与抑制NO生成。
产品关联:实验所用关键产品:Sigma的L-NAME、Y-27362、HGF;免疫印迹实验所用抗体未明确品牌,领域常规使用Cell Signaling Technology等品牌的磷酸化特异性抗体。
3.2 无张力RhoA-NO信号网络计算模型构建与双稳态分析
实验目的是在无力学张力的情况下,分析RhoA-NO相互拮抗网络的动态行为,判断其是否具有双稳态潜力。方法细节为基于已知的生化反应构建计算模型,包含31个生产/消耗反应、11个控制方程,采用Matlab软件进行模拟,通过参数空间搜索、随机初始条件模拟、分岔分析、单参数鲁棒性分析等方法评估双稳态特性。
结果解读:如图2所示,
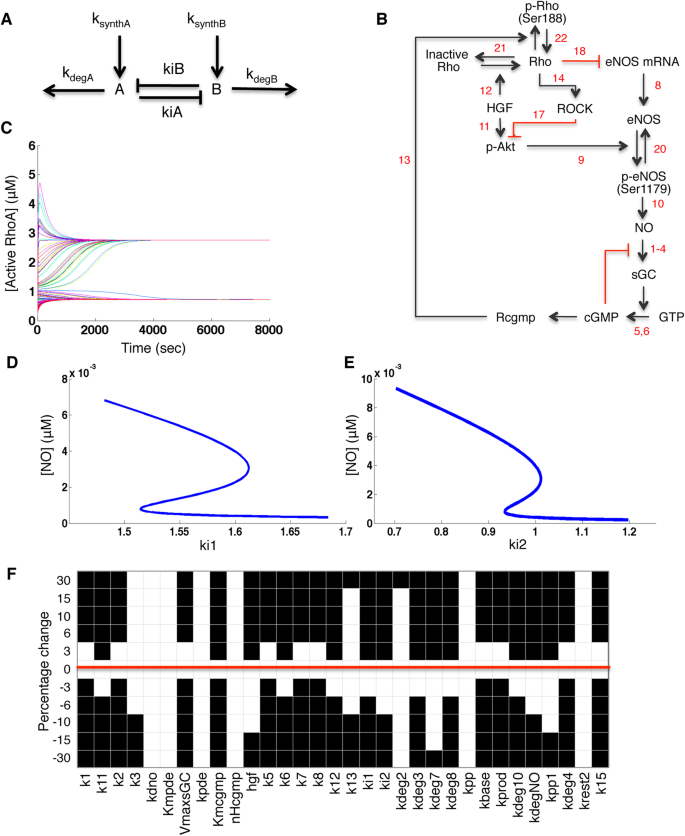
,随机初始条件模拟显示模型可收敛到两个不同的稳态(RhoA高浓度和低浓度),说明无张力模型具有双稳态潜力;但鲁棒性分析显示,多数参数仅需小幅度扰动(如5%)就会导致双稳态消失,说明该模型的双稳态鲁棒性较差。
产品关联:文献未提及具体计算工具版本,领域常规使用Matlab R2020及以上版本、Matcont分岔分析工具。
3.3 含力学张力反馈的扩展模型构建与分析
实验目的是研究力学张力对RhoA-NO网络双稳态的影响,因为RhoA和NO均参与细胞骨架张力的调控,张力反馈可能增强网络的鲁棒性。方法细节为在无张力模型基础上加入细胞张力作为变量,扩展为包含12个控制方程的模型,重复上述模拟和分析方法,重点比较双稳态的范围与鲁棒性变化。
结果解读:如图3所示,
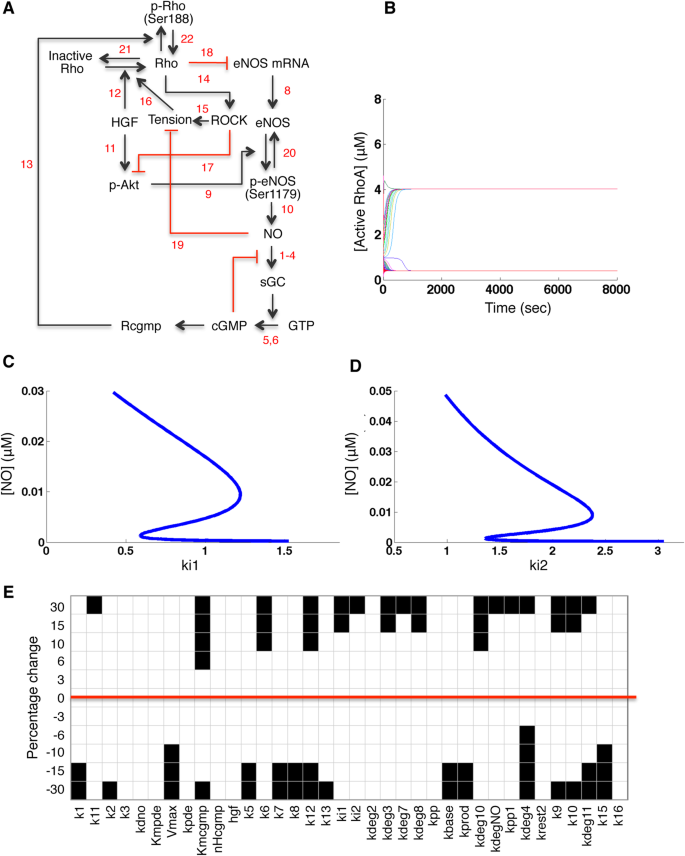
,随机初始条件模拟仍显示收敛到两个稳态,且收敛速度更快;分岔分析显示双稳态的参数范围扩大5倍,两个稳态间的NO浓度差增加5倍;鲁棒性分析显示,36个参数中有33个在10-15%的扰动下仍保持双稳态,仅3个参数(cGMP的Hill方程速率常数、ROCK的合成与降解速率常数)对双稳态影响较大,说明加入张力反馈后双稳态的鲁棒性显著提升。
如图4所示,
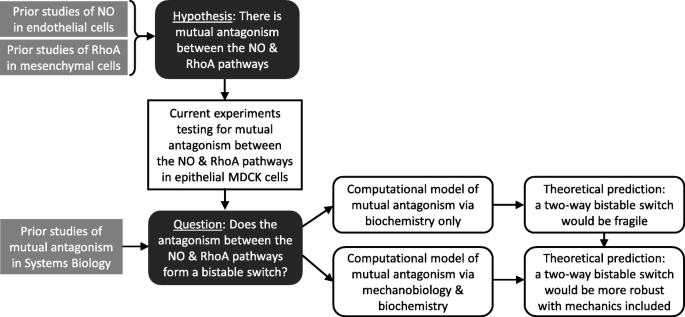
,该流程图清晰展示了本研究从实验验证到理论建模的完整逻辑,明确了当前研究在领域内的定位与贡献。
4. Biomarker研究及发现成果解析
本研究中的Biomarker为细胞内信号分子的功能状态(双稳态),通过实验验证与计算模型分析,明确其筛选/验证逻辑、功能关联与创新性。
Biomarker定位:类型为细胞内信号通路的双稳态功能状态,筛选/验证逻辑为“细胞实验验证双向拮抗→无张力模型验证双稳态潜力→扩展模型验证张力依赖的鲁棒性”,形成完整的逻辑链条。
研究过程详述:Biomarker的来源为细胞内RhoA与NO的信号分子浓度,实验验证方法为免疫印迹检测磷酸化水平以反映通路活性,理论验证方法为计算模型模拟动态变化;特异性与敏感性数据显示,实验中L-NAME处理后RhoA磷酸化水平显著降低(P<0.005,n=3),Y-27632处理后Akt/eNOS磷酸化水平显著升高(P<0.005,n=3);扩展模型中双稳态的NO浓度范围为1-30nM,与生理范围内的NO浓度(如小脑细胞中220nM)处于同一数量级。
核心成果提炼:该双稳态系统具有张力依赖的鲁棒性,可形成尖锐的浓度梯度,参与细胞骨架重塑和迁移过程中的信号域自组织;创新性在于首次在同一上皮细胞系中验证RhoA与NO的双向拮抗,构建包含力学张力的系统级模型,证明其双稳态的生物学可行性,为细胞行为的系统调控提供新的理论框架;统计学结果显示,实验数据均具有显著的统计学差异(P<0.005,n=3),模型分析的参数扰动范围具有明确的量化指标。推测:该双稳态系统的实验验证需依赖更精准的实时生物传感器(如RhoA活性传感器、NO动态检测探针),未来可通过活细胞成像技术进一步验证其在细胞迁移中的功能。
