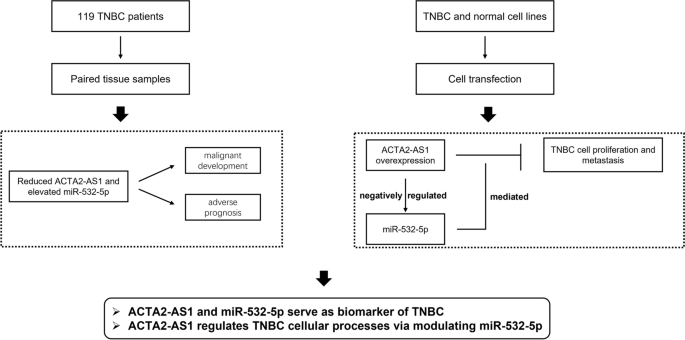
1. 领域背景与文献引入
文献英文标题:lncRNA ACTA2-AS1 predicts malignancy and poor prognosis of triple-negative breast cancer and regulates tumor progression via modulating miR-532-5p;发表期刊:BMC Molecular and Cell Biology;影响因子:未公开;研究领域:三阴性乳腺癌非编码RNA生物标志物与肿瘤调控机制研究。
领域共识:三阴性乳腺癌是乳腺癌中恶性程度最高的亚型,占所有乳腺癌病例的15%~20%,其5年生存率显著低于其他亚型,且因缺乏雌激素受体、孕激素受体及HER2的表达,现有内分泌治疗及靶向治疗方案均不适用,临床治疗选择有限。早期诊断是改善三阴性乳腺癌患者预后的关键,但目前临床主要依赖有创的针吸活检病理诊断,敏感性不足,导致多数患者确诊时已达晚期,出现远处转移。近年来,非编码RNA(包括长链非编码RNA lncRNA和微小RNA miRNA)作为肿瘤生物标志物及调控靶点的研究成为热点,其中ceRNA(内源竞争RNA)机制揭示了lncRNA通过吸附miRNA调控下游靶基因的作用模式,为肿瘤发生发展的研究提供了新方向。但现有研究中,lncRNA ACTA2-AS1和miR-532-5p在三阴性乳腺癌中的表达模式、临床意义及调控机制尚未明确,存在研究空白,因此本研究旨在明确两者在三阴性乳腺癌中的功能及生物标志物潜力,为临床诊疗提供新依据。
2. 文献综述解析
作者在综述部分以三阴性乳腺癌的临床诊疗困境为切入点,系统梳理了非编码RNA在肿瘤发生发展中的调控作用,重点聚焦lncRNA与miRNA的ceRNA调控网络在肿瘤预后预测及治疗中的应用价值。
现有研究已证实ACTA2-AS1在结肠癌、肺癌、胃癌等多种癌症中发挥抑癌或促癌作用,miR-532-5p在胶质瘤中为抑癌因子,在乳腺癌中则促进细胞增殖迁移,但两者在三阴性乳腺癌中的研究仍为空白。现有三阴性乳腺癌生物标志物研究多集中于单个非编码RNA,缺乏对lncRNA-miRNA调控对的联合分析,且多数研究仅停留在表达关联层面,缺乏功能验证及机制阐释。
通过对比现有研究的未解决问题,本研究的创新价值凸显:首次在大样本临床队列中验证了ACTA2-AS1与miR-532-5p的表达负相关性及与三阴性乳腺癌恶性进展、不良预后的关联,并通过细胞实验明确了两者的靶向调控关系及ACTA2-AS1通过miR-532-5p发挥抑癌作用的机制,弥补了现有研究在三阴性乳腺癌非编码RNA调控网络及联合生物标志物研究中的空白,为三阴性乳腺癌的早期诊断及预后预测提供了新的候选标志物。推测:扩大样本量开展多中心研究可进一步验证两者的临床应用价值。
3. 研究思路总结与详细解析
本研究整体遵循“临床样本验证-临床关联分析-细胞功能验证-机制阐释”的闭环研究逻辑,核心目标是明确ACTA2-AS1和miR-532-5p在三阴性乳腺癌中的生物标志物潜力及调控机制,核心科学问题为ACTA2-AS1是否通过靶向miR-532-5p调控三阴性乳腺癌细胞的恶性生物学行为。
3.1 临床样本收集与非编码RNA表达检测
本环节核心目标是检测ACTA2-AS1和miR-532-5p在三阴性乳腺癌组织中的表达水平及相关性。研究团队收集了119例初治三阴性乳腺癌患者的肿瘤组织及配对癌旁正常组织,采用实时荧光定量PCR(qRT-PCR)技术检测两种非编码RNA的相对表达量。结果显示,与癌旁组织相比,三阴性乳腺癌组织中ACTA2-AS1的表达显著下调,miR-532-5p的表达显著上调(n=119,P<0.001),且两者的表达水平呈显著负相关(相关系数r=-0.701,P<0.001)。
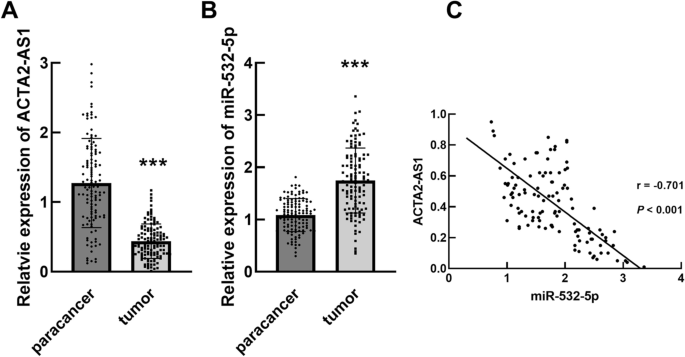
实验所用关键产品:Invitrogen的TRIzol总RNA提取试剂(货号15596018)、TIANGEN的lnRcute lncRNA第一链cDNA合成试剂盒(货号KR202)、miRcute miRNA第一链cDNA合成试剂盒(货号KR201)、Bio-Rad CFX96实时PCR检测系统。
3.2 临床病理特征与预后关联分析
本环节核心目标是明确ACTA2-AS1和miR-532-5p的表达与三阴性乳腺癌患者恶性程度及预后的关联。研究团队以两种非编码RNA的表达均值为界,将患者分为高表达组与低表达组,分析其与患者临床病理特征的相关性,并通过Kaplan-Meier生存分析、Cox多因素回归模型评估两者的预后价值。结果显示,低ACTA2-AS1表达与高miR-532-5p表达均与患者淋巴结转移阳性、高组织学分级、晚期TNM分期显著相关(P<0.05);生存分析显示,低ACTA2-AS1组患者总生存率显著低于高表达组(log rank P=0.034),高miR-532-5p组患者总生存率显著低于低表达组(log rank P=0.018);Cox多因素回归分析证实,ACTA2-AS1(风险比HR=3.247)、miR-532-5p(HR=3.214)与TNM分期、组织学分级、淋巴结转移状态均为三阴性乳腺癌患者的独立预后因素(P<0.05)。
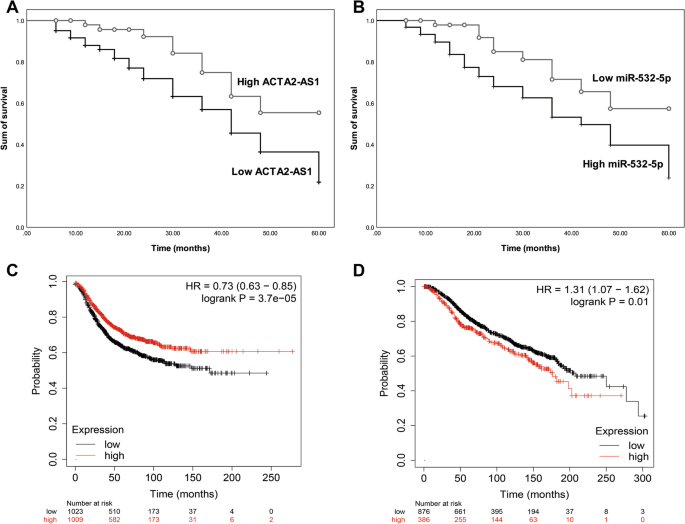
文献未提及具体实验产品,领域常规使用SPSS统计分析软件、Kaplan-Meier Plotter在线数据库。
3.3 细胞模型验证表达模式与靶向调控关系
本环节核心目标是在细胞水平验证ACTA2-AS1与miR-532-5p的表达模式及靶向结合关系。研究团队培养了4种三阴性乳腺癌细胞系(MDA-MB-231、HCC1937、Hs578t、BT-549)及正常乳腺上皮细胞系MCF-10A,采用实时荧光定量PCR检测两种非编码RNA的表达;同时构建ACTA2-AS1的野生型及突变型荧光素酶报告载体,通过双荧光素酶报告实验验证miR-532-5p与ACTA2-AS1的靶向结合。结果显示,与正常乳腺细胞相比,三阴性乳腺癌细胞中ACTA2-AS1表达显著下调,miR-532-5p表达显著上调(P<0.001);过表达miR-532-5p可显著抑制野生型ACTA2-AS1报告载体的荧光素酶活性,而对突变型载体无显著影响(P<0.001),证实两者存在靶向结合关系。
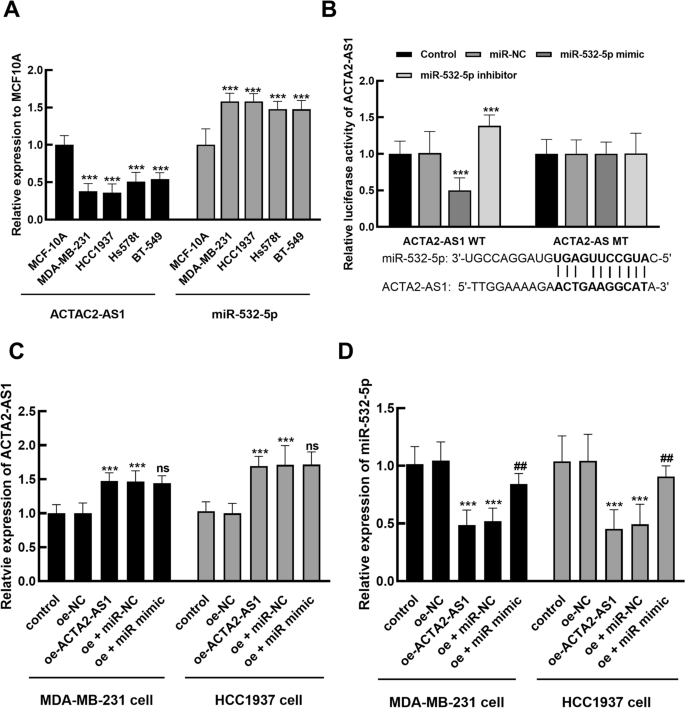
实验所用关键产品:ATCC的细胞系、Gibco的DMEM培养基(货号11995065)、Thermo Fisher Scientific的胎牛血清(FBS,货号10438034)、Promega的pmirGLO荧光素酶报告载体(货号E133A)、双荧光素酶报告检测系统、Invitrogen的Lipofectamine 2000转染试剂(货号11668019)。
3.4 细胞功能实验验证调控机制与生物学作用
本环节核心目标是验证ACTA2-AS1通过靶向miR-532-5p调控三阴性乳腺癌细胞的恶性生物学行为。研究团队通过细胞转染技术在MDA-MB-231和HCC1937细胞中过表达ACTA2-AS1,或同时过表达miR-532-5p,采用CCK-8实验检测细胞增殖能力,Transwell实验检测细胞迁移及侵袭能力。结果显示,过表达ACTA2-AS1可显著抑制三阴性乳腺癌细胞的增殖、迁移及侵袭能力(P<0.01),而同时过表达miR-532-5p可逆转ACTA2-AS1的抑癌作用,恢复细胞的增殖、迁移及侵袭能力(P<0.05),证实ACTA2-AS1通过靶向调控miR-532-5p发挥抑癌作用。
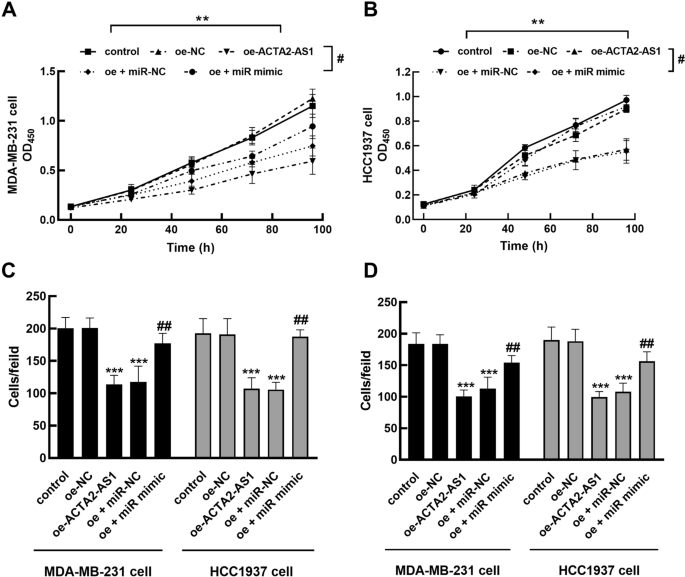
实验所用关键产品:Life Technologies的pcDNA3.1-ACTA2-AS1过表达载体、Dojindo的CCK-8细胞增殖检测试剂(货号CK04)、Corning的Matrigel基质胶(货号356234)。
4. Biomarker研究及发现成果
本研究鉴定的生物标志物为lncRNA ACTA2-AS1和miR-532-5p,两者构成的ceRNA调控对可作为三阴性乳腺癌恶性进展及预后的预测标志物。
Biomarker定位:ACTA2-AS1和miR-532-5p为三阴性乳腺癌的预后生物标志物,筛选及验证逻辑为“临床样本表达检测→临床病理特征关联→预后价值验证→细胞功能及机制验证”的完整链条。两者来源于三阴性乳腺癌患者的肿瘤组织,验证方法包括实时荧光定量PCR检测表达、卡方检验分析与临床病理特征的相关性、Kaplan-Meier生存分析及Cox多因素回归验证预后价值、双荧光素酶报告实验及细胞功能实验验证调控机制。
研究过程详述:在119例三阴性乳腺癌患者肿瘤组织中,ACTA2-AS1表达水平较癌旁组织显著下调,miR-532-5p表达水平显著上调,两者呈显著负相关(r=-0.701,P<0.001,n=119);低ACTA2-AS1表达与高miR-532-5p表达均与患者淋巴结转移、高组织学分级、晚期TNM分期显著相关(P<0.05);Cox多因素回归分析证实两者为独立预后因素,ACTA2-AS1的风险比为3.247,miR-532-5p的风险比为3.214(P<0.05);细胞实验证实ACTA2-AS1通过靶向结合miR-532-5p抑制三阴性乳腺癌细胞的增殖、迁移及侵袭。
核心成果提炼:本研究首次证实ACTA2-AS1和miR-532-5p可作为三阴性乳腺癌的预后生物标志物,两者联合检测可更精准地预测患者的恶性进展及预后;同时明确ACTA2-AS1作为抑癌lncRNA,通过ceRNA机制吸附miR-532-5p发挥调控作用,为三阴性乳腺癌的靶向治疗提供了新的潜在靶点。