1. 领域背景与文献引入
文献英文标题:Copine A, a calcium-dependent membrane-binding protein, transiently localizes to the plasma membrane and intracellular vacuoles in Dictyostelium;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:真核生物膜结合蛋白功能与细胞发育生物学
Copine家族是一类进化保守的可溶性钙依赖膜结合蛋白,广泛存在于除酵母外的多种真核生物中,其核心结构特征为N端包含两个钙依赖磷脂结合的C2结构域,C端包含一个与整合素中von Willebrand A(VWA)结构域同源的A结构域。领域共识:C2结构域通常介导蛋白与膜的钙依赖结合,VWA结构域参与蛋白-蛋白相互作用,因此Copine家族被推测在钙信号转导、膜运输等细胞过程中发挥作用。
现有研究已在拟南芥、秀丽隐杆线虫、哺乳动物等物种中开展Copine功能探索,发现其参与生长调控、细胞死亡、性腺发育、TNF-α信号通路调控等过程,但仍存在核心未解决问题:不同物种中Copine的功能存在差异,且缺乏在兼具单细胞生长与多细胞发育过程的模式生物中对其动态细胞定位的研究,难以明确其在发育过程中的时空功能。盘基网柄菌作为经典的真核模式生物,具有简单的发育分化过程和易于操作的遗传体系,为研究Copine的动态定位与功能提供了理想模型。本文针对这一研究空白,首次鉴定盘基网柄菌基因组中的Copine家族成员,并系统解析其中CpnA的发育表达模式、钙依赖膜结合特性及细胞内定位特征,为Copine家族的功能研究提供新的实验证据与模型系统。
2. 文献综述解析
作者以物种分类为核心维度,对拟南芥、秀丽隐杆线虫、哺乳动物中的Copine研究进行系统评述,明确现有研究的功能方向与局限性,凸显本研究的创新价值。
现有研究中,拟南芥Copine突变体实验表明,CPN1/BON1参与植物生长稳态调控,在低温下表现为微型化表型,低湿度下出现细胞死亡异常与抗病性增强;秀丽隐杆线虫中nem-4编码的Copine可拮抗GON-2阳离子通道,调控性腺细胞分裂;哺乳动物研究则通过酵母双杂交与体外pull-down实验,发现Copine可通过A结构域结合信号通路蛋白,并依赖C2结构域将靶蛋白招募至膜上,参与TNF-α受体信号调控。这些研究的技术方法优势在于利用基因敲除/敲降、蛋白互作分析等手段明确了Copine的部分功能通路,但局限性在于:多数研究聚焦于静态功能验证,缺乏对Copine在活细胞内动态定位的观察;不同物种的功能结论难以统一,且未在兼具单细胞与多细胞发育的模式生物中开展系统研究,无法揭示Copine在发育过程中的时空功能变化。
本文通过在盘基网柄菌中开展研究,填补了这一空白:首次在该模式生物中鉴定出6个Copine家族基因,突破了现有研究仅针对单一物种的局限;通过GFP标记结合活细胞成像,首次观察到Copine在饥饿细胞中的瞬时振荡膜定位,为其参与钙信号动态调控提供了直接细胞生物学证据;同时通过固定细胞免疫荧光实验,明确了Copine与收缩泡、内溶酶体、吞噬体等细胞器的关联,为其参与膜运输的功能推测提供了结构基础。
3. 研究思路总结与详细解析
本研究以“鉴定盘基网柄菌Copine家族→解析CpnA的表达与膜结合特性→观察CpnA的细胞内动态定位→鉴定结合的细胞器”为闭环技术路线,核心研究目标是明确CpnA在盘基网柄菌中的表达模式与细胞定位,为Copine功能研究提供实验依据。
3.1 Copine家族基因鉴定与序列分析
本环节实验目的是确定盘基网柄菌基因组中Copine家族的成员数量与序列特征。方法细节为:以人类Copine I的cDNA序列为探针,搜索盘基网柄菌cDNA与基因组数据库,克隆并测序获得cpnA与cpnB的全长cDNA,进一步通过序列比对预测出另外4个Copine基因(cpnC-F),采用Clustal V方法对6个Copine的氨基酸序列进行比对分析。结果解读:6个Copine基因均具有Copine家族的典型结构,即N端两个C2结构域与C端A结构域,氨基酸序列同源性为28%-60%;其中CpnA具有独特的长C端序列,CpnE具有独特的长N端序列,提示不同Copine成员可能具有功能特异性(对应图1)。产品关联:文献未提及具体实验产品,领域常规使用生物信息学分析工具(如BLAST、Clustal)、基因克隆与测序试剂。

3.2 CpnA发育表达模式检测
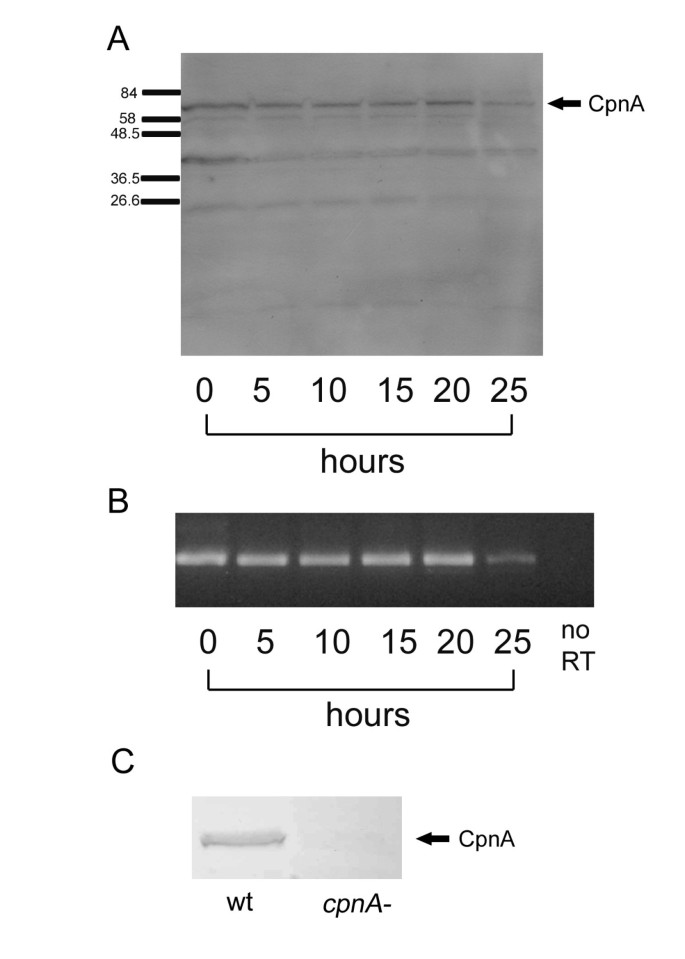
本环节实验目的是分析CpnA在盘基网柄菌发育过程中的表达变化。方法细节为:将野生型NC4A2细胞置于饥饿缓冲液中,在滤纸上进行25小时的发育培养,每5小时收集细胞样本,采用Western blot(抗CpnA多克隆抗体)检测蛋白表达水平,采用RT-PCR检测cpnA mRNA的表达情况。结果解读:Western blot结果显示,CpnA蛋白(分子量约66kDa)在整个发育阶段均有表达,营养细胞(0小时)与20小时(即将进入子实体形成阶段)的表达水平略高,25小时(成熟子实体阶段)表达水平略低;RT-PCR结果显示cpnA mRNA在各发育阶段均持续存在,表明CpnA在盘基网柄菌的整个生命周期中发挥功能(对应图2)。产品关联:实验所用关键产品:抗CpnA多克隆抗体、RT-PCR试剂盒、PVDF膜、ECL化学发光底物。
3.3 CpnA钙依赖膜结合特性验证
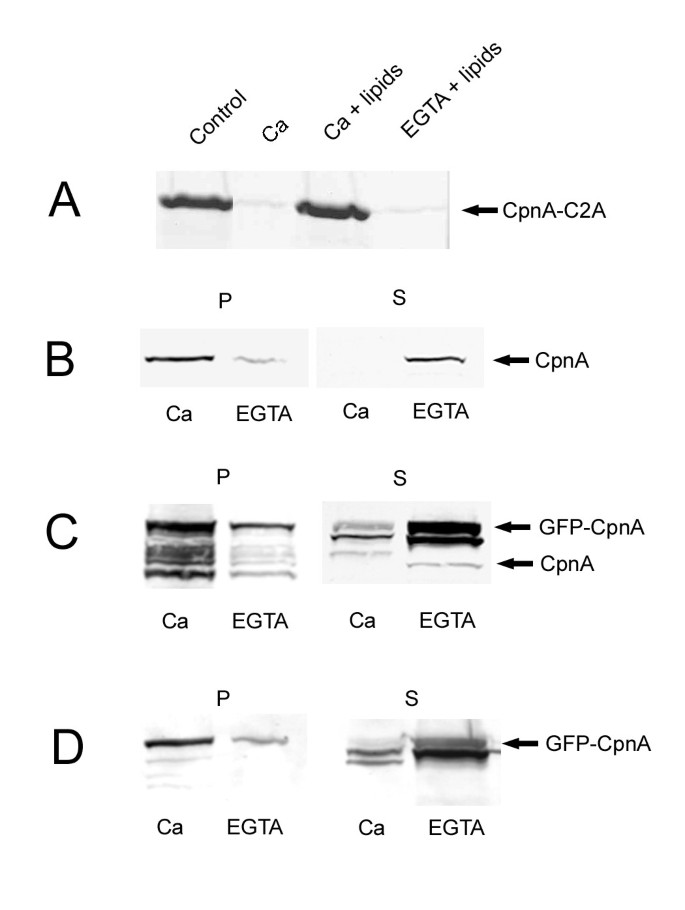
本环节实验目的是验证CpnA的钙依赖膜结合能力。方法细节分为两部分:一是体外磷脂结合实验:通过原核表达系统表达并纯化CpnA的第一个C2结构域(CpnA-C2A),将其与牛脑脂质体在2mM钙或2mM EGTA(钙螯合剂)存在下孵育,离心分离脂质体沉淀与上清,采用SDS-PAGE分析CpnA-C2A的分布;二是细胞内膜结合实验:将野生型细胞与GFP-CpnA表达细胞通过French Press破碎,在钙或EGTA存在下,通过差速离心分离膜组分与上清,采用Western blot检测内源性CpnA与GFP-CpnA的分布。结果解读:体外实验显示,CpnA-C2A在钙存在下与脂质体共沉淀,EGTA存在下几乎不进入沉淀;细胞内实验显示,内源性CpnA与GFP-CpnA在钙存在下主要存在于膜组分,EGTA存在下主要存在于上清,证明CpnA具有钙依赖的膜结合特性,且GFP标记不影响其膜结合功能(对应图3)。产品关联:文献未提及具体实验产品,领域常规使用原核表达载体、脂质体制备试剂、Western blot相关抗体与试剂。
3.4 GFP-CpnA活细胞动态定位观察
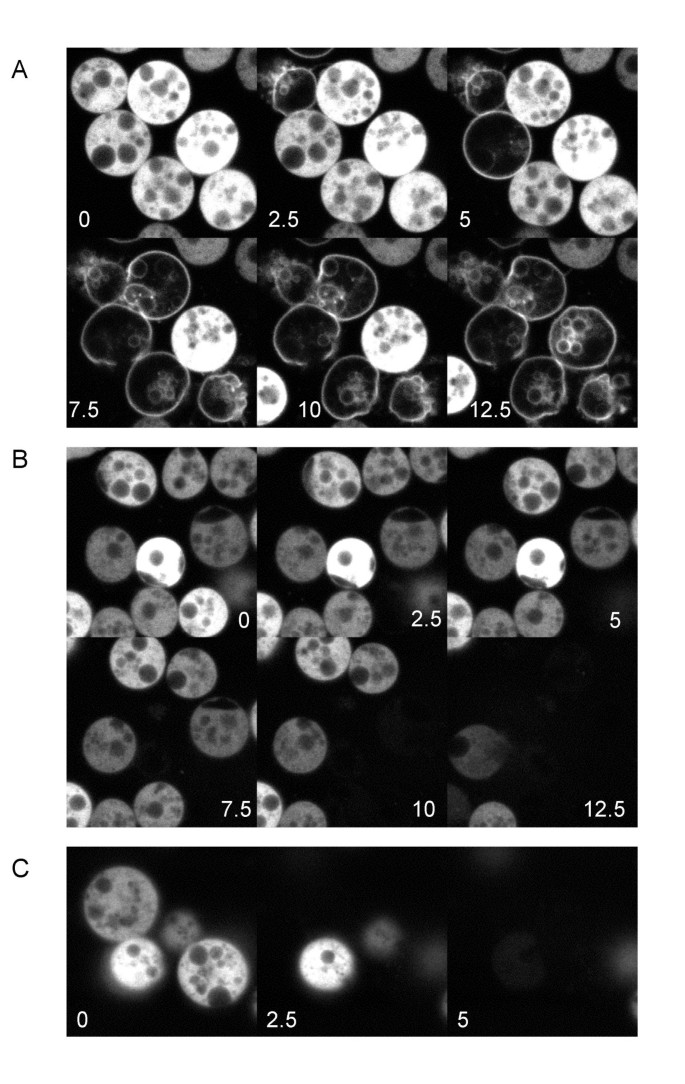
本环节实验目的是观察CpnA在活细胞内的动态定位变化。方法细节为:构建N端融合GFP的CpnA表达载体,通过电穿孔转化野生型盘基网柄菌细胞,筛选获得稳定表达GFP-CpnA的细胞株;分别在营养细胞与饥饿细胞中,采用激光共聚焦显微镜每隔2.5秒进行成像观察。结果解读:营养细胞中,GFP-CpnA均匀分布于细胞质,无明显膜定位;饥饿3-4小时后,部分细胞(每100个细胞中1-4个)出现GFP-CpnA瞬时(通常1-10秒)定位到质膜与细胞内液泡的现象,且部分细胞中该定位呈现振荡式多次发生;饥饿时间延长至8-10小时后,定位持续时间可延长至1-30秒,且部分聚集细胞中可观察到不同细胞先后出现该定位(对应图4)。产品关联:实验所用关键产品:GFP融合表达载体、激光共聚焦显微镜。

3.5 破碎细胞中GFP-CpnA膜结合的钙依赖性验证
本环节实验目的是验证活细胞破碎后GFP-CpnA膜结合的钙依赖性。方法细节为:将GFP-CpnA表达细胞分别置于水或含2mM EGTA的水中,采用100%功率激光扫描导致细胞膜破裂,通过共聚焦显微镜观察GFP的定位变化。结果解读:水中的细胞破裂后,GFP-CpnA仍结合于质膜与细胞内液泡;而含EGTA的水中,细胞破裂后GFP-CpnA扩散至胞外,无膜结合现象,证明GFP-CpnA与膜的结合依赖于钙离子(对应图5)。产品关联:文献未提及具体实验产品,领域常规使用钙螯合剂EGTA、激光共聚焦显微镜。
3.6 固定细胞中GFP-CpnA结合的细胞器鉴定
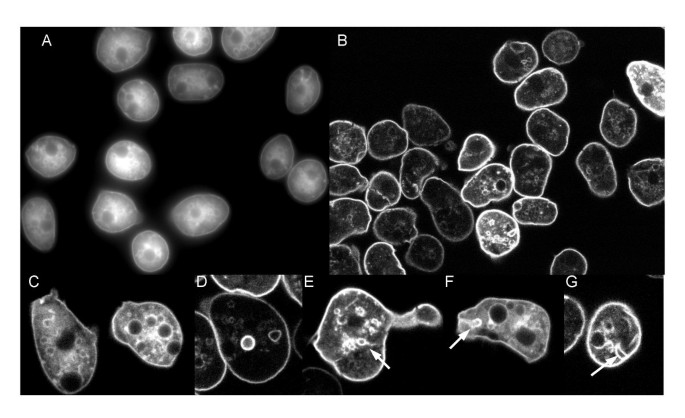
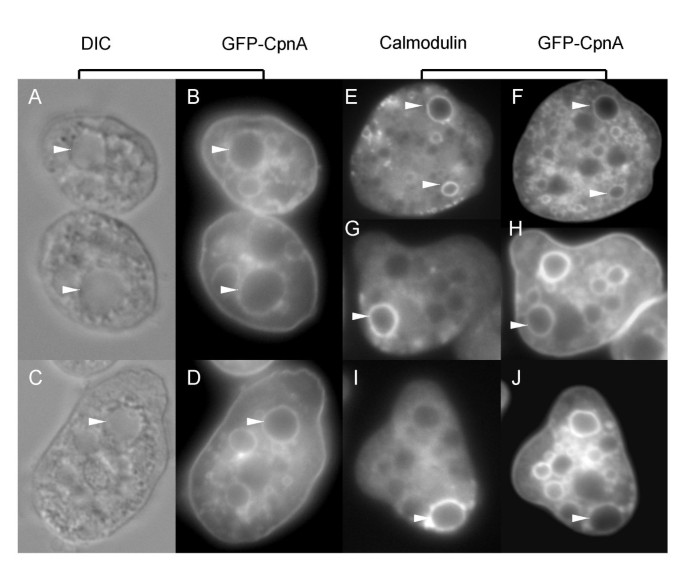
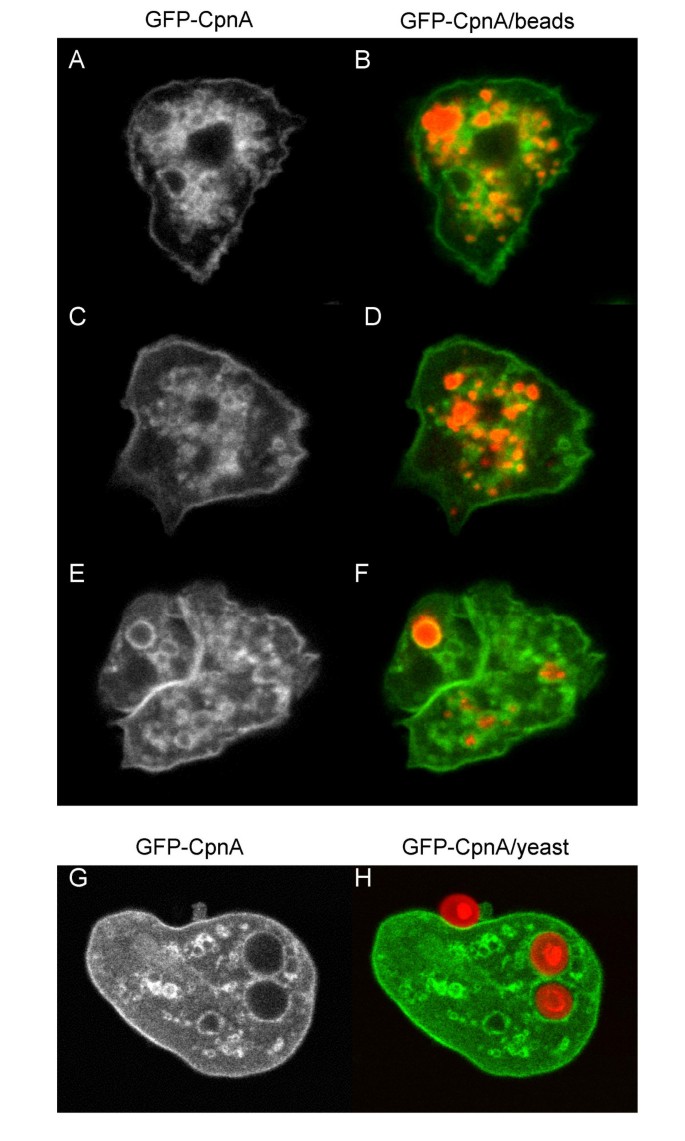
本环节实验目的是明确GFP-CpnA结合的具体细胞器类型。方法细节分为三部分:一是收缩泡鉴定:将细胞置于水中1.5分钟使收缩泡膨大,固定后采用钙调素单克隆抗体进行免疫荧光标记,通过共聚焦显微镜观察GFP与TRITC标记的钙调素的共定位;二是内溶酶体鉴定:将细胞与红色荧光纳米珠共孵育2小时,使纳米珠进入内溶酶体途径,固定后观察GFP与红色荧光的共定位;三是吞噬体鉴定:将细胞与Alexa Fluor-594标记的酵母共孵育1小时,使细胞吞噬酵母,固定后观察GFP与红色荧光的共定位。结果解读:GFP-CpnA与钙调素标记的收缩泡完全共定位,与红色纳米珠标记的内体、溶酶体共定位,且围绕吞噬的酵母细胞分布于吞噬体膜上,证明CpnA可定位于收缩泡、内溶酶体系统细胞器与吞噬体(对应图6、7、8)。产品关联:实验所用关键产品:钙调素单克隆抗体、TRITC标记山羊抗小鼠二抗、红色荧光纳米珠、Alexa Fluor-594标记酵母。
4. Biomarker研究及发现成果
本文中CpnA作为盘基网柄菌发育过程中的钙响应性膜结合蛋白,可作为研究Copine家族功能与发育分化的关键分子标志物,其筛选与验证逻辑为“生物信息学鉴定→发育表达分析→钙依赖膜结合验证→细胞定位与细胞器关联”。
CpnA的来源为盘基网柄菌细胞,验证方法包括:通过Western blot与RT-PCR验证其在整个发育阶段的持续表达;通过体外与细胞内实验验证其钙依赖膜结合特性;通过GFP活细胞成像与固定细胞免疫荧光验证其动态定位与细胞器关联。特异性方面,CpnA仅在饥饿诱导的部分细胞中出现瞬时膜定位,且定位于特定细胞器;敏感性方面,其膜定位响应细胞内钙浓度变化,在钙存在下快速结合膜,钙被螯合后脱离膜(文献未明确提供该数据,基于图表趋势推测)。
核心成果方面,CpnA的功能关联推测为:参与收缩泡的渗透调节功能、内溶酶体系统的膜运输过程及吞噬体的形成与成熟;创新性在于首次在盘基网柄菌中鉴定Copine家族并揭示CpnA的动态定位模式,为Copine参与钙信号调控与发育分化提供了直接证据。研究推测,CpnA在饥饿细胞中的瞬时振荡膜定位可能与细胞内快速钙波有关,且可能参与柄细胞的分化过程,但该结论需进一步通过基因敲除实验验证(文献未明确提供相关统计学数据)。
