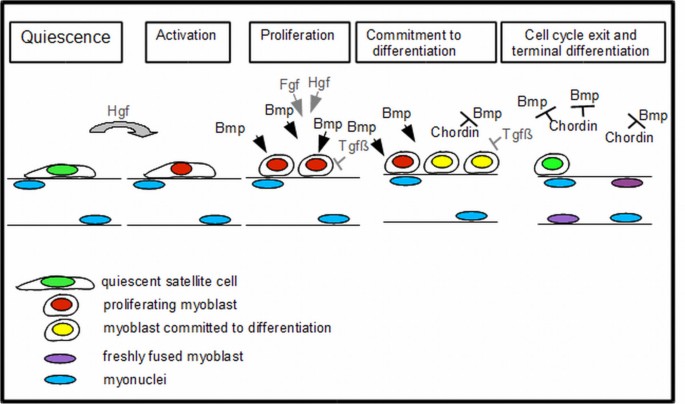
1. 领域背景与文献引入
文献英文标题:BMP signaling balances proliferation and differentiation of muscle satellite cell descendants;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:骨骼肌再生与干细胞生物学。
成体骨骼肌具有强大的生长和损伤再生能力,这一过程完全依赖于肌纤维基底膜下的卫星细胞——一类成体干细胞。1961年Mauro首次发现卫星细胞,后续研究逐渐明确其激活、增殖、分化的调控网络,涉及肝细胞生长因子(HGF)、成纤维细胞生长因子(FGF)、转化生长因子β(TGFβ)等多条信号通路。当前领域研究热点聚焦于卫星细胞命运决定的精细调控机制,尤其是不同信号通路之间的协同与拮抗作用。然而,骨形态发生蛋白(Bone Morphogenetic Protein,BMP)信号在成体卫星细胞分化中的具体作用仍存在争议:此前在永生化肌源性C2C12细胞系中的研究显示BMP信号会诱导细胞向成骨分化,但原代卫星细胞对BMP信号的响应机制尚未明确,且BMP信号在体内肌肉再生过程中的功能也缺乏系统验证,这一空白限制了对肌再生调控网络的全面理解。
结合领域现状,本研究旨在明确BMP信号在原代卫星细胞增殖分化及体内肌肉再生中的调控作用,揭示其平衡增殖与分化的分子机制,为肌再生的临床干预提供理论基础。
2. 文献综述解析
作者以细胞模型差异(永生化细胞系vs原代干细胞)、实验体系维度(体外培养vs体内生理再生)为核心分类逻辑,系统梳理了BMP信号在肌发生领域的研究进展,对比了不同研究体系的结论差异,进而凸显本研究的创新价值。
现有研究中,针对C2C12细胞系的实验证实BMP信号可抑制肌向分化并诱导成骨转分化,这一结论成为早期BMP信号与肌发生研究的核心认知;胚胎肌发生领域的研究则表明BMP信号调控肌前体细胞的增殖与分化,通过与Noggin的负反馈机制维持肌发生的动态平衡。这些研究的技术方法优势在于C2C12细胞系易培养、实验重复性高,胚胎模型能揭示发育过程中的调控规律,但局限性也十分明显:C2C12细胞系是永生化细胞,与原代卫星细胞的生理状态存在显著差异,无法完全反映成体肌再生的真实情况;同时,此前的研究未系统探究BMP信号在成体卫星细胞中的作用,也缺乏体内损伤模型的验证,导致对成体肌再生中BMP信号功能的认知存在缺失。
本研究的创新价值在于突破了传统细胞系研究的局限性,首次明确原代卫星细胞在BMP信号作用下不会向成骨分化,而是维持增殖状态;揭示了BMP信号通过诱导Chordin表达的负反馈机制平衡卫星细胞的增殖与分化;并在体内肌肉损伤模型中验证了BMP信号的功能,填补了成体肌再生中BMP信号调控机制的研究空白,为肌发生领域的信号网络研究提供了新的视角。
3. 研究思路总结与详细解析
本研究的整体研究目标是明确BMP信号在卫星细胞增殖分化及体内肌肉再生中的调控作用,核心科学问题是BMP信号如何通过分子机制平衡卫星细胞的增殖与分化,技术路线遵循“细胞系初步验证→原代细胞机制探究→体内模型功能验证”的闭环逻辑,从体外到体内系统解析BMP信号的调控功能。
3.1 C2C12细胞系中BMP信号对肌分化的调控验证
实验目的:初步探究BMP信号对肌向分化的影响,对比其在肌源性细胞系中对肌分化与成骨分化的调控差异。
方法细节:将C2C12细胞以2×10^4个/cm²的密度接种,培养24小时后换用含2%马血清的分化培养基,同时添加100ng/ml Bmp7或125ng/ml Noggin,每日更换培养基及生长因子;处理3天后,通过免疫组化检测肌球蛋白重链(Myosin Heavy Chain,MHC)表达以评估肌分化,碱性磷酸酶活性检测评估成骨分化,BrdU掺入实验检测细胞增殖,Cleaved Caspase3免疫染色检测细胞凋亡。
结果解读:免疫组化结果显示,Bmp7处理后MHC阳性细胞比例从对照组的5%降至0.5%(n=6,P<0.005),肌向分化显著受抑制;碱性磷酸酶活性检测显示Bmp7处理组出现阳性细胞,而对照组和Noggin处理组无阳性信号,说明BMP信号诱导C2C12细胞向成骨分化。BrdU掺入实验显示Bmp7处理组S期细胞比例从11%升至15%(n=6,P<0.05),细胞增殖增强;Cleaved Caspase3染色显示Bmp7处理组凋亡细胞显著减少,说明BMP信号同时抑制细胞凋亡。Noggin处理则呈现相反效应,MHC阳性细胞比例升至8%(n=6,P<0.005),肌分化增强,无成骨分化,增殖减弱。
产品关联:实验所用关键产品:R&D systems的Bmp7、Noggin;Cell Signaling Technologies的抗Cleaved Caspase-3抗体;DSHB的抗MHC抗体(clone A4.1025)。
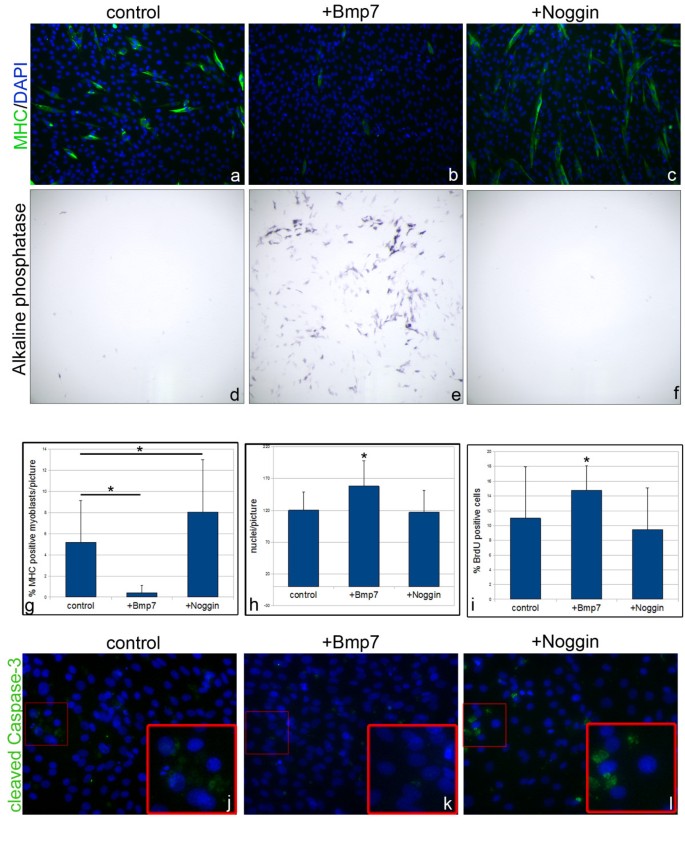
3.2 原代卫星细胞对BMP信号的响应分析
实验目的:明确原代卫星细胞在激活过程中对BMP信号的响应模式,以及BMP信号对卫星细胞标记物Pax7表达的调控作用。
方法细节:分离小鼠趾长伸肌(EDL)的单肌纤维,培养0、24、48、72小时,通过双重免疫荧光染色检测Pax7(静息/激活卫星细胞标记)、MyoD(激活/增殖卫星细胞标记)、Myogenin(分化启动标记)与磷酸化Smad1/5/8(p-Smad1/5/8,BMP信号激活标记)的核定位;同时将肌纤维置于无血清培养基中培养18小时,添加100ng/ml Bmp7,通过荧光强度定量分析Pax7的表达水平。
结果解读:新鲜分离的静息卫星细胞仅表达Pax7,无p-Smad1/5/8信号(n>50);培养24、48小时后,卫星细胞激活并表达Pax7与MyoD,同时p-Smad1/5/8信号阳性,说明激活的卫星细胞响应BMP信号;培养72小时后,部分细胞开始表达Myogenin,且与p-Smad1/5/8共定位,提示分化启动阶段的细胞仍可响应BMP信号。无血清条件下,未添加Bmp7的肌纤维上卫星细胞的Pax7荧光强度降至对照组的50%(n=30,P=0.005),而Bmp7处理组Pax7表达维持在高水平,说明BMP信号可直接维持卫星细胞中Pax7的表达。
产品关联:实验所用关键产品:DSHB的抗Pax7抗体;Santa Cruz的抗MyoD抗体;DAKO cytomation的抗Myogenin抗体;Cell Signaling Technologies的抗p-Smad1/5/8抗体。
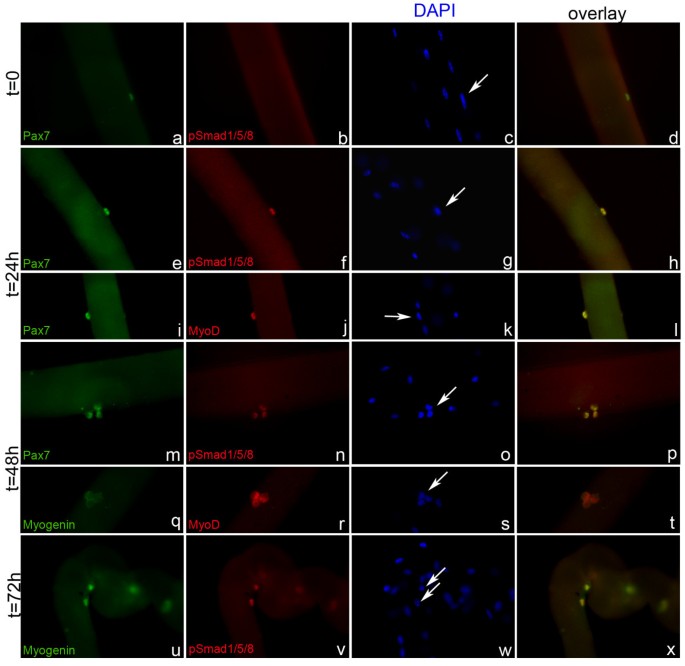
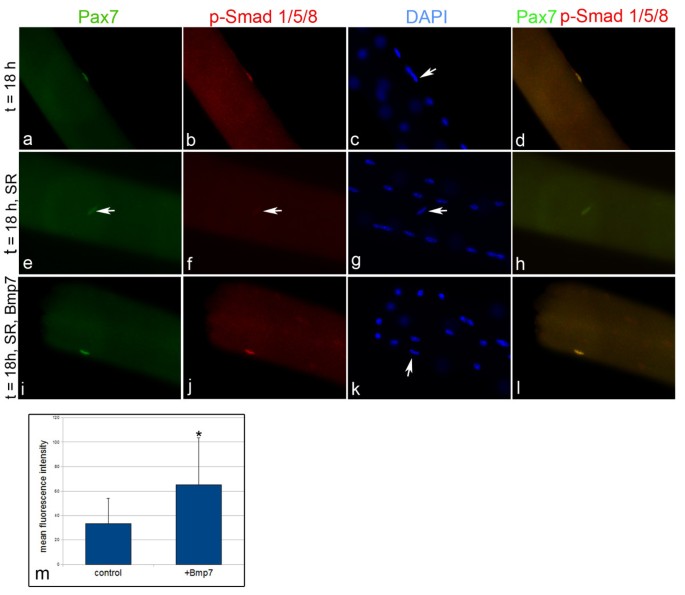
3.3 BMP信号对原代卫星细胞分化的调控机制
实验目的:明确BMP信号对原代卫星细胞分化的具体影响,验证原代细胞是否会像C2C12细胞一样向成骨分化,并探究其对细胞周期退出的调控作用。
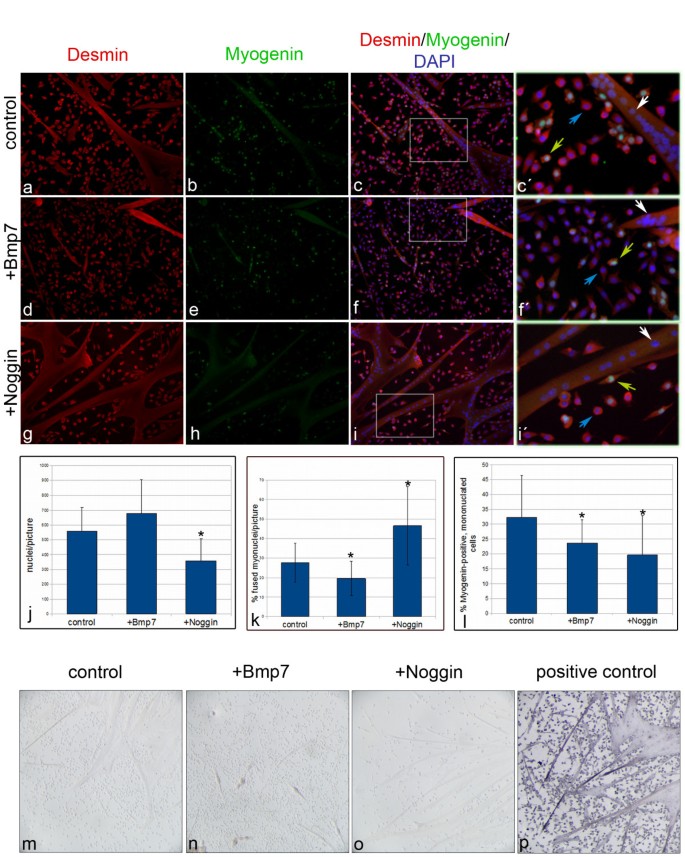
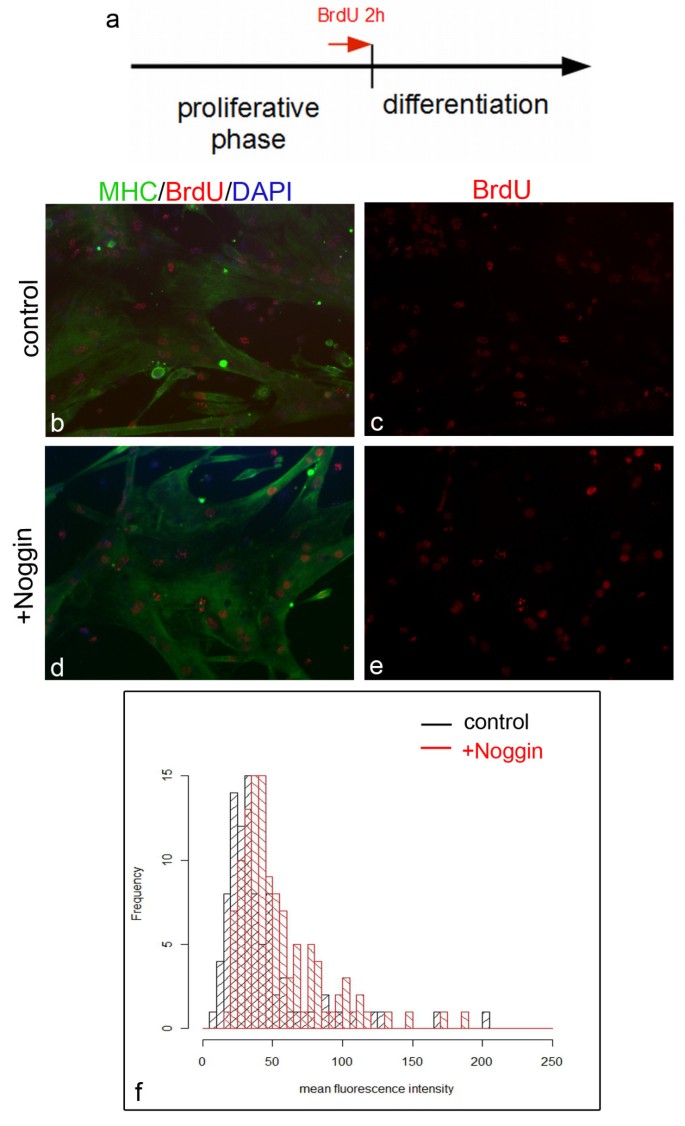
方法细节:将原代卫星细胞接种于Matrigel包被的24孔板,培养4天后换用促分化培养基,添加100ng/ml Bmp7或125ng/ml Noggin,每日更换培养基;处理3天后,通过免疫组化检测Desmin(肌系特异性标记)、碱性磷酸酶(成骨标记)、MHC(肌管标记)的表达,统计总肌核数、融合肌核比例、Myogenin阳性单核细胞比例;同时进行BrdU脉冲追踪实验:在分化前2小时添加BrdU,分化3天后检测肌管中BrdU信号的强度,评估细胞周期退出情况。
结果解读:免疫组化显示,原代卫星细胞在Bmp7或Noggin处理下均表达Desmin,且无碱性磷酸酶阳性细胞,说明原代卫星细胞不会在BMP信号作用下向成骨分化。细胞计数显示,Bmp7处理后总肌核数为对照组的121%(n≥13,P=0.05),但融合肌核比例从28%降至20%(n≥13,P=0.002),肌管形成受抑制;Myogenin阳性单核细胞比例降低,说明分化启动被抑制。Noggin处理后总肌核数为对照组的64%(n≥13,P<0.005),融合肌核比例升至47%(n≥13,P<0.005),肌管形成增强;BrdU脉冲追踪显示Noggin处理组肌管中BrdU强阳性核比例显著高于对照组(n≥92,P<0.005),说明抑制BMP信号可加速细胞周期退出,促进分化。
产品关联:实验所用关键产品:BD Biosciences的Matrigel;Sigma的抗Desmin抗体;Abcam的抗BrdU抗体。
3.4 BMP信号在肌分化后期的响应及Chordin的负反馈调控
实验目的:探究卫星细胞分化后期对BMP信号的响应变化,以及内源性BMP抑制剂Chordin的表达模式与调控作用。
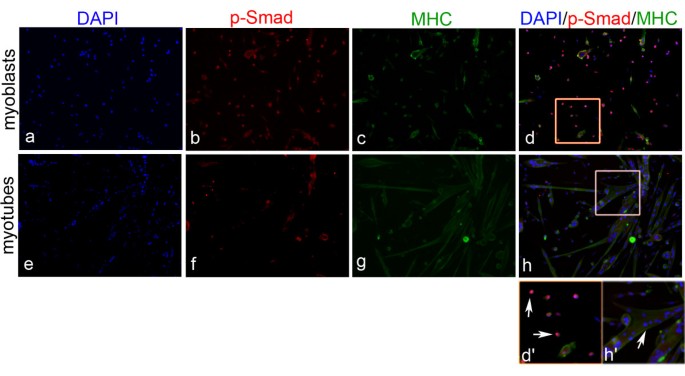
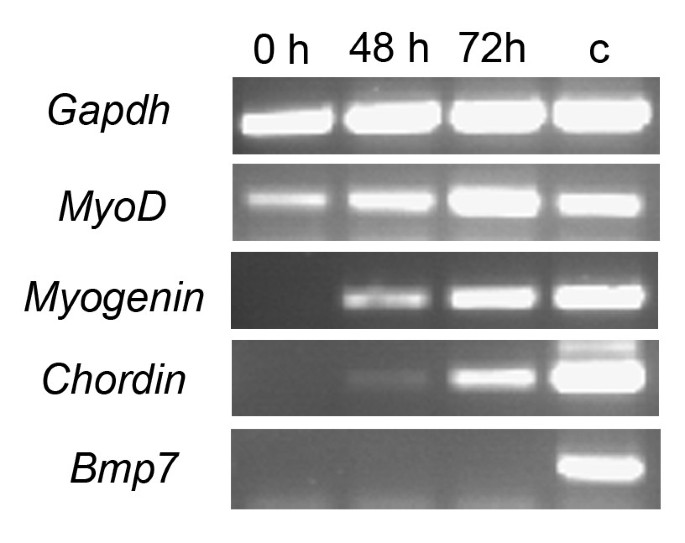
方法细节:将原代卫星细胞培养9天至肌管成熟,通过双重免疫荧光染色检测p-Smad1/5/8与MHC的共定位;同时收集培养0、48、72小时的肌纤维,通过RT-PCR检测MyoD、Myogenin、Chordin的mRNA表达水平。
结果解读:免疫荧光显示,成熟肌管中的肌核无p-Smad1/5/8信号,而周边的单核肌细胞仍为p-Smad阳性,说明分化后期的肌管细胞丧失对BMP信号的响应能力。RT-PCR结果显示,MyoD在新鲜分离的肌纤维中已表达,随培养时间延长表达量升高;Myogenin在培养48小时后出现,72小时表达量显著升高;Chordin在培养48小时后低表达,72小时表达量显著上调,与Myogenin的表达趋势一致,说明分化启动后细胞会上调Chordin表达,负反馈抑制BMP信号,促进肌管成熟。
产品关联:文献未提及具体实验产品,领域常规使用实时荧光定量PCR仪、反转录试剂盒等试剂/仪器。
3.5 体内肌肉再生中BMP信号的功能验证
实验目的:验证BMP信号在体内肌肉损伤再生过程中的调控作用,明确其与卫星细胞激活、分化的关联。
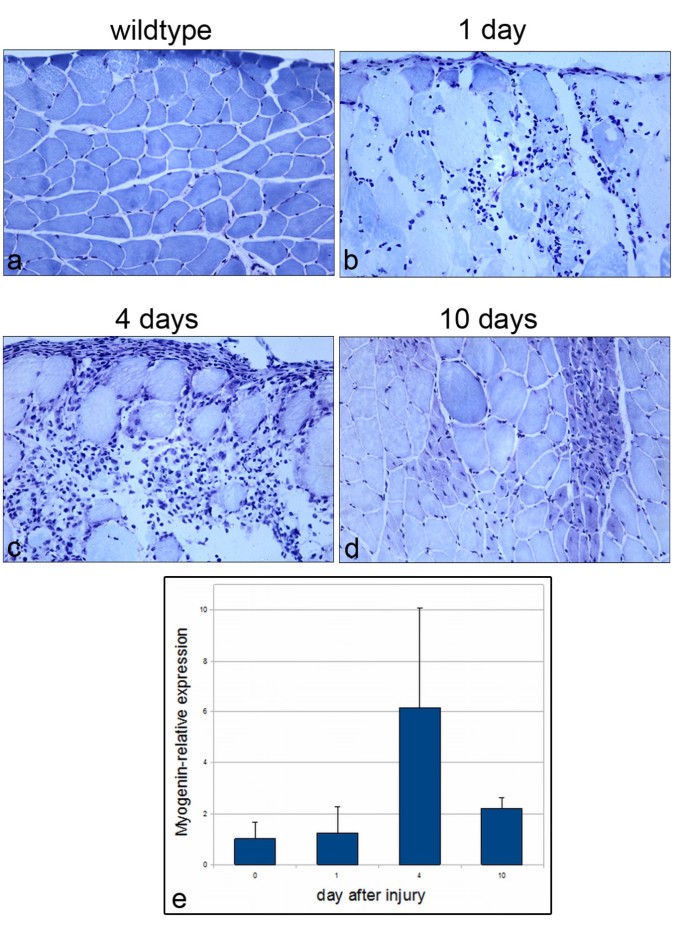
方法细节:建立小鼠腓肠肌钝性损伤模型,在损伤后1、4、10天处死小鼠,取腓肠肌组织;通过甲苯胺蓝染色观察肌肉再生的组织学变化;通过RT-PCR检测Myogenin、Chordin的mRNA表达水平;通过免疫组化检测MyoD、p-Smad1/5/8与Lamininα2(基底膜标记)的共定位,明确BMP信号响应细胞的位置。
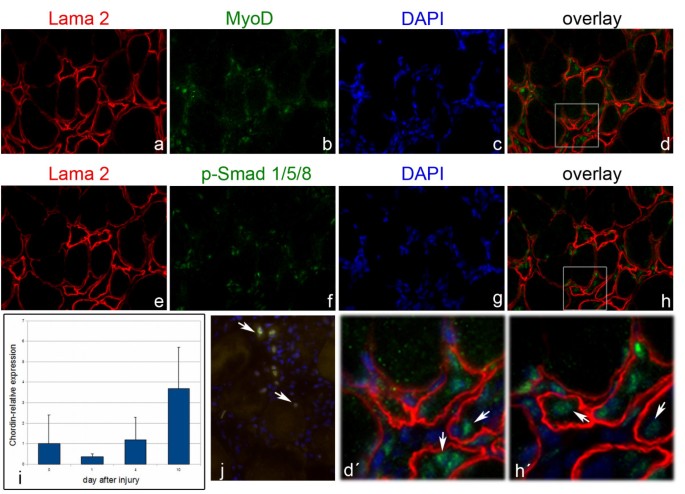
结果解读:组织学染色显示,损伤后1天,损伤区域出现单核细胞浸润;损伤后4天,肌纤维降解,大量单核细胞聚集,Myogenin表达达到峰值(n=3);损伤后10天,肌纤维形态恢复,出现中央核肌纤维,标志再生完成。免疫组化显示,损伤后4天,MyoD阳性的卫星细胞后代位于Lamininα2标记的基底膜下,同时p-Smad1/5/8阳性细胞也位于基底膜下,且部分细胞同时表达MyoD与p-Smad,说明体内激活的卫星细胞可响应BMP信号。RT-PCR显示,损伤后10天Chordin表达显著上调,与体外培养结果一致,提示体内再生后期Chordin通过负反馈抑制BMP信号,促进肌分化成熟。
产品关联:实验所用关键产品:Merck的甲苯胺蓝;Santa Cruz的抗MyoD抗体;Cell Signaling Technologies的抗p-Smad1/5/8抗体。
4. Biomarker研究及发现成果解析
本研究涉及的Biomarker包括BMP信号激活标记p-Smad1/5/8、分化启动标记Myogenin及BMP负调控标记Chordin,三者共同构成了卫星细胞增殖分化状态的分子标记体系,筛选与验证遵循“体外细胞模型→体内损伤模型”的完整逻辑链条。
Biomarker定位:p-Smad1/5/8作为BMP信号通路的激活标记,可用于识别处于激活/增殖状态的卫星细胞;Myogenin作为分化启动标记,标志卫星细胞后代进入分化程序;Chordin作为内源性BMP抑制剂,是分化后期的负调控标记,三者的表达动态反映了卫星细胞从激活到分化的完整命运转变过程。筛选与验证逻辑为:首先在体外肌纤维培养模型中验证p-Smad1/5/8与卫星细胞激活状态的关联,Myogenin与分化启动的关联,Chordin与分化后期的关联;随后通过体内肌肉损伤模型验证三者在生理再生过程中的表达模式,确认其作为状态标记的可靠性。
研究过程详述:p-Smad1/5/8的来源为卫星细胞的细胞核,验证方法为免疫荧光染色,在静息卫星细胞中阴性,激活/增殖卫星细胞中阳性,体内损伤后4天的再生区域基底膜下细胞中阳性;Myogenin的来源为卫星细胞后代的细胞核,验证方法为RT-PCR与免疫组化,体外培养72小时后表达上调,体内损伤后4天达到峰值(n=3);Chordin的来源为卫星细胞后代的mRNA,验证方法为RT-PCR,体外培养72小时后表达上调,体内损伤后10天达到峰值(n=3)。特异性方面,p-Smad1/5/8仅在激活的卫星细胞中阳性,与静息细胞无交叉;Myogenin仅在分化启动后的细胞中表达,可有效区分增殖与分化状态的细胞。
核心成果提炼:p-Smad1/5/8可作为卫星细胞激活状态的特异性Biomarker,为评估卫星细胞的增殖活性提供分子依据;Chordin作为首次在成体肌再生中被明确的BMP负调控Biomarker,其表达与Myogenin正相关,提示其通过负反馈机制促进细胞周期退出与肌管成熟,相关风险比HR数据文献未明确提供;本研究首次揭示了Chordin在成体肌再生中的调控作用,为肌再生的干预提供了新的潜在靶点。