1. 领域背景与文献引入
文献英文标题:Aurora kinase a promotes the progression of papillary thyroid carcinoma by activating the mTORC2-AKT signalling pathway;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:甲状腺癌分子机制与靶向治疗
领域共识:甲状腺癌是最常见的内分泌系统恶性肿瘤,2020年全球新发肿瘤中占比3.0%,中国占比约4.8%。其中乳头状甲状腺癌(PTC)占甲状腺癌的90%-97%,多数患者预后良好,但20%-30%会出现复发,5%-10%发展为难治性甲状腺癌,因此寻找新的个体化干预靶点是当前PTC诊疗的核心需求。Aurora激酶A(AURKA)作为丝氨酸/苏氨酸激酶,在多种肿瘤中调控细胞增殖、迁移等恶性表型,与不良预后相关,但在PTC中的具体功能及分子机制尚未明确,这一研究空白限制了AURKA作为PTC诊疗靶点的开发。本研究针对这一问题,系统解析AURKA在PTC中的作用及调控通路,为PTC的靶向治疗提供新的理论依据。
2. 文献综述解析
作者对领域内现有研究按分子功能与信号通路维度分类,涵盖AURKA在泛肿瘤中的致癌功能、PI3K/AKT信号通路在PTC中的异常激活、mTORC2复合物亚基SIN1的调控机制三个方向。现有研究显示,AURKA在头颈部肿瘤、乳腺癌等多种肿瘤中高表达,通过激活NF-κB、PI3K/AKT等通路促进肿瘤进展,其抑制剂在部分肿瘤中显示出治疗潜力;PI3K/AKT通路在PTC中普遍异常激活,与肿瘤转移、耐药相关;SIN1作为mTORC2的关键亚基,调控AKT的磷酸化激活,但在PTC中的调控机制尚未阐明。现有研究的局限性在于,未明确AURKA在PTC中的具体作用机制,尤其是其与SIN1、泛素化修饰系统的相互作用关系。本研究的创新价值在于首次揭示AURKA通过竞争性结合SIN1,抑制CUL4B介导的泛素化降解,从而激活mTORC2-AKT信号通路促进PTC进展,填补了AURKA在PTC中分子机制的研究空白。
3. 研究思路总结与详细解析
本研究整体遵循“临床表型关联→功能验证→通路筛选→机制解析→效应分子验证”的闭环逻辑,核心目标是明确AURKA在PTC中的致癌功能及分子机制,解决的核心科学问题是AURKA如何调控PTC中mTORC2-AKT通路的激活。
3.1 AURKA在PTC中的表达与临床相关性分析
本环节核心目标是明确AURKA在PTC组织中的表达水平及与临床病理特征的关联。研究采用185例PTC组织芯片进行免疫组化(IHC)染色,结合卡方分析与生存分析,同时选取18对新鲜PTC及配对正常组织进行实时荧光定量PCR(qRT-PCR)检测,8对组织进行蛋白质免疫印迹(WB)检测,还验证了PTC细胞系与正常甲状腺上皮细胞中AURKA的表达差异。结果显示,AURKA在PTC组织的细胞核与细胞质中均有表达,其高表达与T分期、淋巴结转移、TNM分期呈正相关,高表达患者的疾病特异性生存率显著低于低表达组(P<0.001,n=185);PTC组织中AURKA的mRNA与蛋白水平均显著高于正常组织,细胞系中表达趋势一致。
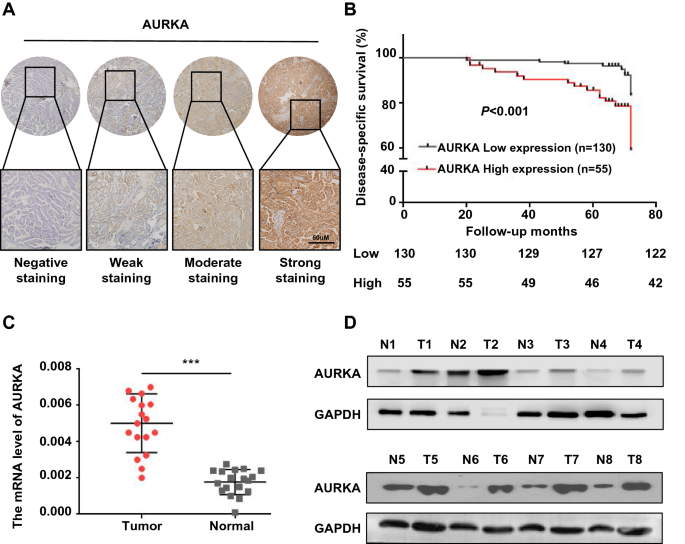
实验所用关键产品:Abcam的AURKA抗体(货号ab1287)、CST的Ki67抗体(货号#9449)、TaKaRa的qRT-PCR试剂等。
3.2 AURKA对PTC细胞恶性表型的调控作用
本环节核心目标是验证AURKA在PTC中的致癌功能。研究构建了AURKA稳定敲低的TPC-1、IHH4细胞系及过表达的KTC、K1细胞系,采用CCK-8法检测细胞活力,克隆形成实验、EdU染色实验检测细胞增殖能力,Transwell实验检测细胞迁移能力,同时构建裸鼠皮下异种移植模型验证体内成瘤能力。结果显示,敲低AURKA可显著降低PTC细胞的活力、克隆形成能力及迁移能力,过表达AURKA则促进上述恶性表型;裸鼠模型中,AURKA敲低组的肿瘤体积与重量显著低于对照组(n=5,P<0.05),免疫组化显示肿瘤组织中Ki-67阳性细胞数减少。
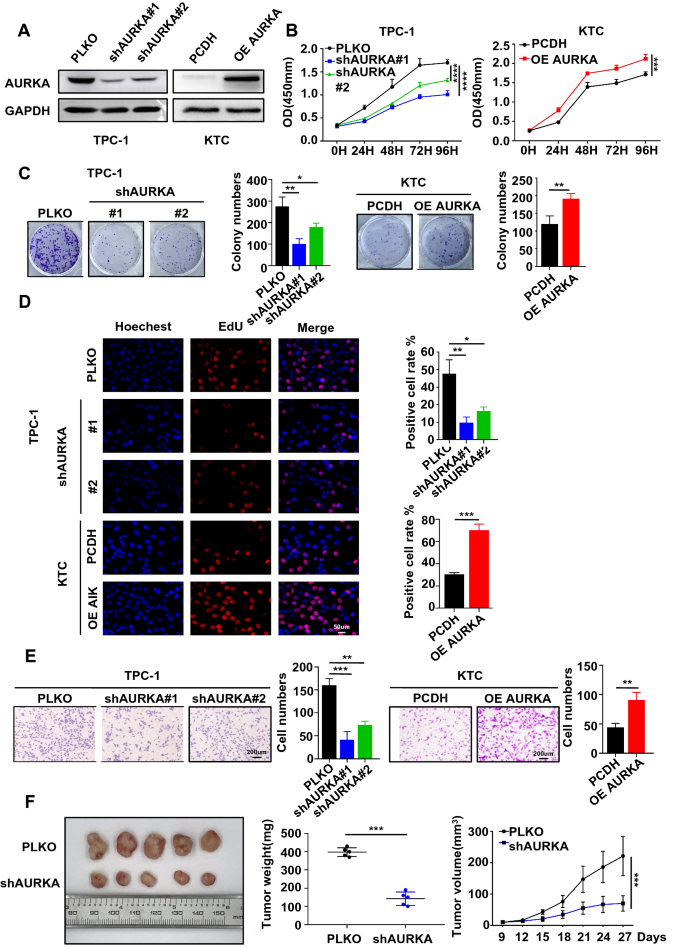
文献未提及具体实验产品,领域常规使用CCK-8试剂盒、EdU染色试剂盒、Transwell小室等。
3.3 AURKA激活PI3K/AKT信号通路的机制初探
本环节核心目标是筛选AURKA调控的下游信号通路。研究对AURKA敲低的TPC-1细胞进行转录组测序(RNA-seq),通过基因本体(GO)与京都基因与基因组百科全书(KEGG)富集分析筛选差异通路,随后用WB验证通路关键蛋白的表达,并用mTOR抑制剂处理细胞验证通路依赖性。结果显示,RNA-seq共鉴定出1695个差异表达基因,其中显著富集于PI3K/AKT信号通路;敲低AURKA可降低磷酸化AKT(p-AKT)的蛋白水平,过表达则升高;mTOR抑制剂Ridaforolimus与tacrolimus可逆转AURKA过表达引起的p-AKT升高及细胞恶性表型增强。
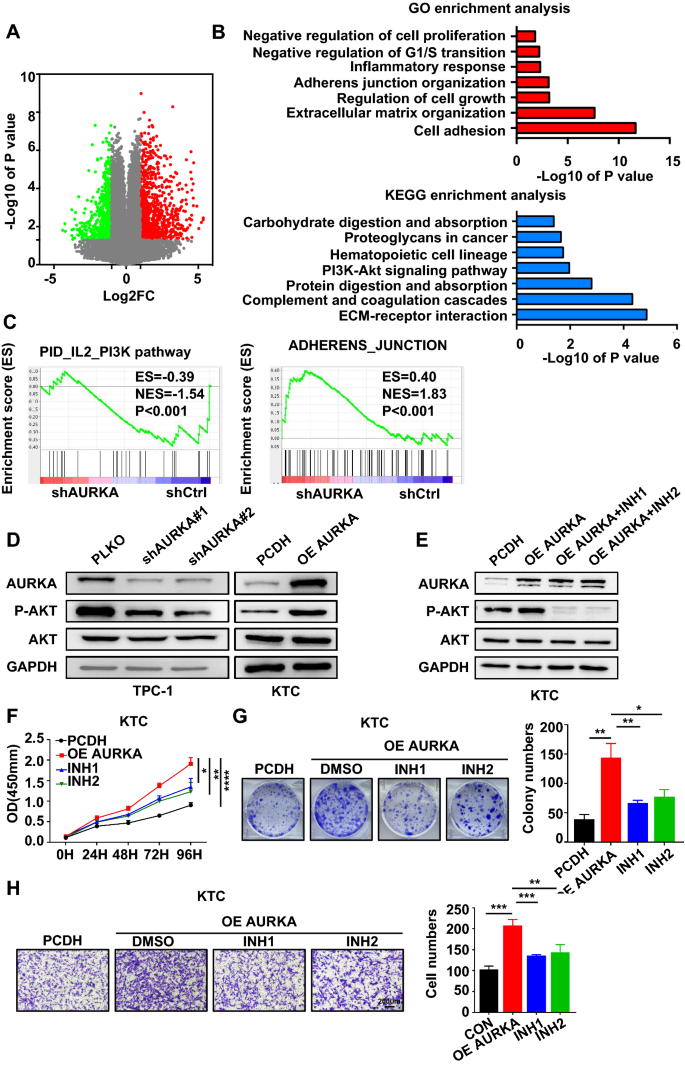
文献未提及具体实验产品,领域常规使用RNA-seq测序服务、mTOR抑制剂等。
3.4 AURKA与SIN1的相互作用及稳定性调控
本环节核心目标是揭示AURKA调控AKT通路的直接分子靶点。研究采用Flag标签的AURKA过表达细胞系进行免疫共沉淀(IP)结合质谱分析,筛选到SIN1为AURKA的结合蛋白,随后通过内源性IP、免疫荧光共定位验证两者的相互作用,用环己酰亚胺(CHX)脉冲追踪实验检测SIN1的蛋白稳定性,泛素化实验检测SIN1的泛素化水平,同时构建SIN1截短体确定结合结构域。结果显示,AURKA与SIN1的PH结构域直接结合;敲低AURKA可加速SIN1的蛋白降解,提高其泛素化水平,而过表达AURKA则抑制SIN1的泛素化降解,且对SIN1的mRNA水平无显著影响,表明AURKA在转录后水平调控SIN1的稳定性。
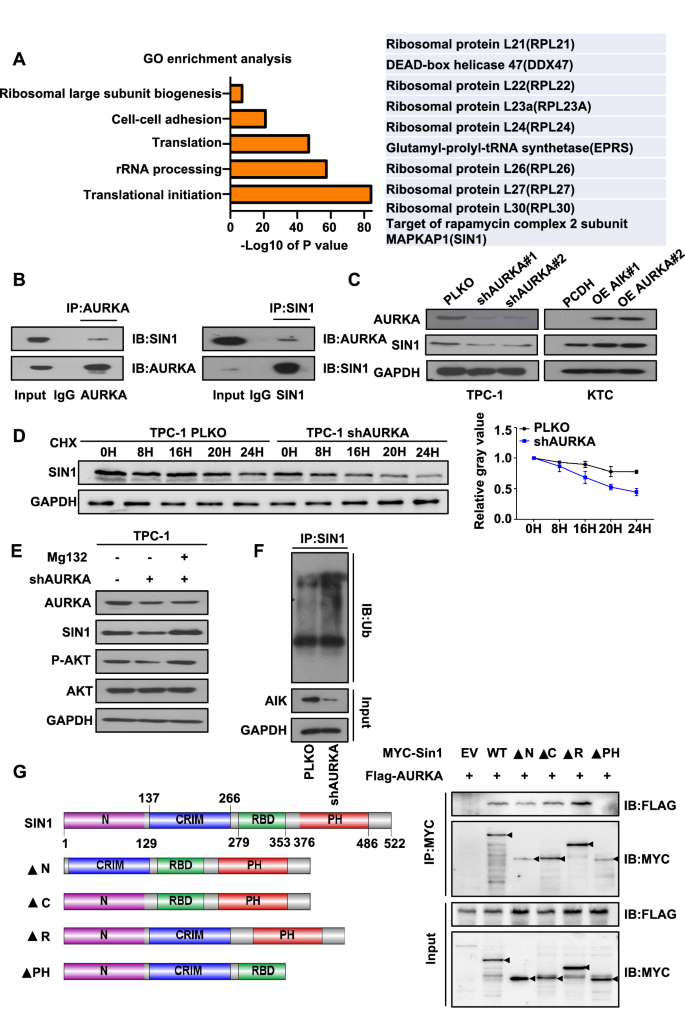
实验所用关键产品:CST的SIN1抗体(货号#12860)、Ubiquitin抗体(货号#3936)等。
3.5 CUL4B介导SIN1的泛素化降解及AURKA的竞争作用
本环节核心目标是明确SIN1的泛素E3连接酶及AURKA的调控机制。研究通过siRNA敲低Cullin家族成员,筛选到CUL4B为调控SIN1蛋白水平的关键分子,随后验证CUL4B与SIN1的相互作用,检测AURKA对两者结合的影响,同时构建SIN1泛素化位点突变体确定关键修饰位点。结果显示,CUL4B与SIN1的PH结构域结合,介导其泛素化降解;AURKA可竞争性结合SIN1的PH结构域,抑制CUL4B与SIN1的相互作用,从而减少SIN1的泛素化;SIN1的K162与K276位点为CUL4B介导的关键泛素化位点,突变这两个位点可显著抑制CUL4B对SIN1的降解作用。
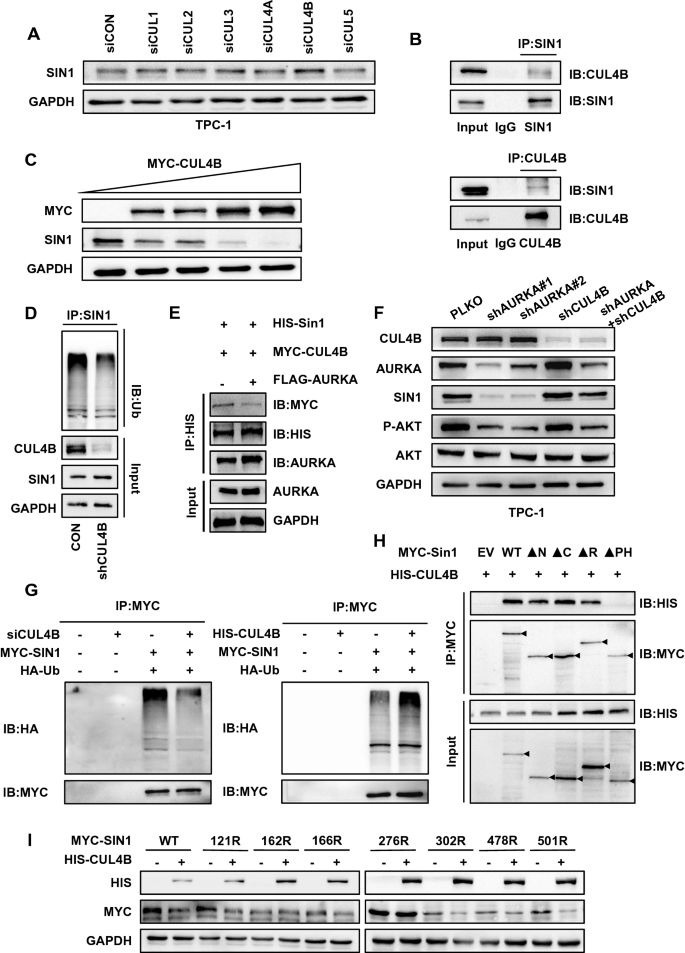
实验所用关键产品:ProteinTech的Cullin4B抗体(货号12916)等。
3.6 SIN1介导AURKA对PTC的调控作用
本环节核心目标是验证SIN1为AURKA功能的下游效应分子。研究在AURKA过表达的细胞中敲低SIN1,检测p-AKT水平及细胞恶性表型的变化,同时构建裸鼠异种移植模型验证体内功能。结果显示,敲低SIN1可逆转AURKA过表达引起的p-AKT升高,同时抑制细胞的增殖、克隆形成及迁移能力;裸鼠模型中,敲低SIN1可显著抑制AURKA过表达细胞的肿瘤生长,免疫组化显示肿瘤组织中p-AKT与SIN1的表达水平降低。
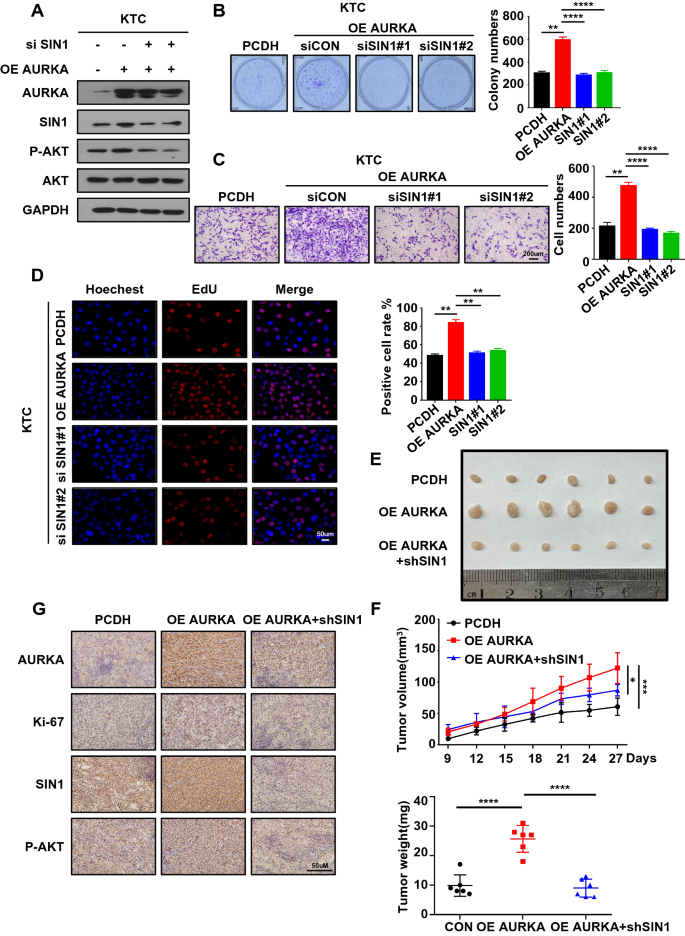
文献未提及具体实验产品,领域常规使用siRNA转染试剂、裸鼠模型等。
4. Biomarker研究及发现成果解析
本研究中涉及的Biomarker为AURKA,属于蛋白类肿瘤标志物,其筛选与验证逻辑为“大样本临床组织验证表达与预后相关性→细胞系与动物模型验证功能→机制解析明确调控通路”。
AURKA的研究过程涵盖多维度验证:来源为185例PTC临床组织样本、18对新鲜组织样本及多种PTC细胞系;验证方法包括免疫组化、qRT-PCR、WB等,其中免疫组化显示AURKA高表达与PTC患者不良预后显著相关,生存分析的ROC曲线数据未明确提供,但生存曲线显示高表达组患者的疾病特异性生存率为76.4%,低表达组为93.8%(n=185,P<0.001)。
核心成果方面,AURKA作为PTC的预后标志物,其高表达患者的死亡风险是低表达组的3.8倍(23.6% vs 6.2%);同时,本研究首次揭示AURKA通过调控SIN1-mTORC2-AKT信号通路促进PTC进展,为AURKA作为PTC的靶向治疗靶点提供了理论依据。该Biomarker的创新性在于,首次在PTC中明确了AURKA与泛素化修饰系统的相互作用关系,完善了AURKA在肿瘤中的调控网络。
