1. 领域背景与文献引入
文献英文标题:MIIP downregulation drives colorectal cancer progression through inducing peri-cancerous adipose tissue browning;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:结直肠癌肿瘤微环境与脂肪组织交互调控
结直肠癌是全球第三大常见癌症,尽管筛查和治疗手段取得一定进展,但其发病率和死亡率仍居高不下。癌周脂肪组织富集是结直肠癌的显著特征,可加速疾病进展并恶化患者预后,肿瘤细胞与邻近脂肪细胞的通讯在这一过程中发挥关键作用,但两者间精确的调控机制尚未完全阐明。现有研究显示,脂肪细胞可通过分泌细胞因子、外泌体及上调代谢酶,促进结直肠癌细胞增殖、转移、化疗耐药和干性维持;同时,肿瘤可诱导邻近白色脂肪组织褐变,通过脂解释放游离脂肪酸为肿瘤细胞供能,但结直肠癌中调控这一交互过程的关键因子仍未被充分揭示。迁移和侵袭抑制蛋白(MIIP)在多种肿瘤中发挥肿瘤抑制作用,但其在结直肠癌与癌周脂肪组织通讯中的功能尚未见报道。本文聚焦MIIP在结直肠癌与癌周脂肪组织交互中的调控作用,旨在阐明MIIP下调如何重塑肿瘤-脂肪细胞通讯并促进结直肠癌进展,为结直肠癌的精准治疗提供新靶点。
2. 文献综述解析
作者从结直肠癌与癌周脂肪组织的交互作用、脂肪组织褐变的调控机制、MIIP的肿瘤抑制功能三个核心维度展开综述,系统梳理领域内现有研究的进展与空白。首先,作者总结了结直肠癌中癌周脂肪组织的促癌作用,指出脂肪细胞可通过分泌细胞因子、外泌体及上调代谢酶,促进结直肠癌细胞增殖、转移、化疗耐药和干性维持,但两者间复杂的双向调控机制仍需深入解析,现有研究多聚焦脂肪细胞对肿瘤的单向作用,缺乏对肿瘤细胞反向调控脂肪组织的机制探讨。其次,作者梳理了肿瘤诱导白色脂肪组织褐变的研究进展,指出β-肾上腺素能受体(β-AR)和AMPK信号通路是脂肪褐变的关键调控通路,肿瘤分泌的IL-6、TNF-α、AZGP1等因子可诱导脂肪褐变和脂解,但结直肠癌中这一过程的具体调控因子尚未明确,且缺乏对调控因子翻译后修饰的研究。最后,作者回顾了MIIP在多种肿瘤中的肿瘤抑制作用,包括抑制细胞侵袭、增殖、上皮间质转化等,但MIIP在结直肠癌与脂肪组织交互中的作用尚未见报道。通过对比现有研究的未解决问题,作者凸显了本研究的创新价值:首次揭示MIIP通过调控AZGP1的N-糖基化和分泌,参与结直肠癌与癌周脂肪组织的通讯,为结直肠癌进展的调控机制提供新视角,同时为结直肠癌的联合治疗策略提供实验依据。
3. 研究思路总结与详细解析
本研究以“临床样本关联分析→细胞模型功能验证→动物模型体内验证→分子机制解析→治疗策略探索”为核心技术路线,旨在阐明MIIP在结直肠癌与癌周脂肪组织通讯中的调控机制及功能,核心科学问题是MIIP下调如何通过AZGP1调控脂肪组织褐变并促进结直肠癌进展。
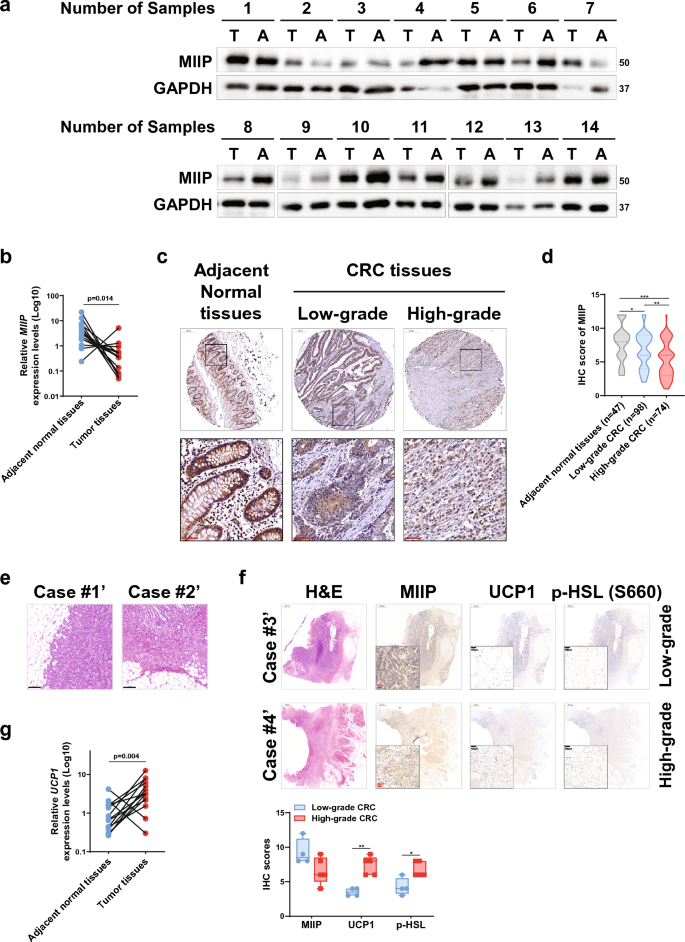
3.1 临床样本中MIIP表达与癌周脂肪褐变的关联分析
实验目的是明确MIIP在结直肠癌组织中的表达变化及其与癌周脂肪褐变的相关性。研究人员收集14对结直肠癌及癌旁正常组织样本,通过免疫印迹、实时荧光定量PCR检测MIIP的蛋白和mRNA表达;利用包含172例结直肠癌患者和47例癌旁正常组织的组织芯片,通过免疫组化染色分析MIIP表达与肿瘤分化程度的关系;通过免疫组化检测脂肪褐变标志物解偶联蛋白1(UCP1)和脂解关键酶磷酸化激素敏感性脂肪酶(p-HSL)的表达,分析其与MIIP表达的相关性。结果显示,结直肠癌组织中MIIP的蛋白和mRNA表达显著低于癌旁正常组织(n=14,P<0.01);组织芯片免疫组化结果显示,高分化结直肠癌组织中MIIP高表达率为28.6%,低分化组织中仅为18.9%,显著低于癌旁正常组织的42.6%(P<0.05);低MIIP表达的结直肠癌样本中UCP1和p-HSL的表达显著升高,提示MIIP表达与癌周脂肪褐变呈负相关。
产品关联:文献提及的关键产品包括免疫组化抗体(如MIIP抗体PA5-100572、UCP1抗体23673-1-AP等)、免疫印迹抗体、实时荧光定量PCR引物等,领域常规使用Proteintech、Cell Signaling Technology等品牌的抗体。
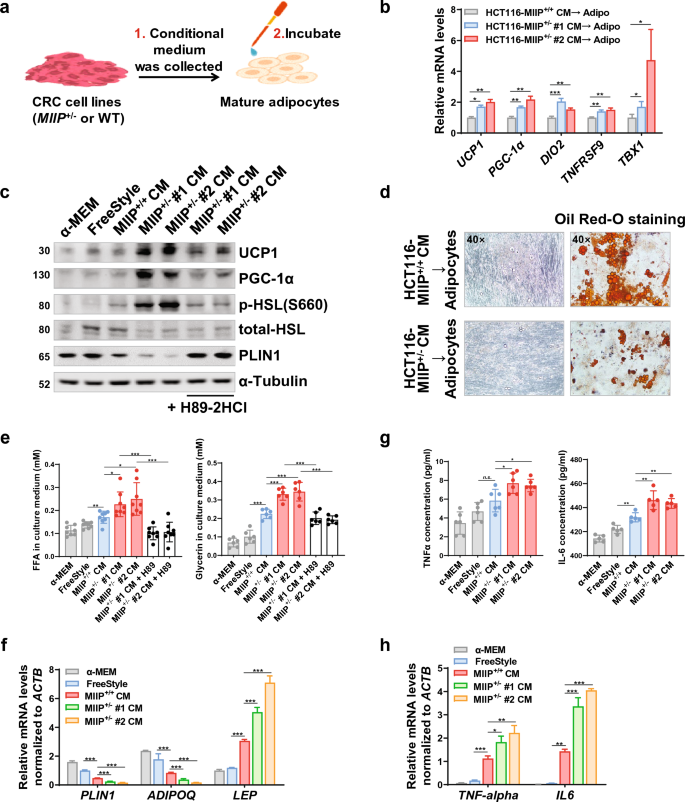
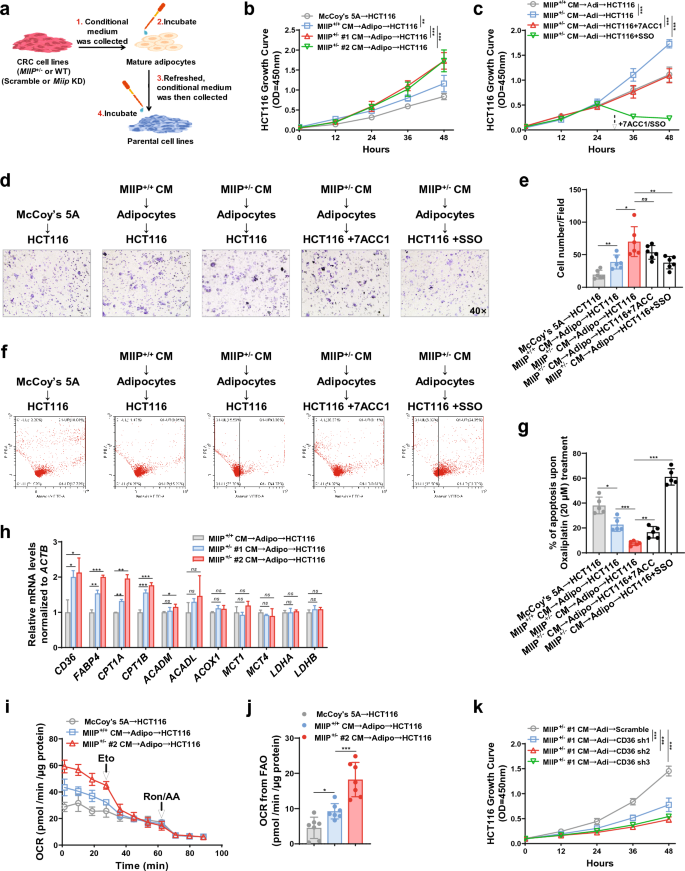
3.2 细胞模型中MIIP下调对脂肪细胞褐变的调控作用
实验目的是验证MIIP下调的结直肠癌细胞是否能诱导脂肪细胞褐变和脂解。研究人员构建MIIP半合子缺失的HCT116细胞系(MIIP+/−),收集其条件培养基处理人原代脂肪干细胞分化的成熟脂肪细胞;通过实时荧光定量PCR检测脂肪褐变相关基因的表达,免疫印迹检测UCP1、p-HSL等蛋白的表达;通过油红O染色观察脂滴变化,检测培养基中游离脂肪酸和甘油的含量;使用PKA抑制剂H89-2HCl处理脂肪细胞,验证信号通路。结果显示,MIIP+/−细胞条件培养基处理的脂肪细胞中,褐变相关基因UCP1、PGC-1α等的表达显著上调(n=6,P<0.001);UCP1蛋白表达和HSL磷酸化水平显著升高,脂滴保护蛋白PLIN1表达降低;脂滴数量和体积显著减少,培养基中游离脂肪酸和甘油含量显著升高(n=8,P<0.001);H89-2HCl处理可逆转上述效应,提示MIIP下调通过cAMP-PKA通路诱导脂肪细胞褐变和脂解。
产品关联:文献提及的关键产品包括PKA抑制剂H89-2HCl(TopScienceBiochem)、油红O染色试剂等,领域常规使用类似试剂。
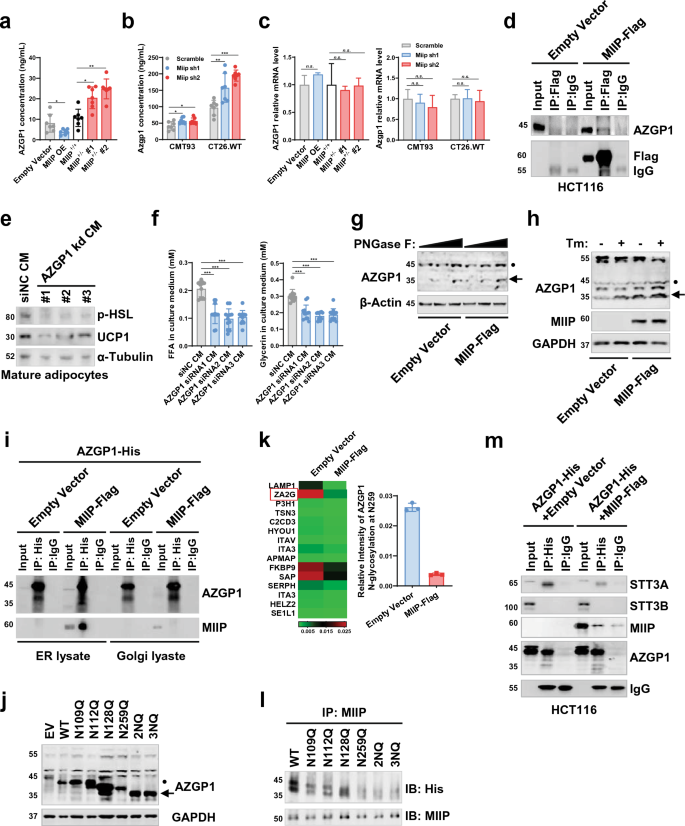
3.3 MIIP调控AZGP1糖基化与分泌的机制解析
实验目的是阐明MIIP调控脂肪褐变的下游效应分子及机制。研究人员通过蛋白质组学分析MIIP+/−和野生型HCT116细胞条件培养基中的差异分泌蛋白,筛选出α-2-糖蛋白1锌结合蛋白(AZGP1);通过免疫共沉淀验证MIIP与AZGP1的相互作用;通过PNGase F处理、衣霉素处理分析AZGP1的糖基化状态;构建AZGP1的N-糖基化位点突变体,通过免疫共沉淀、LC-MS/MS分析MIIP对AZGP1糖基化的调控位点;通过免疫共沉淀分析MIIP与STT3A的竞争结合作用。结果显示,MIIP+/−细胞中AZGP1分泌显著增加;MIIP与AZGP1直接相互作用;MIIP过表达可降低AZGP1的N-糖基化水平,LC-MS/MS结果显示MIIP过表达使AZGP1第259位天冬酰胺的N-糖基化强度降低至对照组的0.149倍(n=3,P<0.01);MIIP与STT3A竞争结合AZGP1,抑制其N-糖基化和分泌;AZGP1敲低可逆转MIIP+/−细胞条件培养基诱导的脂肪褐变和脂解。
产品关联:文献提及的关键产品包括PNGase F(New England BioLabs)、衣霉素(TopScienceBiochem)、LC-MS/MS检测服务等,领域常规使用类似产品。
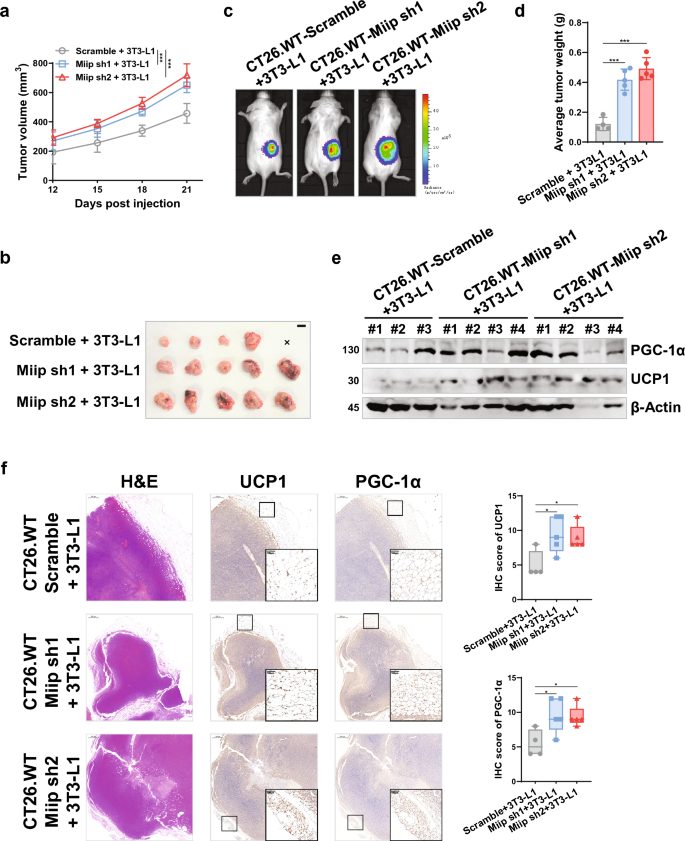
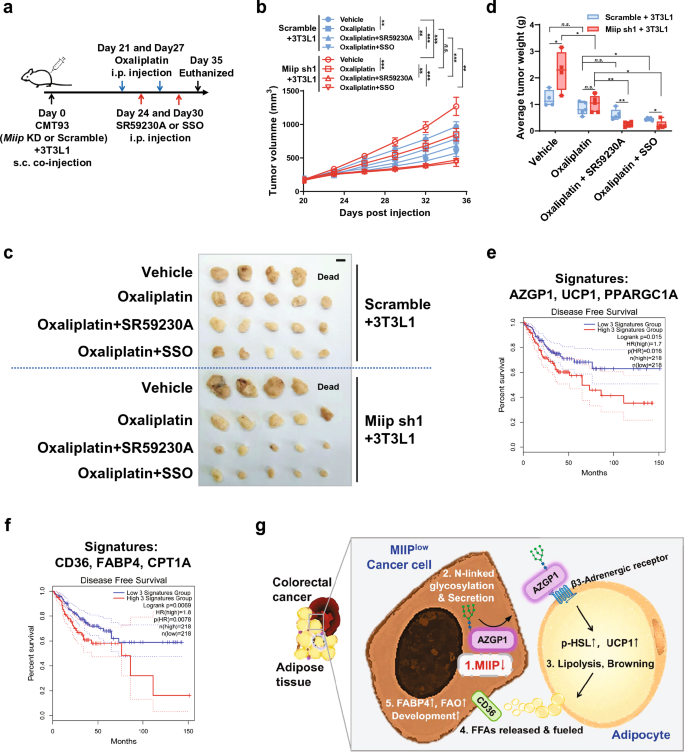
3.4 动物模型中MIIP下调对肿瘤-脂肪交互的调控作用
实验目的是在体内验证MIIP下调对结直肠癌与脂肪组织交互的调控作用。研究人员构建稳定敲低Miip的小鼠结直肠癌细胞系CT26.WT和CMT93,与3T3-L1脂肪细胞共注射到BALB/c或C57BL/6小鼠背部,建立皮下移植瘤模型;通过活体成像、肿瘤称重监测肿瘤生长;通过免疫组化、免疫印迹检测肿瘤组织中UCP1、CD36等蛋白的表达;构建HCT116 MIIP+/−与成熟脂肪细胞共注射的裸鼠模型,验证人源细胞的效应。结果显示,共注射Miip敲低细胞与脂肪细胞的小鼠肿瘤生长速度显著快于对照组,肿瘤体积和重量显著增加(n=5,P<0.001);肿瘤组织中UCP1表达显著升高,提示脂肪褐变增强;裸鼠模型中,MIIP+/−细胞与脂肪细胞共注射的肿瘤体积和重量显著大于单独注射组(n=5,P<0.01),且肿瘤组织中CD36、FABP4等游离脂肪酸转运蛋白表达显著升高。
产品关联:文献未提及具体实验产品,领域常规使用裸鼠、BALB/c小鼠等动物模型,以及活体成像系统等仪器。
3.5 游离脂肪酸对结直肠癌细胞的促癌作用及治疗策略探索
实验目的是明确脂肪褐变释放的游离脂肪酸对结直肠癌细胞的作用,并探索联合治疗策略。研究人员通过两步条件培养基处理,将脂肪细胞经MIIP+/−细胞条件培养基处理后,收集其条件培养基处理结直肠癌细胞,通过CCK-8、Transwell实验检测细胞增殖、侵袭能力;通过流式细胞术检测奥沙利铂诱导的细胞凋亡;使用游离脂肪酸转运抑制剂磺基琥珀酰亚胺油酸酯(SSO)、乳酸转运抑制剂7ACC1处理细胞,验证游离脂肪酸的作用;在动物模型中,使用奥沙利铂联合β-肾上腺素能受体抑制剂SR59230A或SSO处理,评估治疗效果。结果显示,两步条件培养基处理的结直肠癌细胞增殖、侵袭能力显著增强,奥沙利铂诱导的凋亡显著减少(n=5,P<0.01);SSO处理可显著逆转上述效应,而7ACC1作用较弱,提示游离脂肪酸是主要促癌因子;动物模型中,奥沙利铂联合SR59230A或SSO可显著抑制MIIP下调肿瘤的生长,肿瘤体积和重量显著低于单独奥沙利铂组(n=5,P<0.001)。
产品关联:文献提及的关键产品包括SSO(TopScienceBiochem)、7ACC1(TopScienceBiochem)、奥沙利铂(MedChemExpress)等,领域常规使用类似试剂。
4. Biomarker研究及发现成果解析
本文涉及的Biomarker包括MIIP、AZGP1、UCP1、CD36等,其中MIIP作为结直肠癌的预后Biomarker,筛选逻辑为临床样本分析→细胞模型验证→动物模型验证;AZGP1作为MIIP的下游效应Biomarker,筛选逻辑为蛋白质组学筛选→功能验证→机制解析;UCP1和CD36作为脂肪褐变和游离脂肪酸利用的Biomarker,验证逻辑为临床样本关联→动物模型验证→数据库预后分析。
MIIP的来源为临床结直肠癌组织,验证方法包括免疫印迹、实时荧光定量PCR、免疫组化,特异性表现为结直肠癌组织中表达显著低于癌旁正常组织,且与肿瘤分化程度负相关,低分化组织中MIIP高表达率仅为18.9%,显著低于癌旁正常组织的42.6%(P<0.05);AZGP1的来源为结直肠癌细胞分泌,验证方法包括ELISA、免疫印迹,特异性表现为MIIP下调细胞中AZGP1的N-糖基化和分泌显著增加,通过cAMP-PKA通路诱导脂肪褐变;UCP1的来源为癌周脂肪组织,验证方法包括免疫组化、实时荧光定量PCR,敏感性表现为低MIIP表达的结直肠癌样本中UCP1表达显著升高(P<0.01);CD36的来源为结直肠癌细胞,验证方法为免疫组化,特异性表现为MIIP下调且与脂肪细胞共注射的肿瘤组织中CD36表达显著升高,与游离脂肪酸利用相关。
核心成果方面,MIIP作为结直肠癌的肿瘤抑制因子,其下调与癌周脂肪褐变及结直肠癌不良预后相关,临床样本分析显示低MIIP表达与肿瘤高恶性程度正相关;AZGP1作为MIIP的下游效应分子,首次被揭示在结直肠癌中通过N-糖基化调控分泌,介导肿瘤-脂肪交互;UCP1和CD36作为脂肪褐变和游离脂肪酸利用的Biomarker,其高表达与结直肠癌不良预后相关,GEPIA2数据库分析显示,脂肪褐变基因签名(AZGP1、UCP1、PPARGC1A)和游离脂肪酸转运氧化基因签名(CD36、FABP4、CPT1A)高表达的结直肠癌患者无病生存期显著缩短(P<0.05)。此外,研究证实奥沙利铂联合β-肾上腺素能受体抑制剂或游离脂肪酸转运抑制剂,可显著改善MIIP异常表达结直肠癌的治疗效果,为临床治疗提供新策略。
