1. 领域背景与文献引入
文献英文标题:PEX5R/Trip8b-HCN2 channel regulating neuroinflammation involved in perioperative neurocognitive disorders;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:围手术期神经认知障碍(PND)发病机制研究
围手术期神经认知障碍是老年手术患者常见的临床并发症,根据定义涵盖术前、术后30天内及术后30天至1年的所有认知损伤。领域共识:65岁以上老年患者术后1周PND发病率约为54%,心脏手术患者发病率可高达60%,其高发病率不仅严重影响患者术后康复,还显著增加全球医疗系统负担及患者家庭照护压力。PND的发病机制复杂,涉及多层面病理生理过程,目前临床及基础研究已证实神经炎症是其核心病理环节,而中枢神经系统内的小胶质细胞作为固有免疫细胞,是神经炎症的首要响应者,其激活可促进海马区炎症因子(白细胞介素-1β、白细胞介素-6、肿瘤坏死因子-α)释放,最终导致认知功能损伤。然而,麻醉药物诱导神经炎症及小胶质细胞激活的具体分子机制尚未完全明确,这一空白限制了PND精准防治策略的开发。
此前研究已发现,临床常用吸入麻醉药七氟烷可抑制超极化激活环核苷酸门控(HCN)通道,且HCN通道敲除或使用选择性阻滞剂ZD7288可增强七氟烷的麻醉效能;同时体外实验证实HCN通道在原代小胶质细胞表达并调控其功能,但七氟烷是否通过HCN通道介导小胶质细胞激活及神经炎症进而触发PND的体内机制尚未阐明。针对这一研究空白,本研究旨在明确七氟烷通过PEX5R/Trip8b-HCN2通道调控神经炎症参与PND的具体机制,为PND的防治提供新的潜在靶点,具有重要的临床转化价值。
2. 文献综述解析
作者对领域内现有研究的分类维度主要围绕PND的流行病学与危害、神经炎症与小胶质细胞的核心作用、七氟烷与HCN通道的关联三个层面展开。现有研究已明确PND的高发病率及严重临床危害,证实神经炎症是PND发生的关键病理过程,小胶质细胞激活是驱动神经炎症的核心环节,抑制小胶质细胞激活可显著改善PND大鼠的认知功能;同时研究也揭示七氟烷可直接抑制HCN通道,且HCN通道在小胶质细胞表达并调控其分泌及功能。现有研究的技术方法优势在于通过动物模型模拟PND病理过程,结合行为学实验、分子生物学技术等多维度验证机制,但仍存在局限性:多数研究聚焦于手术联合麻醉诱导的PND,单独七氟烷暴露诱导PND的机制研究不足;且HCN通道在体内调控小胶质细胞参与PND的具体机制尚未得到证实。
通过对比现有研究的未解决问题,本研究的创新价值凸显:首次在体内实验层面证实七氟烷通过下调PEX5R/Trip8b-HCN2通道,激活小胶质细胞并诱导神经炎症,最终导致大鼠认知障碍及焦虑样行为;明确了HCN2通道是七氟烷诱导PND的关键作用靶点,填补了七氟烷通过HCN通道介导PND体内机制的研究空白,为PND的防治提供了新的分子靶点。
3. 研究思路总结与详细解析
本研究的核心目标是探究七氟烷通过PEX5R/Trip8b-HCN2通道调控神经炎症参与PND的机制,核心科学问题为HCN2通道在七氟烷诱导小胶质细胞激活及神经炎症中的作用及调控方式,技术路线遵循“假设提出→动物模型构建→多组学筛选→分子生物学验证→抑制剂功能验证”的闭环逻辑。
3.1 PND大鼠模型构建与行为学评估
实验目的是验证七氟烷暴露是否可诱导大鼠出现认知障碍及焦虑样行为。方法细节:选用13-16月龄雄性SD大鼠,随机分为对照组(暴露于纯氧4小时)和PND组(暴露于3%七氟烷4小时);采用Morris水迷宫(MWM)评估大鼠空间学习记忆能力,开场实验(OFT)和高架十字迷宫(EPM)评估焦虑样行为,所有行为学实验中实验者均采用盲法分组及结果判定。结果解读:MWM实验显示,PND组大鼠在探针实验中进入平台象限的次数及停留时间显著低于对照组(n=8,P<0.05或P<0.01);OFT显示PND组大鼠进入中央区域的次数、停留时间及直立次数均显著减少(n=8,P<0.05或P<0.01);EPM显示PND组大鼠进入开放臂的比例及停留比例显著降低(n=8,P<0.05或P<0.01),表明七氟烷暴露可成功诱导大鼠出现认知障碍及焦虑样行为。
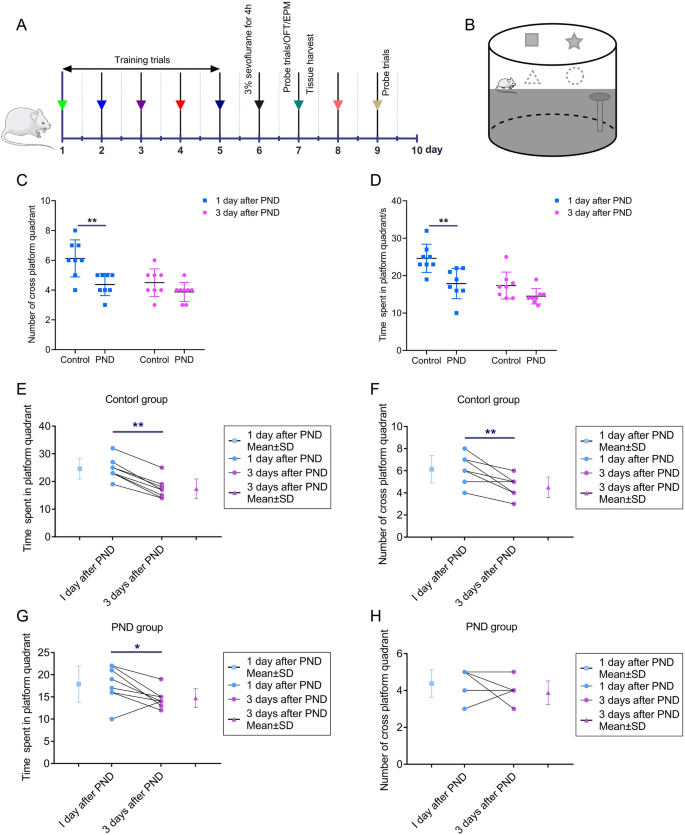
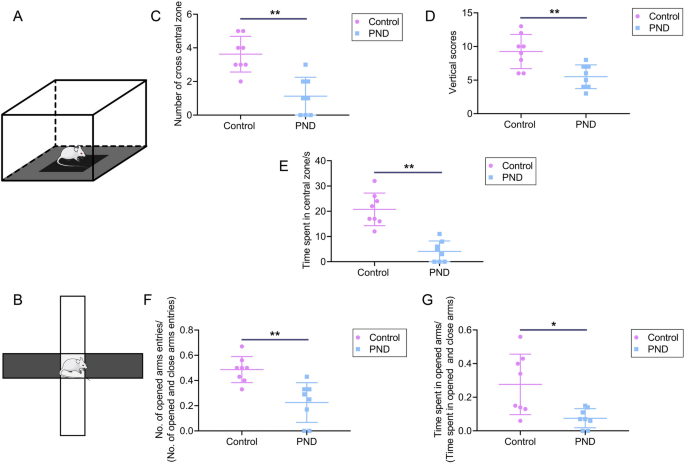
产品关联:文献未提及具体实验产品,领域常规使用动物行为学分析系统、麻醉诱导箱及监护仪等仪器。
3.2 转录组测序与差异基因功能分析
实验目的是筛选七氟烷诱导PND的关键差异基因及调控通路。方法细节:取PND组和对照组大鼠海马组织进行RNA测序,以|log₂(倍数变化)|>1且校正P<0.05为标准筛选差异表达基因(DEGs),通过Metascape进行基因本体(GO)富集分析及蛋白-蛋白互作网络分析。结果解读:共筛选出132个DEGs,其中86个基因上调、46个基因下调,HCN2基因显著下调;GO富集分析显示DEGs主要富集于系统过程调控、谷氨酸分泌正调控、突触传递调控、学习记忆等生物学过程;蛋白-蛋白互作网络分析显示核心基因富集于神经退行性疾病通路,提示七氟烷诱导的基因改变可能与神经退行性疾病存在共同致病通路。
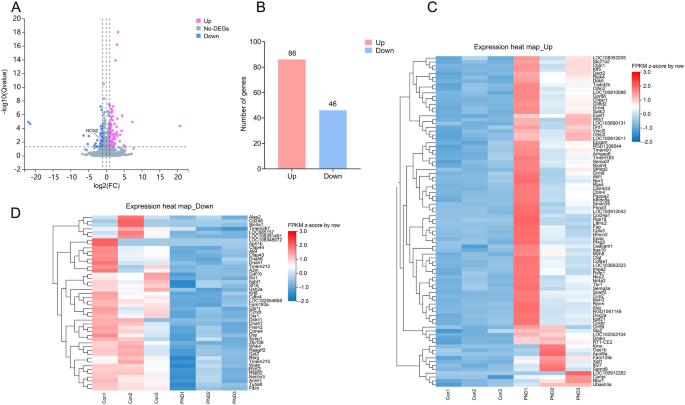
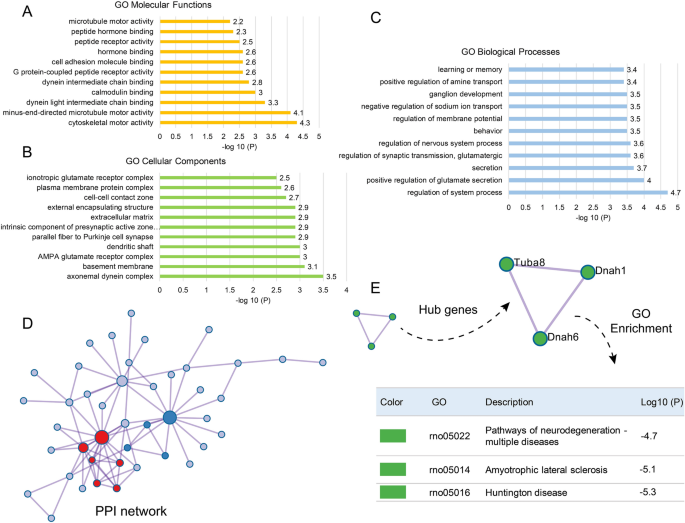
产品关联:文献未提及具体实验产品,领域常规使用Illumina测序平台、Metascape等生物信息学分析工具。
3.3 HCN通道及PEX5R/Trip8b表达验证与细胞定位
实验目的是验证七氟烷对HCN通道及其辅助亚基PEX5R/Trip8b表达的影响,并明确HCN2在中枢神经细胞的定位。方法细节:采用实时荧光定量PCR(RT-PCR)和蛋白质免疫印迹(WB)检测海马组织中HCN1-4及PEX5R/Trip8b的mRNA和蛋白表达;采用免疫荧光(IF)染色检测HCN2与神经元(Neun)、星形胶质细胞(GFAP)、小胶质细胞(iba1)的共定位情况及表达变化。结果解读:RT-PCR显示七氟烷暴露可显著下调HCN1-4及PEX5R/Trip8b的mRNA表达(n=4,P<0.05或P<0.01);WB显示HCN2和PEX5R/Trip8b蛋白表达显著下调,小胶质细胞激活标志物iba1蛋白表达显著上调(n=3,P<0.05或P<0.01);免疫荧光染色显示HCN2与神经元、星形胶质细胞、小胶质细胞均存在共定位,七氟烷暴露后HCN2与神经元、小胶质细胞的共定位数量显著减少(n=4,P<0.05或P<0.01)。
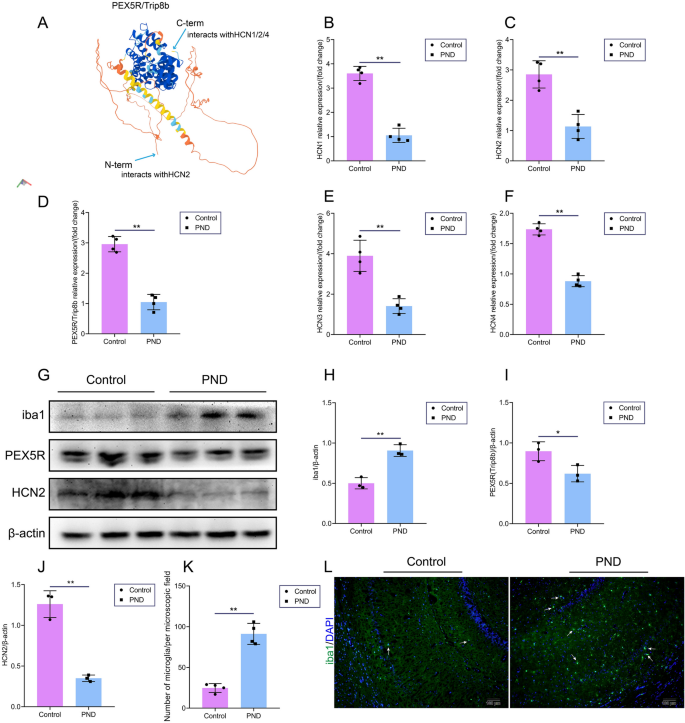
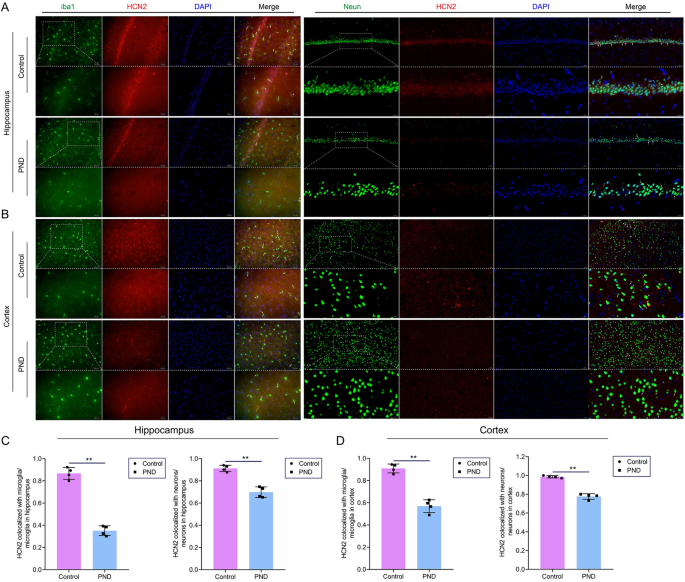
产品关联:实验所用关键产品:anti-HCN2(Invitrogen)、anti-PEX5R(Santa Cruz Biotechnology)、anti-iba1(Abcam)、EntiLink™ 1st Strand cDNA Synthesis Kit(ELK Biotechnology)、EnTurbo™ SYBR Green PCR SuperMix kit(ELK Biotechnology)、BCA蛋白测定试剂盒(Biosharp)、PVDF膜(Millipore)等。
3.4 脑内神经炎症水平检测
实验目的是验证七氟烷暴露是否可诱导大鼠脑内神经炎症反应。方法细节:采用酶联免疫吸附试验(ELISA)检测海马和皮层组织中白细胞介素-1β、白细胞介素-6、肿瘤坏死因子-α的水平;采用苏木精-伊红(HE)染色观察脑组织病理变化。结果解读:ELISA显示PND组大鼠海马和皮层中三种炎症因子水平均显著高于对照组(n=4,P<0.05或P<0.01);HE染色显示PND组大鼠海马和皮层组织中有炎症细胞浸润,神经元形态未出现明显损伤。
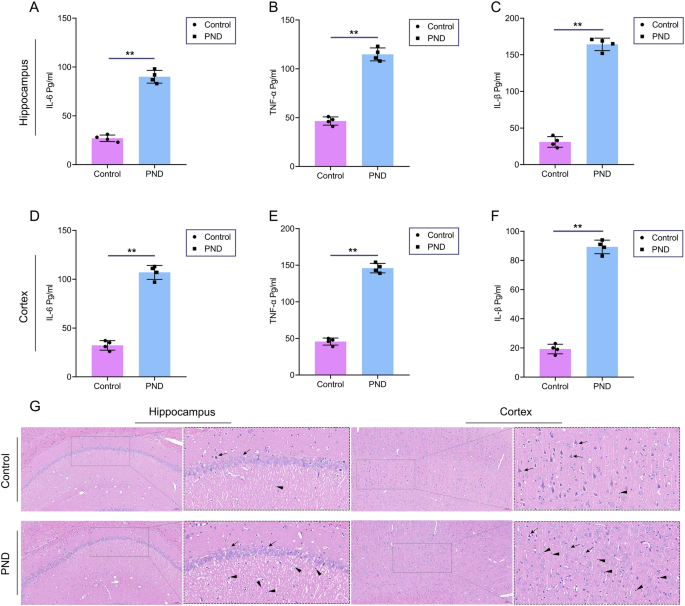
产品关联:实验所用关键产品:ELISA试剂盒(Bioswamp)、HE染色试剂盒(Solarbio)、酶标仪(Thermo Fisher Scientific)等。
3.5 HCN2抑制剂ZD7288功能验证实验
实验目的是验证HCN2通道在七氟烷诱导PND中的调控作用。方法细节:将PND大鼠随机分为PND-NS组(侧脑室注射生理盐水)和PND-HCN-B组(侧脑室注射HCN2选择性抑制剂ZD7288,10μg/5μl),再次评估大鼠行为学变化、小胶质细胞激活及神经炎症水平。结果解读:行为学实验显示,PND-HCN-B组大鼠的认知障碍及焦虑样行为较PND-NS组进一步加重(n=7,P<0.05或P<0.01);WB显示PND-HCN-B组大鼠HCN2蛋白表达进一步下调,iba1蛋白表达进一步上调(n=3,P<0.05或P<0.01);ELISA显示PND-HCN-B组大鼠海马和皮层中炎症因子水平显著升高(n=4,P<0.05或P<0.01),表明阻断HCN2通道可加重七氟烷诱导的PND。
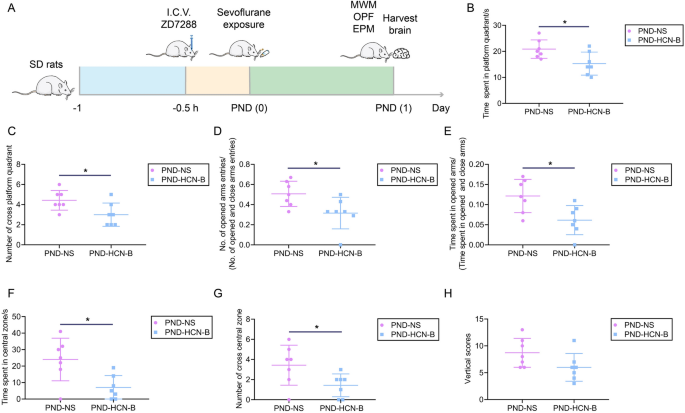
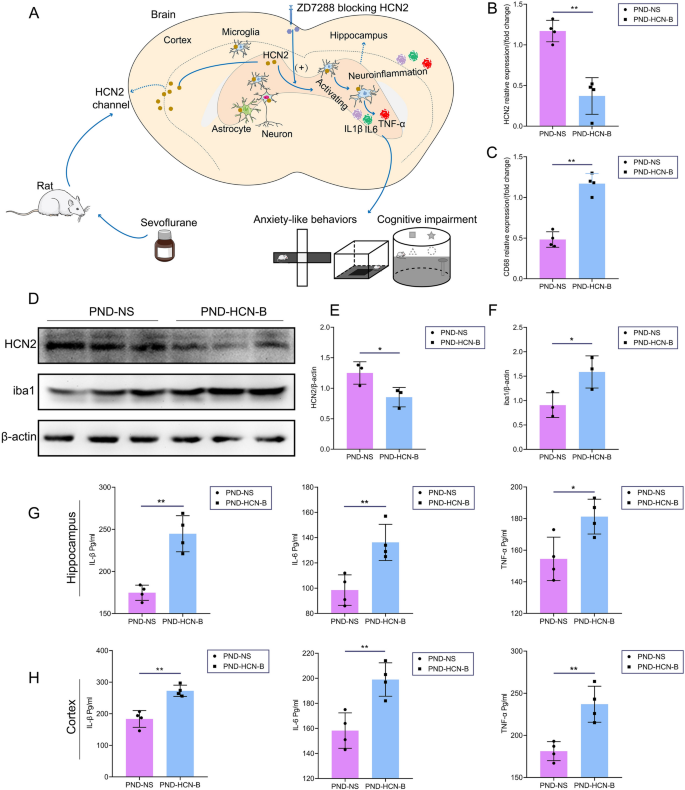
产品关联:实验所用关键产品:ZD7288(Sigma-Aldrich)、立体定位仪(RWD)等。
4. Biomarker研究及发现成果
Biomarker定位
本研究中涉及的Biomarker为HCN2通道,其筛选与验证逻辑为:首先通过转录组测序筛选出七氟烷暴露后显著下调的HCN2基因,随后通过RT-PCR、WB验证其mRNA及蛋白表达变化,再通过免疫荧光明确其在神经细胞的定位,最后通过HCN2抑制剂ZD7288的功能实验验证其在七氟烷诱导PND中的调控作用,形成完整的筛选-验证链条。
研究过程详述
HCN2来源于大鼠海马及皮层组织,采用RT-PCR、WB验证其在七氟烷暴露后表达显著下调;通过免疫荧光染色明确其在神经元、星形胶质细胞、小胶质细胞均有表达,且七氟烷暴露后HCN2与神经元、小胶质细胞的共定位数量显著减少(n=4,P<0.05);采用HCN2抑制剂ZD7288处理后,大鼠的认知障碍、焦虑样行为及神经炎症水平进一步加重,表明HCN2通道的下调与七氟烷诱导PND的发生密切相关。本研究未提供HCN2作为PND诊断Biomarker的特异性与敏感性数据,仅验证了其功能调控作用。
核心成果提炼
本研究的核心成果为明确HCN2通道是七氟烷诱导PND的关键调控靶点,七氟烷通过下调PEX5R/Trip8b-HCN2通道,激活小胶质细胞并诱导神经炎症,最终导致大鼠认知障碍及焦虑样行为;首次在体内实验层面证实HCN2通道在七氟烷诱导PND中的作用,为PND的防治提供了新的分子靶点。统计学结果显示,七氟烷暴露可使HCN2 mRNA表达显著下调(n=4,P<0.05),ZD7288处理可使炎症因子水平显著升高(n=4,P<0.05)。推测:HCN2通道可能通过调控小胶质细胞的吞噬功能及炎症因子分泌参与PND的发生发展,需进一步体外实验验证具体分子机制。
