1. 领域背景与文献引入
文献英文标题:The balance between NANOG and SOX17 mediated by TET proteins regulates specification of human primordial germ cell fate;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:人类原始生殖细胞命运调控、表观遗传学
原始生殖细胞(PGCs)是连接亲代与子代的生殖细胞前体,在胚胎发育早期经历全基因组DNA甲基化重编程,建立表观遗传空白状态,为后续生殖细胞发育奠定基础。领域关键节点包括2015年Guo等和Tang等分别解析了人类PGCs的转录组与甲基组特征,2017年Kojima等揭示了人类PGC特化的独特转录调控程序。当前研究热点聚焦于表观遗传修饰(如TET家族蛋白介导的5mC氧化去甲基化)在PGC命运决定中的作用,以及物种间调控机制的差异。未解决的核心问题包括人类PGC特化起始阶段TET蛋白与关键转录因子的相互调控机制,以及DNA甲基化与去甲基化的平衡如何影响PGC命运决定。
结合领域现状,现有研究在小鼠中已明确Tet蛋白通过调控Nodal信号通路影响原肠胚形成,但人类中TET蛋白对PGC特化的调控机制仍不清晰,且物种间的调控差异未被系统揭示。本研究针对这一空白,通过构建TET家族蛋白全敲除的人胚胎干细胞(hESC)系,结合体外PGC样细胞(hPGCLCs)诱导模型,解析了TET蛋白调控人类PGCLCs特化的表观遗传机制,为人类生殖细胞发育的表观调控研究提供了新的视角。
2. 文献综述解析
作者以物种(人、小鼠)为核心分类维度,结合转录调控与表观调控两个研究层次,系统综述了PGC命运决定领域的现有研究,明确了人类与小鼠PGC调控的差异,凸显了本研究的创新价值。
现有研究中,小鼠模型的研究表明,Tet家族蛋白全敲除会导致Lefty1/2基因表达下调,Nodal信号通路过度激活,进而引发原肠胚形成缺陷;而人类领域的研究则聚焦于PGC特化的转录调控网络,发现SOX17是人类PGC特化的关键转录因子,NODAL信号通路调控其表达,但TET蛋白在人类PGC特化中的作用及与转录因子的相互作用机制尚未被揭示。现有研究的优势在于建立了稳定的人类hPGCLCs体外诱导模型,解析了PGC特化过程中的转录组与甲基组动态变化;局限性在于缺乏对表观调控因子与转录因子相互作用的机制研究,且未充分阐明物种间PGC调控的核心差异。
通过对比现有研究的未解决问题,本研究的创新点在于首次在人类系统中证明TET家族蛋白通过调控NODAL信号通路及NANOG/SOX17启动子的甲基化平衡,调控hPGCLCs特化,明确了与小鼠模型的调控差异,同时揭示了DNA甲基转移酶DNMT3B在其中的拮抗作用,完善了人类PGC特化的表观调控网络。
3. 研究思路总结与详细解析
本研究的整体研究框架围绕“TET蛋白调控人类hPGCLCs特化的机制”展开,研究目标是明确TET家族蛋白在人类hPGCLCs特化中的功能及表观调控机制,核心科学问题是TET蛋白如何通过调控DNA甲基化平衡关键转录因子NANOG与SOX17的表达,进而决定hPGCLCs命运,技术路线遵循“基因敲除→表型分析→机制解析→功能验证”的闭环逻辑,通过多组学分析与分子生物学实验相结合,系统揭示了调控机制。
3.1 TET敲除hESC系构建与hPGCLCs诱导缺陷验证
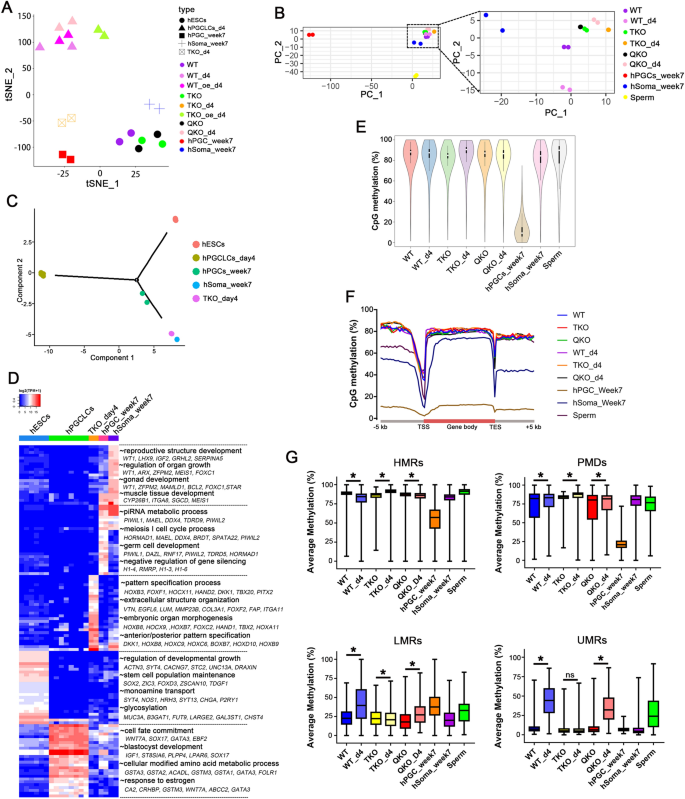
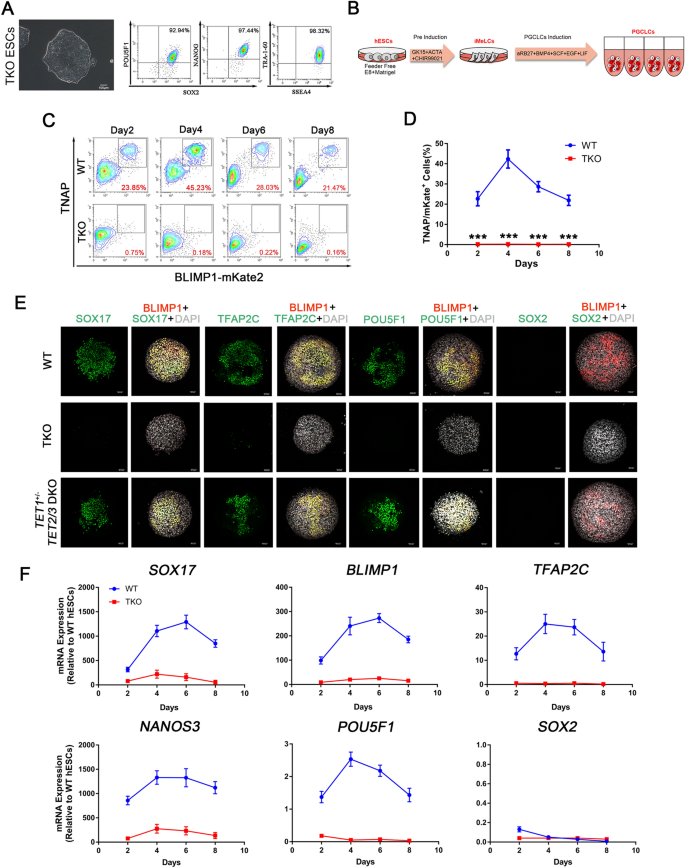
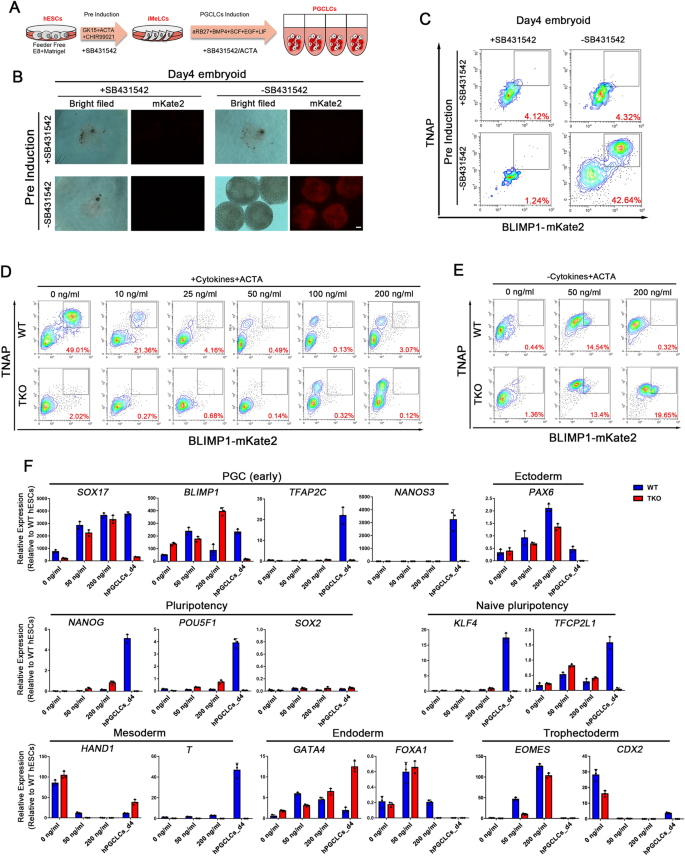
实验目的是验证TET家族蛋白对人类hPGCLCs特化的必要性。方法细节上,研究人员利用CRISPR-Cas9基因编辑技术,构建了携带BLIMP1-2A-mKate2报告基因的TET1、TET2、TET3三敲除(TKO)H1 hESC系,通过DNA测序验证基因敲除效率;采用优化的hPGCLCs体外诱导方案,将hESCs诱导为类内胚层样细胞(iMeLCs)后,进一步诱导形成hPGCLCs;通过流式细胞术(FACS)检测组织非特异性碱性磷酸酶(TNAP)与BLIMP1双阳性细胞比例,评估hPGCLCs诱导效率;同时利用RNA测序(RNA-seq)与全基因组亚硫酸氢盐测序(WGBS)分析转录组与甲基组变化。结果解读显示,TKO hESCs的5-羟甲基胞嘧啶(5hmC)水平显著降低,且无5hmC信号检测到(n=3,P<0.001),但5-甲基胞嘧啶(5mC)水平与野生型(WT)hESCs无差异;TKO hESCs在诱导hPGCLCs时,TNAP/BLIMP1双阳性细胞比例从诱导第2天到第8天均为0(n=3,P<0.001),关键hPGC基因如SOX17、BLIMP1、TFAP2C等的mRNA与蛋白表达水平显著下调。实验所用关键产品:CRISPR载体pX330-U6-Chimeric_BB-CBh-hSpCas9,流式抗体FITC-conjugated anti-human/mouse TNAP、PerCP-Cy™5.5 Mouse anti-Oct3/4,RNA-seq与WGBS测序平台Illumina系列。
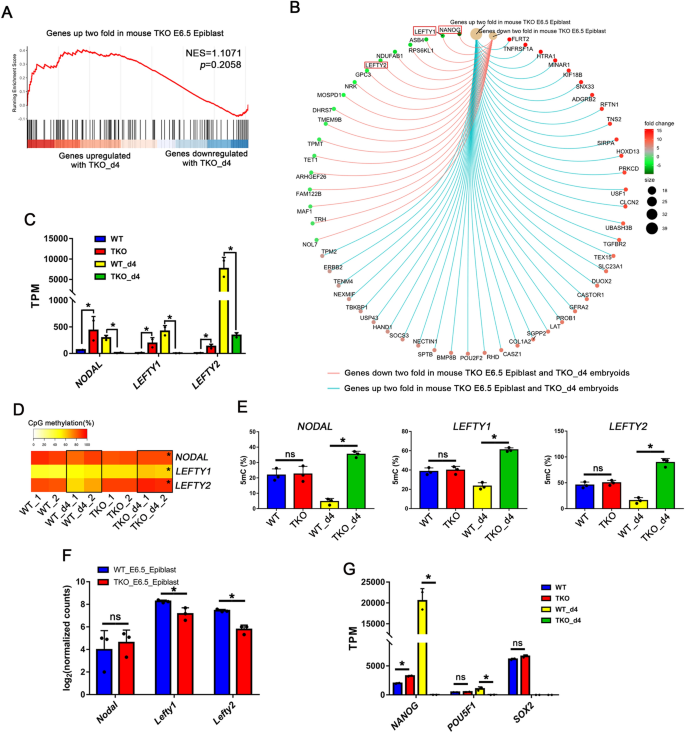
3.2 NODAL信号通路在TET调控hPGCLCs中的作用解析
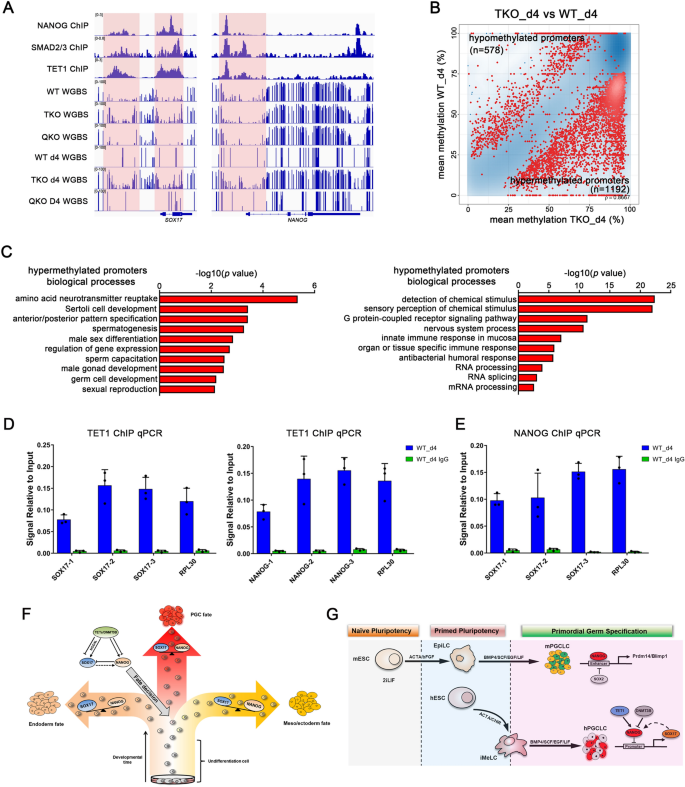
实验目的是探究TET家族蛋白是否通过调控NODAL信号通路影响hPGCLCs特化。方法细节上,研究人员分别使用NODAL信号通路抑制剂SB431542与激活剂Activin A处理细胞,通过流式细胞术检测hPGCLCs诱导效率;利用染色质免疫沉淀-定量PCR(ChIP-qPCR)验证TET蛋白与NODAL、LEFTY1、LEFTY2启动子的结合情况;通过Epimark甲基化分析检测上述基因启动子的甲基化水平。结果解读显示,TKO hESCs中NODAL、LEFTY1、LEFTY2的启动子区域呈现高甲基化状态(n=3,P<0.05),其mRNA表达水平显著低于WT hESCs诱导的hPGCLCs;抑制NODAL信号通路可完全阻断WT hESCs的hPGCLCs诱导,而单独激活NODAL信号通路仅能上调SOX17表达,无法维持NANOG的表达,不能诱导形成功能性hPGCLCs。实验所用关键产品:NODAL抑制剂SB431542(Selleck,S1067),激活剂Activin A(PEPRO TECH,120-14E),ChIP试剂盒SimpleChIP Plus Enzymatic Chromatin IP kit(Cell Signaling Technology,9003S)。
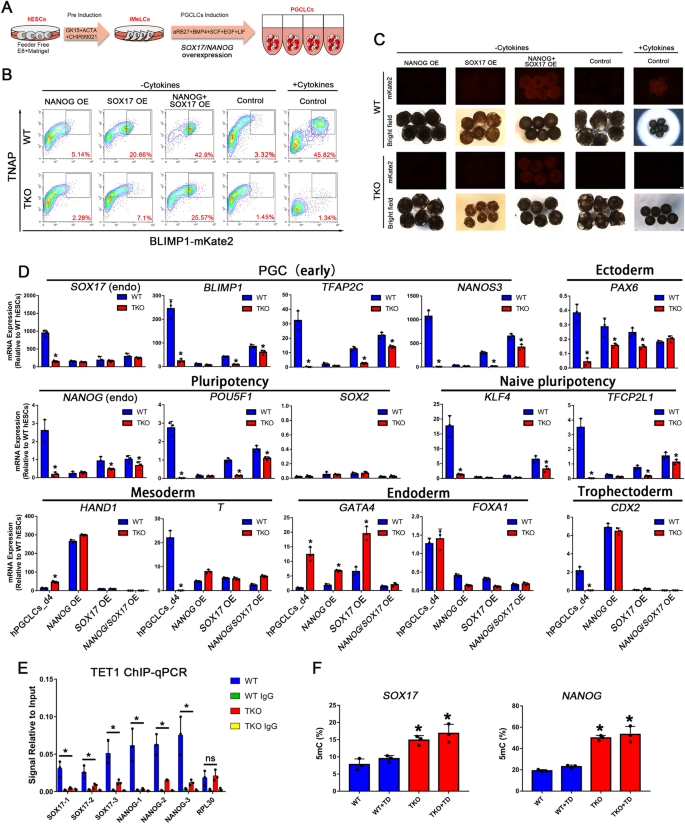
3.3 NANOG与SOX17的甲基化平衡调控机制验证
实验目的是验证TET家族蛋白通过调控NANOG与SOX17启动子的甲基化平衡,调控hPGCLCs特化。方法细节上,研究人员基于Gateway系统构建了可诱导过表达NANOG与SOX17的hESC系,通过添加诱导剂doxycycline与Trimethoprim实现基因过表达,利用流式细胞术检测hPGCLCs诱导效率;通过染色质免疫沉淀-定量PCR验证TET蛋白与NANOG启动子的结合,以及NANOG蛋白与SOX17启动子的结合;通过Epimark甲基化分析检测NANOG与SOX17启动子的甲基化水平。结果解读显示,TKO hESCs中NANOG与SOX17的启动子区域呈现高甲基化状态(n=3,P<0.05),其mRNA与蛋白表达水平显著下调;同时过表达NANOG与SOX17可部分恢复TKO hESCs的hPGCLCs诱导效率,而单独过表达其中一个基因则无法有效恢复;染色质免疫沉淀-定量PCR结果证实NANOG可直接结合SOX17的启动子区域,调控其表达。实验所用关键产品:Gateway系统载体(Thermo Fisher Scientific),诱导剂doxycycline(Sigma-Aldrich,D9891)、Trimethoprim(Sigma-Aldrich,T7883)。
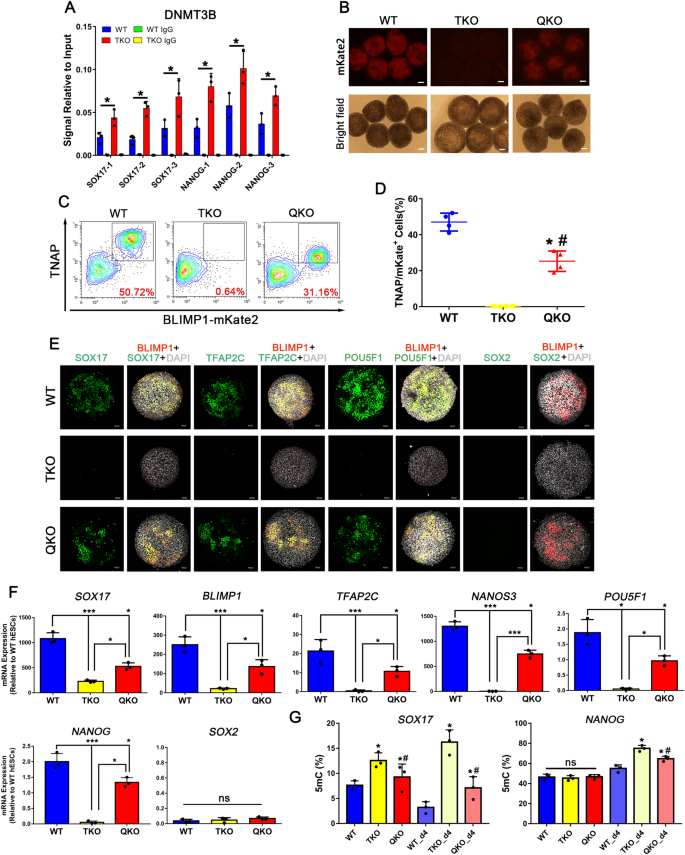
3.4 DNMT3B的拮抗作用验证
实验目的是验证DNA甲基转移酶DNMT3B在TET调控hPGCLCs特化中的拮抗作用。方法细节上,研究人员利用CRISPR-Cas9技术构建了TET1/2/3与DNMT3B四敲除(QKO)的hESC系,通过DNA测序与Western blot验证基因敲除效率;利用流式细胞术检测QKO hESCs的hPGCLCs诱导效率;通过Epimark甲基化分析检测NANOG与SOX17启动子的甲基化水平;通过RT-qPCR与免疫荧光检测关键基因的表达水平。结果解读显示,QKO hESCs中NANOG与SOX17启动子的甲基化水平显著降低(n=3,P<0.05),hPGCLCs诱导效率部分恢复,TNAP/BLIMP1双阳性细胞比例约为30%(n=4,P<0.05);同时NODAL信号通路基因与hPGC关键基因的表达水平也部分恢复。实验所用关键产品:CRISPR载体pX330,Western blot检测试剂Thermo Scientific Pierce ECL Western Substrate(Thermofisher,32106),免疫荧光抗体Alexa Fluor® 647 Mouse anti-SOX2等。
4. Biomarker研究及发现成果
本研究的核心Biomarker为NANOG与SOX17启动子区域的DNA甲基化水平,以及两者的表达平衡状态,属于表观遗传类Biomarker,其筛选与验证遵循“甲基组差异分析→功能验证→机制解析”的完整逻辑链条。
Biomarker定位方面,该Biomarker属于人类PGCLCs特化的表观调控节点,筛选逻辑是通过对比TKO hESCs与WT hESCs诱导的hPGCLCs的全基因组甲基组数据,发现NANOG与SOX17启动子区域的甲基化水平存在显著差异,随后通过功能实验验证其与hPGCLCs特化的相关性。研究过程详述中,Biomarker的来源为hESC与诱导的hPGCLCs细胞基因组DNA;验证方法包括全基因组亚硫酸氢盐测序(WGBS)、Epimark甲基化分析、染色质免疫沉淀-定量PCR等;特异性与敏感性数据显示,TKO hESCs中NANOG启动子的甲基化水平较WT hESCs诱导的hPGCLCs高约25%(n=3,P<0.05),SOX17启动子的甲基化水平高约30%(n=3,P<0.05),且该甲基化差异与hPGCLCs诱导效率呈负相关。
核心成果提炼方面,该Biomarker的功能关联在于,NANOG与SOX17启动子的甲基化平衡是人类hPGCLCs特化的关键调控节点,TET家族蛋白通过介导去甲基化维持该平衡,而DNMT3B则通过介导从头甲基化拮抗这一过程,两者的相互作用调控NANOG与SOX17的表达平衡,进而决定hPGCLCs的命运。创新性在于首次在人类系统中揭示了这一表观调控机制,明确了与小鼠模型的调控差异,为人类生殖细胞发育的表观调控研究提供了新的Biomarker与调控靶点。