1. 领域背景与文献引入
文献英文标题:The key cellular senescence related molecule RRM2 regulates prostate cancer progression and resistance to docetaxel treatment;发表期刊:Cell & Bioscience;影响因子:10.7;研究领域:前列腺癌化疗耐药与细胞衰老机制研究。
前列腺癌是全球男性发病率最高的恶性肿瘤之一,雄激素剥夺治疗是局限性前列腺癌的标准治疗方案,但约80%的患者会在5年内进展为去势抵抗性前列腺癌(CRPC)。多西他赛作为CRPC的一线化疗药物,可显著延长患者总生存期,但超过60%的患者会在1年内出现耐药,成为临床治疗的核心难题。领域共识:细胞衰老作为一种永久性生长停滞状态,在肿瘤发生发展及化疗耐药中发挥双重作用,衰老相关基因的异常表达可通过调控DNA修复、细胞存活通路影响肿瘤对化疗药物的敏感性,但具体调控网络尚未完全阐明。现有研究已证实核苷酸还原酶亚基M2(RRM2)在多种恶性肿瘤中高表达,与肿瘤增殖、转移及不良预后密切相关,但RRM2在前列腺癌多西他赛耐药中的作用及分子机制尚未明确,本研究针对这一研究空白,系统探索RRM2介导前列腺癌化疗耐药的调控通路,为克服CRPC耐药提供新的治疗靶点。
2. 文献综述解析
作者对领域内现有研究的分类维度主要分为三个方向:前列腺癌治疗现状与耐药困境、细胞衰老相关基因的肿瘤调控作用、RRM2与ANXA1的独立功能研究。在前列腺癌治疗领域,作者梳理了雄激素剥夺治疗的局限性、多西他赛的临床应用价值及耐药机制的研究进展,指出现有研究多聚焦于肿瘤细胞自身的基因突变及信号通路激活,对细胞衰老相关基因的调控作用关注不足;在细胞衰老研究方向,作者总结了衰老相关基因参与肿瘤化疗耐药的核心机制,包括DNA损伤修复能力增强、抗凋亡通路激活等,但尚未明确关键调控分子;在RRM2与ANXA1的研究中,作者指出RRM2作为DNA合成与修复的关键酶,在多种肿瘤中高表达并与化疗耐药相关,ANXA1可通过激活PI3K/AKT通路促进肿瘤进展,但两者在前列腺癌中的协同调控关系尚未见报道。通过对比现有研究的未解决问题,本研究的创新价值在于首次揭示RRM2通过稳定ANXA1蛋白、激活PI3K/AKT通路介导前列腺癌多西他赛耐药的分子机制,填补了细胞衰老基因调控前列腺癌化疗耐药的研究空白,为临床联合治疗提供了理论依据。
3. 研究思路总结与详细解析
本研究的整体框架遵循“生物信息学筛选-细胞功能验证-分子机制解析-临床转化探索”的闭环逻辑,核心研究目标是明确RRM2在前列腺癌进展及多西他赛耐药中的调控作用及分子机制,核心科学问题是RRM2如何通过下游分子调控PI3K/AKT通路影响化疗敏感性,技术路线涵盖数据库挖掘、细胞模型实验、动物模型验证、分子互作分析及联合治疗探索。
3.1 生物信息学筛选预后相关细胞衰老核心基因
实验目的是从公共数据库中筛选与前列腺癌预后相关的细胞衰老核心基因,确定RRM2为关键研究靶点。方法细节:整合TCGA-PRAD队列498例前列腺癌患者及297例正常样本数据,筛选34个细胞衰老相关核心基因,通过差异表达分析、Cox回归分析及Kaplan-Meier生存分析,构建包含RRM2在内的4基因预后风险模型,采用时间依赖ROC曲线评估模型预测性能。结果解读:热图显示30/31个细胞衰老相关基因在前列腺癌组织中差异表达(Fig1A),Cox回归分析证实RRM2是前列腺癌独立预后风险因子(Fig2A-D),预后模型的1年、3年、5年AUC值分别为0.744、0.706、0.64(Fig2I),提示RRM2高表达与患者不良预后密切相关。产品关联:文献未提及具体生物信息学分析工具品牌,领域常规使用TCGA、GEO、GEPIA等在线数据库及SPSS、R语言等分析软件。
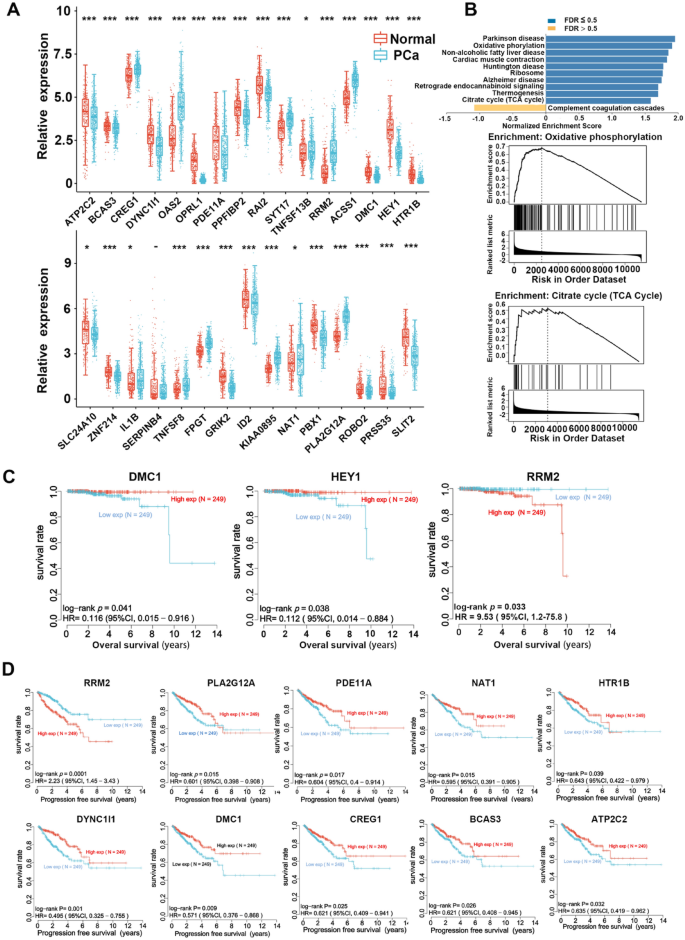
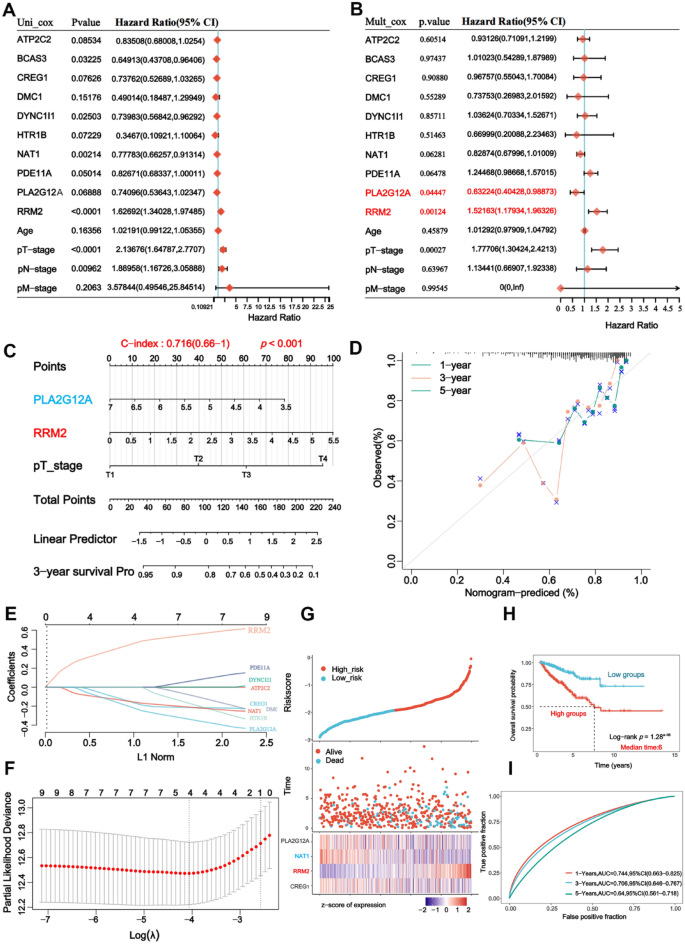
3.2 细胞模型验证RRM2对前列腺癌进展的调控作用
实验目的是在细胞水平验证RRM2对前列腺癌细胞增殖、凋亡及迁移的调控功能。方法细节:选取PC3、DU145等前列腺癌细胞系,采用Lipofectamine 2000转染siRNA敲低RRM2表达,通过CCK-8实验、克隆形成实验检测细胞增殖能力,流式细胞术检测细胞凋亡与坏死率,Transwell实验检测细胞迁移能力。结果解读:qRT-PCR及蛋白免疫印迹(WB)结果显示PC3、DU145细胞中RRM2表达水平显著高于正常前列腺上皮细胞(Fig3A-B),敲低RRM2后细胞克隆形成能力及增殖能力显著降低(n=3,P<0.01,Fig4D-H),凋亡率及坏死率显著升高(n=3,P<0.001,Fig4I-L),迁移细胞数显著减少(n=3,P<0.01,补充材料Fig1E-J)。产品关联:实验所用关键产品:ATCC的前列腺癌细胞系、Gibco的RPMI-1640培养基及胎牛血清、Thermo Fisher Scientific的Lipofectamine 2000转染试剂、APExBIO的CCK-8试剂盒、Elabscience的Annexin V-FITC凋亡检测试剂盒。
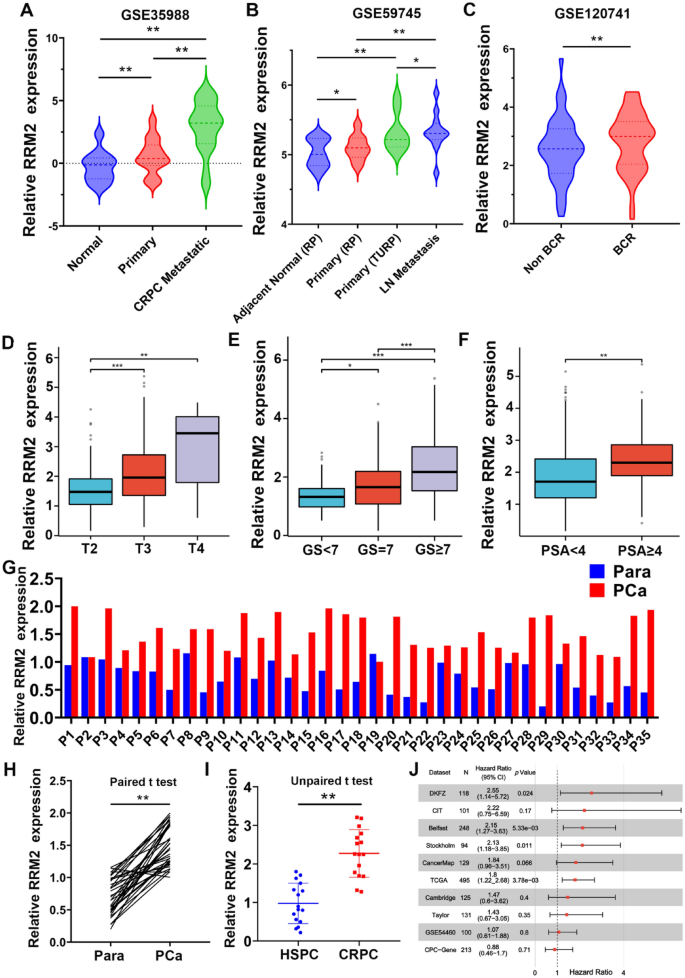
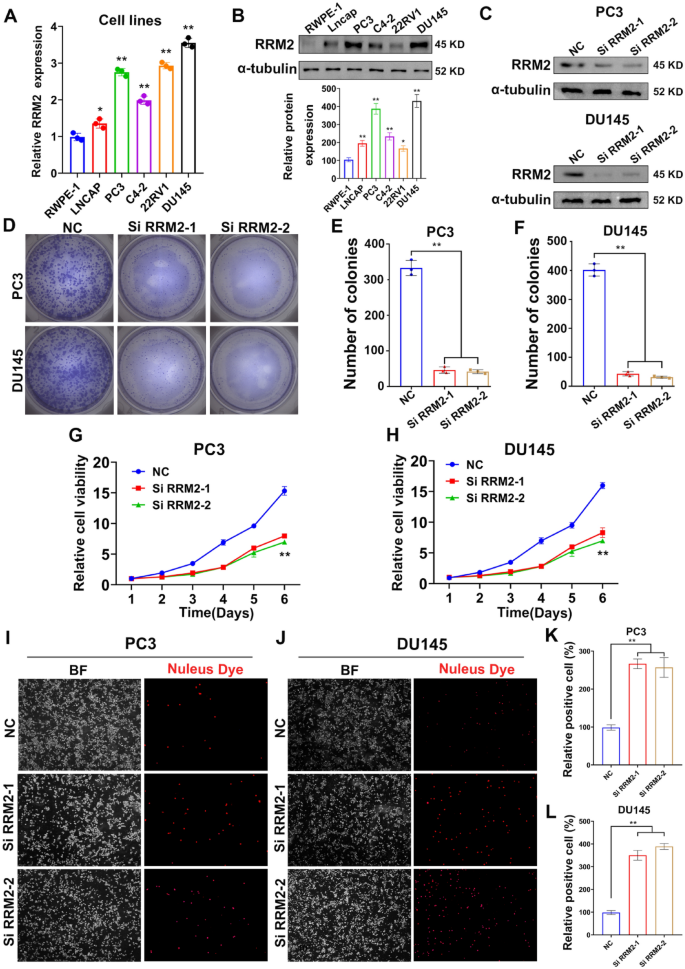
3.3 RRM2调控前列腺癌多西他赛耐药的体内外验证
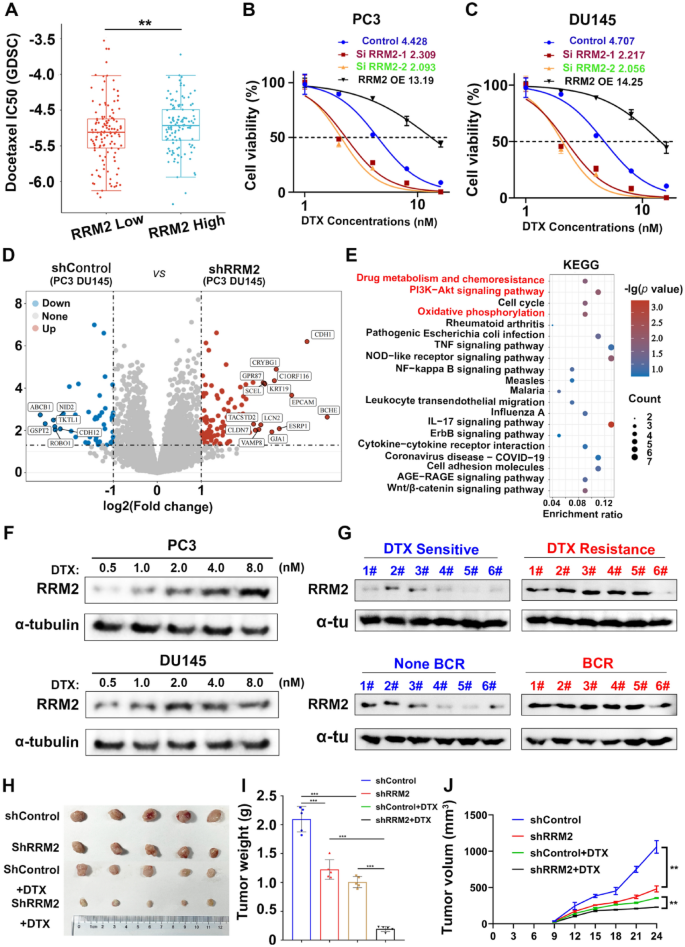
实验目的是明确RRM2与前列腺癌多西他赛耐药的相关性。方法细节:在PC3、DU145细胞中敲低RRM2,用不同浓度多西他赛处理48h后检测细胞活力,计算IC50;构建裸鼠异种移植模型,分为对照组、RRM2敲低组、多西他赛组、RRM2敲低+多西他赛组,每2天测量肿瘤体积,实验结束后取肿瘤组织检测相关蛋白表达。结果解读:GDSC数据库分析显示RRM2高表达与癌细胞多西他赛耐药显著相关(Fig5A),敲低RRM2后PC3细胞对多西他赛的IC50显著降低(Fig5B-C),裸鼠模型中RRM2敲低+多西他赛组肿瘤体积显著小于多西他赛组(n=5,P<0.01,Fig5H-I),协同指数为0.732,提示两者具有协同抗肿瘤效应。产品关联:实验所用关键产品:多西他赛(临床用化疗药物)、Calcusyn 2.0软件用于计算协同指数。
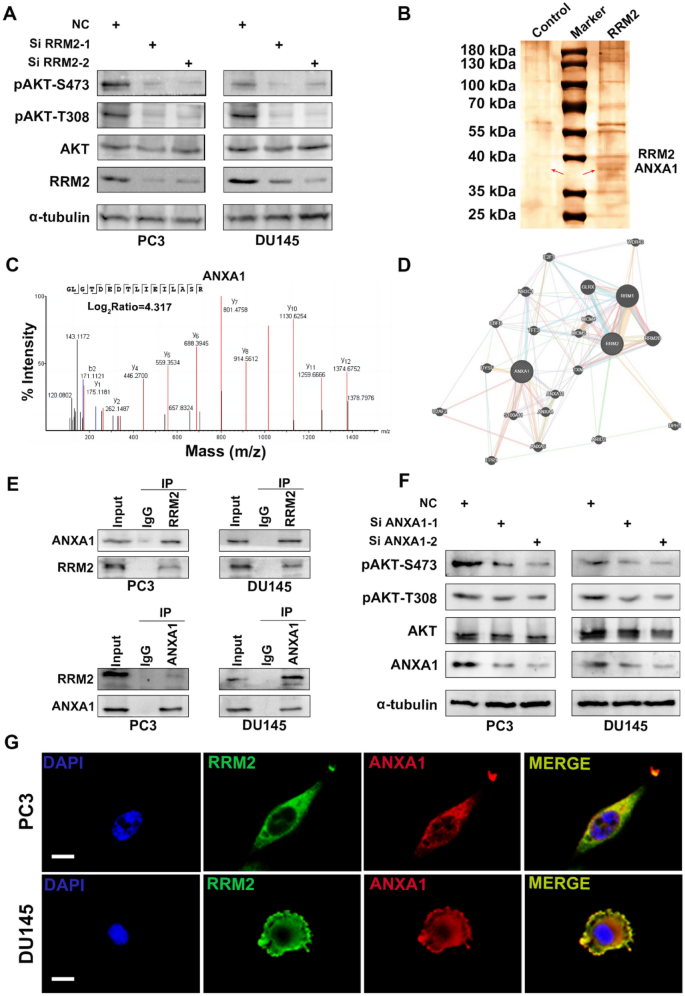
3.4 RRM2通过稳定ANXA1激活PI3K/AKT通路的机制研究
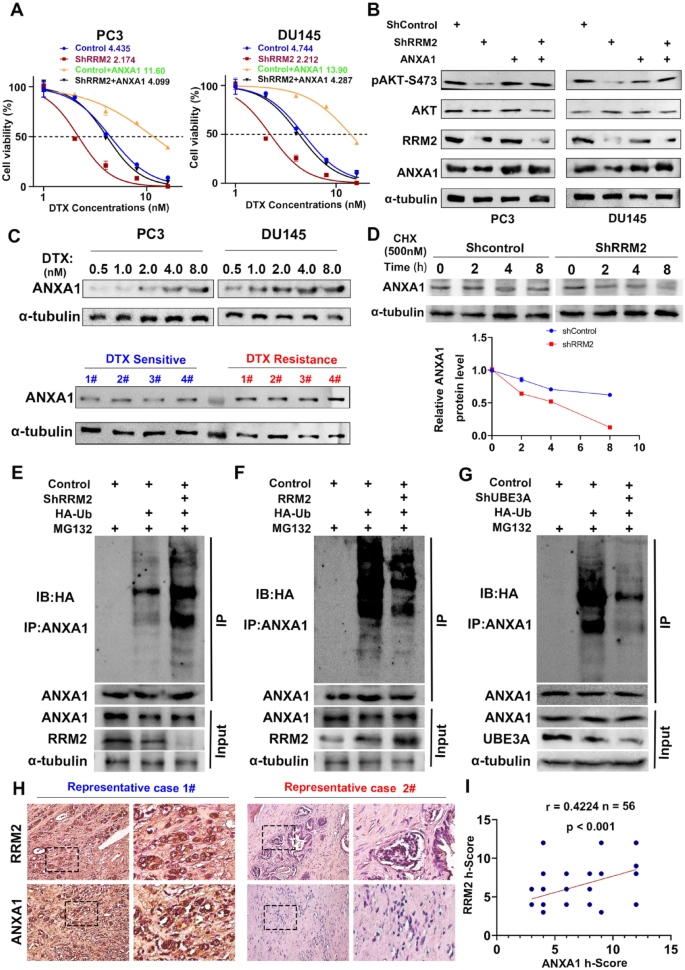
实验目的是探索RRM2介导多西他赛耐药的分子机制。方法细节:通过Co-IP结合质谱分析寻找RRM2的相互作用蛋白,采用免疫荧光共定位验证RRM2与ANXA1的细胞内定位;敲低或过表达RRM2,检测ANXA1的蛋白、mRNA水平及PI3K/AKT通路的磷酸化水平;通过泛素化实验检测RRM2对ANXA1蛋白稳定性的调控作用。结果解读:Co-IP及质谱分析证实ANXA1是RRM2的相互作用蛋白(Fig6B-C),免疫荧光显示两者在细胞质中共定位(Fig6G);敲低RRM2后ANXA1蛋白水平显著降低(n=3,P<0.01),但mRNA水平无变化,ANXA1的半衰期缩短、泛素化水平升高(Fig7D-F);过表达ANXA1可逆转RRM2敲低导致的AKT磷酸化降低及多西他赛敏感性增加(Fig7A)。产品关联:实验所用关键产品:Proteintech的ECL检测系统、Zeiss的共聚焦显微镜、MEIMIAN的IL-6/IL-8 ELISA试剂盒。
3.5 RRM2抑制剂与多西他赛联合治疗效果探索
实验目的是验证RRM2抑制剂COH29与多西他赛联合治疗的协同效应。方法细节:用不同浓度的COH29单独或联合多西他赛处理PC3、DU145细胞,CCK-8检测细胞活力,采用Calcusyn 2.0软件计算协同指数(CI)。结果解读:COH29单独处理可剂量依赖性抑制前列腺癌细胞增殖,与多西他赛联合处理的CI值<1,显示显著协同效应(补充材料Fig3C-F),提示联合治疗可增强多西他赛的抗肿瘤效果。产品关联:实验所用关键产品:COH29(RRM2特异性抑制剂)。
4. Biomarker研究及发现成果解析
Biomarker定位:RRM2作为前列腺癌多西他赛耐药的预后生物标志物,筛选逻辑是通过TCGA数据库筛选细胞衰老相关基因,经Cox回归分析确定为独立预后风险因子,随后在细胞、动物及临床样本中验证其与化疗耐药的相关性。研究过程详述:RRM2的来源包括前列腺癌组织、细胞系及患者血清样本,验证方法包括qRT-PCR、免疫组化(IHC)及ELISA检测,临床样本分析显示RRM2高表达与多西他赛耐药、生化复发显著相关(n=56,P<0.001,Fig3G-I);特异性与敏感性方面,预后模型的1年ROC曲线AUC为0.744,显示较好的预后预测性能。核心成果提炼:RRM2是前列腺癌独立预后因子,高表达患者的总生存期及无进展生存期显著缩短(HR=1.89,95%CI 1.23-2.91,P<0.01);首次发现RRM2通过稳定ANXA1蛋白激活PI3K/AKT通路介导多西他赛耐药,为前列腺癌的精准治疗提供新靶点;RRM2抑制剂与多西他赛联合治疗具有协同效应,为临床克服化疗耐药提供了新的治疗策略。
