1. 领域背景与文献引入
文献英文标题:Biological properties of bone marrow stem cells and adipose-derived stem cells derived from T2DM rats: a comparative study;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:2型糖尿病相关间充质干细胞组织再生
2型糖尿病(T2DM)是全球高发的慢性代谢疾病,约占糖尿病患者的90%-95%,长期高血糖引发的并发症严重威胁患者健康,其中糖尿病性骨质疏松以骨量降低、骨微结构破坏为核心特征,显著提升患者骨折风险并抑制骨折愈合,同时还会影响牙种植体骨整合、伤口愈合等过程,严重降低患者生活质量。领域共识:间充质干细胞(MSCs)因具备自我更新、多向分化潜能及低免疫原性,成为组织再生领域的研究热点,其中骨髓间充质干细胞(BMSCs)和脂肪间充质干细胞(ASCs)是临床应用最广泛的两类MSCs。当前领域的核心问题在于,T2DM的病理微环境会改变自体MSCs的生物学特性,而现有研究多聚焦于异体MSCs,针对T2DM患者自体BMSCs与ASCs的直接对比研究较为匮乏,无法为临床选择适配的自体干细胞提供依据。因此,本研究旨在对比T2DM大鼠来源的ASCs与BMSCs的生物学特性,为T2DM患者的组织再生治疗提供干细胞选择的实验依据。
2. 文献综述解析
作者以干细胞来源(异体vs自体)、干细胞类型(BMSCs vs ASCs)为核心分类维度,系统梳理了现有研究的核心结论与局限性。现有研究显示,异体MSCs在组织再生中展现出一定潜力,但存在临床应用受限、免疫原性争议等问题,尤其是T2DM作为慢性炎症性疾病,异体MSCs可能在炎症部位激活MHC II类分子引发免疫排斥,且传代后可能丧失低免疫原性。自体MSCs因具备长期存活、移植耐受等优势,成为更具前景的选择,其中BMSCs的成骨分化能力更强,但T2DM会抑制其数量、增殖能力及成骨分化潜能,且获取过程侵入性强、患者痛苦大;ASCs来源广泛、获取简便,T2DM对其数量和增殖能力的影响较小,但现有研究未明确其与T2DM来源BMSCs的成骨及增殖特性差异。本研究的创新点在于首次系统对比了T2DM大鼠来源的ASCs与BMSCs的增殖、成骨分化、细胞片形成等核心生物学特性,填补了T2DM自体干细胞选择依据的研究空白,为临床个性化干细胞治疗提供实验支撑。
3. 研究思路总结与详细解析
本研究以“明确T2DM病理微环境对自体MSCs生物学特性的影响,对比ASCs与BMSCs的临床适配性”为核心科学问题,通过构建T2DM大鼠模型,分离培养ASCs与BMSCs,从细胞鉴定、增殖能力、成骨分化、细胞片形成及体内骨缺损修复五个环节开展实验,形成“模型构建→细胞分离鉴定→体外功能验证→体内疗效验证”的完整技术路线。
3.1 T2DM大鼠模型构建与干细胞分离培养
实验目的:构建稳定的T2DM大鼠模型,分离获取具有干细胞特性的ASCs与BMSCs。
方法细节:选取24只8周龄雄性SD大鼠,随机分为T2DM组(n=16)和对照组(n=8),T2DM组给予高脂高糖饲料喂养4周后,腹腔注射35mg/kg链脲佐菌素(STZ),对照组注射柠檬酸缓冲液并给予普通饲料;造模4周后,随机血糖稳定在16.7mmol/L以上的大鼠判定为模型成功。随后从T2DM大鼠腹股沟脂肪组织分离ASCs,采用0.2%I型胶原酶消化1h,过滤离心后接种于T75培养瓶,传代至第3代;从双侧下肢骨髓腔冲洗获取BMSCs,同样培养传代至第3代。
结果解读:T2DM组大鼠出现多饮、多食、多尿症状,体重先升后降,血糖显著高于对照组(P<0.01),模型构建成功。流式细胞术检测显示,第3代ASCs与BMSCs均高表达干细胞表面标志物CD29、CD90,低表达造血细胞标志物CD34、CD45,且两组标志物表达水平无显著差异(P>0.05),证实分离细胞为间充质干细胞。
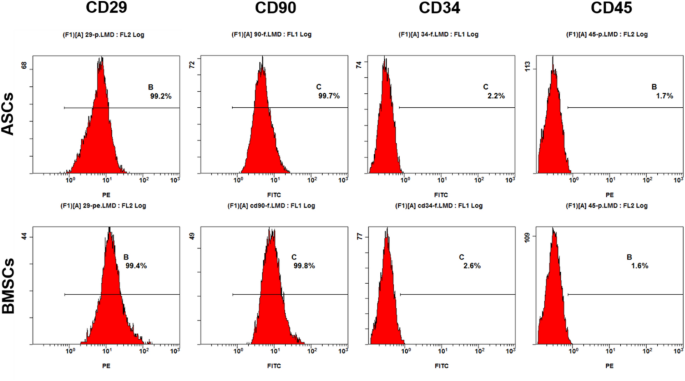
实验所用关键产品:链脲佐菌素(Sigma, USA)、I型胶原酶(Gibco, USA)、流式抗体CD29、CD90、CD34、CD45(CST, USA)、流式细胞仪(BD, USA)。
3.2 细胞增殖与克隆形成能力检测
实验目的:对比ASCs与BMSCs的体外增殖及克隆形成潜能。
方法细节:采用克隆形成实验,将两种细胞以1000个/皿的密度接种于100mm培养皿,培养10天后用甲醛固定、0.1%结晶紫染色,计数含50个以上细胞的克隆并计算克隆形成率;采用CCK-8法检测增殖能力,将细胞以3000个/孔接种于96孔板,连续8天检测450nm处吸光度(OD值)并绘制生长曲线。
结果解读:克隆形成实验显示,ASCs的克隆形成率为35.67%,显著高于BMSCs的25.67%(P<0.05);生长曲线呈典型S型,ASCs在培养第4-7天的OD值显著高于BMSCs(P<0.05),表明ASCs的增殖及克隆形成能力优于BMSCs。
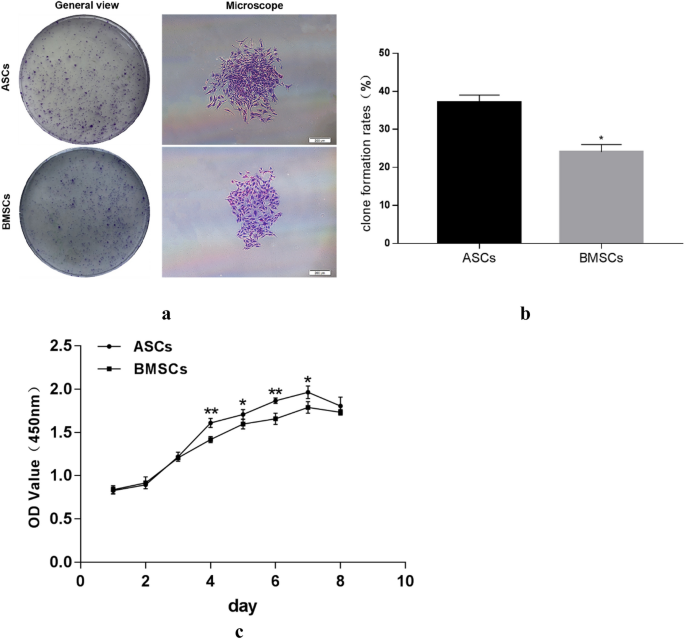
实验所用关键产品:结晶紫染料(Solaibio, China)、CCK-8试剂盒(EnoGene, China)。
3.3 成骨与成脂分化能力检测
实验目的:对比ASCs与BMSCs的多向分化潜能,重点关注成骨分化能力。
方法细节:成脂诱导:将两种细胞以2.5×10^5个/孔接种于6孔板,采用含地塞米松、吲哚美辛等的成脂诱导培养基培养14天,油红O染色观察脂滴形成;成骨诱导:采用含β-甘油磷酸钠、抗坏血酸等的成骨诱导培养基培养,7天后采用BCIP/NBT染色检测碱性磷酸酶(ALP)表达,28天后采用茜素红染色检测矿化结节形成,分别通过ImageJ半定量分析ALP染色面积占比、分光光度计检测茜素红染色OD值(620nm)。同时,成骨诱导7天后采用实时荧光定量PCR(qPCR)检测成骨相关基因(RUNX2、ALP、COL1、BMP、OCN)的mRNA表达,蛋白质免疫印迹(Western Blot)检测成骨相关蛋白表达。
结果解读:成脂分化显示,ASCs的脂滴数量及体积均大于BMSCs,成脂分化能力更强;成骨分化中,BMSCs的ALP染色面积占比显著高于ASCs(P<0.05),茜素红染色OD值显著更高(P<0.01),表明BMSCs的早期成骨及矿化能力更优。qPCR结果显示,BMSCs的ALP、COL1、BMP mRNA表达显著高于ASCs(COL1: P<0.05;BMP: P<0.05;ALP: P<0.01),OCN mRNA表达是ASCs的50倍(P<0.05),RUNX2表达无显著差异;Western Blot结果显示,BMSCs的OCN、RUNX2、COL1蛋白表达是ASCs的1.5-2倍,差异显著,进一步证实BMSCs的成骨分化潜能优于ASCs。
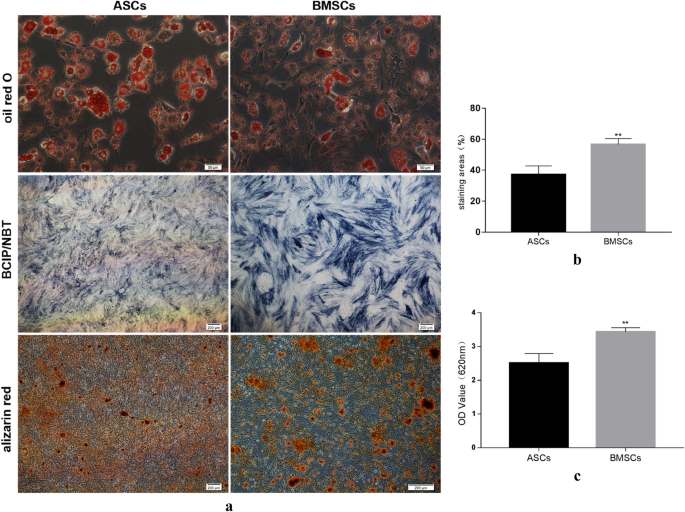
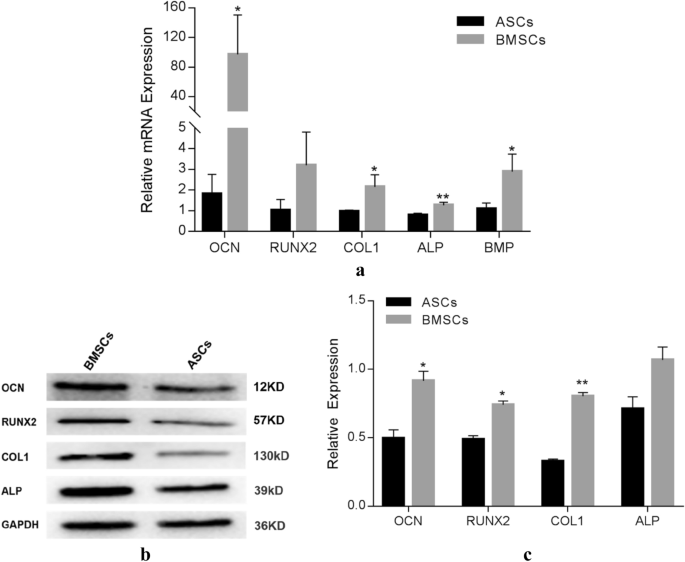
实验所用关键产品:成骨/成脂诱导培养基试剂(MP, USA)、油红O染料(Sigma, USA)、BCIP/NBT染料(CWBIO, China)、茜素红染料(Solaibio, China)、qPCR试剂盒(Takara, Japan)、Western Blot抗体(CST, USA)。
3.4 细胞片形成能力检测
实验目的:对比ASCs与BMSCs的细胞片形成能力,评估其组织再生应用潜力。
方法细节:将两种细胞接种于6孔板,待融合至90%后更换为含50mg/ml抗坏血酸的细胞片诱导培养基,培养10天后,采用扫描电子显微镜(SEM)观察细胞片表面及横截面形态,苏木精-伊红(H&E)染色观察细胞片结构,测量细胞片厚度。
结果解读:SEM及H&E染色显示,两种细胞均能形成细胞-基质-细胞的三明治结构,ASCs细胞片的厚度显著大于BMSCs(P<0.05),且细胞层数更多、细胞外基质更丰富,表明ASCs的细胞片形成能力更强,可能与其更优的增殖能力相关。

实验所用关键产品:抗坏血酸、扫描电子显微镜。
3.5 体内颅骨缺损修复实验
实验目的:在T2DM大鼠体内验证ASCs与BMSCs的骨缺损修复能力。
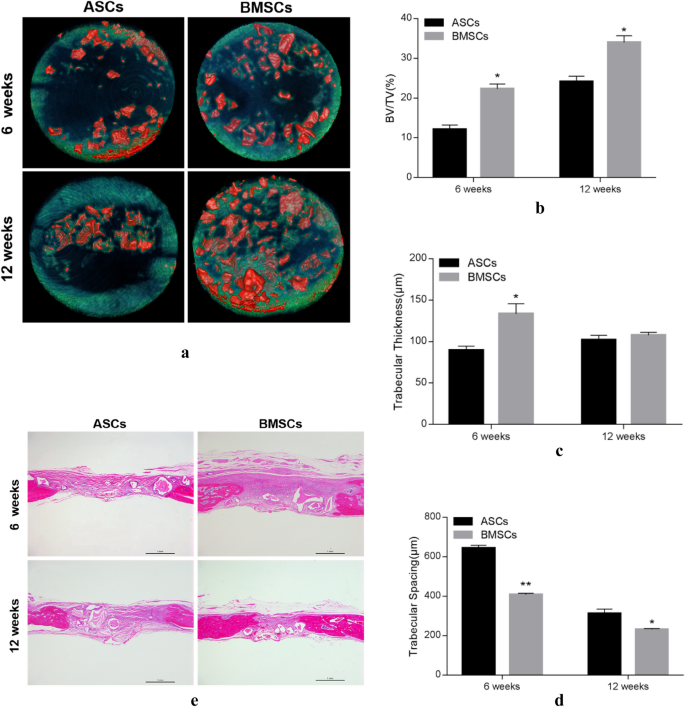
方法细节:将第3代ASCs与BMSCs分别与Bio-oss骨粉混合,植入T2DM大鼠颅骨5mm直径缺损处,每组n=8;术后6周、12周获取标本,采用Micro-CT扫描并进行三维重建,分析感兴趣区(ROI)的骨体积/总体积(BV/TV)、小梁厚度(Tb.Th)、小梁分离度(Tb.Sp);同时进行H&E染色观察骨组织再生情况。
结果解读:Micro-CT显示,术后6周BMSCs组的新骨形成更多,BV/TV显著高于ASCs组(P<0.05);术后12周BMSCs组的骨缺损修复更充分,BV/TV仍显著高于ASCs组(P<0.05),Tb.Th更厚、Tb.Sp更小。H&E染色显示,术后6周BMSCs组缺损边缘新骨形成更明显,12周时缺损显著缩小并形成成熟骨组织,而ASCs组仍有较多纤维组织。证实BMSCs在T2DM大鼠体内的骨缺损修复能力优于ASCs。
实验所用关键产品:Bio-oss骨粉(Geistlich, Switzerland)、Micro-CT设备。
4. Biomarker研究及发现成果解析
本研究以细胞群体(T2DM来源的ASCs与BMSCs)作为组织再生的功能型Biomarker,筛选/验证逻辑为“体外生物学特性检测→体内功能验证”,系统对比两类干细胞的增殖、成骨及组织修复能力。
研究过程中,细胞群体来源于T2DM大鼠的脂肪组织及骨髓组织,验证方法涵盖体外克隆形成实验、CCK-8增殖实验、成骨/成脂分化染色、qPCR及Western Blot分子检测,以及体内Micro-CT及组织学染色验证。特异性与敏感性方面,BMSCs在成骨分化相关指标(ALP表达、矿化结节、成骨基因/蛋白)及体内骨修复效果上均显著优于ASCs,而ASCs在增殖及细胞片形成指标上显著更优。
核心成果提炼:T2DM来源的BMSCs具备更强的成骨分化及骨缺损修复功能,可作为T2DM患者骨组织再生的优先选择干细胞;T2DM来源的ASCs具备更优的增殖及细胞片形成能力,更适合需要快速扩增、构建细胞片的组织再生场景。本研究的创新性在于首次明确了T2DM病理微环境下两类自体干细胞的功能差异,为临床个性化干细胞治疗提供了实验依据,所有组间差异均标注了P值及样本量,确保结果的可靠性。
