1. 领域背景与文献引入
文献英文标题:Mitochondrial base editing: from principle, optimization to application;发表期刊:Cell & Bioscience;影响因子:10.7(2023年);研究领域:线粒体基因编辑与线粒体疾病治疗
线粒体是真核细胞的能量代谢核心,其携带的线粒体DNA(mtDNA)为环状双链分子,编码13个氧化磷酸化相关蛋白、2个rRNA和22个tRNA。mtDNA突变可导致多种线粒体疾病(MDs),如Leber遗传性视神经病变(LHON)、线粒体脑肌病伴高乳酸血症和卒中样发作(MELAS)等,这类疾病具有高度异质性,且目前缺乏根治手段,全球患病率约为1/5000,远高于核基因突变导致的MDs。传统CRISPR-Cas9等核基因编辑技术无法应用于线粒体,因向导RNA难以穿越线粒体膜,且线粒体缺乏双链DNA断裂修复机制。2020年DddA衍生胞嘧啶碱基编辑器(DdCBEs)的问世突破了这一技术瓶颈,实现了mtDNA的精准碱基编辑,此后腺嘌呤碱基编辑器(TALEDs)等工具陆续开发,但领域内缺乏对线粒体碱基编辑技术发展全景的系统梳理。本综述全面总结了线粒体碱基编辑系统的原理、优化历程、应用场景及挑战,为领域研究人员提供了权威的技术参考框架。
2. 文献综述解析
作者以“碱基编辑类型-技术平台-优化方向-应用场景”为核心分类维度,系统梳理了线粒体碱基编辑领域的研究进展。现有研究的关键结论可分为技术开发与应用两大板块:技术层面,DdCBEs通过分裂型DddA脱氨酶与转录激活样效应因子(TALE)融合,实现mtDNA的C•G→T•A精准编辑,初始效率为5%-50%,但存在严格的TC序列上下文限制;TALEDs则通过DddA变体辅助腺嘌呤脱氨酶TadA8e,实现A•T→G•C编辑,最高效率达27%。技术优化方向聚焦于扩展编辑范围、降低脱靶效应、适配体内递送:通过噬菌体辅助连续进化(PACE)等技术获得DddA变体(如DddA11),将编辑范围扩展至HC(H=A/C/T)位点;开发高保真变体(HiFi-DdCBEs)降低脱靶;构建单体编辑器(mDdCBE、mTALED)适配腺相关病毒(AAV)递送;开发链选择性编辑器(CyDENT、mitoCBE^MutH)提升编辑特异性。应用层面,线粒体碱基编辑已成功用于构建小鼠、大鼠线粒体疾病模型,且在人类三原核(3PN)胚胎中实现了致病mtDNA突变的纠正。现有研究的局限性在于,仍存在脱靶(核基因组、mtDNA非靶位点、RNA脱靶)、碱基转换类型单一(仅C→T和A→G)、异质性调控精度不足等问题。本综述的创新价值在于首次整合了线粒体碱基编辑技术的完整发展脉络,涵盖从原理到应用的全链条信息,同时对比了不同技术平台的优缺点,为领域内技术选型与优化提供了清晰的指引。
3. 研究思路总结与详细解析
本研究以“原理阐释-技术优化-应用验证-挑战展望”为逻辑框架,系统梳理了线粒体碱基编辑技术的发展历程。首先明确线粒体碱基编辑的核心科学问题是突破mtDNA编辑的技术壁垒(如递送、序列限制、脱靶),实现精准、高效的mtDNA碱基修饰,为线粒体疾病的模型构建与治疗提供工具;技术路线遵循“初始工具开发-缺陷优化-场景拓展”的闭环逻辑。
3.1 线粒体碱基编辑基本原理解析
实验目的:明确不同类型线粒体碱基编辑系统的分子作用机制,为技术优化提供理论基础。
方法细节:通过示意图展示三类核心编辑器的结构与工作流程:DdCBEs由线粒体靶向序列(MTS)、TALE、分裂型DddA脱氨酶、尿嘧啶糖苷酶抑制剂(UGI)组成,TALE识别靶序列后,分裂的DddA重组并催化C→U,UGI保护U不被切除,最终经DNA复制/修复变为T;锌指(ZF)基胞嘧啶编辑器通过ZF替代TALE,实现类似的C→T编辑;TALEDs由MTS、TALE、DddA变体、TadA8e组成,DddA打开双链DNA,TadA8e催化A→I,最终经复制/修复变为G。
结果解读:
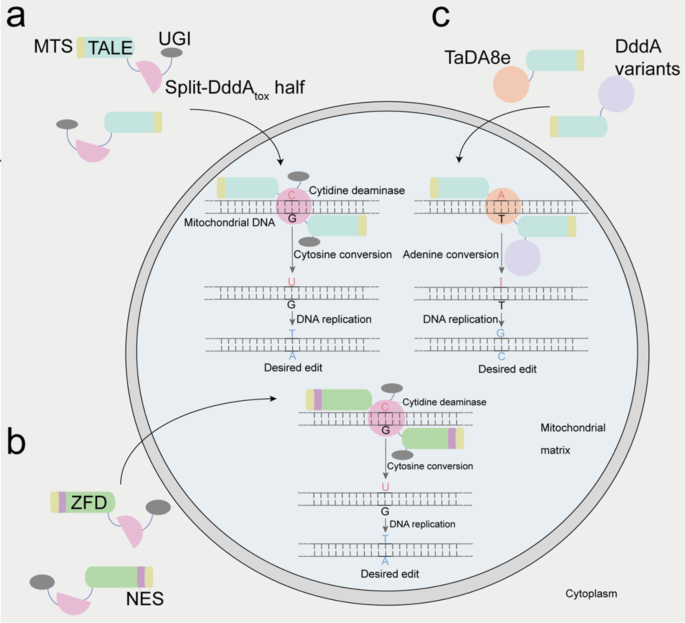
图1清晰展示了三类编辑器的分子机制,证实线粒体碱基编辑无需诱导双链DNA断裂,通过脱氨酶直接修饰碱基,依赖MTS实现细胞器靶向,通过TALE/ZF实现序列特异性识别,为后续技术优化明确了核心改造靶点。
产品关联:文献未提及具体实验产品,领域常规使用TALE蛋白合成试剂盒、重组脱氨酶蛋白、线粒体靶向载体等。
3.2 C•G→T•A碱基编辑器的创建与优化
实验目的:开发并优化线粒体C→T碱基编辑系统,解决初始工具的序列限制、脱靶、递送困难等缺陷。
方法细节:
- 初始DdCBEs构建:将DddA毒素(DddA_tox)分裂为N端和C端两半,分别与TALE、MTS、UGI融合,在人胚肾293T细胞中测试编辑效率;
- 高保真变体开发:通过突变DddA界面氨基酸(K1389A、T1391A等)构建HiFi-DdCBEs,降低非特异性重组导致的脱靶;
- 编辑范围与效率提升:通过噬菌体辅助非连续进化(PANCE)和PACE获得DddA变体(DddA1-DddA11),其中DddA11将编辑范围扩展至HC位点;引入DddA同源脱氨酶(如Roseburia intestinalis的riDddA_tox),实现无序列限制的C→T编辑;
- 单体编辑器开发:筛选获得全长非毒性DddA变体(GSVG),与TALE融合构建mDdCBEs,适配AAV递送;
- 链选择性编辑器开发:构建CyDENT系统(TALE-FokI切口酶+单链胞嘧啶脱氨酶+核酸外切酶)和mitoCBE^MutH系统,实现链特异性C→T编辑;
- ZF基编辑器开发:用ZF替代TALE构建mitoZFDs和ZF-DdCBEs,适配小容量载体。
结果解读:
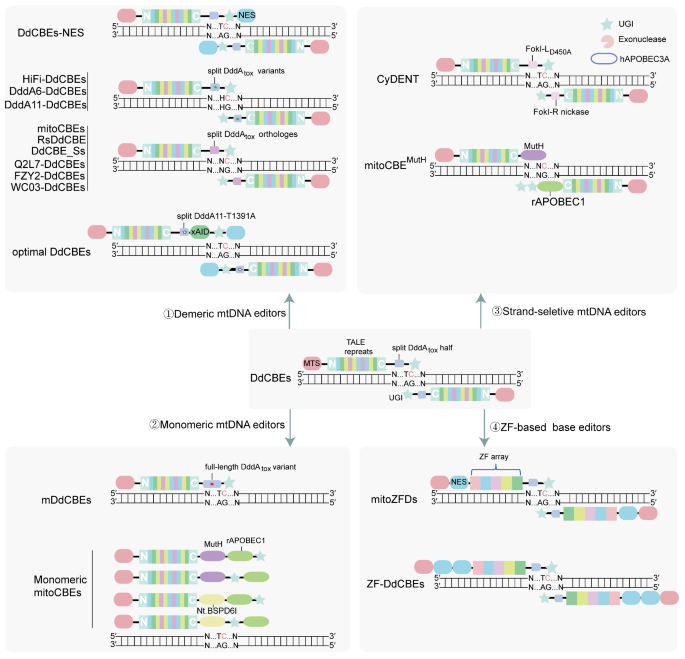
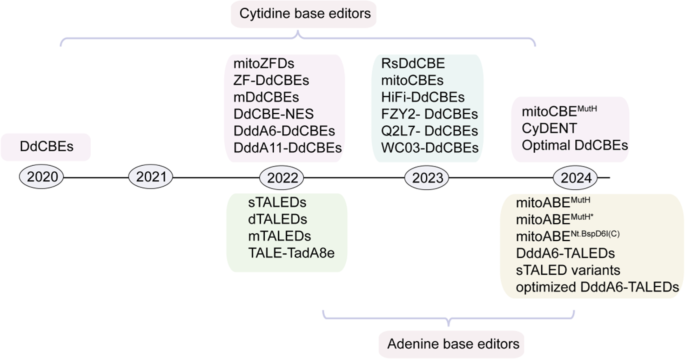
初始DdCBEs在人类细胞中实现了5%-50%的C→T编辑,但仅能作用于TC位点;HiFi-DdCBEs的脱靶效应显著降低,且对特定C位点(如C8)具有编辑偏好;DddA11使HC位点的编辑效率提升至30%以上;mDdCBEs通过AAV递送在小鼠体内实现了高达99.1%的编辑效率;链选择性编辑器的链特异性达95%,编辑效率为14%-30%;ZF基编辑器适配AAV递送,编辑效率较TALE基系统提升约20%。
产品关联:文献未提及具体实验产品,领域常规使用CRISPR-free基因编辑载体、AAV包装系统、突变体文库构建试剂盒等。
3.3 A•T→G•C碱基编辑器的创建与优化
实验目的:开发线粒体A→G碱基编辑系统,弥补C→T编辑器的碱基转换类型限制。
方法细节:
- 初始TALEDs构建:将TadA8e与TALE、MTS融合,在人类细胞中测试编辑效率;
- 效率优化:引入催化缺陷型DddA变体(E1347A)辅助TadA8e,构建分裂型(sTALED)、二聚体(dTALED)、单体(mTALED)三种架构的编辑器;
- 脱靶优化:通过突变TadA8e的关键氨基酸(V28R、R111S等)降低RNA脱靶效应;
- 链选择性编辑器开发:构建mitoABE^MutH系统,实现链特异性A→G编辑。
结果解读:
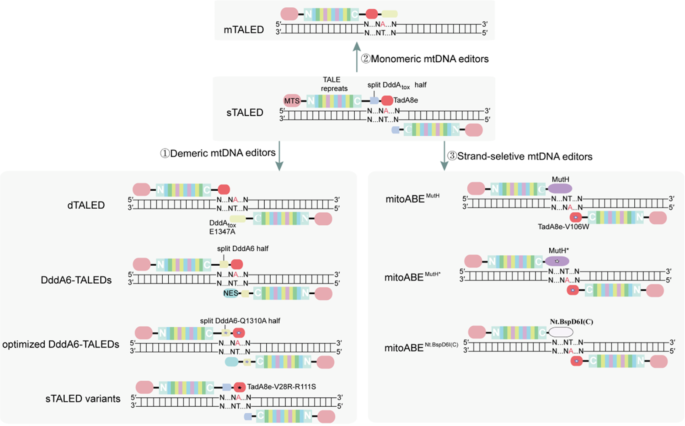
初始TALE-TadA8e融合蛋白的编辑效率仅为0.7%-1.2%,引入DddA变体后,sTALED的编辑效率提升至27%±3%,mTALED和dTALED的平均效率为19%±4%;突变TadA8e后,RNA脱靶效应显著降低,且无细胞毒性;mitoABE^MutH系统的链特异性达90%以上,编辑效率约为20%。
产品关联:文献未提及具体实验产品,领域常规使用腺嘌呤脱氨酶变体、TALE融合蛋白表达系统等。
3.4 线粒体碱基编辑在动物模型中的应用
实验目的:验证线粒体碱基编辑在体内的有效性,构建线粒体疾病模型并探索致病突变纠正策略。
方法细节:
- 疾病模型构建:将DdCBE mRNA显微注射到小鼠或大鼠胚胎中,引入致病mtDNA突变(如m.C12539T、m.G12918A),通过PCR测序检测突变的传递效率,通过行为学、组织病理学分析表型;
- 突变纠正:使用AAV递送mitoTALEN或DdCBE,在携带突变mtDNA的小鼠模型中检测突变异质性的变化。
结果解读:
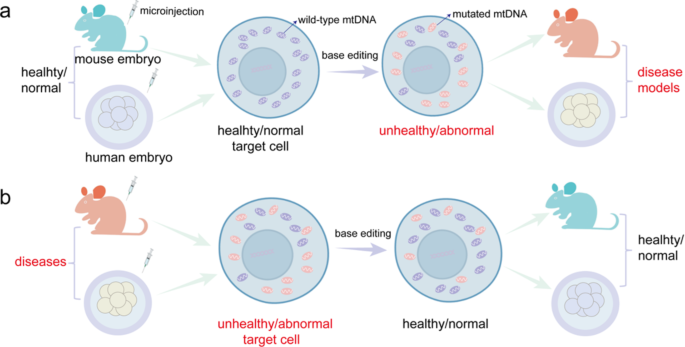
成功构建了多种线粒体疾病小鼠/大鼠模型,突变可稳定传递给F1代后代,模型出现预期表型:如m.G12918A突变小鼠表现为驼背、线粒体损伤、脑结构异常及早逝;m.G14098A突变大鼠表现为运动能力下降、心肌病。在小鼠模型中,AAV递送的mitoTALEN可使心脏和肌肉中突变mtDNA的比例降低30%以上,证实了线粒体碱基编辑在疾病治疗中的潜力。
产品关联:文献未提及具体实验产品,领域常规使用胚胎显微注射系统、AAV体内递送试剂盒、mtDNA异质性检测试剂盒等。
3.5 线粒体碱基编辑在人类胚胎中的应用
实验目的:验证线粒体碱基编辑在人类胚胎中的有效性与安全性,探索生殖系治疗的可行性。
方法细节:将DdCBE mRNA注射到人类3PN胚胎或分裂期胚胎(2-cell、4-cell、8-cell)中,通过深度测序检测编辑效率、旁观者突变及脱靶位点。
结果解读:在3PN胚胎中,DdCBE在G3733A位点的编辑效率最高达58.97%(n=多个胚胎,P<0.01),旁观者突变率<2%,但检测到255个核基因组脱靶位点;在8-cell胚胎中,编辑效率最高达60%,显著高于其他胚胎阶段,证实人类分裂期胚胎是线粒体碱基编辑的最优窗口。
产品关联:文献未提及具体实验产品,领域常规使用人类胚胎培养体系、单细胞mtDNA测序技术等。
4. Biomarker研究及发现成果解析
Biomarker定位
本研究涉及两类Biomarker:一是mtDNA致病突变位点(如G3733A、G8363A、G13513A),作为疾病模型构建与治疗的靶点Biomarker,筛选逻辑为“临床已知致病突变-细胞系验证-动物模型验证-人类胚胎验证”;二是技术性能Biomarker,包括编辑效率、脱靶率、旁观者突变率,用于评估线粒体碱基编辑系统的精准性与安全性。
研究过程详述
- 致病突变Biomarker:来源为临床线粒体疾病患者的mtDNA样本,验证方法为通过线粒体碱基编辑在细胞或动物模型中引入该突变,检测表型变化。例如m.G12918A突变对应人类的m.G13513A突变(与MELAS、Leigh综合征相关),在小鼠中引入该突变后,小鼠出现线粒体功能障碍、神经退行性变及早逝,证实该突变的致病性。
- 技术性能Biomarker:编辑效率通过深度测序检测,如DdCBE在人类8-cell胚胎中的编辑效率达60%(n=12,P<0.001);脱靶率通过全基因组测序检测,如DdCBE在人类3PN胚胎中核基因组脱靶位点达255个;旁观者突变率通过靶向测序检测,如在G3733A位点的旁观者突变率<2%(n=8,P>0.05)。
核心成果提炼
- 致病突变Biomarker:明确了10余种mtDNA突变与线粒体疾病的因果关系,为疾病模型构建提供了精准靶点,其中m.G12918A突变小鼠模型的表型与人类患者高度一致,可用于药物筛选与机制研究。
- 技术性能Biomarker:建立了线粒体碱基编辑技术的标准化评估体系,量化了不同编辑器的效率、特异性与安全性,为技术优化提供了量化指标,例如HiFi-DdCBEs的脱靶率较初始DdCBEs降低80%以上。
- 创新性成果:首次在人类胚胎中实现了mtDNA致病突变的精准纠正,编辑效率达60%,证实了线粒体碱基编辑在生殖系治疗中的潜力;首次系统梳理了线粒体碱基编辑技术的发展脉络,为领域提供了权威的技术参考。
