1. 领域背景与文献引入
文献英文标题:Detection of 8-oxoguanine and apurinic/apyrimidinic sites using a fluorophore-labeled probe with cell-penetrating ability;发表期刊:BMC Molecular and Cell Biology;影响因子:未公开;研究领域:氧化损伤DNA检测与分子探针开发(分子生物学与细胞生物学交叉领域)。
活性氧(ROS)诱导的DNA损伤是癌症、神经退行性疾病、衰老等多种疾病发生发展的关键分子基础,其中8-氧代-7,8-二氢鸟嘌呤(8-oxoG)和无嘌呤/无嘧啶(AP)位点是最具代表性的氧化损伤类型,其积累水平可直接反映细胞氧化应激状态。领域发展关键节点可追溯至20世纪80年代,8-oxoG的结构与致突变性被首次阐明;90年代碱基切除修复(BER)通路被确立为清除这类损伤的核心机制;2000年后,针对8-oxoG的检测技术逐步迭代,涵盖色谱-质谱联用法、酶联免疫吸附实验(ELISA)等,但这些方法均存在操作复杂、需破坏细胞结构、无法实现活细胞原位检测的局限性。当前研究热点聚焦于开发兼具高特异性、细胞穿透性、细胞器靶向性的分子探针,以实现活细胞内氧化损伤DNA的实时可视化检测。目前领域未解决的核心问题包括:现有探针大多依赖细胞透化处理,无法在生理状态下检测活细胞内的损伤;部分探针特异性不足,难以同时区分8-oxoG和AP位点;针对线粒体(ROS主要产生位点,其DNA损伤与疾病关联最为紧密)的靶向检测工具匮乏,限制了线粒体氧化损伤相关疾病机制的研究。
针对上述研究空白,本研究基于人核糖体蛋白S3(hRpS3)对8-oxoG和AP位点的天然高亲和力,结合HIV-1反式激活因子(TAT)的高效细胞穿透特性,构建了TAT-S3荧光探针,旨在实现活细胞内(尤其是线粒体)8-oxoG和AP位点的特异性、无透化检测,为氧化损伤相关疾病的机制研究与药物筛选提供新型可视化工具。
2. 文献综述解析
作者在综述部分以“现有检测技术的局限性”为核心分类维度,系统梳理了8-oxoG与AP位点检测方法的发展现状与不足,明确了本研究的创新定位。
现有8-oxoG检测方法主要分为三类,色谱-质谱联用法定量精度高,但需提取基因组DNA,无法实现活细胞原位检测;基于抗体的免疫检测法(如ELISA)操作相对简便,但抗体难以穿透细胞膜,且存在非特异性结合风险;早期开发的hRpS3衍生肽探针虽能特异性结合8-oxoG,但缺乏细胞穿透能力,无法进入活细胞内部。针对AP位点的检测则主要依赖醛反应探针(ARP)和甲氧基胺(MX),这类试剂虽能标记AP位点,但同样需要细胞透化处理,且无法同时检测8-oxoG。整体而言,现有研究的局限性集中在三个方面:无法在活细胞生理状态下检测损伤、缺乏细胞器靶向能力、无法同时识别多种氧化损伤类型,这些不足严重限制了氧化损伤DNA的动态研究。
本研究通过将TAT细胞穿透肽与hRpS3特异性肽段融合,首次构建了兼具细胞穿透性、线粒体靶向性的双靶点荧光探针,解决了现有探针无法在活细胞内同时检测8-oxoG和AP位点的核心问题。与传统检测方法相比,该探针无需细胞透化,可在生理状态下实时可视化氧化损伤,且具备线粒体靶向能力,填补了线粒体氧化损伤DNA原位检测工具的空白,为氧化损伤相关疾病的研究提供了全新的技术范式。
3. 研究思路总结与详细解析
本研究以“开发活细胞内氧化损伤DNA可视化探针”为核心目标,围绕“探针结合特异性→细胞穿透与靶向性→损伤响应功能→体内验证”的逻辑链条展开,通过体外实验、细胞实验、体内模型验证的层层递进,系统证实了TAT-S3探针的检测性能。
3.1 TAT-S3探针的合成与基本特性验证
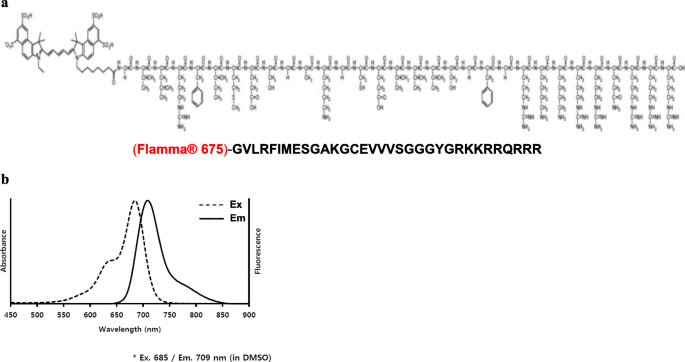
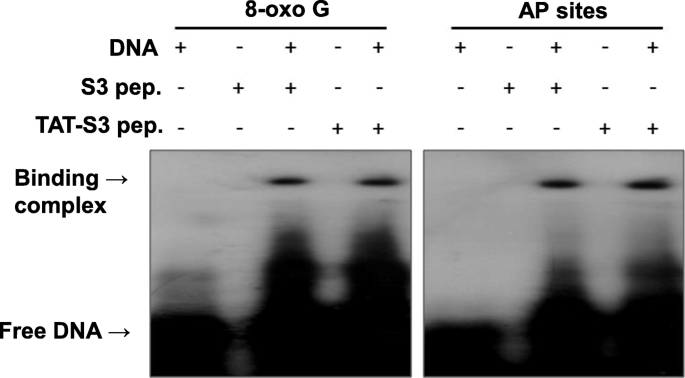
实验目的为合成兼具细胞穿透性与损伤结合特异性的TAT-S3荧光探针,并验证其光谱特性与DNA损伤位点结合能力。方法细节上,以hRpS3的特异性肽段为基础,在C端通过甘氨酸-甘氨酸(GG)连接子连接TAT细胞穿透肽,N端标记Flamma-675荧光染料;通过DNA结合实验,将探针与含单个8-oxoG或AP位点的39mer核苷酸双链在37℃下孵育3小时,采用非变性聚丙烯酰胺凝胶电泳分析结合复合物的条带;同时在体外二甲基亚砜(DMSO)环境中检测探针的吸收与发射光谱。结果解读显示,TAT-S3探针的吸收峰位于685nm,发射峰位于709nm,光谱特性稳定(图1);DNA结合实验结果显示,TAT-S3探针与S3探针对含8-oxoG或AP位点的底物结合能力相当,条带强度一致,表明TAT肽的引入未影响探针与损伤位点的结合特异性(图3)。实验所用关键产品:Flamma-675荧光染料(BioActs, 韩国仁川)、非变性聚丙烯酰胺凝胶电泳试剂(Bio Basic Inc., 加拿大马克姆)。
3.2 TAT-S3探针的细胞毒性与线粒体靶向性验证
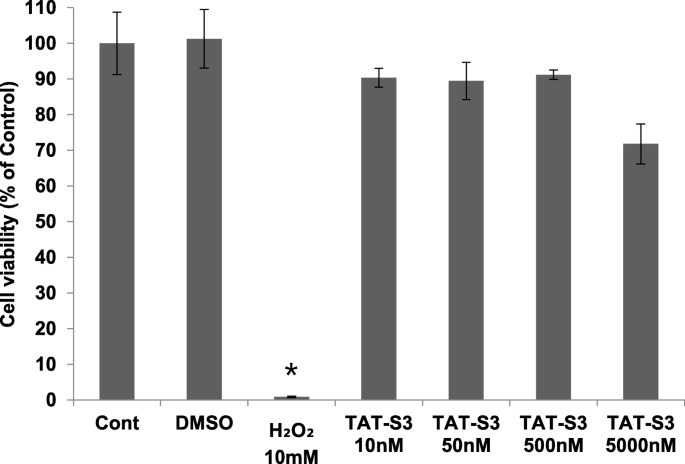
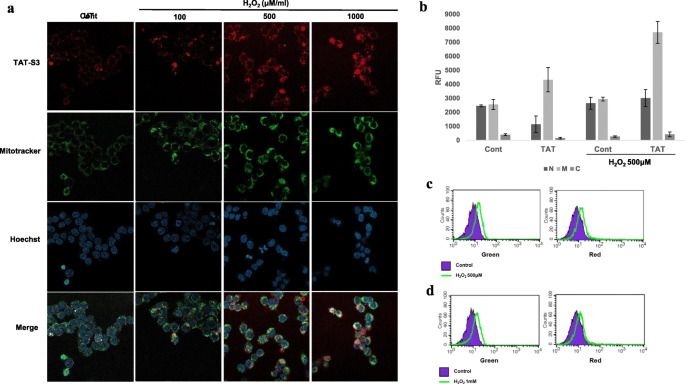
实验目的为评估TAT-S3探针的细胞毒性,验证其细胞穿透能力及线粒体靶向性。方法细节上,采用MTT法检测不同浓度(0、5、500、5000nM)TAT-S3探针处理24小时后HeLa细胞的存活率;通过共聚焦激光扫描显微镜观察探针与细胞核染料Hoechst、线粒体染料MitoTracker的共定位情况;采用细胞分离技术,将H₂O₂处理后的HeLa细胞分离为细胞核、线粒体、细胞质组分,检测各组分的探针荧光强度;同时通过流式细胞术验证探针与MitoTracker的共定位。结果解读显示,MTT实验显示,除5000nM浓度下细胞存活率降至71%(n=3,P<0.01)外,其余浓度探针无明显细胞毒性(图2);共聚焦显微镜与细胞分离实验显示,超过90%的探针荧光定位于线粒体组分,H₂O₂处理后线粒体中探针荧光强度是未处理组的1.8倍,是细胞核组分的2.5倍(n=3,P<0.05),表明探针可穿透细胞膜并特异性靶向损伤线粒体(图4)。实验所用关键产品:MTT试剂(Sigma-Aldrich)、MitoTracker Green FM(Invitrogen, 美国卡尔斯巴德)、共聚焦激光扫描显微镜(LSM 800, Carl Zeiss, 德国奥伯科亨)。
3.3 TAT-S3探针的损伤响应特异性验证
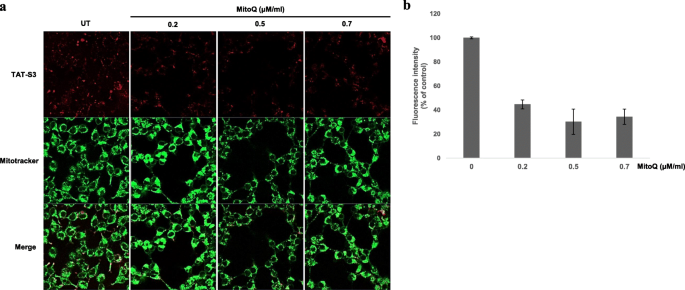
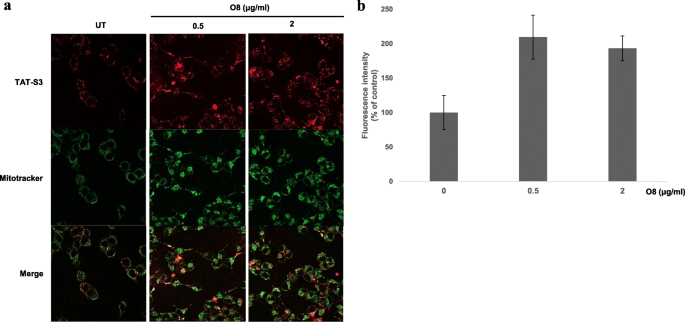
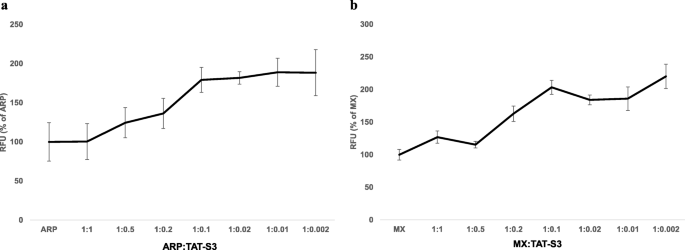
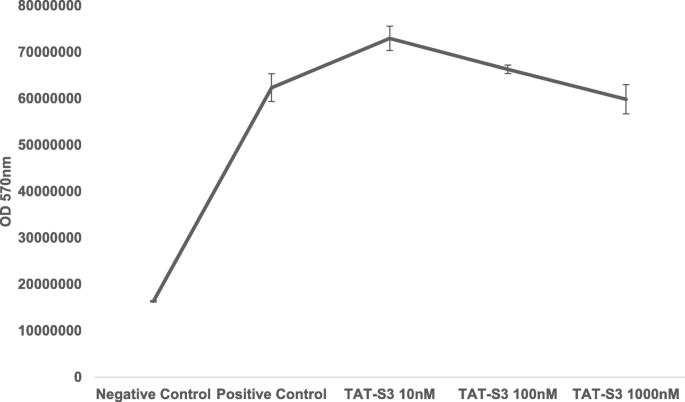
实验目的为验证TAT-S3探针对ROS诱导的DNA损伤的响应特异性,确认其可区分8-oxoG和AP位点。方法细节上,用线粒体靶向抗氧化剂MitoQ处理H₂O₂损伤的HeLa细胞,检测探针荧光强度变化;用OGG1抑制剂O8处理细胞,观察探针荧光变化;通过竞争实验,将探针与ARP、MX共同孵育,检测探针与AP位点的竞争性结合情况;同时检测不同浓度探针处理后细胞的ATP水平,评估探针对线粒体功能的影响。结果解读显示,MitoQ处理后探针荧光强度呈剂量依赖性降低,最高降幅约60%(n=3,P<0.01),表明探针荧光与ROS诱导的线粒体损伤正相关(图5);O8处理后探针荧光强度升高约2倍(n=3,P<0.01),说明探针可检测OGG1抑制后积累的8-oxoG(图6);竞争实验显示,TAT-S3探针与ARP、MX竞争性结合AP位点,当探针浓度为ARP的2倍时,结合能力是ARP的1.2倍,为MX的1.6倍(n=3,P<0.05),证实其对AP位点的特异性结合(图7);ATP检测显示,各浓度探针处理后细胞ATP水平与对照组无显著差异(n=3,P>0.05),表明探针不影响线粒体功能(图8)。实验所用关键产品:MitoQ(BioVision, 美国米尔皮塔斯)、O8抑制剂(Sigma-Aldrich)、ATP检测试剂盒(Promega, 美国麦迪逊)。
3.4 TAT-S3探针的体内模型验证
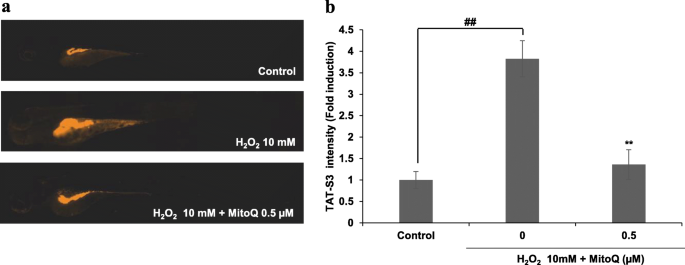
实验目的为在斑马鱼体内验证TAT-S3探针对ROS诱导的氧化损伤的检测能力。方法细节上,构建H₂O₂诱导的斑马鱼氧化损伤模型,预处理MitoQ后,用TAT-S3探针处理斑马鱼幼鱼,共聚焦显微镜观察荧光强度变化,并用ImageJ定量分析。结果解读显示,H₂O₂处理组斑马鱼幼鱼的探针荧光强度显著高于对照组(n=15,P<0.01),而MitoQ预处理组荧光强度显著降低(n=15,P<0.01),表明探针在体内模型中同样可检测ROS诱导的氧化损伤(图9)。实验所用关键产品:MS-222麻醉剂(Sigma-Aldrich)、显微镜成像系统(Gen 5 version 3.03, BioTek, 美国威努斯基)。
4. Biomarker研究及发现成果解析
本研究聚焦于ROS诱导的DNA损伤Biomarker——8-oxoG和AP位点,通过构建TAT-S3探针实现了活细胞内的特异性检测,形成了完整的“筛选→验证→应用”研究链条。
Biomarker定位方面,8-oxoG和AP位点是ROS诱导DNA氧化损伤的核心Biomarker,其积累与癌症、神经退行性疾病、衰老等密切相关。本研究的筛选与验证逻辑为:基于hRpS3对两种Biomarker的天然高亲和力设计探针,先通过体外DNA结合实验验证探针的特异性结合能力,再通过HeLa细胞实验验证其活细胞内检测能力,最后通过斑马鱼体内模型验证其在生理环境中的检测性能,形成了“体外验证→细胞验证→体内验证”的完整闭环。
研究过程详述:Biomarker的来源为H₂O₂诱导的HeLa细胞线粒体DNA损伤及斑马鱼幼鱼体内的氧化损伤DNA;验证方法包括共聚焦荧光显微镜成像、细胞组分分离荧光定量、竞争结合实验;特异性数据显示,TAT-S3探针与8-oxoG和AP位点的结合特异性与S3探针相当,在活细胞中可特异性定位于线粒体,荧光强度与损伤程度正相关;敏感性方面,探针在100nM浓度下即可在活细胞中检测到损伤信号,MitoQ处理后荧光强度呈剂量依赖性降低,最高降幅约60%(n=3,P<0.01),O8处理后荧光强度升高约2倍(n=3,P<0.01),统计学结果证实了探针响应的显著性。
核心成果提炼:该研究首次实现了活细胞内(无需透化)同时检测8-oxoG和AP位点两种氧化损伤Biomarker,且探针具有线粒体靶向性,可特异性识别线粒体DNA损伤;功能关联上,探针荧光强度可直接反映ROS诱导的线粒体损伤程度,可作为氧化损伤相关疾病机制研究与药物筛选的可视化工具;创新性在于将细胞穿透肽与损伤特异性肽段融合,突破了现有检测方法无法活细胞原位检测的技术瓶颈;统计学结果显示,细胞实验样本量n=3,斑马鱼实验样本量n=15,各实验组间差异均具有显著性(P<0.01或P<0.05),证实了探针检测性能的可靠性。
