1. 领域背景与文献引入
文献英文标题:The scaffolding protein GRASP/Tamalin directly binds to Dock180 as well as to cytohesins facilitating GTPase crosstalk in epithelial cell migration;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:上皮细胞迁移与小GTP酶信号调控。
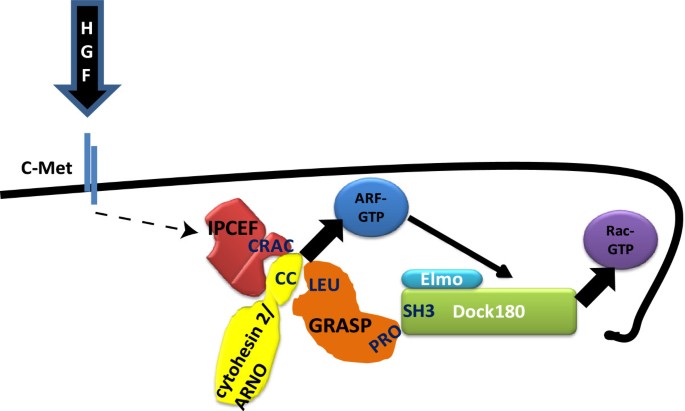
领域共识:上皮细胞迁移是发育、伤口修复和肿瘤转移的核心细胞过程,受多种生长因子和信号通路的精密调控。小GTP酶家族(如Arf、Rac)是调控细胞迁移的关键分子,其中Arf6负责调控膜转运与细胞骨架重排,Rac1调控细胞前沿突起形成与黏附动态,两者的协同激活是上皮细胞迁移的核心信号事件。领域发展关键节点:2001年研究明确Arf6激活可通过下游Rac1调控上皮细胞迁移;2005年发现cytohesin 2(Arf鸟苷酸交换因子,GEF)与Dock180(Rac GEF)的相互作用介导Arf到Rac的信号串话;2010年进一步发现支架蛋白CNK3/IPCEF负责招募cytohesin 2到细胞膜,但GRASP/Tamalin的具体功能尚未阐明。当前研究热点聚焦解析调控Arf-Rac信号串话的支架蛋白机制,未解决的核心问题是:cytohesin 2与Dock180如何在空间和功能上协同,GRASP是否作为桥接支架蛋白介导两者的相互作用,进而调控上皮细胞迁移。
结合领域现状,本研究针对GRASP在Arf-Rac信号串话中的功能空白,提出“GRASP通过同时结合cytohesin 2和Dock180,介导Arf6到Rac1的信号激活,进而调控HGF诱导的上皮细胞迁移”的科学假设,旨在明确GRASP的分子作用机制,为上皮细胞迁移的调控网络提供新的理论依据和潜在靶点。
2. 文献综述解析
作者按“上游生长因子刺激→GEF激活→支架蛋白介导→下游GTP酶激活”的信号通路层级,对上皮细胞迁移的现有研究进行分类评述,重点聚焦Arf与Rac信号串话的调控机制。
现有研究关键结论:HGF通过激活c-Met受体,启动下游Arf6和Rac1的级联激活;cytohesin 2作为Arf6的GEF,可通过与Dock180的相互作用间接激活Rac1;支架蛋白CNK3/IPCEF负责将cytohesin 2招募到细胞膜,但其无法直接桥接cytohesin 2与Dock180。技术方法优势:前期研究采用GST-PBD pulldown检测Rac激活、免疫共沉淀验证蛋白相互作用,具有较高的特异性和可靠性;局限性:缺乏对GRASP与Dock180直接相互作用的结构域解析,以及GRASP在活细胞内功能的直接验证,无法完整阐明Arf-Rac信号串话的支架蛋白调控机制。
本研究的创新价值在于,通过对比现有研究中支架蛋白仅负责招募的单一功能,首次明确GRASP作为双功能支架蛋白,同时结合cytohesin 2和Dock180的不同结构域,直接介导两者的物理桥接和功能协同,填补了Arf到Rac信号串话中支架蛋白具体作用机制的空白,为上皮细胞迁移的分子调控网络提供了更完整的模型。
3. 研究思路总结与详细解析
本研究的研究目标是验证GRASP通过结合cytohesin 2和Dock180介导Arf6到Rac1的信号串话,调控HGF诱导的上皮细胞迁移;核心科学问题是GRASP与Dock180的相互作用结构域及功能意义;技术路线遵循“假设提出→分子互作验证→结构域定位→细胞功能验证→机制整合”的闭环逻辑,通过多层次实验验证GRASP的功能与机制。
3.1 HGF诱导的Rac激活与细胞迁移依赖cytohesin和Dock180
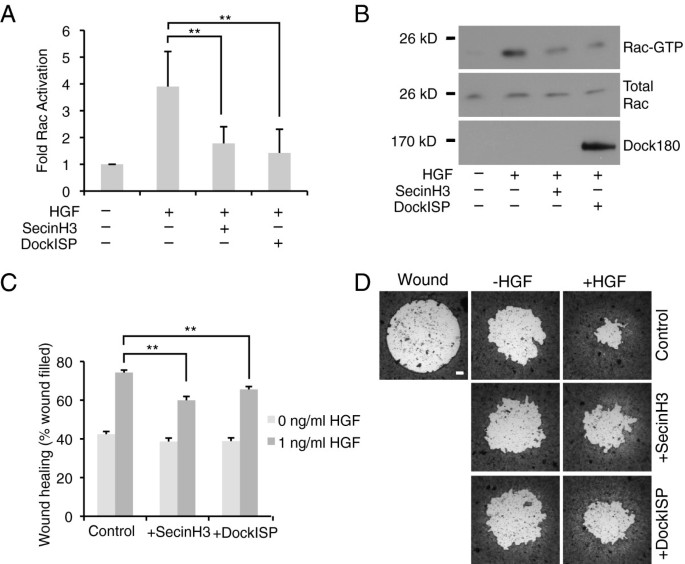
实验目的:验证HGF诱导的上皮细胞迁移和Rac激活是否依赖cytohesin家族和Dock180的GEF活性。方法细节:采用Madin-Darby犬肾(MDCK)细胞,分为对照组、cytohesin抑制剂SecinH3处理组(15μM)、显性负性Dock180突变体(DockISP)表达组,用20ng/ml HGF处理6小时后,通过GST-PBD pulldown实验分离活性形式的Rac-GTP,并用免疫印迹检测Rac和Dock180表达;同时采用Oris迁移小室进行伤口愈合实验,1ng/ml HGF处理18小时后,通过ImageJ软件分析剩余伤口面积。结果解读:GST-PBD pulldown结果显示,抑制cytohesin或Dock180活性后,HGF诱导的Rac-GTP水平显著降低,定量分析显示活性Rac水平较对照组降低约50%(n=4,P<0.01);伤口愈合实验显示,处理组的HGF诱导迁移能力显著低于对照组,对照组伤口愈合率为62%±4%,SecinH3组为38%±5%,DockISP组为35%±6%(对照组n=67,SecinH3组n=37,DockISP组n=24,P<0.01),而基础迁移能力在各组间无显著差异。产品关联:实验所用关键产品:GST-PBD探针、SecinH3抑制剂、Oris迁移小室(Platypus technologies)、抗Rac抗体、抗Dock180抗体。
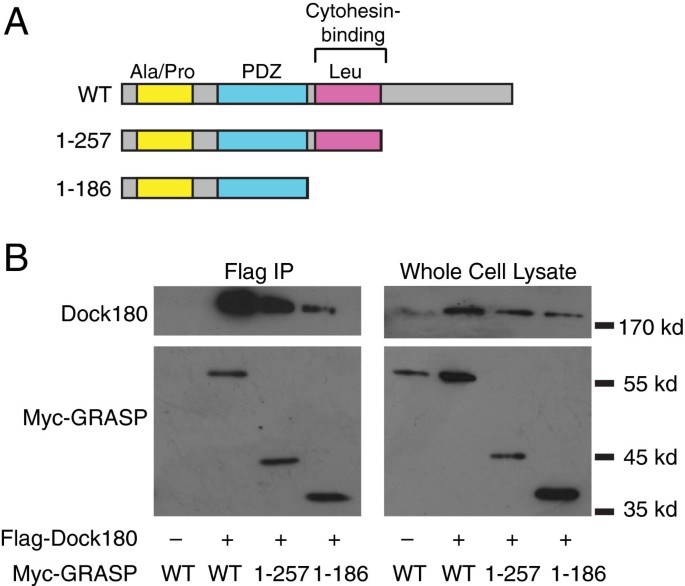
3.2 GRASP独立结合cytohesin 2和Dock180
实验目的:验证GRASP是否能不依赖cytohesin 2而直接结合Dock180。方法细节:构建GRASP的系列截短突变体,包括缺失cytohesin结合结构域(亮氨酸富集区)的突变体,与Flag标记的Dock180共转染人胚肾293(HEK293)细胞,通过M2-Flag树脂进行免疫共沉淀实验,并用免疫印迹检测GRASP与Dock180的结合情况;同时以野生型GRASP与Dock180共转染作为阳性对照。结果解读:免疫共沉淀结果显示,即使GRASP缺失cytohesin结合结构域,仍能与Dock180共沉淀,证明GRASP与Dock180的相互作用独立于其与cytohesin 2的结合,提示GRASP可同时结合两种GEF分子。产品关联:实验所用关键产品:M2-Flag树脂、抗myc抗体(检测GRASP突变体)、抗Dock180抗体、HEK293细胞系。
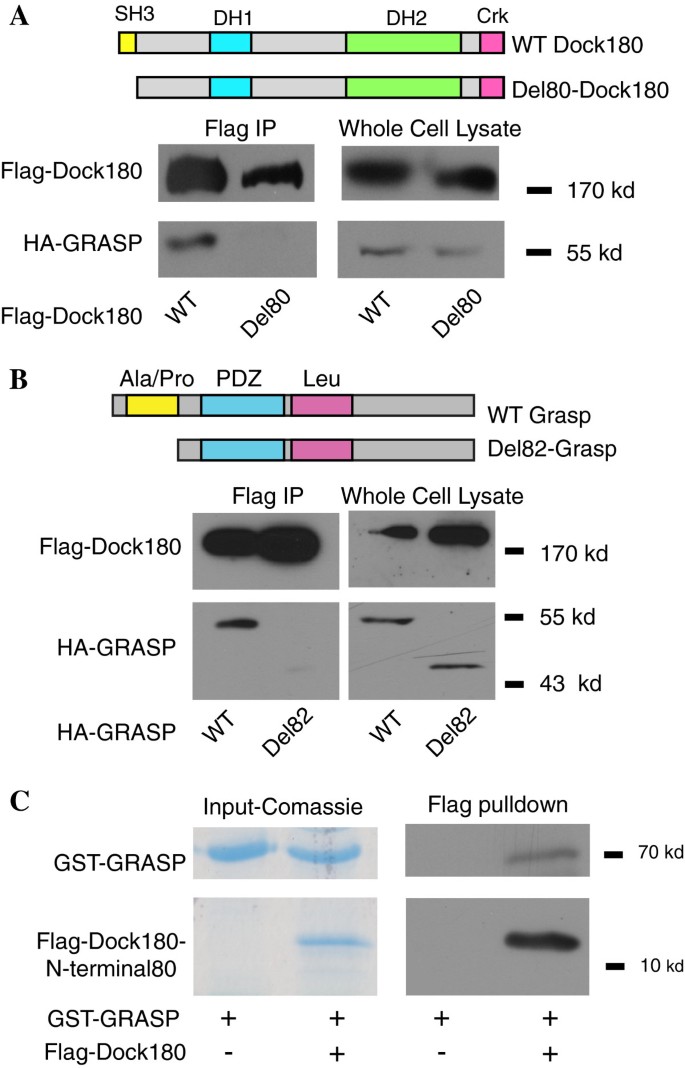
3.3 GRASP与Dock180的相互作用结构域定位
实验目的:确定GRASP与Dock180相互作用的具体结构域。方法细节:构建Dock180的N端截短突变体(缺失前80个氨基酸,即SH3结构域),与HA标记的野生型GRASP共转染HEK293细胞;同时构建GRASP的N端截短突变体(缺失前82个氨基酸,即脯氨酸富集区,Del82-GRASP),与Flag标记的Dock180共转染,通过免疫共沉淀检测相互作用;此外,通过原核表达GST融合的GRASP和Flag融合的Dock180 N端80aa,进行体外结合实验验证直接互作。结果解读:免疫共沉淀显示,缺失SH3结构域的Dock180无法与GRASP结合,缺失脯氨酸富集区的Del82-GRASP也无法与Dock180结合;体外结合实验进一步验证,GST-GRASP可直接结合Flag-Dock180 N端80aa,证明两者通过Dock180的SH3结构域与GRASP的脯氨酸富集结构域直接相互作用。产品关联:实验所用关键产品:GST融合蛋白表达系统、Glutathione-Sepharose beads、抗HA抗体、抗Dock180抗体。
3.4 活细胞内GRASP与Dock180的相互作用验证
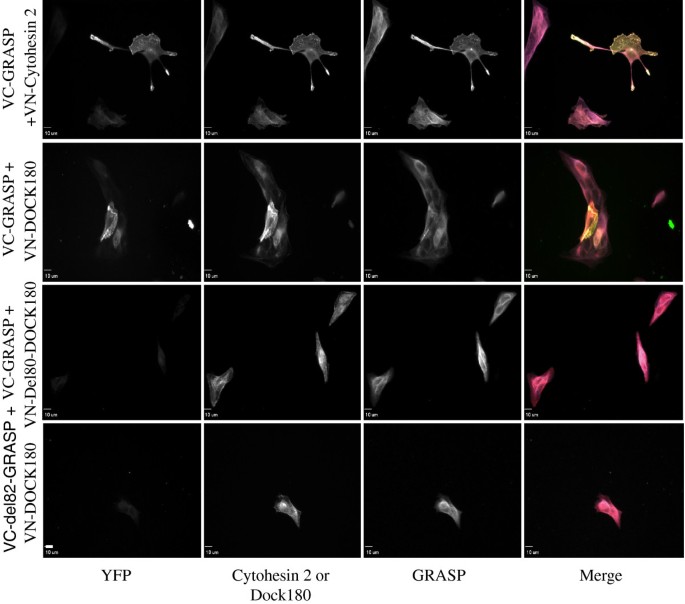
实验目的:在活细胞内验证GRASP与Dock180的相互作用。方法细节:采用双分子荧光互补(BiFC)实验,构建Venus荧光蛋白N端片段融合的Dock180(VN-Dock180)和C端片段融合的GRASP(VC-GRASP)表达载体,共转染MDCK细胞;同时以VN-cytohesin 2和VC-GRASP作为阳性对照,转染后固定细胞,通过免疫荧光标记Dock180和GRASP,并用荧光显微镜观察YFP荧光信号。结果解读:共转染VN-Dock180和VC-GRASP的细胞中检测到明显的YFP荧光信号,且荧光信号与Dock180、GRASP的免疫荧光信号共定位;而共转染缺失SH3结构域的VN-Del80-Dock180与VC-GRASP,或VN-Dock180与缺失脯氨酸富集区的VC-Del82-GRASP的细胞中,未检测到YFP荧光信号,进一步验证活细胞内GRASP与Dock180的结构域特异性相互作用。产品关联:实验所用关键产品:BiFC载体系统、Dylight系列荧光二抗、Olympus IX81荧光显微镜。
3.5 GRASP敲低抑制HGF诱导的Rac激活与细胞迁移
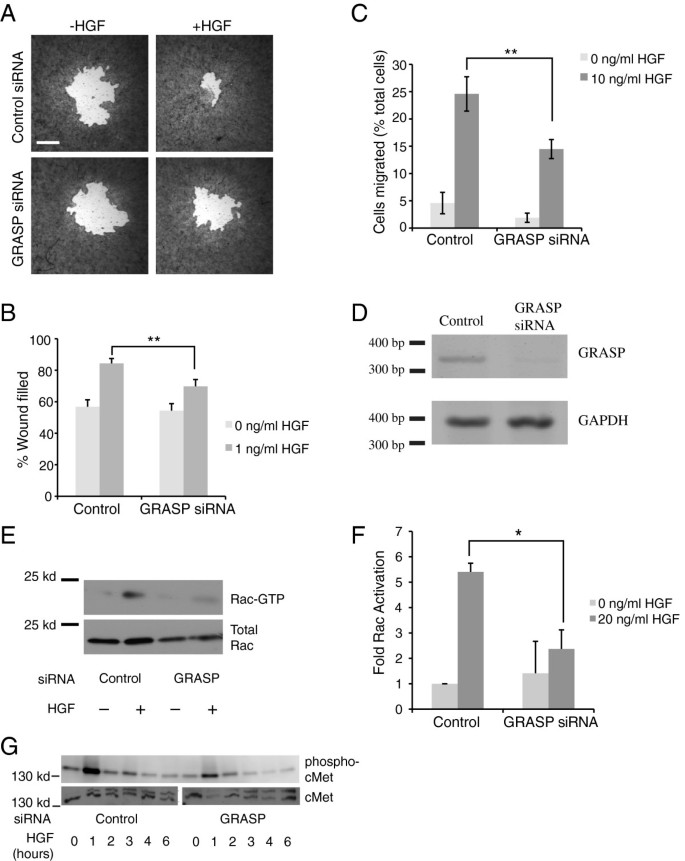
实验目的:验证GRASP在HGF诱导的Rac激活和上皮细胞迁移中的功能。方法细节:采用siRNA靶向敲低MDCK细胞中GRASP的表达,通过RT-PCR验证敲低效率;然后通过伤口愈合实验和Transwell迁移实验检测1ng/ml HGF诱导的迁移能力;同时用20ng/ml HGF处理细胞5小时后,通过GST-PBD pulldown检测Rac激活水平;并用免疫印迹检测不同时间点c-Met的磷酸化水平,排除上游受体激活异常。结果解读:RT-PCR显示GRASP mRNA表达水平较对照组降低约70%;伤口愈合实验显示,GRASP敲低组HGF诱导的伤口愈合率为42%±5%,对照组为63%±4%(n≥15,P<0.01);Transwell实验显示,敲低组迁移细胞数为对照组的62%±6%(n≥15,P<0.01),基础迁移能力在两组间无显著差异;GST-PBD pulldown显示,敲低组HGF诱导的Rac激活水平为对照组的58%±7%(n=4,P<0.05);免疫印迹显示,c-Met的磷酸化水平在敲低组和对照组中无显著差异,排除上游受体激活异常。产品关联:实验所用关键产品:GRASP靶向siRNA、Transwell小室、抗磷酸化c-Met抗体、抗总c-Met抗体、GST-PBD探针。
4. Biomarker研究及发现成果解析
本研究发现的核心Biomarker为支架蛋白GRASP/Tamalin,属于功能型Biomarker,其通过介导Arf与Rac信号串话调控上皮细胞迁移,为上皮细胞迁移相关疾病(如肿瘤转移、伤口愈合障碍)提供潜在的调控靶点。
Biomarker定位:GRASP是调控上皮细胞迁移的功能型Biomarker,筛选与验证逻辑遵循“文献假设驱动→分子互作验证→结构域特异性定位→细胞功能敲低验证→信号通路整合”的完整链条。研究过程详述:Biomarker来源为上皮细胞内源性表达的支架蛋白,验证方法包括免疫共沉淀、体外蛋白结合实验、双分子荧光互补活细胞验证、siRNA功能敲低、GTP酶活性检测等;特异性方面,GRASP通过不同结构域特异性结合cytohesin 2(亮氨酸富集区)和Dock180(SH3结构域),不影响上游c-Met受体的磷酸化激活;功能敏感性方面,GRASP敲低后,HGF诱导的Rac激活水平降低约42%(n=4,P<0.05),HGF诱导的上皮细胞迁移能力降低约38%(n≥15,P<0.01)。核心成果提炼:GRASP作为双功能支架蛋白,通过同时结合cytohesin 2和Dock180,在空间上桥接Arf6与Rac1的GEF分子,促进Arf到Rac的信号串话,是HGF诱导上皮细胞迁移的关键调控分子;其创新性在于首次明确GRASP的脯氨酸富集结构域与Dock180的SH3结构域的直接相互作用,完善了Arf-Rac信号串话的调控模型;统计学结果显示,所有功能验证实验均具有显著的统计学差异(P<0.05或P<0.01),样本量满足实验重复性要求。