1. 领域背景与文献引入
文献英文标题:Mesenchymal stem cells and myoblast differentiation under HGF and IGF-1 stimulation for 3D skeletal muscle tissue engineering;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:骨骼肌组织工程、干细胞肌源性分化。
骨骼肌占人体体重约50%,是执行躯体运动的核心组织,具有一定的自然再生能力,依赖于静息状态的肌卫星细胞激活增殖分化。但创伤、肿瘤术后等导致的容积性肌肉丢失(Volumetric Muscle Loss)远超骨骼肌自然再生阈值,目前临床主要采用自体游离肌瓣移植修复,该方法不可避免会造成供区组织损伤与功能障碍,是临床亟待解决的难题。骨骼肌组织工程被认为是未来替代自体肌瓣的核心方向,其核心需求包括可扩增的种子细胞、具有仿生结构的3D支架,以及可调控细胞分化的微环境因子。
现有研究显示,传统肌卫星细胞作为种子细胞存在传代后分化能力快速下降的局限性,而骨髓来源间充质干细胞(MSCs)具有易获取、体外可大量扩增、多向分化潜能等优势,是极具潜力的替代细胞来源。但单独培养的MSCs肌源性分化效率较低,与肌成纤维细胞共培养可通过细胞间接触或旁分泌作用增强其肌分化能力。肝细胞生长因子(HGF)和胰岛素样生长因子-1(IGF-1)是已知参与骨骼肌增殖与分化的关键生长因子,但现有研究对其作用浓度、时间效应的结论存在争议,且针对MSCs与肌成纤维细胞共培养体系的系统研究较少;同时,3D支架的类型与结构对共培养细胞肌分化的影响仍需进一步优化。本研究针对上述领域空白,系统探索MSCs单培养与共培养的肌源性分化潜力,明确HGF/IGF-1的调控作用,并筛选适配的3D仿生支架,为骨骼肌组织工程的临床转化提供实验依据。
2. 文献综述解析
本文献综述部分以“细胞培养体系-生长因子调控-培养环境”为核心分类维度,系统梳理了骨骼肌组织工程领域的现有研究进展与未解决问题。
现有研究表明,肌卫星细胞是骨骼肌再生的天然种子细胞,具有高效的肌源性分化能力,但体外传代3-4次后分化能力显著下降,难以满足大规模组织工程需求;MSCs可通过诱导向肌源性 lineage 分化,但单独培养时分化效率低、分化程度有限,与肌成纤维细胞共培养可通过旁分泌生长因子或细胞间直接接触,显著提升MSCs的肌分化潜能。HGF和IGF-1在骨骼肌发育与再生中发挥双重作用,HGF主要参与肌卫星细胞的激活与增殖,IGF-1可同时调控肌细胞的增殖与分化,但不同研究对生长因子的最优浓度、作用时间结论不一,部分研究显示低浓度HGF促进分化,高浓度则抑制,而IGF-1的作用也存在细胞系特异性差异。在培养环境方面,3D培养体系比2D更接近体内骨骼肌的生理微环境,可显著增强肌细胞的分化与肌管形成能力,现有研究已探索了纤维蛋白凝胶、胶原支架、电纺纳米纤维等多种3D载体,但针对MSCs与肌成纤维细胞共培养体系的3D支架对比研究仍较缺乏。
现有研究的核心局限性在于,尚未系统阐明HGF/IGF-1对MSCs单培养与共培养肌分化的时间-浓度效应,IGF结合蛋白(IGFBPs)作为HGF/IGF-1的调控因子,其在肌分化中的作用机制也未明确;同时,缺乏针对共培养细胞的3D支架优化研究。本研究的创新价值在于,首次系统对比了HGF、IGF-1及联合刺激对MSCs单培养与共培养肌分化的影响,明确了生长因子的非必需性;首次分析了IGFBPs在不同培养体系中的表达模式与肌分化的关联;并筛选出平行电纺聚己内酯-胶原I(PCL-胶原I)纳米纤维支架作为共培养细胞的理想3D载体,为骨骼肌组织工程的种子细胞优化与支架设计提供了新的实验依据。
3. 研究思路总结与详细解析
本研究以“明确MSCs肌分化潜力-解析生长因子调控作用-优化3D培养支架”为核心逻辑,构建了“细胞分离鉴定→体外培养调控→分子与细胞水平验证→3D支架适配”的完整研究闭环。研究目标是验证MSCs在单培养与共培养体系中的肌源性分化能力,明确HGF/IGF-1的调控作用,筛选适配的3D仿生支架;核心科学问题包括MSCs能否在无外源性生长因子刺激下实现肌分化、HGF/IGF-1对共培养细胞肌分化的调控机制、哪种3D支架最利于共培养细胞的肌分化与定向排列。
3.1 细胞分离与培养体系建立
实验目的:获取高纯度的原代大鼠肌成纤维细胞与骨髓来源MSCs,建立稳定的体外培养与分化体系。
方法细节:从雄性Lewis大鼠后肢骨骼肌分离肌卫星细胞(肌成纤维细胞前体),采用含25%胎牛血清、2.5ng/ml碱性成纤维细胞生长因子(bFGF)的Ham’s F-10培养基培养,传代3代后通过肌分化因子MyoD免疫染色验证肌源性;从雄性Lewis大鼠骨髓分离MSCs,通过慢病毒转染实现绿色荧光蛋白(GFP)稳定标记,采用含10%胎牛血清的DMEM Ham’s F-12培养基培养,传代11-12代后通过成软骨、成脂、成骨分化实验验证多能性。分化基础培养基含2%马血清、0.4μg/ml地塞米松、1ng/ml bFGF,在此基础上添加不同浓度HGF(10、30、60、100ng/ml)、IGF-1(5、10、30、60ng/ml)或联合刺激(10ng/ml HGF+10ng/ml IGF-1),设置MSCs单培养、肌成纤维细胞单培养、MSCs-肌成纤维细胞共培养(1:1细胞比例)三组,培养时间为2、7、14天。
结果解读:成功分离并鉴定了高纯度的肌成纤维细胞(MyoD阳性率≥90%)与MSCs(具有三向分化潜能),建立了稳定的体外培养与分化体系,为后续实验提供了可靠的细胞模型。
产品关联:实验所用关键产品:Abcam的MyoD抗体(货号5.8.A)、Thermo Fisher Scientific的抗结蛋白抗体(货号AB-1 (D33))、抗肌球蛋白重链2抗体(货号MYSN02)、Abcam的抗α-肌动蛋白抗体(货号EA-53)、Santa Cruz Biotechnology的抗MEF2抗体(货号MEF2A, B-4)、Qiagen的RNeasy Mini Kit、QuantiTect逆转录试剂盒、Bio-Rad的SsoAdvanced Universal SYBR Green PCR Supermix等。
3.2 生长因子对肌源性标志物mRNA表达的调控
实验目的:从转录水平分析HGF、IGF-1及联合刺激对不同培养体系中肌源性标志物表达的时间与浓度效应。
方法细节:采用实时荧光定量PCR(qRT-PCR)检测结蛋白(DES)、肌细胞增强因子2(MEF2)、肌球蛋白重链2(MyHC2)、α-肌动蛋白(ACTN2)、肌生成素(MYOG)及IGF结合蛋白4/5/6(IGFBP4/5/6)的mRNA表达,以核糖体蛋白L13a(RPL13a)为内参基因,采用2^(-ΔΔCt)法计算相对表达量,每组实验重复3次,采用单因素方差分析进行统计学检验。
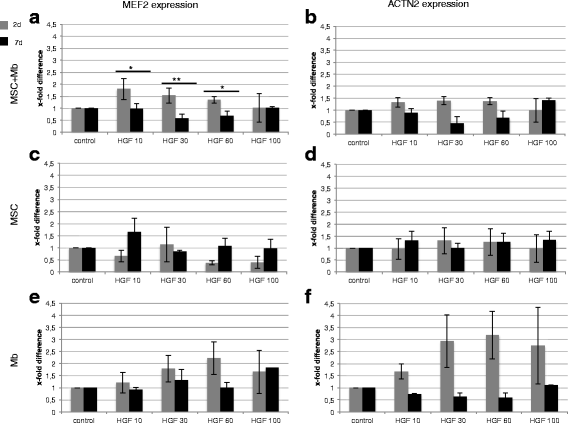
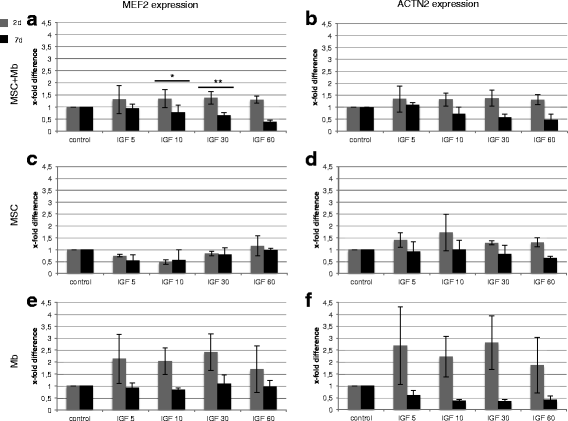
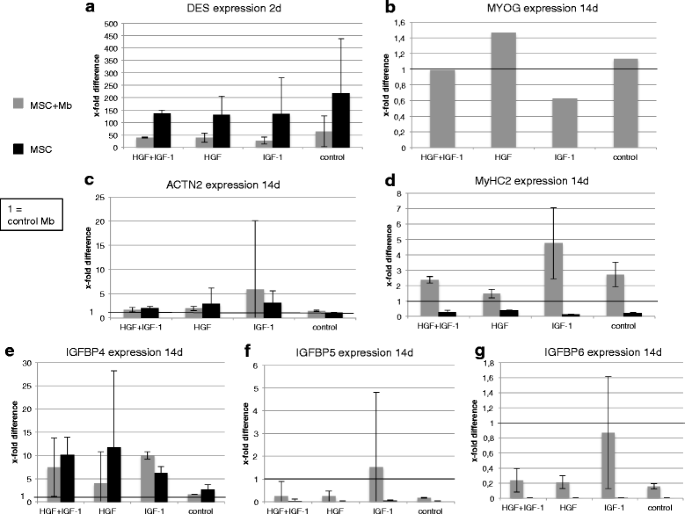
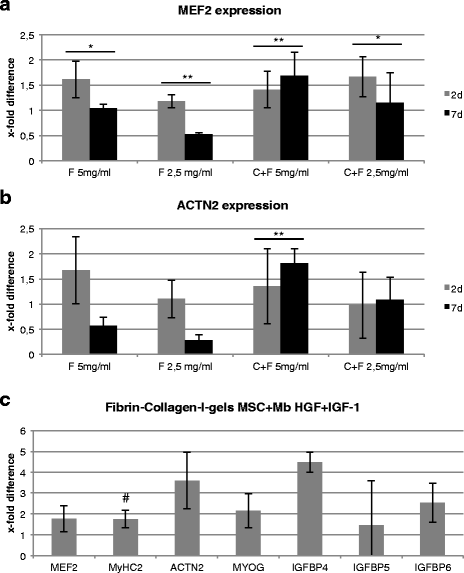
结果解读:HGF刺激下,共培养与肌成纤维细胞单培养体系中,早期(2天)MEF2与ACTN2的mRNA表达显著高于晚期(7天),且呈现一定的浓度依赖性下降;MSCs单培养体系中,晚期(7天)10ng/ml HGF组MEF2表达最高(1.6±0.6倍,n=3)。IGF-1刺激下,共培养体系中早期(2天)10、30ng/ml组MEF2表达显著高于晚期(7天)(P≤0.01),MSCs单培养体系中早期(2天)60ng/ml IGF-1组MEF2表达最高(1.2±0.4倍,n=3)。联合刺激下,MSCs单培养与共培养体系中早期(2天)DES表达显著高于肌成纤维细胞单培养;共培养体系中晚期(14天)IGF-1组ACTN2与MyHC2表达最高,分别为5.9±14倍、4.8±2.3倍(n=3);IGFBPs在共培养IGF-1组表达显著升高,与MyHC2、ACTN2的表达呈正相关。
3.3 肌源性分化的蛋白水平验证与细胞融合分析
实验目的:从蛋白水平验证MSCs的肌源性分化潜力,观察共培养体系中MSCs与肌成纤维细胞的融合现象。
方法细节:采用免疫荧光染色检测MyHC2、MEF2、结蛋白的蛋白表达与定位,通过GFP标记识别共培养体系中的MSCs;采用多色流式细胞术检测MEF2与ACTN2的细胞阳性率,以L6肌成纤维细胞系为阳性对照;采用活细胞追踪技术,连续5天观察共培养细胞的融合过程。
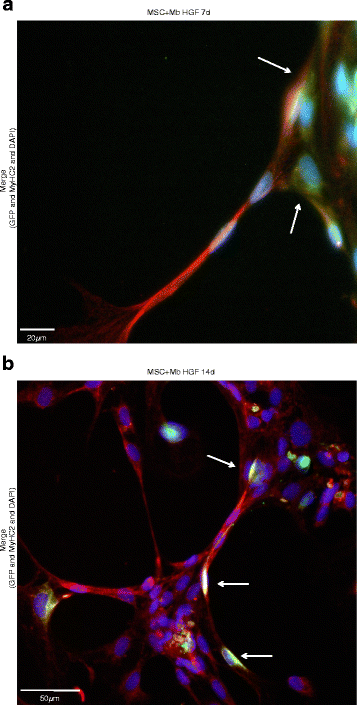
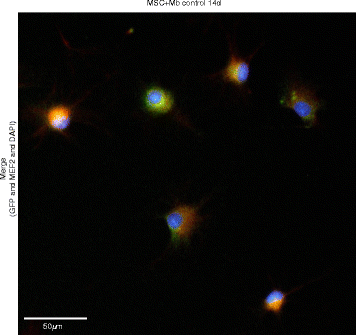
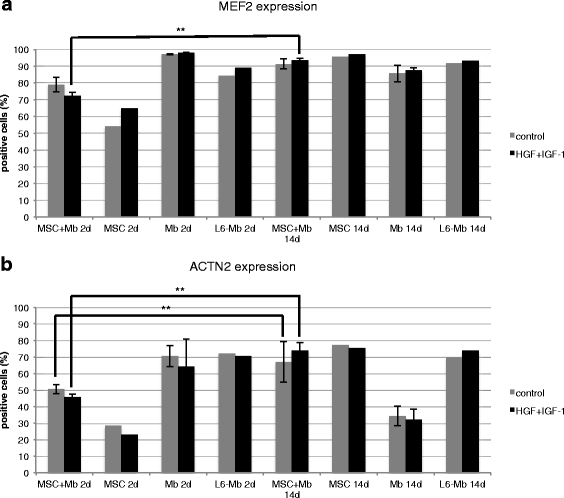
结果解读:免疫荧光结果显示,无论是否添加HGF/IGF-1,MSCs单培养与共培养体系中均可见MyHC2、MEF2的阳性表达,共培养体系中GFP阳性的MSCs参与多核肌管的形成;流式细胞术结果显示,共培养体系中HGF+IGF-1刺激14天后,MEF2阳性率从2天的72.3%升至93.6%(P≤0.01,n=3),ACTN2阳性率从2天到14天显著升高,MSCs单培养14天后MEF2与ACTN2的阳性率与L6细胞相当;活细胞追踪观察到MSCs与肌成纤维细胞的动态融合过程,进一步证实MSCs的肌源性分化潜力。
3.4 3D支架对肌源性分化的调控作用
实验目的:对比不同3D支架对共培养细胞肌源性分化的影响,筛选适配的仿生支架。
方法细节:制备三种3D培养体系:2.5mg/ml纤维蛋白凝胶、5mg/ml纤维蛋白凝胶、2.5mg/ml纤维蛋白-胶原I凝胶、5mg/ml纤维蛋白-胶原I凝胶,将共培养细胞接种后培养2、7天,采用qRT-PCR检测肌源性标志物表达;采用静电纺丝技术制备平行排列的PCL-胶原I纳米纤维支架,接种共培养细胞后培养7天,通过扫描电镜观察细胞排列,免疫荧光检测结蛋白表达。
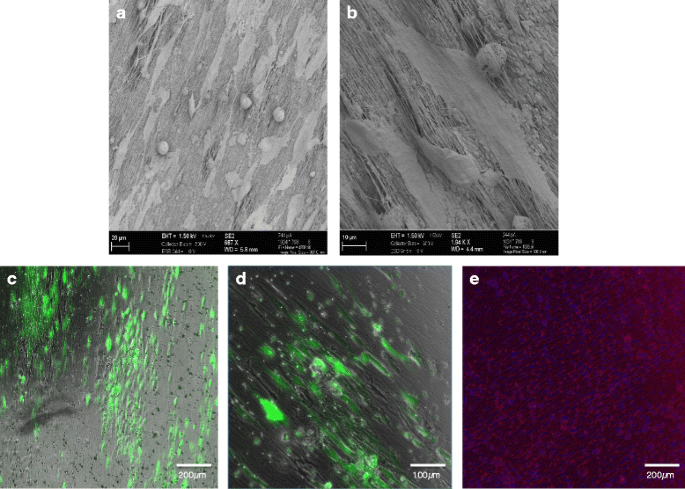
结果解读:qRT-PCR结果显示,5mg/ml纤维蛋白-胶原I凝胶中MEF2与ACTN2的mRNA表达随培养时间显著升高(P≤0.01,n=3),而纯纤维蛋白凝胶中表达随时间下降;扫描电镜结果显示,平行电纺PCL-胶原I纳米纤维支架具有均匀的平行结构,接种细胞后细胞沿纤维方向平行排列,免疫荧光显示细胞结蛋白阳性表达,表明该支架可诱导细胞定向排列与肌源性分化。
4. Biomarker研究及发现成果解析
本研究聚焦肌源性分化关键Biomarker与调控型Biomarker两类,肌源性Biomarker包括早期标志物(结蛋白、MEF2)与晚期标志物(MyHC2、ACTN2、MYOG),调控型Biomarker为IGFBPs(IGFBP4/5/6),筛选逻辑基于骨骼肌分化的已知关键分子,通过多维度实验验证其在不同培养体系中的表达模式与功能关联。
Biomarker定位与筛选逻辑
肌源性Biomarker的筛选基于骨骼肌发育与分化的经典分子通路,结蛋白是肌细胞骨架的核心成分,MEF2是肌分化的关键转录因子,二者作为早期Biomarker可反映MSCs的肌源性启动;MyHC2、ACTN2是成熟肌细胞的收缩装置成分,MYOG是晚期分化的关键调控因子,作为晚期Biomarker反映肌分化的成熟程度。IGFBPs作为HGF/IGF-1的结合蛋白,可调控生长因子的生物活性,因此被选为潜在的调控型Biomarker。验证逻辑为:先通过qRT-PCR检测mRNA表达的时间与浓度效应,再通过免疫荧光与流式细胞术验证蛋白水平的表达与定位,最后在3D支架体系中确认其表达模式。
研究过程详述
肌源性Biomarker的样本来源为2D与3D培养的细胞样本,验证方法包括qRT-PCR(定量mRNA表达)、免疫荧光(蛋白定位与表达)、流式细胞术(蛋白阳性率定量)。早期Biomarker中,MEF2在共培养早期(2天)HGF/IGF-1刺激下表达显著升高(P≤0.05,n=3),14天后共培养与MSCs单培养的MEF2阳性率可达90%以上;结蛋白在MSCs单培养早期表达显著高于共培养,提示其为MSCs的固有标志物之一。晚期Biomarker中,MyHC2在共培养晚期(14天)IGF-1刺激下表达最高(4.8±2.3倍,n=3),ACTN2的表达模式与MyHC2一致;MYOG仅在共培养体系中少量检测到,提示其为肌分化终末阶段的标志物。调控型Biomarker中,IGFBP4/5/6在共培养IGF-1组表达显著升高,与MyHC2、ACTN2的表达呈正相关,提示其可能参与IGF-1调控的肌分化过程。
核心成果提炼
本研究明确了MEF2、结蛋白可作为MSCs肌源性分化的早期Biomarker,MyHC2、ACTN2作为晚期Biomarker,MSCs在单培养与共培养体系中均可表达这些标志物,表明其具有固有肌源性分化潜力;HGF/IGF-1可上调这些Biomarker的表达,但并非肌分化的必需条件,基础分化培养基中的地塞米松、bFGF以及细胞间的旁分泌/直接接触作用已可支持MSCs的肌源性分化;IGFBPs在肌分化中发挥调控作用,不同IGFBPs的功能随培养体系变化,其具体机制需进一步研究;3D纤维蛋白-胶原I凝胶可显著增强肌源性Biomarker的表达,平行电纺PCL-胶原I纳米纤维支架可诱导细胞定向排列,是骨骼肌组织工程的理想仿生支架。这些成果为MSCs在骨骼肌组织工程中的应用提供了关键实验依据,明确了种子细胞优化与支架设计的核心方向,为后续体内实验与临床转化奠定了基础。
