1. 领域背景与文献引入
文献英文标题:Isolation of mouse mesenchymal stem cells with normal ploidy from bone marrows by reducing oxidative stress in combination with extracellular matrix;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:干细胞生物学(间充质干细胞分离与培养)
间充质干细胞(MSCs)由Friedenstein于1976年首次发现,具有向成骨细胞、软骨细胞、脂肪细胞等多谱系分化的潜能,在再生医学、细胞治疗、疾病模型构建等领域具有广泛应用前景。领域共识:人、牛、大鼠等物种的骨髓MSCs可通过塑料贴壁法成功分离,但小鼠骨髓MSCs(mMSCs)的分离与长期培养始终存在核心挑战——传统20%氧浓度培养条件下,mMSCs易被过度增殖的造血细胞污染,且氧化损伤会导致染色体不稳定、自发永生化甚至恶性转化,严重限制了其研究与应用价值。现有研究中,低氧培养或细胞外基质(ECM)包被可部分改善mMSCs的增殖能力,但单独使用仍无法有效解决染色体异常问题,缺乏能稳定获得具有正常倍性原代mMSCs的系统性方法。针对这一领域空白,本研究旨在通过低氧环境、小鼠胚胎成纤维细胞来源ECM(MEF-ECM)、抗氧化剂与低密度接种的组合策略,建立可有效降低核型异常的mMSCs分离与短期培养体系。
2. 文献综述解析
作者按培养条件的差异对现有研究进行分类评述,核心逻辑围绕“mMSCs培养体系的优化方向与局限性”展开。首先,传统20%氧浓度培养体系的研究显示,尽管尝试优化基质、培养基、生长因子等多种条件,mMSCs仍会在培养3-4代后停止生长,随后自发永生化并出现广泛染色体异常,部分细胞系甚至具有体内致瘤性,这一结论与多项前期研究结果一致。其次,低氧培养相关研究表明,2%氧浓度可显著促进mMSCs增殖、减少氧化损伤,同时降低造血细胞污染,但仍无法完全避免染色体异常的发生;MEF-ECM培养的研究则显示,ECM可增强mMSCs的增殖能力、维持干细胞干性,但其单独使用也仅能部分改善染色体稳定性。作者进一步指出,现有方法的核心不足在于无法有效抑制氧化损伤的累积,导致mMSCs在短期培养后仍出现核型异常,而将低氧、ECM、抗氧化剂等策略结合的研究尚未见报道。本研究的创新价值在于首次系统整合多种抗氧化损伤策略,显著提高了原代mMSCs的正常倍性比例,且通过成功生成诱导多能干细胞(iPSCs)验证了分离细胞的功能完整性,为mMSCs的标准化培养提供了新的技术范式。
3. 研究思路总结与详细解析
本研究的核心目标是建立可分离获得正常倍性原代mMSCs的培养体系,核心科学问题是如何通过组合策略抑制氧化损伤导致的染色体不稳定,技术路线遵循“问题验证→单因素优化→组合策略构建→功能验证”的闭环逻辑。
3.1 20%氧浓度下mMSCs的永生化与致瘤性验证
实验目的:验证传统常氧培养条件下mMSCs的遗传不稳定性与致瘤风险。
方法细节:将小鼠骨髓细胞接种于不同基质(明胶、纤连蛋白或未包被)、不同培养基(DMEM、RPMI 1640)及添加不同生长因子的体系中,在20%氧浓度下培养;对永生化细胞系进行核型分析、端肽核酸(PNA)探针端粒荧光原位杂交(FISH)检测;选取高增殖能力的细胞系,将2×10^6细胞接种于免疫缺陷裸鼠腹腔,观察肿瘤形成情况并进行组织病理学分析。
结果解读:所有永生化细胞系均表现出广泛核型异常,端粒信号显著减弱且存在染色体端-端融合现象(图1);其中1株细胞系形成骨肉瘤样肿瘤,可见矿化区域,另一株形成包含内胚层、中胚层、外胚层组织的畸胎瘤样肿瘤(图1B-G),证明传统常氧培养条件下mMSCs易发生恶性转化。
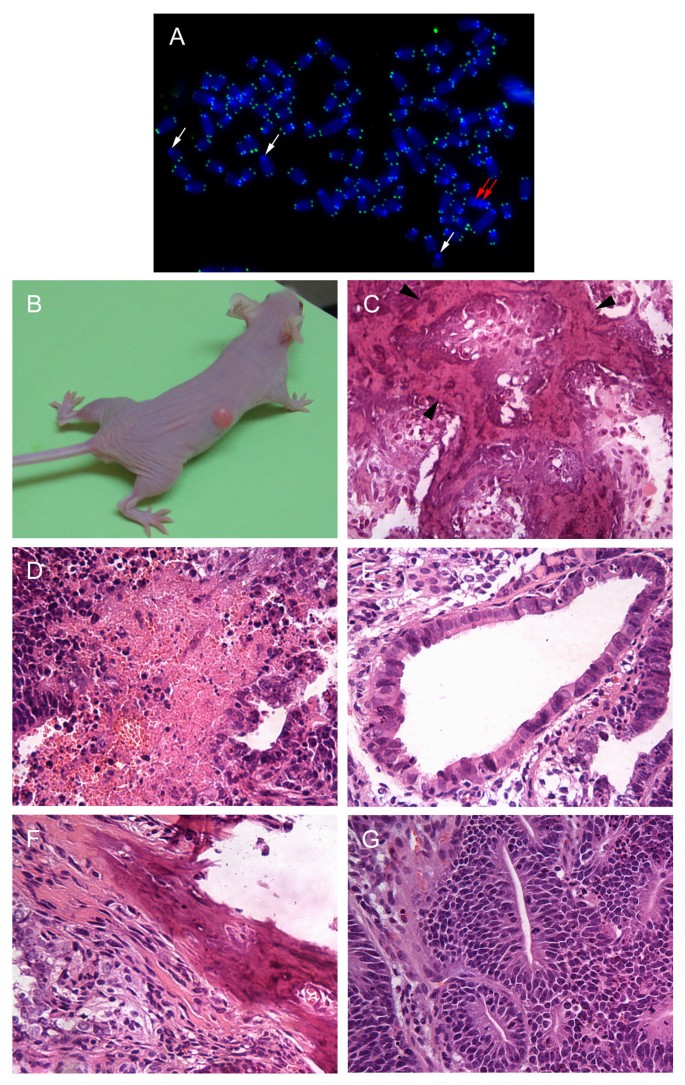
产品关联:文献未提及具体实验产品,领域常规使用流式抗体、核型分析试剂盒、免疫缺陷小鼠等试剂/仪器。
3.2 低氧(2%)培养对mMSCs纯化与增殖的影响
实验目的:探究低氧环境对mMSCs增殖、纯化及氧化损伤的改善作用。
方法细节:将小鼠骨髓细胞分别在20%和2%氧浓度下培养5天,计数细胞数量;通过免疫磁珠去除CD45+、Ter119+造血细胞后,采用微核实验检测DNA损伤;利用流式细胞术分析细胞表面标志物(CD45、CD11b、Sca-1、CD44)的表达;并通过诱导分化实验验证细胞的多向分化潜能。
结果解读:2%氧浓度下mMSCs的增殖倍数约为10.5±1.4倍(n=3,P<0.01),显著高于20%氧组(图2B);微核形成率显著降低(图2D),表明氧化损伤水平下降;流式分析显示低氧组CD45、CD11b阳性造血细胞污染显著减少,同时高表达Sca-1、CD44等mMSCs特异性标志物(图3A);细胞可成功分化为脂肪细胞(油红O染色阳性)、成骨细胞(茜素红染色阳性)和软骨细胞(阿利新蓝染色阳性)(图3C),证明低氧可有效纯化并维持mMSCs的功能特性。
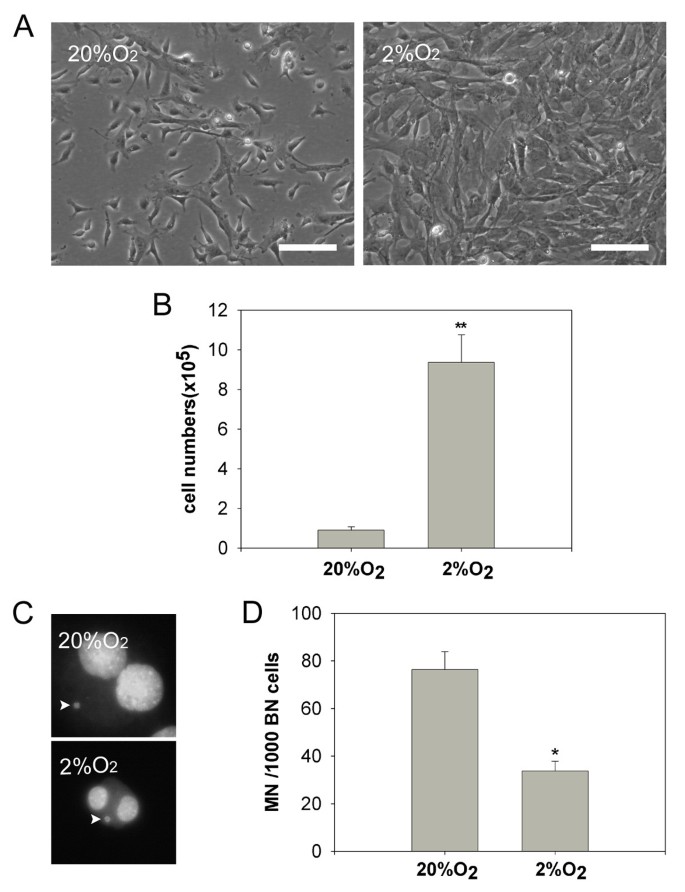
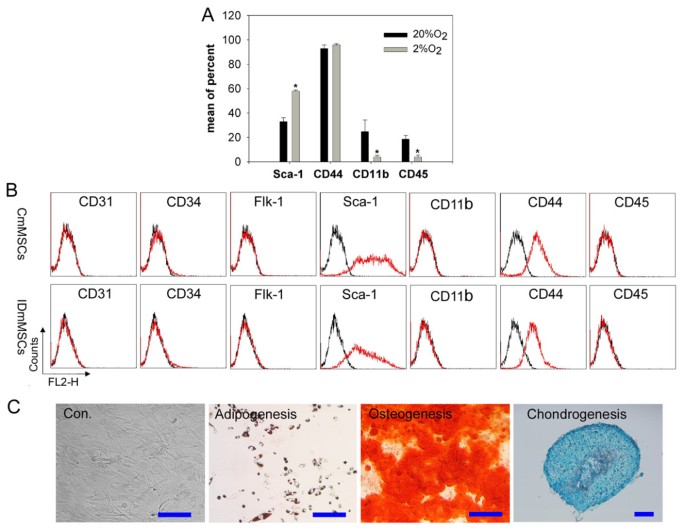
产品关联:文献未提及具体实验产品,领域常规使用细胞计数板、流式细胞仪、分化诱导培养基等试剂/仪器。
3.3 MEF-ECM对mMSCs增殖与染色体稳定性的作用
实验目的:验证MEF来源ECM对mMSCs增殖及氧化损伤的调控作用。
方法细节:将低氧培养的mMSCs以1000细胞/cm²的密度接种于MEF-ECM包被或未包被的培养板上,培养4天后比较细胞增殖情况;通过流式细胞术检测细胞内活性氧(ROS)水平和γ-H2AX(DNA双链损伤标志物)的表达;进行微核实验和核型分析,评估染色体稳定性。
结果解读:MEF-ECM组细胞增殖速度更快,群体倍增数显著高于塑料培养组(图4B);ROS水平和γ-H2AX表达显著降低(图4C、D),微核形成率减少(图4E),表明氧化损伤进一步降低;核型分析显示,MEF-ECM组1代细胞中56%(28/50)具有正常40条染色体,显著高于塑料组的30%(15/50),证明MEF-ECM可部分改善mMSCs的染色体稳定性。
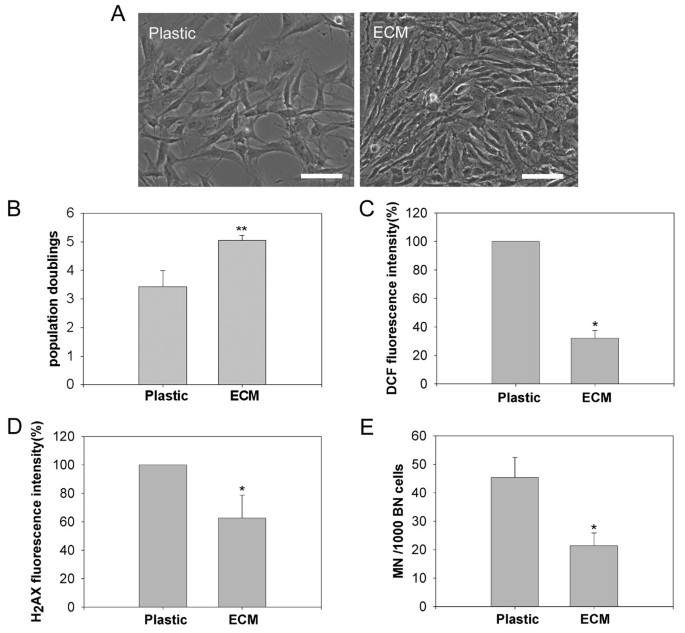
产品关联:文献未提及具体实验产品,领域常规使用ECM包被试剂盒、ROS检测探针、γ-H2AX抗体等试剂/仪器。
3.4 抗氧化剂对mMSCs增殖与染色体稳定性的增强作用
实验目的:探究抗氧化剂是否可进一步抑制氧化损伤,改善mMSCs的长期染色体稳定性。
方法细节:在低氧+MEF-ECM培养体系中添加800μM α-苯基叔丁基硝酮(PBN)和5mM N-乙酰半胱氨酸(NAC)两种抗氧化剂,检测细胞增殖、微核形成率及核型;通过添加H2O2诱导氧化应激,验证抗氧化剂的保护作用;并观察细胞在长期培养(8代)中的增殖情况与核型变化。
结果解读:抗氧化剂显著降低了原代mMSCs的微核形成率(图5A),提高了细胞增殖能力(图5B),并增加了1代细胞的正常核型比例;H2O2处理导致细胞增殖抑制和微核率升高,而抗氧化剂可有效缓解该效应;长期培养至8代时,抗氧化剂+MEF-ECM组仍有28%(14/50)的细胞具有正常核型,远高于其他实验组的几乎无正常核型的结果(图5F),证明抗氧化剂与MEF-ECM的组合可显著改善mMSCs的长期染色体稳定性。
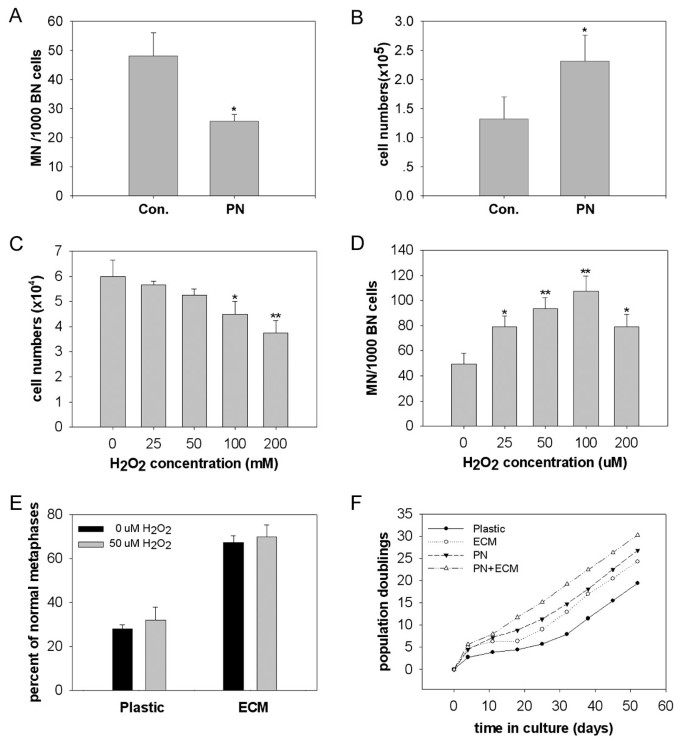
产品关联:文献未提及具体实验产品,领域常规使用抗氧化剂试剂、H2O2、核型分析系统等试剂/仪器。
3.5 组合策略分离正常倍性mMSCs及iPSCs生成验证
实验目的:验证低氧+MEF-ECM+抗氧化剂+低密度接种的组合策略,是否可分离获得具有正常倍性且功能完整的mMSCs。
方法细节:将小鼠骨髓细胞以5×10^4细胞/cm²的低密度直接接种于MEF-ECM包被的培养板上,在低氧+抗氧化剂条件下培养;通过流式细胞术检测细胞表面标志物,验证细胞纯度;进行核型分析,统计正常倍性细胞比例;通过慢病毒载体转染Oct4、Sox2、Klf4、c-Myc四个因子,诱导生成iPSCs,检测碱性磷酸酶活性及多能性标志物(Oct4、Nanog、SSEA1)的表达。
结果解读:分离的mMSCs几乎无造血细胞污染,可成功向脂肪、成骨、软骨三系分化(图6B),且超过80%的细胞具有正常核型(图6A);成功生成碱性磷酸酶阳性的iPSCs克隆,其多能性标志物的表达模式与尾尖成纤维细胞来源的iPSCs一致(图7),证明分离的mMSCs功能完整,可用于后续的重编程研究。
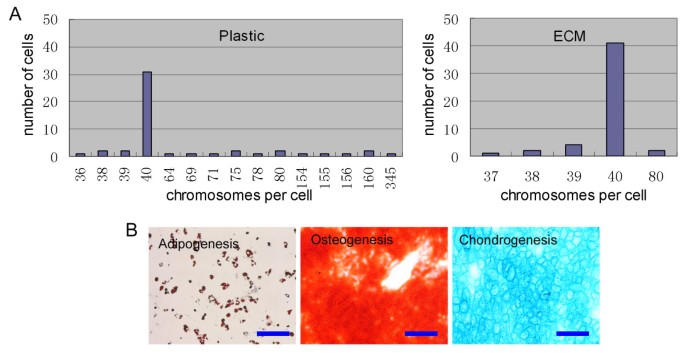
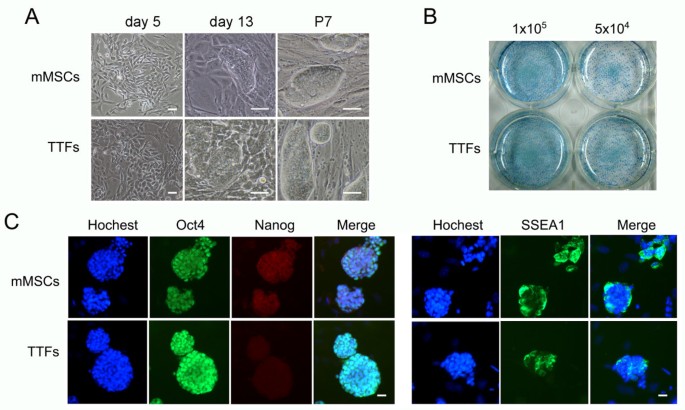
产品关联:文献未提及具体实验产品,领域常规使用慢病毒载体、iPSCs诱导培养基、多能性标志物抗体等试剂/仪器。
4. Biomarker研究及发现成果解析
本文未针对特定Biomarker进行筛选与验证,核心成果在于建立了可获得高比例正常倍性mMSCs的培养体系,其中mMSCs的鉴定标志物为表面分子Sca-1+、CD44+、CD45-、CD11b-,验证逻辑为“流式细胞术检测→多向分化潜能验证→核型分析→iPSCs生成验证”的完整链条。
研究过程中,通过流式细胞术对分离的mMSCs进行表面标志物检测,结果显示细胞群体几乎不表达造血细胞标志物CD45、CD11b,高表达mMSCs特异性标志物Sca-1、CD44;核型分析显示,采用组合策略分离的原代mMSCs中,超过80%的细胞具有正常40条染色体(n=50,文献未明确提供具体P值);iPSCs生成实验进一步验证了细胞的功能完整性,证明该体系获得的mMSCs具有正常的生物学功能。
核心成果总结:本研究首次建立了整合低氧、MEF-ECM、抗氧化剂与低密度接种的mMSCs培养体系,可显著降低原代mMSCs的核型异常率,为mMSCs的标准化分离与短期培养提供了可靠方法;该体系获得的mMSCs可成功生成iPSCs,证明其遗传稳定性与功能完整性,为干细胞研究、疾病模型构建等领域提供了高质量的细胞来源。