1. 领域背景与文献引入
文献英文标题:Interaction between NSMCE4A and GPS1 links the SMC5/6 complex to the COP9 signalosome;发表期刊:BMC Molecular and Cell Biology;影响因子:未公开;研究领域:染色体结构维持与DNA损伤修复。
真核生物表达三类结构维持染色体(SMC)复合物,分别为黏连蛋白、凝缩蛋白和SMC5/6,其中黏连蛋白负责姐妹染色单体的黏连,凝缩蛋白参与有丝分裂前的染色质浓缩,而SMC5/6是研究相对较少的一类,已知其参与同源重组修复及有丝分裂、减数分裂过程中的染色体分离,但具体调控机制仍不明确。COP9信号体(CSN)是一个由8个亚基组成的复合物,主要通过对Cullin-RING E3泛素连接酶(CRLs)进行去NEDD化修饰来调控其活性,广泛参与细胞周期调控、DNA复制、转录调控及蛋白质质量控制等过程,其中在DNA损伤响应中,GPS1的缺失会影响DNA末端切除,进而抑制同源重组修复,但CSN与SMC5/6之间的关联尚未被探索。目前领域内尚未有研究直接证实SMC5/6与CSN复合物之间存在物理或功能相互作用,这一空白限制了对DNA损伤修复和染色体分离调控网络的全面理解。
针对这一研究空白,本研究以SMC5/6复合物的kleisin亚基NSMCE4A为研究对象,通过酵母双杂交筛选其相互作用蛋白,首次发现并验证了NSMCE4A与CSN复合物的GPS1亚基之间的相互作用,进而揭示了CSN复合物对SMC5/6在细胞周期进程及DNA损伤响应中的调控作用,为完善染色体结构维持与DNA损伤修复的调控网络提供了新的实验依据。
2. 文献综述解析
作者对领域内现有研究的分类维度为SMC复合物的功能分类及CSN复合物的调控机制分类,系统梳理了三类SMC复合物的结构与功能,以及CSN对CRLs的调控作用及其在细胞进程中的功能。
现有研究已明确三类SMC复合物的基本结构,均由两个SMC ATP酶、一个保守的kleisin亚基及其他辅助蛋白组成,其中黏连蛋白的核心功能是在S期到后期维持姐妹染色单体的黏连,凝缩蛋白则在有丝分裂前介导染色质浓缩以保障染色体正常分离;SMC5/6虽被证实参与DNA损伤修复和染色体分离,但具体的调控因子和分子机制仍不清晰。CSN复合物的研究则主要聚焦于其对CRLs的去NEDD化调控,已知CSN通过这一功能参与细胞周期、DNA损伤响应等多个过程,在DNA损伤修复中,GPS1的缺失会影响DNA末端切除,进而抑制同源重组修复,但CSN与SMC5/6之间的关联尚未被探索。现有研究的技术方法多采用酵母双杂交、免疫共沉淀、免疫荧光等经典分子生物学技术,能够有效验证蛋白相互作用及细胞内定位,但局限性在于未将SMC5/6与CSN这两个功能相关的复合物进行关联分析,缺乏对两者相互作用及功能调控的直接研究。
本研究通过酵母双杂交筛选首次发现NSMCE4A与GPS1的相互作用,突破了现有研究中对SMC5/6和CSN复合物独立研究的局限,通过一系列实验验证了两者的物理相互作用发生在完整复合物层面,并进一步揭示了CSN对SMC5/6在DNA损伤响应中的调控作用,填补了领域内关于SMC5/6调控机制的空白,为深入理解DNA损伤修复和染色体分离的调控网络提供了新的方向。
3. 研究思路总结与详细解析
本研究的整体研究目标是筛选并验证NSMCE4A的相互作用蛋白,探索SMC5/6与CSN复合物的相互作用及功能关联;核心科学问题为NSMCE4A与GPS1是否存在特异性相互作用,以及CSN复合物如何调控SMC5/6在细胞周期和DNA损伤响应中的功能;技术路线遵循“筛选验证→定位分析→功能探究”的闭环逻辑,通过酵母双杂交筛选相互作用蛋白,免疫共沉淀验证物理相互作用,细胞内共定位分析探究相互作用的细胞内效应,最后通过GPS1敲低和CSN功能抑制实验揭示其功能调控关系。
3.1 酵母双杂交筛选NSMCE4A的相互作用蛋白
实验目的:筛选能够与SMC5/6复合物的kleisin亚基NSMCE4A发生相互作用的蛋白,为探索SMC5/6的调控机制提供候选分子。
方法细节:以小鼠NSMCE4A为诱饵蛋白,构建酵母双杂交诱饵载体,与小鼠睾丸cDNA文库的猎物载体共转化酵母菌株Y190,通过在添加金担子素A、腺嘌呤缺失、组氨酸缺失的选择性培养基上生长筛选阳性克隆,经过多轮验证减少假阳性结果,最终对阳性克隆进行测序分析。
结果解读:初始筛选得到121个阳性克隆,经过验证后得到28个阳性克隆对应16个基因,其中GPS1被多个不同长度的cDNA片段所编码,进一步的片段分析显示,GPS1的C端PCI结构域(257-526氨基酸)是与NSMCE4A相互作用的关键区域,而N端区域(1-288氨基酸)无相互作用,且全长GPS1的相互作用强度弱于缺失N端77个氨基酸的片段,提示N端可能对相互作用存在负调控作用。
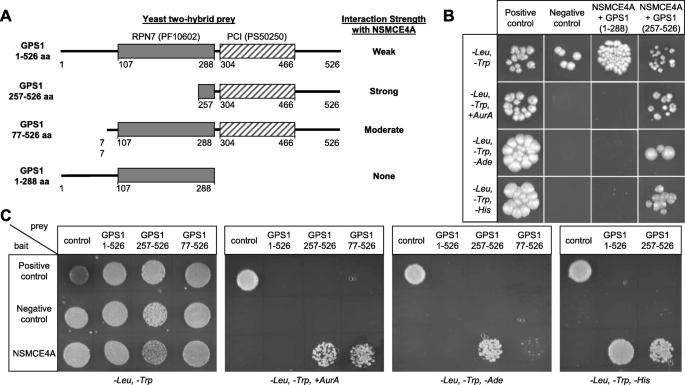
产品关联:文献未提及具体实验产品,领域常规使用酵母双杂交系统(如Clontech Matchmaker系统)。
3.2 免疫共沉淀验证NSMCE4A与GPS1的相互作用
实验目的:在哺乳动物细胞中验证NSMCE4A与GPS1的物理相互作用,并确认该相互作用是否发生在完整的SMC5/6和CSN复合物层面。
方法细节:在HEK293T细胞中分别或共表达HA标签的NSMCE4A和FLAG标签的GPS1,细胞裂解后分别用抗FLAG抗体和抗HA抗体进行免疫共沉淀,通过免疫印迹检测沉淀复合物中的蛋白成分。
结果解读:抗FLAG抗体的免疫共沉淀能够检测到共表达的HA-NSMCE4A,抗HA抗体的免疫共沉淀也能检测到FLAG-GPS1,同时在FLAG免疫沉淀复合物中检测到SMC5/6的另一个亚基NSMCE1,在HA免疫沉淀复合物中检测到CSN的亚基CSN3,说明NSMCE4A与GPS1的相互作用并非孤立存在,而是发生在完整的SMC5/6和CSN复合物之间。

产品关联:实验所用关键产品:GeneTex的抗HA抗体(货号GTX628489)、Sigma的抗FLAG抗体(货号F3165)、Life Technologies的Dynabeads共免疫沉淀试剂盒。
3.3 细胞内共定位与核质分布分析
实验目的:检测NSMCE4A与GPS1在细胞内的定位及共定位情况,探究相互作用对NSMCE4A细胞内分布的影响。
方法细节:在HeLa细胞中单独或共表达HA-NSMCE4A和FLAG-GPS1,用免疫荧光染色标记两种蛋白,通过激光共聚焦显微镜观察细胞内定位,利用图像分析软件定量分析NSMCE4A的核质比,并分析其与GPS1核质比的相关性。
结果解读:单独表达时NSMCE4A主要定位于细胞核,共表达时两者主要在细胞核共定位,当GPS1出现在细胞质中时,NSMCE4A的细胞质信号也显著增强,核质比显著降低(n=未明确提供,P=5.41×10^-6),且NSMCE4A与GPS1的核质比呈显著正相关(Pearson相关系数0.639,Spearman相关系数0.655),提示两者的相互作用可能阻碍了NSMCE4A的核输入。此外,内源性表达的GPS1与NSMCE4A、SMC6在间期细胞核和细胞质中均有共定位,在有丝分裂中期则共同定位于浓缩的染色体周围。
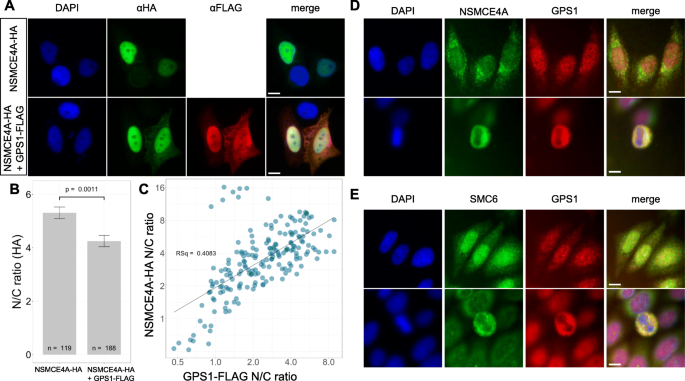
产品关联:文献未提及具体实验产品,领域常规使用免疫荧光染色试剂盒、激光共聚焦显微镜(如Zeiss LSM系列)、图像分析软件(如Fiji、GraphPad Prism)。
3.4 GPS1敲低对SMC5/6在DNA损伤位点定位的影响
实验目的:探究GPS1缺失对SMC5/6在DNA损伤响应中的定位及功能的影响。
方法细节:在U-2 OS细胞中用siRNA敲低GPS1的表达,48小时后用405nm激光诱导DNA损伤条纹,免疫荧光染色标记SMC6,通过图像分析定量损伤位点的SMC6信号强度与细胞核背景信号强度的比值。
结果解读:GPS1敲低后,SMC6在激光诱导DNA损伤位点的信号强度显著高于对照组(n=未明确提供,P=0.0006),提示GPS1的缺失会促进SMC5/6在DNA损伤位点的积累,可能影响其在DNA损伤修复中的功能。
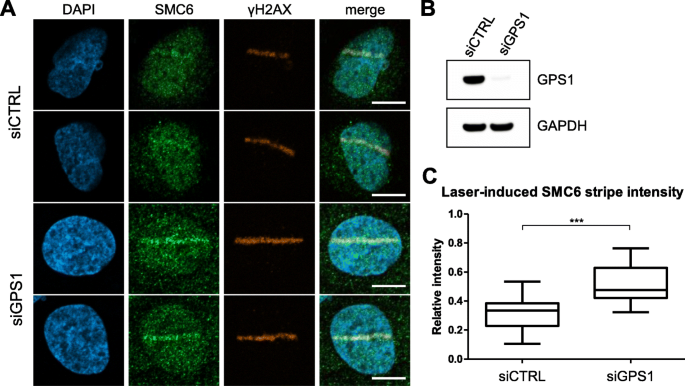
产品关联:实验所用关键产品:Dharmacon的ON-TARGETplus Human GPS1 siRNA SMARTpool(货号L-012272-00-0005)、Invitrogen的Lipofectamine RNAiMAX。
3.5 CSN去NEDD化功能抑制对SMC5/6定位的影响
实验目的:验证CSN复合物的去NEDD化功能对SMC5/6在DNA损伤响应中定位的调控作用。
方法细节:在U-2 OS细胞中分别用溶剂对照、NEDD8 E1抑制剂MLN4924和CSN去NEDD化抑制剂CSN5i-3处理1小时,激光诱导DNA损伤后,免疫荧光染色检测SMC6的定位,同时通过免疫印迹检测CUL4A的NEDD化水平以验证抑制剂的效果。
结果解读:CSN5i-3处理后,CUL4A的NEDD化水平显著升高,说明CSN的去NEDD化功能被有效抑制;同时,SMC6在激光诱导DNA损伤位点的信号强度显著高于对照组(n=未明确提供,P<0.0001),提示CSN的去NEDD化功能参与调控SMC5/6在DNA损伤位点的定位。
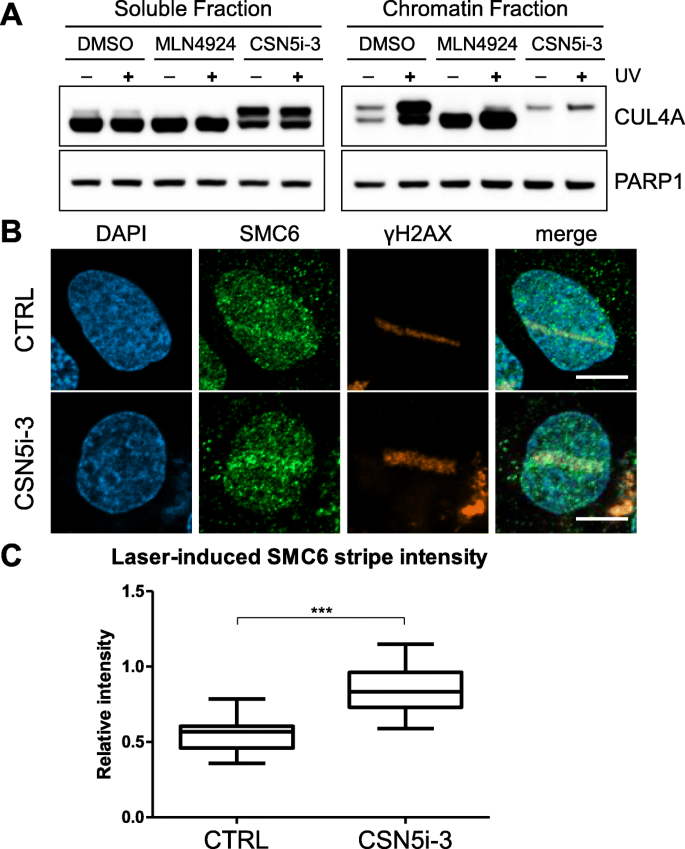
产品关联:实验所用关键产品:Novartis的CSN5i-3、Active Biochem的MLN4924。
4. Biomarker研究及发现成果
本研究中涉及的功能调控节点为NSMCE4A与GPS1的蛋白-蛋白相互作用,其作为SMC5/6与CSN复合物功能关联的关键分子,筛选与验证逻辑为酵母双杂交初步筛选→免疫共沉淀验证物理相互作用→细胞内共定位验证→功能实验验证调控效应。
该相互作用的来源为哺乳动物细胞内的内源性蛋白复合物,验证方法包括酵母双杂交、免疫共沉淀、免疫荧光染色及激光诱导DNA损伤实验;特异性方面,GPS1的C端PCI结构域是与NSMCE4A相互作用的关键区域,N端区域对相互作用存在负调控;功能敏感性方面,GPS1敲低或CSN去NEDD化功能抑制均会导致SMC5/6在DNA损伤位点的信号强度显著升高,提示该相互作用对SMC5/6的DNA损伤响应功能具有调控作用。
本研究首次证实SMC5/6与CSN复合物存在物理和功能相互作用,NSMCE4A与GPS1的相互作用是两者复合物关联的关键节点;功能上,CSN复合物通过去NEDD化功能调控SMC5/6在DNA损伤位点的定位,进而影响其在DNA损伤修复中的功能;统计学结果包括核质比分析的P=5.41×10^-6,GPS1敲低后SMC6信号强度的P=0.0006,CSN功能抑制后SMC6信号强度的P<0.0001。该发现为完善染色体结构维持与DNA损伤修复的调控网络提供了新的视角,同时为进一步探索CSN对SMC5/6稳定性的调控作用提供了研究方向。