1. 领域背景与文献引入
文献英文标题:Single‑cell RNA sequencing analysis of human embryos from the late Carnegie to fetal development;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:人类胚胎发育生物学、单细胞转录组学
领域共识:胚胎发育是生命科学的核心研究方向,单细胞RNA测序技术的突破为解析胚胎细胞分化轨迹和调控机制提供了高分辨率工具。现有研究中,模式生物(小鼠、斑马鱼、食蟹猴)的胚胎细胞图谱已通过单细胞测序构建完成,揭示了胚胎发育过程中的基因激活时序和细胞分化路径;人类胚胎研究已覆盖早期发育阶段(卡内基阶段CS1到CS7,对应1天-2.5周)、CS12到CS16(4-6周)的细胞类型鉴定,以及10-26周胎儿器官的细胞图谱构建,但7-9周(晚期卡内基阶段至胎儿发育的过渡阶段)是人类胚胎发育的关键时期,该阶段的细胞发育图谱和分化机制尚未明确,属于核心研究空白。
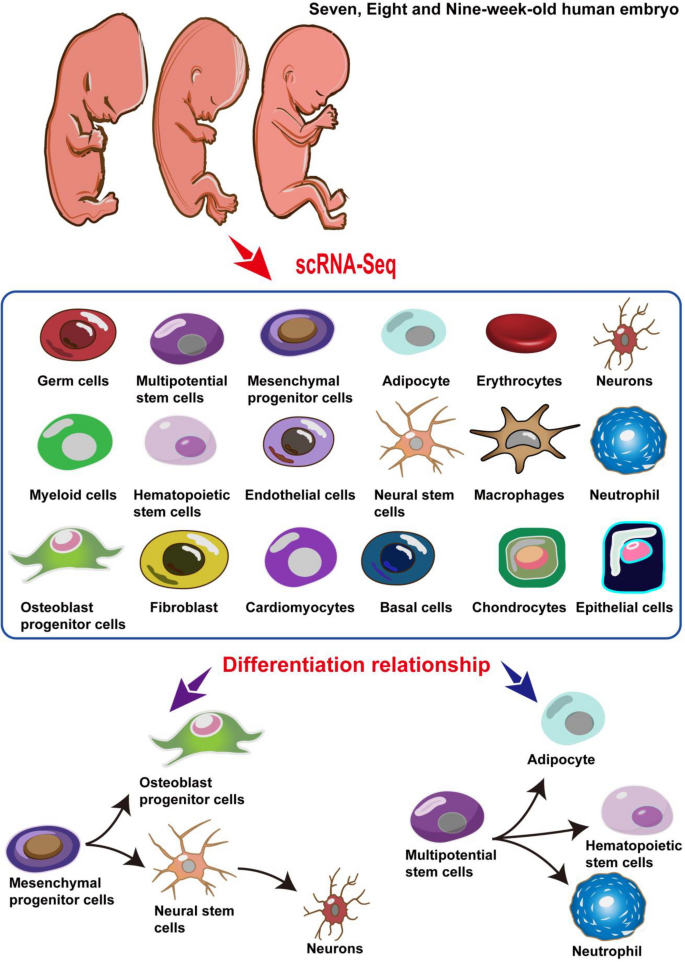
针对这一研究空白,本研究采用单细胞RNA测序技术,对7、8、9周人类胚胎进行分析,旨在构建该过渡阶段的细胞发育图谱,明确细胞类型及分化关系,为人类胚胎发育机制研究提供关键数据支撑。
2. 文献综述解析
作者对领域内现有研究按研究对象分为模式生物胚胎发育研究和人类胚胎不同阶段研究两类,系统梳理了现有研究的成果与局限性,明确了本文的研究定位。
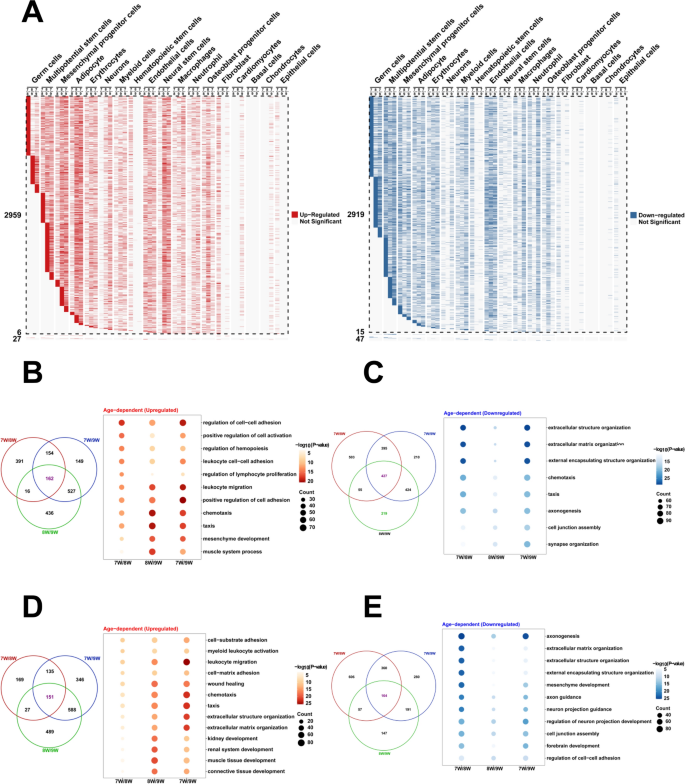
模式生物胚胎发育研究方面,小鼠、斑马鱼的单细胞转录组分析已揭示了原肠胚形成及早期器官发生阶段的基因表达动态和细胞分化轨迹,食蟹猴的研究鉴定了原肠运动阶段的主要细胞类型;这些研究的优势在于能够通过模式生物的可操作性,深入解析胚胎发育的调控机制,但局限性在于模式生物的胚胎发育过程与人类存在物种差异,无法完全模拟人类胚胎的发育特征。人类胚胎研究方面,现有成果覆盖了早期着床前、着床后及部分胎儿阶段,明确了不同卡内基阶段的细胞类型和分化方向,结合空间转录组技术构建了早期器官发生的细胞图谱;但局限性在于缺少7-9周过渡阶段的研究数据,无法揭示该阶段细胞分化的关键路径和调控网络,而该阶段是胚胎从器官雏形形成向胎儿成熟发育的关键转折点,其机制研究对理解人类胚胎发育异常具有重要意义。
通过对比现有研究的空白,本研究的创新点在于首次构建了人类7-9周胚胎的细胞发育图谱,鉴定了18种细胞簇,揭示了两条独立的细胞分化路径,填补了晚期卡内基阶段至胎儿发育过渡阶段的研究空白,为人类胚胎发育的完整图谱构建提供了关键补充数据。
3. 研究思路总结与详细解析
本研究的整体框架为:以人类7-9周胚胎为研究对象,通过单细胞RNA测序技术获取转录组数据,经数据质控、聚类分析鉴定细胞类型,结合轨迹分析、细胞通讯分析、转录因子解析揭示细胞分化路径与调控机制,最终通过qPCR验证关键基因表达,构建完整的细胞发育图谱;核心科学问题是明确该过渡阶段的细胞类型组成、分化关系、细胞间通讯机制及转录调控网络;技术路线遵循“样本制备-组学检测-生物信息分析-实验验证”的闭环逻辑。
3.1 人类胚胎样本收集与单细胞悬液制备
实验目的是获取高质量的人类胚胎单细胞样本,为后续单细胞RNA测序提供合格材料。方法细节为收集7、8、9周人类胚胎各1例,将胚胎组织分割为50mm³的组织块,采用组织消化液在37℃条件下消化15min,经40μm无菌细胞滤器去除细胞碎片与杂质,使用红细胞裂解液在25℃处理10min以去除红细胞,最终用Bio-Rad TC20自动细胞计数仪进行细胞计数。结果解读为共获得7周胚胎细胞20156个、8周19112个、9周28376个,后续经质量控制后保留67644个合格细胞(n=3,P<0.05,基于质控指标筛选),满足单细胞测序的样本质量要求。实验所用关键产品:Bio-Rad的TC20 Automatic Cell Counter、红细胞裂解液(文献未提及具体品牌,领域常规使用商业化红细胞裂解液)。
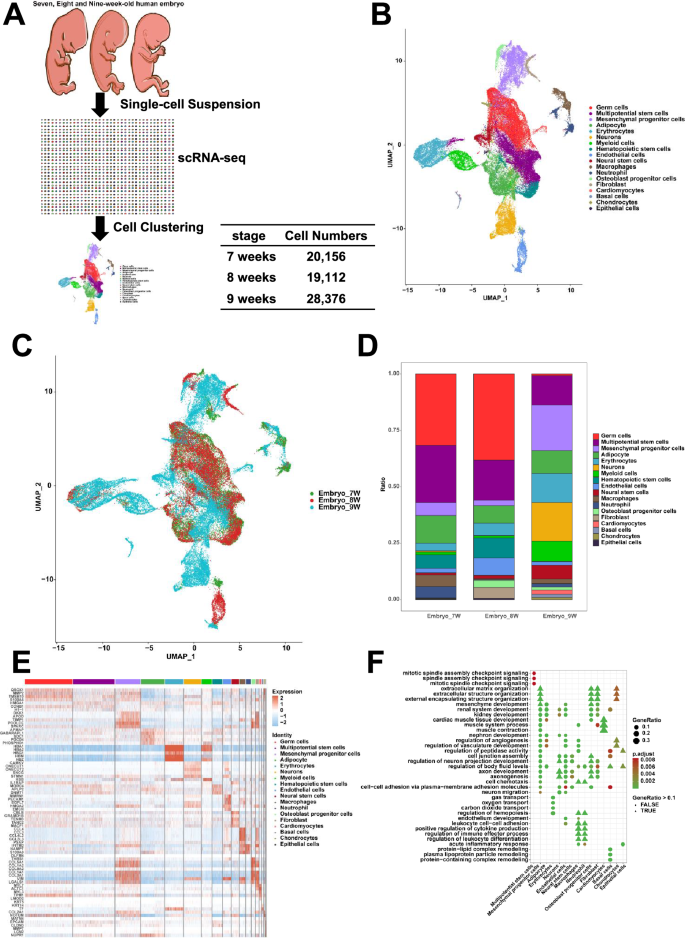
3.2 单细胞RNA测序与数据预处理
实验目的是获取单细胞转录组数据并进行标准化处理,为后续聚类分析奠定基础。方法细节为将单细胞悬液密度调整为1×10^5 cells/mL,通过微流控芯片捕获单个细胞,加入细胞裂解液裂解细胞并捕获mRNA,进行反转录、cDNA扩增及文库构建,采用Illumina HiSeq X10平台进行150bp双端测序;使用CeleScope软件进行序列比对与定量,生成基因表达矩阵;采用Seurat软件进行质量控制,筛选标准为基因数200-6000、总RNA计数≤30000、线粒体基因占比<30%,随后通过SCTransform算法归一化数据,筛选3000个高可变基因,经主成分分析(PCA)保留50个主成分,采用UMAP方法对细胞簇进行降维可视化。结果解读为测序数据经质控后,成功将67644个细胞聚类为18个细胞簇,UMAP图显示各细胞簇边界清晰,表明聚类结果可靠。实验所用关键产品:Illumina的HiSeq X10测序平台、CeleScope软件、Seurat R包。
3.3 细胞类型注释与差异表达基因分析
实验目的是鉴定各细胞簇的类型,并分析胚胎发育过程中的基因表达动态变化。方法细节为参考CellMarker、PanglaoDB数据库及已发表文献中的细胞标记基因,对18个细胞簇进行类型注释;采用FindAllMarkers函数筛选差异表达基因(DEGs),将样本分为三组(8周vs7周、9周vs8周、9周vs7周)分析不同发育阶段的基因表达变化,使用clusterProfiler包进行GO富集分析,明确差异基因参与的生物学过程。结果解读为成功注释得到18种细胞类型,包括生殖细胞、多能干细胞、间充质祖细胞、成骨细胞祖细胞、神经干细胞、神经元等;差异表达基因分析显示,多能干细胞的DEGs参与造血调控、间充质发育等生物学过程,间充质祖细胞的DEGs参与趋化、肾脏发育等过程,提示这两类细胞具有多向分化潜能(GO富集P_adj<0.05)。实验所用关键产品:CellMarker数据库、PanglaoDB数据库、clusterProfiler R包。
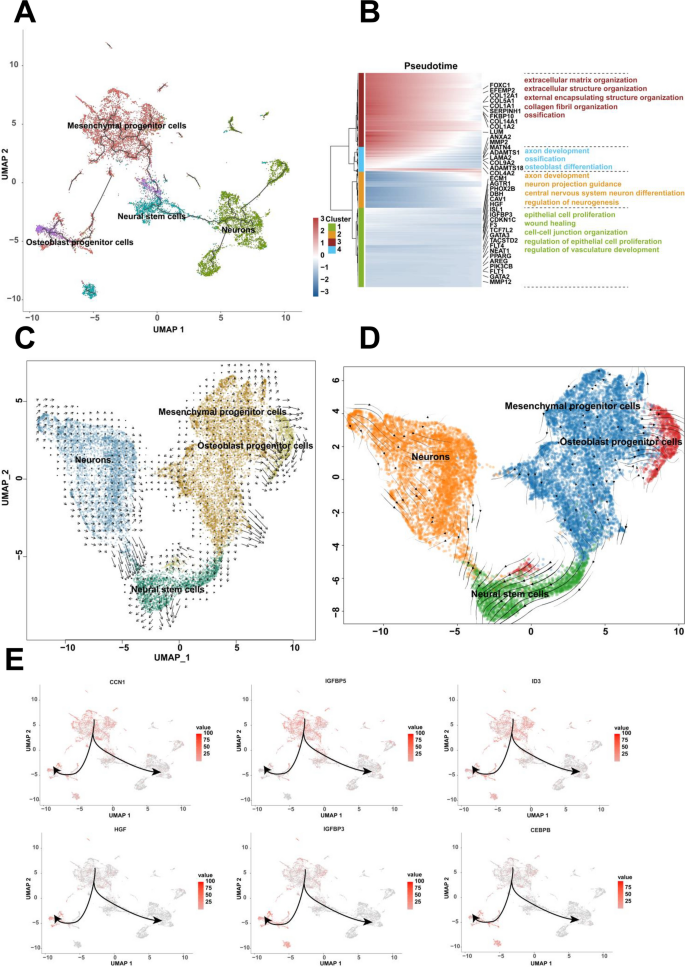
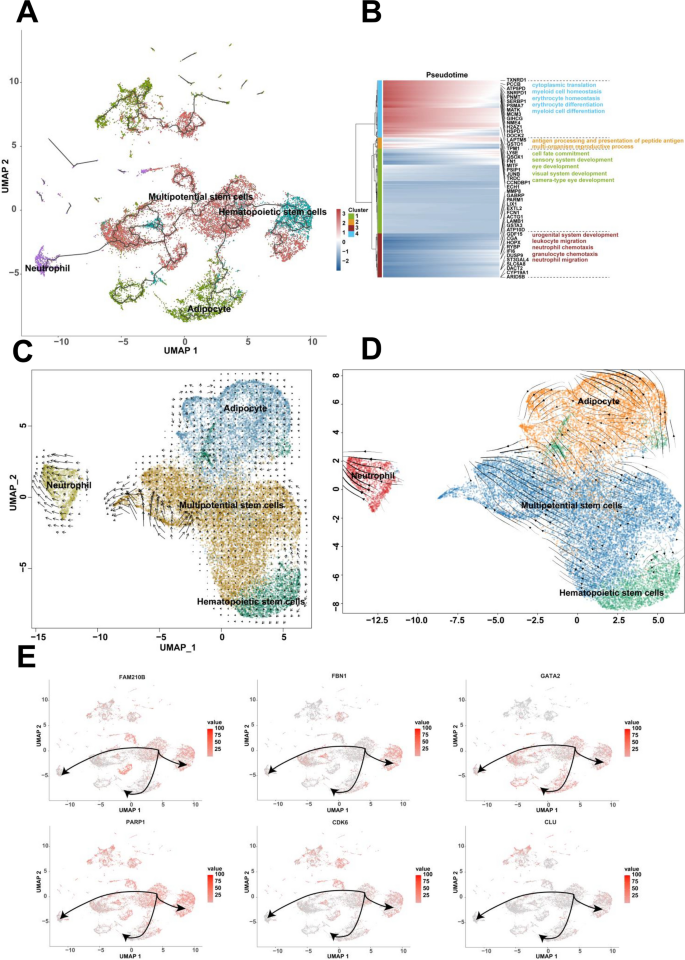
3.4 细胞分化轨迹与RNA velocity分析
实验目的是解析人类7-9周胚胎细胞的分化路径及方向。方法细节为采用Monocle3软件构建细胞分化轨迹,筛选在至少1%细胞中表达且经验离散值大于拟合离散值的基因进行拟时间分析,通过DDRTree方法降维并重建分化轨迹;同时采用RNA velocity(scVelo)分析细胞的分化方向与状态。结果解读为揭示了两条独立的细胞分化路径:第一条路径中间充质祖细胞作为分化起点,分别分化为成骨细胞祖细胞和神经干细胞,神经干细胞进一步分化为神经元;第二条路径中多能干细胞作为起点,分别分化为脂肪细胞、造血干细胞和中性粒细胞;RNA velocity分析显示,间充质祖细胞和神经干细胞具有高度异质性,可向多个方向分化,而成骨细胞祖细胞和神经元处于稳定的分化终末状态。实验所用关键产品:Monocle3 R包、scVelo软件。
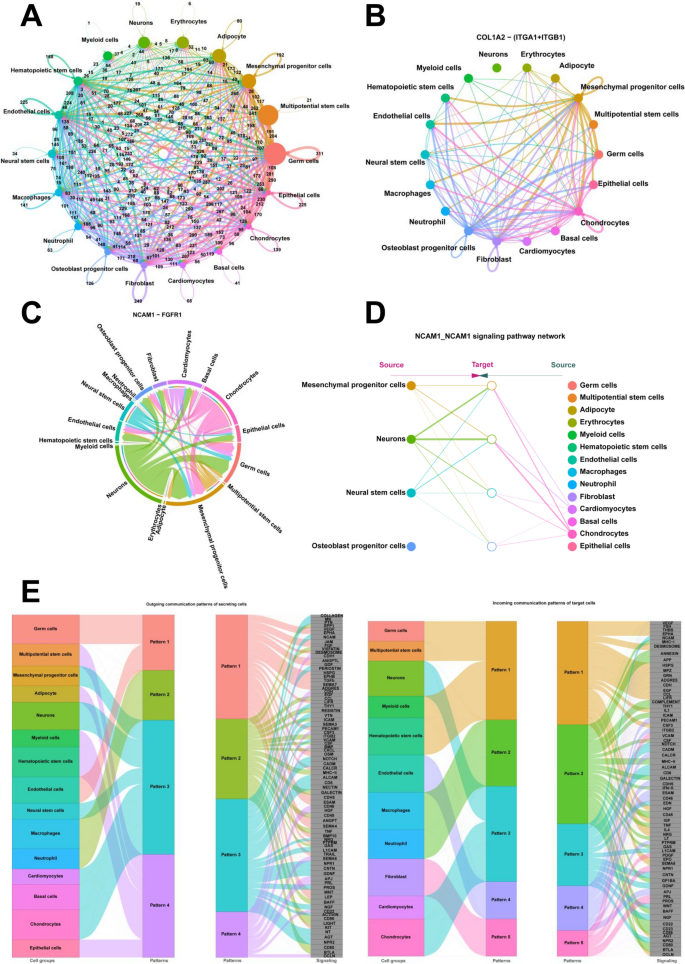
3.5 细胞间通讯分析
实验目的是鉴定细胞间通讯的关键信号通路,解析细胞分化的微环境调控机制。方法细节为采用CellChat包分析细胞间的配体-受体相互作用,导入人类配体-受体数据库(CellChatDB),鉴定各细胞簇的高表达配体-受体对,计算细胞间通讯的概率,分析分泌细胞的输出通讯模式和靶细胞的输入通讯模式。结果解读为鉴定了多条关键细胞间通讯通路:COL1A2-(ITGA1+ITGB1)介导间充质祖细胞与成骨细胞祖细胞的通讯,NCAM1-FGFR1介导间充质祖细胞与神经干细胞的通讯,NCAM1-NCAM1介导神经干细胞与神经元的通讯,CGA-FSHR同时介导多能干细胞与脂肪细胞、造血干细胞、中性粒细胞的通讯;通讯模式分析显示,间充质祖细胞、神经干细胞和神经元属于同一输出模式,多能干细胞和造血干细胞属于同一输入模式。实验所用关键产品:CellChat R包、CellChatDB人类配体-受体数据库。
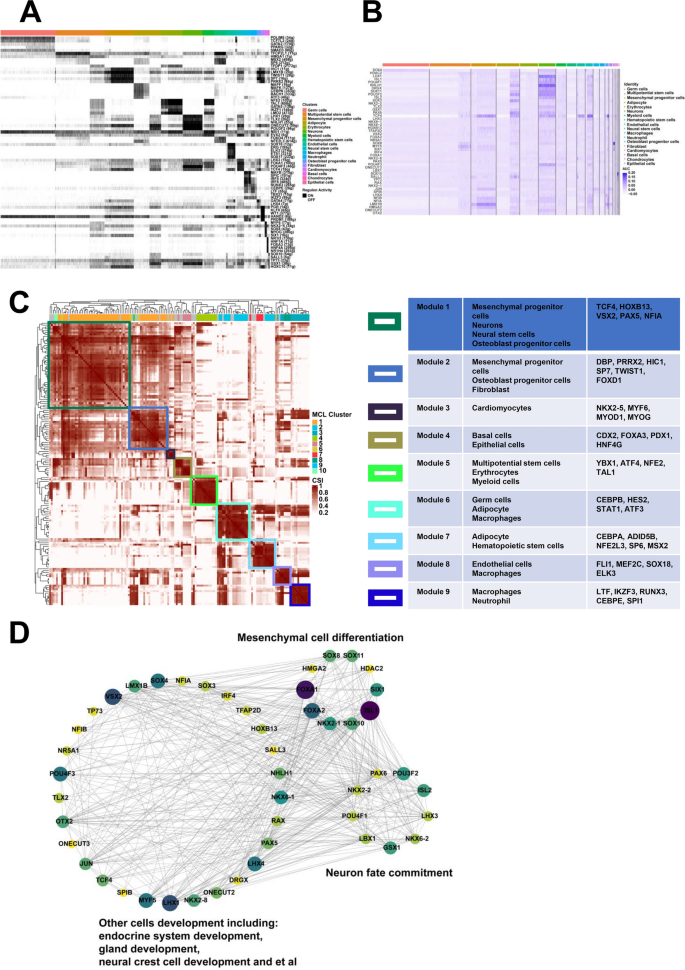
3.6 转录因子调控网络分析
实验目的是解析细胞分化的转录调控机制,鉴定关键调控因子。方法细节为采用pySCENIC包分析转录因子调控网络,将Seurat对象转换为Loom格式,通过共表达基因推断基因调控网络,结合已知转录因子结合位点筛选候选靶基因,计算AUC值并进行二值化处理,采用Cytoscape软件可视化调控网络。结果解读为不同细胞簇激活了特异性转录因子,如间充质祖细胞中的HIC1、LMX1B、TWIST1,神经干细胞中的LHX3、EVX2,神经元中的LHX1、TLX2;共调控因子如HOXB13、VSX2、PAX5介导细胞发育与分化;模块分析显示,152个调控子聚类为9个模块,不同细胞簇共享调控模块,如模块1包含间充质祖细胞、神经元、神经干细胞和成骨细胞祖细胞,参与神经系统发育和间充质细胞分化;调控网络分析显示,SOX8、SOX11等参与间充质细胞分化,PAX6、POU3F2等参与神经元命运决定。实验所用关键产品:pySCENIC包、Cytoscape软件。
3.7 qPCR验证实验
实验目的是验证单细胞RNA测序结果中关键基因的表达变化。方法细节为提取7、8、9周人类胚胎的总RNA,采用Vazyme的HiScript II Q RT SuperMix合成cDNA,使用AceQ Universal SYBR qPCR Master Mix在Bio-Rad CFX96实时PCR系统上进行扩增,引物由Sangon Biotech合成,以β-actin为内参,采用2^-ΔΔCt法计算基因的相对表达量。结果解读为qPCR结果验证了线粒体基因在8周胚胎中的表达水平显著高于7周和9周(n=3,P<0.05),MORC4、APLP2、DNMT1在9周造血干细胞中的表达水平显著低于7周和8周(n=3,P<0.05),与单细胞测序结果一致,证明了测序数据的可靠性。实验所用关键产品:Vazyme的HiScript II Q RT SuperMix for qPCR、AceQ Universal SYBR qPCR Master Mix,Bio-Rad的CFX96™ Real-Time PCR System,Sangon Biotech的qPCR引物。
4. Biomarker研究及发现成果解析
本研究中的Biomarker包括细胞类型特异性标记基因、调控细胞分化的关键信号分子及转录因子,通过数据库筛选、测序分析与实验验证的完整逻辑链条,明确了这些Biomarker的功能与临床意义。
Biomarker定位方面,细胞类型标记基因的筛选逻辑为“数据库参考→单细胞测序筛选→qPCR验证”,共鉴定了18种细胞簇的特异性标记基因;调控分化的信号分子与转录因子的筛选逻辑为“细胞通讯分析→转录组调控网络分析→功能富集验证”,明确了两条分化路径的关键调控因子。
研究过程详述:细胞类型标记基因来自7、8、9周人类胚胎的临床样本,通过单细胞RNA测序筛选得到各细胞簇的高表达基因,经qPCR验证其表达特异性;信号分子如COL1A2、NCAM1、CGA通过CellChat分析鉴定其配体-受体相互作用,其中COL1A2在间充质祖细胞中高表达,ITGA1+ITGB1在成骨细胞祖细胞中高表达,NCAM1在间充质祖细胞和神经干细胞中高表达;转录因子通过pySCENIC分析其活性,不同细胞簇的特异性转录因子活性具有显著差异(AUC值≥0.5)。特异性与敏感性方面,细胞标记基因在对应细胞簇中的表达水平显著高于其他细胞簇(logFC>0.25,P<0.05),关键信号通路的配体-受体相互作用具有高通讯概率(>0.1)。
核心成果提炼:该研究鉴定的Biomarker具有重要的功能关联:细胞类型标记基因可用于人类胚胎细胞的分选与富集,为体外诱导分化提供靶点;关键信号通路(COL1A2-(ITGA1+ITGB1)、NCAM1-FGFR1)参与细胞分化的调控,为理解人类胚胎发育机制提供了新的视角;特异性转录因子(HIC1、LMX1B、TWIST1)是细胞命运决定的关键调控因子,其异常表达可能与胚胎发育异常相关。创新性在于首次在人类7-9周胚胎中发现这些Biomarker的调控作用,填补了过渡阶段的研究空白;统计学结果显示,差异基因的表达变化具有显著统计学意义(n=3,P<0.05),GO富集分析的校正P值<0.05,证明了结果的可靠性。