1. 领域背景与文献引入
文献英文标题:HIV co-opts a cellular antiviral mechanism, activation of stress kinase PKR by its RNA, to enable splicing of rev/tat mRNA;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:HIV分子生物学、病毒-宿主相互作用
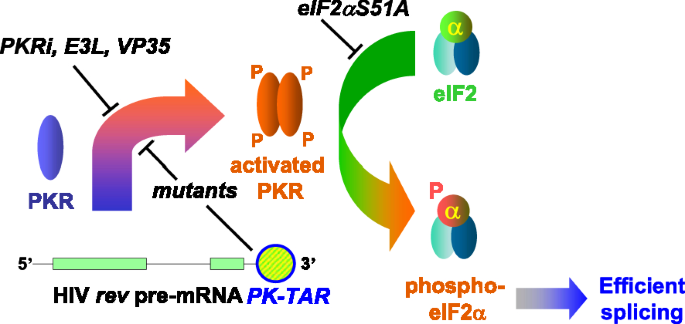
RNA依赖性蛋白激酶(PKR)是宿主先天免疫防御的核心分子,经典功能为识别病毒双链RNA后激活,通过磷酸化真核翻译起始因子2α(eIF2α)抑制宿主与病毒的蛋白质翻译,构成宿主抗病毒的关键防线(领域共识)。近年来研究拓展了PKR的功能边界,发现其可调控细胞内部分基因的mRNA剪接,如肿瘤坏死因子-α(TNF-α)、珠蛋白基因的高效剪接依赖PKR激活及eIF2α磷酸化,打破了PKR仅参与翻译调控的认知。当前病毒-宿主相互作用领域的研究热点集中于病毒编码PKR拮抗剂实现免疫逃逸的机制,但关于病毒是否主动利用PKR非经典功能促进自身复制的研究仍为空白。本研究针对这一认知缺口,探索HIV对PKR剪接调控功能的利用机制,其学术价值在于首次揭示病毒劫持宿主抗病毒机制实现自身RNA加工的新范式,为HIV治疗靶点开发提供全新方向。
2. 文献综述解析
作者以PKR功能的演化逻辑为综述主线,从经典抗病毒功能过渡到非经典的细胞基因剪接调控功能,进而提出病毒是否利用该机制的科学问题。
现有研究主要聚焦于PKR的经典抗病毒作用,明确了PKR通过eIF2α磷酸化抑制病毒翻译的分子机制,同时发现多种病毒编码PKR拮抗剂(如痘苗病毒E3L、埃博拉病毒VP35),通过结合PKR或其激活RNA元件阻断PKR激活,实现免疫逃逸;这些研究的优势在于清晰阐释了宿主抗病毒与病毒逃逸的双向博弈,但局限性在于仅关注PKR对病毒的抑制作用,未涉及PKR对病毒RNA加工的调控,也未考虑病毒利用PKR非经典功能的可能性。此外,现有研究已证实细胞内部分基因的剪接依赖PKR激活,但未延伸至病毒基因的调控。本文的创新价值在于突破传统认知,首次发现HIV并非被动逃逸PKR,而是主动利用PKR激活机制促进自身rev/tat mRNA剪接,将PKR的功能研究从宿主细胞拓展至病毒-宿主相互作用的新维度,为病毒利用宿主因子的研究提供了新视角。
3. 研究思路总结与详细解析
本研究的核心目标是明确HIV rev/tat mRNA剪接是否依赖PKR激活及eIF2α磷酸化,核心科学问题是HIV通过何种RNA元件介导PKR激活以促进剪接,技术路线遵循“现象观察→简化模型验证→分子机制解析→功能元件鉴定→保守性验证”的闭环逻辑。
3.1 PKR激活对HIV mRNA表达的调控验证
实验目的:验证PKR激活是否参与HIV各类mRNA的产生过程,排除TAR元件的潜在干扰。
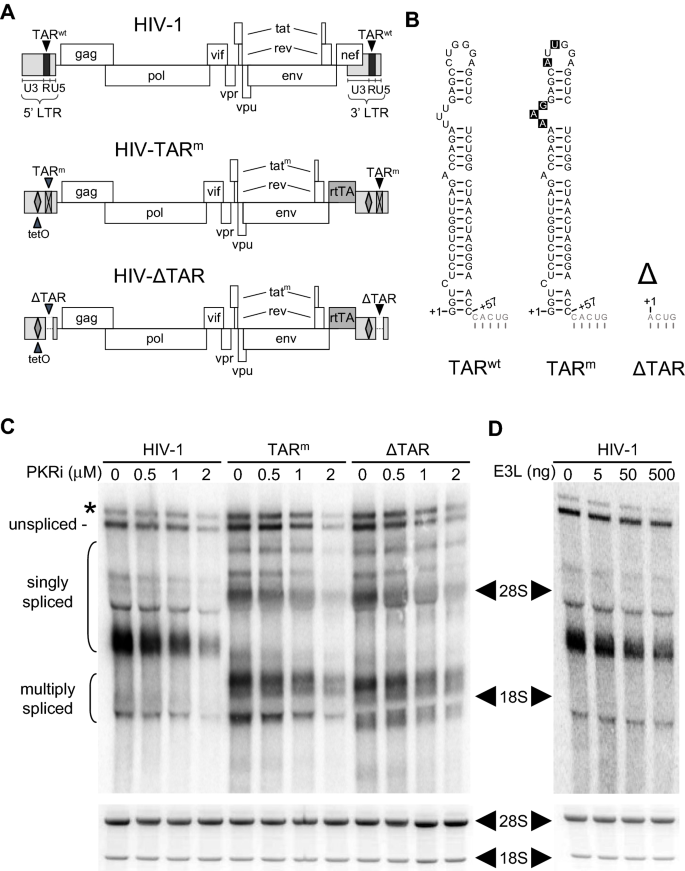
方法细节:采用人胚胎肾(HEK-293T)细胞转染野生型HIV-1全基因组载体(LAI株)、TAR突变体载体(TARm)及TAR缺失载体(ΔTAR),分别加入不同剂量的PKR小分子抑制剂(PKRi)或共表达痘苗病毒PKR拮抗剂E3L,转染后48小时提取总RNA,通过Northern blot检测未剪接(~9kb)、单次剪接(~4kb)及多次剪接(~2kb)mRNA的水平。
结果解读:Northern blot结果显示,PKRi以剂量依赖性方式抑制所有HIV mRNA的产生,共表达E3L也呈现类似的抑制效果;即使TAR元件缺失(ΔTAR载体),HIV mRNA的产生仍对PKRi敏感,说明除TAR外,HIV基因组中存在其他激活PKR的RNA元件。
产品关联:实验所用关键产品:Lipofectamine 2000(Thermo Fisher Scientific)、RNeasy总RNA提取试剂盒(QIAGEN)、High Prime DNA标记试剂盒(Roche Diagnostics)、PhosphorImager(Amersham Biosciences)等。
3.2 简化模型下PKR对rev/tat剪接的直接调控验证
实验目的:排除Tat和Rev蛋白的干扰,直接验证PKR激活对rev/tat mRNA剪接的调控作用。
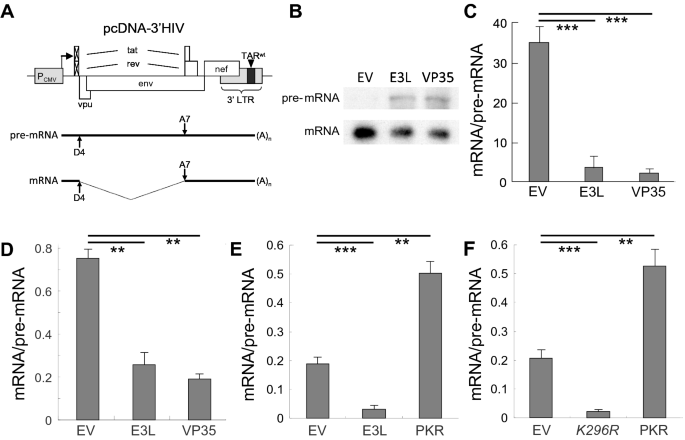
方法细节:构建仅包含HIV-1 3"端基因组的载体(pcDNA-3"HIV),该载体起始于rev和tat的AUG下游,无法表达功能性Tat和Rev,仅保留rev/tat内含子的剪接供体和受体位点;采用幼仓鼠肾(BHK-21)细胞共转染该载体与PKR拮抗剂(E3L、VP35)、野生型PKR或PKR显性负突变体(K296R),转染后12-18小时提取总RNA,通过核糖核酸酶(RNase)保护分析和实时荧光定量聚合酶链反应(qRT-PCR)检测剪接效率(mRNA/前体mRNA比值)。
结果解读:RNase保护分析和qRT-PCR结果均显示,共表达E3L或VP35显著降低rev/tat剪接效率,而过表达野生型PKR则显著提升剪接效率;表达K296R突变体完全阻断剪接,证实PKR激活是rev/tat mRNA剪接的必要条件。
产品关联:实验所用关键产品:Turbofect转染试剂(Fermentas)、TRIZOL总RNA提取试剂(Invitrogen)、Verso RT-PCR试剂盒(ABgene)、Rotor-Gene 6000实时荧光定量PCR仪(Corbett Life Science)等。
3.3 eIF2α磷酸化在剪接中的必要性验证
实验目的:明确PKR下游的eIF2α磷酸化是否为rev/tat剪接的关键调控节点。
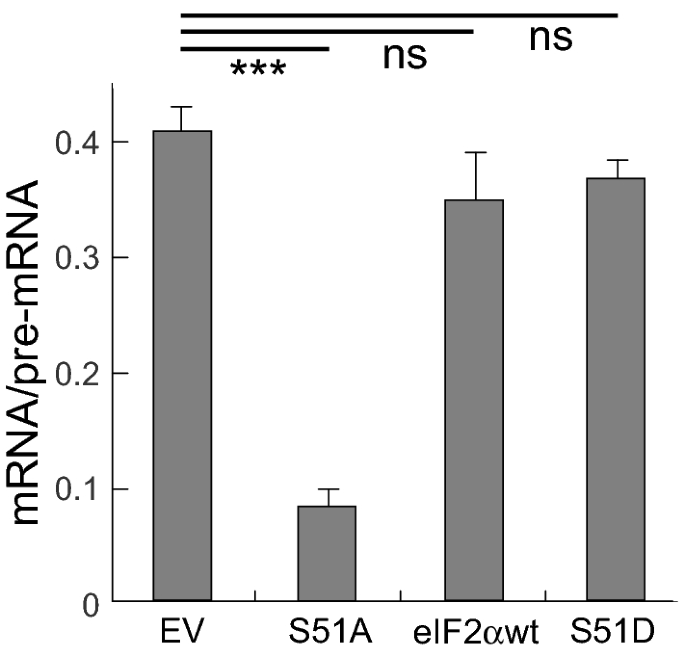
方法细节:采用BHK-21细胞共转染pcDNA-3"HIV载体与非磷酸化突变体eIF2αS51A、野生型eIF2α、磷酸化模拟突变体eIF2αS51D的表达载体,转染后20小时提取总RNA,通过qRT-PCR检测剪接效率。
结果解读:qRT-PCR结果显示,共表达eIF2αS51A突变体显著降低剪接效率,而野生型eIF2α对剪接无明显影响;eIF2αS51D突变体对剪接效率无显著影响,说明只有真实的eIF2α磷酸化而非模拟磷酸化状态才能支持剪接,证实eIF2α磷酸化是PKR调控剪接的关键下游事件。
产品关联:文献未提及具体实验产品,领域常规使用真核表达载体、qRT-PCR相关试剂等。
3.4 HIV RNA中PKR激活元件的鉴定与功能验证
实验目的:鉴定HIV-1 3"端RNA中激活PKR的功能性元件,并验证其对剪接的调控作用。
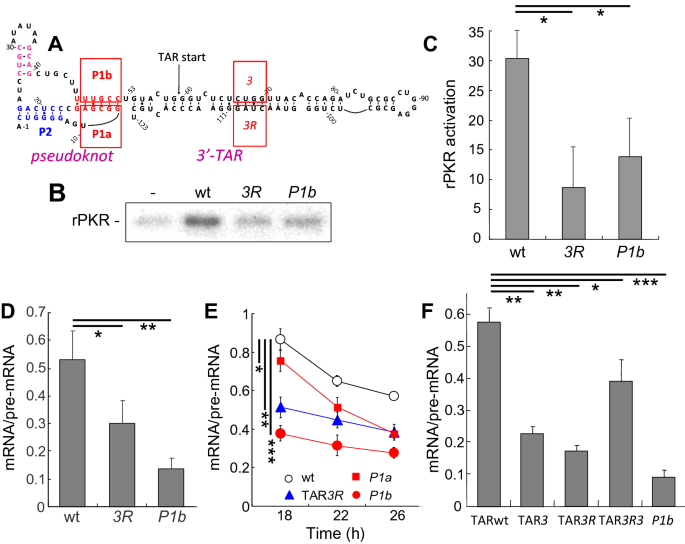
方法细节:首先通过生物信息学分析预测HIV-1 3"端TAR上游的RNA假结结构,然后构建TAR突变体(TAR3R)和假结突变体(P1b、P1a),通过体外重组PKR激活实验检测RNA元件对PKR磷酸化的影响,同时将突变体导入pcDNA-3"HIV载体,通过qRT-PCR检测剪接效率的变化;此外构建TAR互补突变体(TAR3R3)验证TAR的功能互补性。
结果解读:体外实验显示,TAR3R和P1b突变均显著降低PKR磷酸化水平,其中P1b突变的抑制作用更显著;细胞内实验显示,P1b突变对剪接效率的抑制作用强于TAR3R突变,TAR3R3互补突变体可部分恢复剪接效率,说明假结与TAR协同激活PKR,且假结的作用更关键。
产品关联:实验所用关键产品:重组PKR蛋白(原核表达纯化)、T7转录试剂盒(Promega)、SDS-聚丙烯酰胺凝胶电泳相关试剂等。
3.5 RNA元件的保守性分析
实验目的:验证PKR激活元件在HIV及相关慢病毒中的进化保守性,明确其功能的重要性。
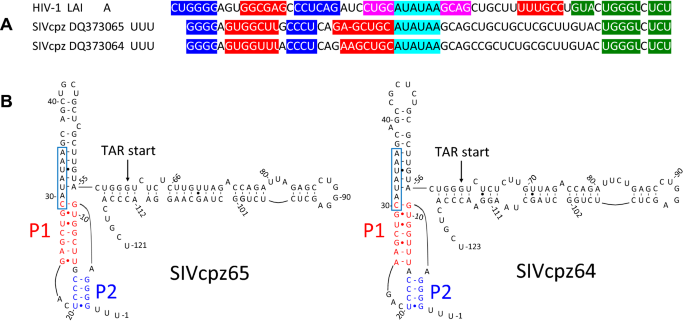
方法细节:通过Los Alamos HIV数据库获取HIV-1 M组各亚型的序列,以及黑猩猩免疫缺陷病毒(SIVcpz)的序列,采用PknotsRG工具分析RNA假结结构的保守性,通过序列比对验证假结茎区的碱基配对保守性。
结果解读:序列比对结果显示,HIV-1 M组各亚型的假结茎区(P1、P2)高度保守,即使碱基发生突变也维持碱基配对能力;SIVcpz的序列也可形成类似的假结结构,说明该元件在慢病毒进化中具有重要功能,是病毒复制所必需的。
产品关联:实验所用关键产品:生物信息学分析工具PknotsRG、Los Alamos HIV数据库序列资源等。

4. Biomarker研究及发现成果
本研究鉴定的功能性Biomarker为HIV-1 3"端TAR上游的保守RNA假结结构,属于病毒RNA的功能性调控元件,其筛选与验证遵循“现象推测→生物信息学预测→功能实验验证→进化保守性分析”的完整逻辑链。
Biomarker定位
该Biomarker为RNA二级结构元件,存在于HIV-1及SIVcpz的3"端基因组RNA中,筛选逻辑是先通过全基因组实验发现TAR缺失后HIV mRNA仍依赖PKR激活,进而通过生物信息学分析预测潜在的PKR激活RNA结构,再通过突变实验验证其激活PKR和促进剪接的功能,最后通过序列比对验证其在慢病毒中的保守性。
研究过程详述
该Biomarker来源于HIV-1 3"端基因组RNA,验证方法包括体外重组PKR激活实验和细胞内剪接功能实验,体外实验显示假结突变体(P1b)使PKR磷酸化水平降低约70%(n=3,P<0.001),细胞内实验显示P1b突变使剪接效率降低约85%(n=3,P<0.001),其对PKR激活和剪接的调控作用强于TAR元件;特异性方面,该假结结构仅存在于HIV及相关慢病毒中,且茎区碱基配对高度保守;敏感性方面,单个碱基对的突变即可显著降低其功能。
核心成果提炼
该假结结构与TAR协同激活PKR,通过eIF2α磷酸化促进rev/tat mRNA剪接,是HIV利用宿主机制的关键元件;其创新性在于首次发现病毒利用宿主抗病毒机制促进自身RNA加工,突破了病毒仅被动逃逸宿主免疫的认知;该元件在不同HIV亚型及SIVcpz中高度保守(序列一致性>90%),说明其在病毒复制中具有不可或缺的功能,为开发靶向RNA结构的HIV治疗药物提供了精准靶点。