1. 领域背景与文献引入
文献英文标题:Mechanism of hERG inhibition by gating-modifier toxin, APETx1, deduced by functional characterization;发表期刊:BMC Molecular and Cell Biology;影响因子:未公开;研究领域:电压门控钾通道与毒素相互作用机制
人类ether-à-go-go相关基因钾通道(hERG,Kv11.1)是一类关键的电压门控钾通道,主要表达于心肌细胞,介导动作电位复极化过程中的快速延迟整流钾电流(IKr),其功能异常会导致长QT综合征,进而引发致命性心律失常。近年来研究还发现,hERG通道与精神分裂症的发病风险、肿瘤细胞的增殖与转移密切相关,因此针对hERG通道的特异性配体开发具有重要的临床价值。
现有研究中,海葵毒素APETx1是一种典型的门控修饰毒素,通过结合hERG通道的电压传感结构域(VSD)并稳定其静息态(S4-down构象),从而抑制通道的电压依赖性激活。此前的半胱氨酸扫描分析已鉴定出hERG通道S3-S4区域的两个残基参与APETx1的结合,但由于只能依赖天然APETx1产物,无法对APETx1进行定点突变分析,因此APETx1与hERG静息态VSD的相互作用位点、具体结合方式及抑制机制仍不明确,这一空白限制了基于APETx1结构的hERG特异性配体的设计与开发。
本文旨在建立重组APETx1的高效制备方法,通过电生理实验结合定点突变技术,系统鉴定APETx1与hERG通道相互作用的关键残基,并构建符合实验结果的分子对接模型,从而解析APETx1抑制hERG通道的分子机制。
2. 文献综述解析
作者围绕hERG通道的结构功能、APETx1的抑制效应及现有研究局限三个维度展开综述,明确了当前领域的研究进展与未解决的核心问题。
现有研究可分为三类:第一类是hERG通道的生理病理功能与结构解析,已明确hERG通道在心肌电生理、精神疾病及肿瘤中的关键作用,且通过冷冻电镜技术解析了hERG通道的S4-up激活态结构,但静息态(S4-down)结构因技术限制尚未解析;第二类是APETx1作为hERG抑制剂的功能研究,已证实APETx1通过稳定hERG静息态发挥抑制作用,且半胱氨酸扫描分析鉴定了hERG通道上的部分结合残基;第三类是门控修饰毒素与电压门控离子通道的相互作用机制研究,已明确毒素主要结合通道VSD的胞外区域,但针对APETx1与hERG的具体相互作用位点仍缺乏系统研究。
现有研究的优势在于奠定了hERG通道的生理病理基础及APETx1的抑制效应框架,局限性主要体现在:无法获得重组APETx1以开展突变分析,导致APETx1上的关键结合残基未知;缺乏hERG静息态结构,无法明确APETx1与静息态VSD的结合方式;未构建符合实验数据的分子对接模型,难以从结构层面解析抑制机制。
本文的创新价值在于:首次建立了重组APETx1的制备与纯化方法,突破了天然产物的限制;通过定点突变结合电生理实验,系统鉴定了APETx1与hERG通道相互作用的关键残基,填补了APETx1结合位点的空白;构建了首个符合实验结果的APETx1-hERG静息态VSD对接模型,为解析门控修饰毒素的抑制机制提供了结构基础。
3. 研究思路总结与详细解析
本文的研究目标是解析APETx1抑制hERG通道的分子机制,核心科学问题是APETx1与hERG静息态VSD的相互作用位点及结合方式,技术路线遵循“重组蛋白制备→结构功能验证→突变体筛选→关键残基鉴定→对接模型构建”的闭环逻辑,通过多技术手段的整合实现研究目标。
3.1 重组APETx1的制备与结构功能验证
实验目的:获得可用于定点突变分析的重组APETx1蛋白,并验证其与天然产物的结构和功能一致性。
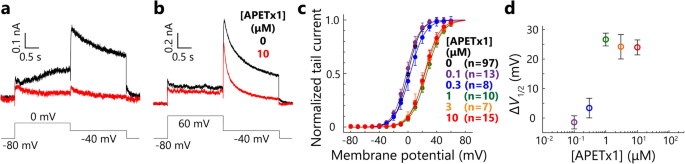
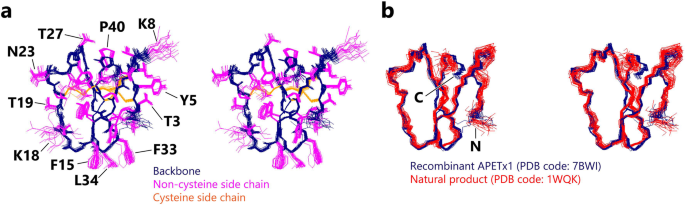
方法细节:采用大肠杆菌原核表达系统,将APETx1基因与His标签及烟草蚀病毒(TEV)酶切位点融合,转化至C41(λDE3)菌株中诱导表达,蛋白以包涵体形式存在;经尿素溶解包涵体后,通过镍亲和层析纯化,再通过透析复性形成三对分子内二硫键;用TEV酶切去除His标签,反相高效液相色谱(HPLC)进一步纯化,最终通过基质辅助激光解吸电离飞行时间质谱(MALDI-TOF MS)鉴定分子量;采用核磁共振(NMR)光谱技术分析重组APETx1的结构,并与天然产物的NMR数据对比;分别采用全细胞膜片钳(HEK293-hERG细胞系)和双电极电压钳(非洲爪蟾卵母细胞)记录hERG电流,分析重组APETx1的浓度依赖性抑制效应。
结果解读:MALDI-TOF MS结果显示,重组APETx1的分子量约为4551 Da,与天然产物一致;NMR化学位移分析表明,重组APETx1的结构与天然产物完全相同;电生理实验结果显示,重组APETx1以剂量依赖方式使hERG通道的半最大激活电压(V1/2)向正电位偏移,10 μM浓度下ΔV1/2为23.9±2.5 mV(n=8,P<0.05);基于双电极电压钳数据拟合得到的解离常数(Kd)在0.23 μM至1.7 μM之间,与天然产物的抑制活性一致。
产品关联:实验所用关键产品:SB Drug Discovery Limited的SB-HEK-hERG稳定细胞系;Bruker Avance系列NMR光谱仪;Nanion SyncroPatch 384PE自动化膜片钳系统;岛津MALDI-8020质谱仪;Sigma HIS-Select® Nickel Affinity Gel;Waters Sep-Pak® C18纯化柱;YMC ODS-AM反相HPLC柱。
3.2 APETx1突变体的功能分析与关键残基鉴定
实验目的:系统鉴定APETx1蛋白中参与hERG通道抑制的关键残基。
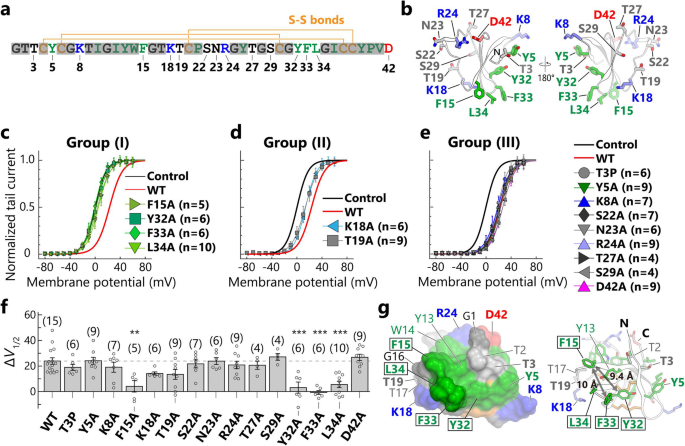
方法细节:基于APETx1的表面暴露残基,选择15个候选残基进行定点突变,其中T3突变为脯氨酸(对应天然突变体APETx3),其余残基突变为丙氨酸;采用NMR光谱验证突变体的结构与野生型APETx1的一致性;采用自动化膜片钳记录HEK293-hERG细胞的电流,分析10 μM浓度下各突变体处理后的ΔV1/2变化,通过单因素方差分析(ANOVA)结合Tukey检验进行统计学分析。
结果解读:NMR分析显示,所有突变体的结构与野生型APETx1无显著差异;电生理实验结果显示,F15A、Y32A、F33A、L34A突变体的ΔV1/2显著降低(与野生型相比,n=5-12,P<0.001),其中F15A突变体ΔV1/2降至约5 mV,表明这些疏水残基是APETx1与hERG相互作用的关键位点;K18A、T19A突变体的ΔV1/2呈下降趋势但无统计学差异;其余突变体的ΔV1/2与野生型无显著差异;重组APETx3(T3P)的ΔV1/2与野生型相近,表明T3残基不参与hERG通道的抑制。
产品关联:实验所用关键产品:Takara In-Fusion HD定点突变试剂盒;TEV蛋白酶;Bruker Avance NMR光谱仪;Nanion SyncroPatch 384PE自动化膜片钳系统。
3.3 hERG通道突变体的功能分析与关键残基鉴定
实验目的:鉴定hERG通道VSD区域中与APETx1相互作用的关键残基。
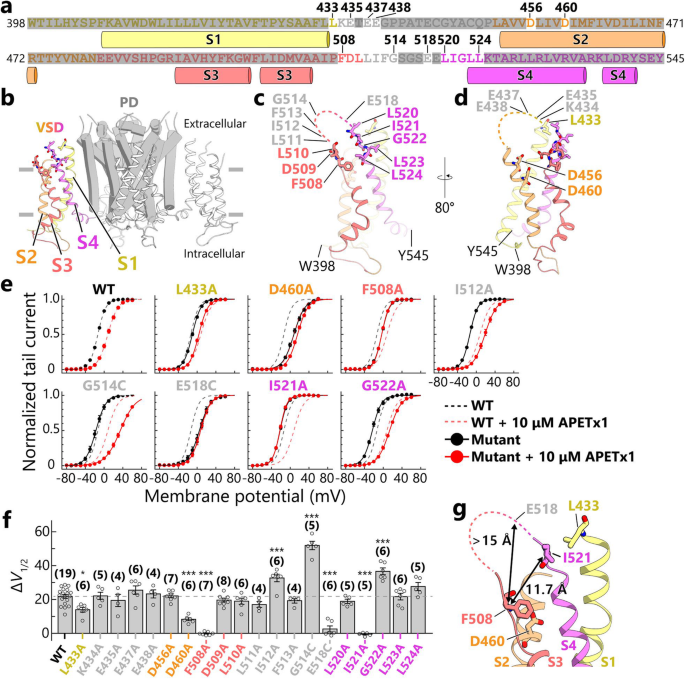
方法细节:针对hERG通道VSD的S1-S2区域(L433、D460)和S3-S4区域(F508、I512、G514、E518、I521、G522等)构建定点突变体,通过体外转录获得互补RNA(cRNA)并注射至非洲爪蟾卵母细胞中表达;采用双电极电压钳记录卵母细胞的hERG电流,分析10 μM APETx1处理后的ΔV1/2变化,进行统计学分析。
结果解读:所有突变体均能正常表达并产生典型的hERG钩状尾电流,表明突变未改变通道的整体结构;电生理实验结果显示,F508A、I521A、E518C突变体的ΔV1/2显著降低(与野生型相比,n=4-9,P<0.001),其中E518C突变体ΔV1/2降至约8 mV,表明这些残基是APETx1的关键结合位点;I512A、G514C、G522A突变体的ΔV1/2显著升高,提示这些残基的突变消除了空间位阻或优化了结合表面,增强了APETx1的结合亲和力;L433A、D460A突变体的ΔV1/2也显著降低,表明S1-S2区域也参与APETx1与hERG的相互作用。
产品关联:实验所用关键产品:Ambion mMessage mMachine SP6转录试剂盒;Warner OC-725C双电极电压钳放大器;Molecular Devices Digidata 1440A AD-DA转换器;pCLAMP 10.7电生理记录软件。
3.4 APETx1-hERG VSD对接模型的构建与验证
实验目的:构建符合突变分析结果的APETx1与hERG静息态VSD的分子对接模型,解析两者的结合方式。
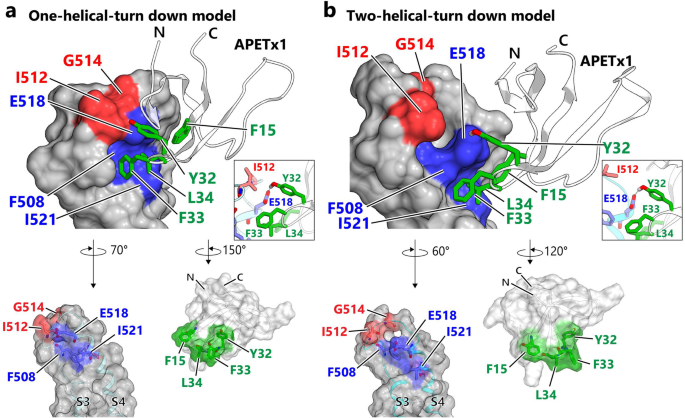
方法细节:以大鼠EAG1通道的冷冻电镜结构为模板,采用MODELLER 9.23构建hERG VSD的S4-up激活态、S4-down(1个螺旋转角下移、2个螺旋转角下移)静息态同源模型;基于突变分析鉴定的关键残基,设置距离约束(APETx1的F15/Y32/F33/L34与hERG的F508/E518/I521的Cβ原子距离≤3.0 Å)及氢键约束(APETx1 Y32与hERG E518),采用HADDOCK2.4服务器进行分子对接;分析对接模型的合理性,并结合突变实验结果进行验证。
结果解读:S4-down静息态模型中,hERG的F508、E518、I521残基形成一个疏水凹槽,与APETx1的四个疏水残基(F15、Y32、F33、L34)的分布高度互补;对接模型显示,APETx1的疏水残基嵌入hERG的凹槽中,Y32与E518形成氢键,疏水相互作用与氢键共同介导两者的结合;I512A突变消除了对APETx1结合的空间位阻,解释了该突变体抑制效应增强的原因;而S4-up激活态模型中,关键残基的分布无法与APETx1的关键残基互补,进一步支持APETx1优先结合hERG静息态的结论。
产品关联:实验所用关键产品:MODELLER 9.23同源建模软件;HADDOCK2.4 web对接服务器;CueMol分子图形可视化软件。
4. Biomarker研究及发现成果解析
本文中的Biomarker为APETx1与hERG通道相互作用的关键功能残基,作为hERG通道抑制机制的核心分子靶点,其筛选与验证遵循“表面残基选择→定点突变→电生理验证→模型构建”的完整逻辑链条。
Biomarker定位:涉及的Biomarker分为两类,一类是APETx1上的关键残基(F15、Y32、F33、L34),另一类是hERG通道上的关键残基(F508、E518、I521、L433、D460),筛选逻辑为:基于蛋白表面暴露残基选择候选位点,通过定点突变结合电生理实验,筛选ΔV1/2发生显著变化的残基,再通过分子对接模型验证其相互作用。
研究过程详述:APETx1的关键残基来自重组蛋白的定点突变体,hERG的关键残基来自细胞系及卵母细胞表达的突变体;验证方法为全细胞膜片钳和双电极电压钳记录,通过测定ΔV1/2的变化评估残基的重要性;统计学结果显示,关键残基突变体的ΔV1/2与野生型相比差异显著(P<0.001),其中APETx1的F15A突变体ΔV1/2降至约5 mV,hERG的E518C突变体ΔV1/2降至约8 mV,表明这些残基是相互作用的核心位点。
核心成果提炼:首次鉴定了APETx1与hERG通道相互作用的关键疏水残基和极性残基,明确了疏水相互作用与氢键是介导结合的主要作用力;构建了首个符合实验结果的APETx1-hERG静息态VSD对接模型,揭示了APETx1通过嵌入hERG VSD的疏水凹槽稳定静息态的抑制机制;该成果为设计靶向hERG VSD的新型特异性配体提供了结构基础,具有重要的药物开发价值;其中hERG的E518残基作为极性相互作用位点,其突变导致APETx1结合亲和力显著降低(P<0.001),可作为后续配体设计的关键靶点。
