1. 领域背景与文献引入
文献英文标题:mTOR direct interactions with Rheb-GTPase and raptor: sub-cellular localization using fluorescence lifetime imaging;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:细胞信号转导(哺乳动物雷帕霉素靶蛋白通路)。
哺乳动物雷帕霉素靶蛋白通路是调控细胞生长、增殖、代谢及自噬等核心生物学过程的关键信号通路,2002年哺乳动物雷帕霉素靶蛋白复合物1(mTORC1)和哺乳动物雷帕霉素靶蛋白复合物2(mTORC2)的鉴定是领域发展的关键节点,为通路的功能分区调控研究奠定了基础。当前领域研究热点聚焦于复合物的动态组装机制、亚细胞定位对功能的调控作用,以及外界信号(如营养状态、药物)对通路的调控模式,但仍存在多个未解决的核心问题:一是脑富集Ras同源蛋白(Rheb)作为哺乳动物雷帕霉素靶蛋白复合物1的上游调控因子,与哺乳动物雷帕霉素靶蛋白的直接相互作用仅通过细胞裂解液实验间接推测,活细胞内的直接证据缺失;二是此前研究认为脑富集Ras同源蛋白仅定位于细胞质,其是否存在核定位及核内功能尚不明确;三是雷帕霉素对哺乳动物雷帕霉素靶蛋白与哺乳动物雷帕霉素靶蛋白调节相关蛋白(raptor)相互作用的影响存在争议,部分研究认为雷帕霉素会解离两者结合,而另一部分研究未观察到该效应。
针对上述研究空白,本研究采用荧光共振能量转移-荧光寿命成像(FRET-FLIM)技术,在活细胞中实时检测哺乳动物雷帕霉素靶蛋白与脑富集Ras同源蛋白、哺乳动物雷帕霉素靶蛋白调节相关蛋白的直接相互作用,并系统分析三者的亚细胞定位特征,同时探究氨基酸饥饿、雷帕霉素处理对相互作用的影响,为哺乳动物雷帕霉素靶蛋白通路的调控机制提供直接的活细胞实验证据,弥补了传统生化方法无法实时、原位研究蛋白相互作用的局限性。
2. 文献综述解析
本文献综述部分以哺乳动物雷帕霉素靶蛋白复合物的分子相互作用网络为核心分类维度,从脑富集Ras同源蛋白与哺乳动物雷帕霉素靶蛋白的调控关系、哺乳动物雷帕霉素靶蛋白与哺乳动物雷帕霉素靶蛋白调节相关蛋白的复合物组装、现有研究方法的局限性三个层面展开评述,明确领域内的研究进展与未解决问题。
现有研究的关键结论显示,脑富集Ras同源蛋白是哺乳动物雷帕霉素靶蛋白复合物1通路的上游激活因子,通过结合哺乳动物雷帕霉素靶蛋白的催化结构域调控其激酶活性;哺乳动物雷帕霉素靶蛋白调节相关蛋白作为哺乳动物雷帕霉素靶蛋白复合物1的核心支架蛋白,负责招募下游底物并介导哺乳动物雷帕霉素靶蛋白的催化功能。技术方法层面,传统的免疫共沉淀、pull-down等生化方法能够鉴定蛋白间的相互作用关系,但其优势仅在于批量分析细胞裂解液中的蛋白复合物,局限性在于无法在活细胞中实时观察相互作用的动态变化,且实验过程中的细胞裂解、蛋白纯化步骤可能引入非特异性结合的人工假象,无法区分直接相互作用与间接相互作用;同时,传统成像技术的灵敏度不足,难以检测到低丰度的核内蛋白定位。
通过对比现有研究的缺陷,本研究的创新价值凸显为三个方面:一是首次在活细胞中直接证实哺乳动物雷帕霉素靶蛋白与脑富集Ras同源蛋白、哺乳动物雷帕霉素靶蛋白调节相关蛋白的物理相互作用,解决了长期以来仅通过间接实验推测相互作用的问题;二是首次发现脑富集Ras同源蛋白在细胞核内的定位,拓展了对脑富集Ras同源蛋白亚细胞分布及功能的认知;三是采用荧光共振能量转移-荧光寿命成像技术实现了亚细胞水平的相互作用分析,能够区分细胞质与细胞核中相互作用的差异,为哺乳动物雷帕霉素靶蛋白通路的区域化调控提供了新的研究视角。
3. 研究思路总结与详细解析
本研究的整体研究目标是在活细胞中验证哺乳动物雷帕霉素靶蛋白与脑富集Ras同源蛋白、哺乳动物雷帕霉素靶蛋白调节相关蛋白的直接相互作用,明确三者的亚细胞定位特征,并探究营养状态(氨基酸饥饿)与雷帕霉素处理对这些相互作用的调控机制;核心科学问题包括脑富集Ras同源蛋白是否与哺乳动物雷帕霉素靶蛋白存在直接物理相互作用、脑富集Ras同源蛋白是否存在核定位、雷帕霉素及氨基酸饥饿如何影响哺乳动物雷帕霉素靶蛋白复合物的组装;技术路线遵循“载体构建与功能验证→亚细胞定位观察→活细胞相互作用检测→处理因素效应分析”的闭环逻辑,采用荧光共振能量转移-荧光寿命成像技术作为核心检测手段。
3.1 荧光标记蛋白载体构建与功能验证
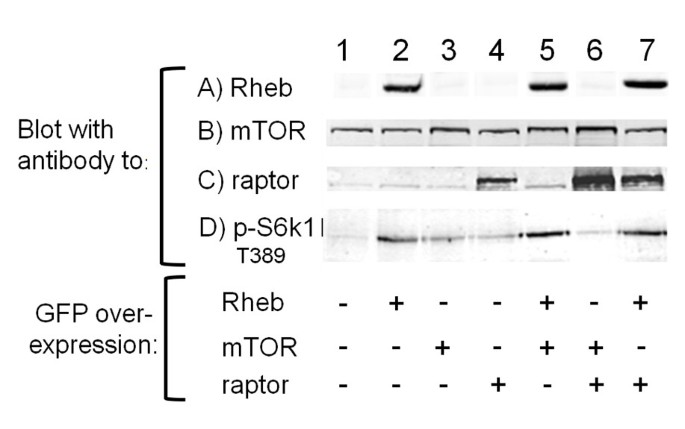
本环节的实验目的是构建带有增强型绿色荧光蛋白(EGFP)或红色荧光蛋白(DsRed)标记的脑富集Ras同源蛋白、哺乳动物雷帕霉素靶蛋白、哺乳动物雷帕霉素靶蛋白调节相关蛋白表达载体,并验证标记蛋白的生物学功能是否与内源性蛋白一致。方法细节上,研究人员通过PCR扩增目的基因的编码序列,分别构建N端标记增强型绿色荧光蛋白的脑富集Ras同源蛋白、哺乳动物雷帕霉素靶蛋白载体,以及N端标记红色荧光蛋白的脑富集Ras同源蛋白、哺乳动物雷帕霉素靶蛋白调节相关蛋白载体,同时构建C端标记增强型绿色荧光蛋白的哺乳动物雷帕霉素靶蛋白载体以排除标记位置对功能的影响;将载体转染至HEK293、HeLa、CHO细胞系,通过免疫印迹实验检测标记蛋白的表达水平,并通过检测哺乳动物雷帕霉素靶蛋白复合物1下游底物磷酸化S6激酶(Thr389)的活性验证标记蛋白的功能。结果解读显示,免疫印迹实验证实所有标记蛋白均正确表达,增强型绿色荧光蛋白标记的脑富集Ras同源蛋白转染后细胞中磷酸化S6激酶的水平显著升高(n=3,P<0.05),说明标记蛋白能够有效激活哺乳动物雷帕霉素靶蛋白复合物1通路,功能正常;增强型绿色荧光蛋白标记的哺乳动物雷帕霉素靶蛋白与红色荧光蛋白标记的哺乳动物雷帕霉素靶蛋白调节相关蛋白转染后也能维持通路活性,进一步验证了载体的功能性。产品关联:实验所用关键产品包括脑富集Ras同源蛋白抗体(Santa Cruz Biotechnology)、哺乳动物雷帕霉素靶蛋白抗体、哺乳动物雷帕霉素靶蛋白调节相关蛋白抗体及磷酸化S6激酶(Thr389)抗体(Cell Signalling Technology, Inc.),转染试剂为Fugene HD(Roche, UK),细胞器标记试剂内质网追踪红染料、BODIPY TR C5神经酰胺购自Invitrogen。
3.2 亚细胞定位观察
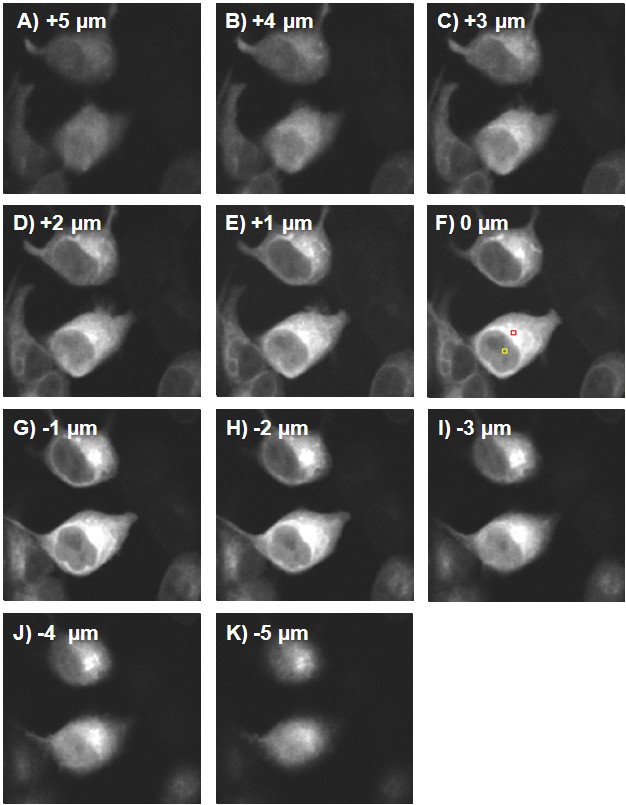
本环节的实验目的是明确脑富集Ras同源蛋白、哺乳动物雷帕霉素靶蛋白、哺乳动物雷帕霉素靶蛋白调节相关蛋白在活细胞中的亚细胞分布特征,尤其是脑富集Ras同源蛋白是否存在核定位。方法细节上,转染荧光标记蛋白后,采用共聚焦显微镜观察活细胞的荧光分布,通过多光子时间相关单光子计数(TCSPC)技术获取3D Z-stack成像以分析核内荧光信号;同时使用内质网追踪红染料标记内质网、BODIPY TR C5神经酰胺标记高尔基体,进行共定位分析;此外通过免疫荧光染色实验验证内源性脑富集Ras同源蛋白的定位。结果解读显示,脑富集Ras同源蛋白主要定位于胞质的高尔基体、内质网等核周区域,同时在细胞核内也存在显著的荧光信号,通过光子计数分析估算核内脑富集Ras同源蛋白的表达水平约为胞质的40%(n=3);哺乳动物雷帕霉素靶蛋白主要定位于胞质,核内有少量分布;哺乳动物雷帕霉素靶蛋白调节相关蛋白仅定位于胞质,未检测到核内信号;共定位实验证实脑富集Ras同源蛋白与内质网、高尔基体标记物存在共定位,说明其主要分布在膜性细胞器上。
3.3 荧光共振能量转移-荧光寿命成像检测哺乳动物雷帕霉素靶蛋白与脑富集Ras同源蛋白的直接相互作用
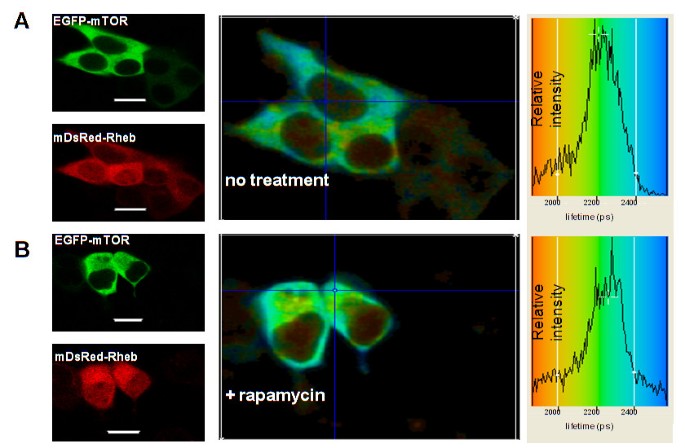
本环节的实验目的是在活细胞中验证哺乳动物雷帕霉素靶蛋白与脑富集Ras同源蛋白的直接物理相互作用,并探究雷帕霉素处理对该相互作用的影响。方法细节上,首先单独转染增强型绿色荧光蛋白标记的哺乳动物雷帕霉素靶蛋白,检测增强型绿色荧光蛋白的荧光寿命作为对照;然后共转染增强型绿色荧光蛋白标记的哺乳动物雷帕霉素靶蛋白与红色荧光蛋白标记的脑富集Ras同源蛋白,通过荧光寿命成像技术检测增强型绿色荧光蛋白的荧光寿命变化,若发生荧光共振能量转移则说明两者存在直接相互作用;设置雷帕霉素处理组(100 nM处理24h),对比处理前后的荧光寿命变化。结果解读显示,单独转染时增强型绿色荧光蛋白标记的哺乳动物雷帕霉素靶蛋白的平均荧光寿命约为2400±100 ps,共转染后胞质中增强型绿色荧光蛋白的寿命降至2200±50 ps,核内寿命降至2000±100 ps(n=3,P<0.01),说明哺乳动物雷帕霉素靶蛋白与脑富集Ras同源蛋白在胞质和细胞核内均存在直接相互作用,且核内的相互作用更为紧密;雷帕霉素处理后,增强型绿色荧光蛋白的荧光寿命无显著变化,说明雷帕霉素不影响两者的直接相互作用。
3.4 荧光共振能量转移-荧光寿命成像检测哺乳动物雷帕霉素靶蛋白与哺乳动物雷帕霉素靶蛋白调节相关蛋白的直接相互作用
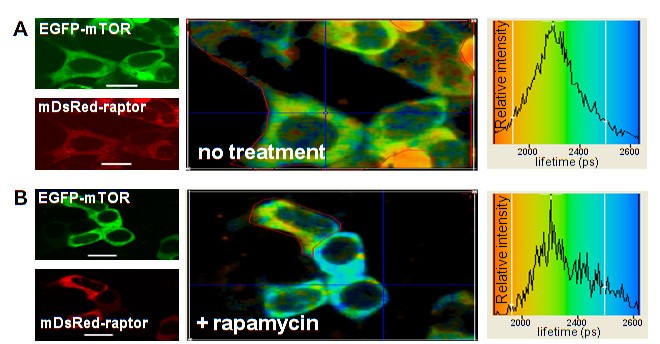
本环节的实验目的是验证哺乳动物雷帕霉素靶蛋白与哺乳动物雷帕霉素靶蛋白调节相关蛋白的直接相互作用,并探究雷帕霉素及脑富集Ras同源蛋白与哺乳动物雷帕霉素靶蛋白调节相关蛋白的相互作用关系。方法细节上,共转染增强型绿色荧光蛋白标记的哺乳动物雷帕霉素靶蛋白与红色荧光蛋白标记的哺乳动物雷帕霉素靶蛋白调节相关蛋白,检测增强型绿色荧光蛋白的荧光寿命;设置雷帕霉素处理组观察相互作用的变化;同时共转染增强型绿色荧光蛋白标记的脑富集Ras同源蛋白与红色荧光蛋白标记的哺乳动物雷帕霉素靶蛋白调节相关蛋白作为对照,检测是否存在荧光共振能量转移效应。结果解读显示,共转染哺乳动物雷帕霉素靶蛋白与哺乳动物雷帕霉素靶蛋白调节相关蛋白后,增强型绿色荧光蛋白的平均荧光寿命降至2300±100 ps(n=3,P<0.05),说明两者存在直接相互作用;雷帕霉素处理后荧光寿命无显著变化,说明雷帕霉素不影响两者的直接结合;而增强型绿色荧光蛋白标记的脑富集Ras同源蛋白与红色荧光蛋白标记的哺乳动物雷帕霉素靶蛋白调节相关蛋白共转染时,增强型绿色荧光蛋白的荧光寿命与单独转染时无差异,说明脑富集Ras同源蛋白与哺乳动物雷帕霉素靶蛋白调节相关蛋白之间不存在直接相互作用,信号需通过哺乳动物雷帕霉素靶蛋白传递至哺乳动物雷帕霉素靶蛋白调节相关蛋白。
3.5 氨基酸饥饿对哺乳动物雷帕霉素靶蛋白复合物相互作用的影响
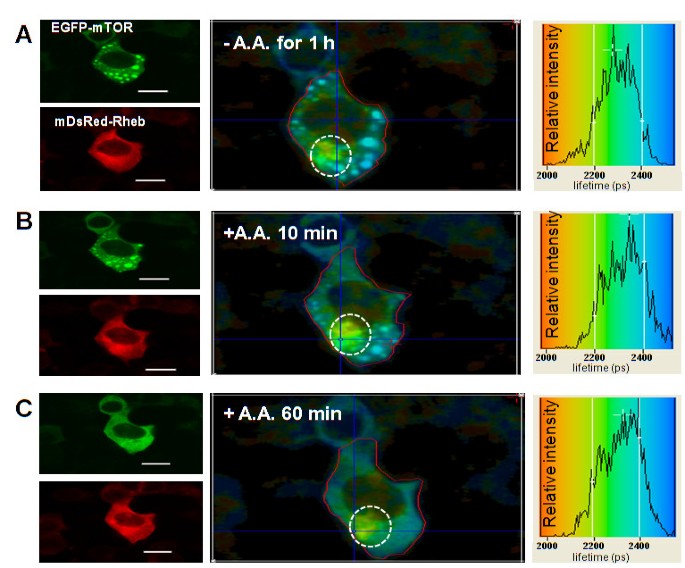
本环节的实验目的是探究营养状态(氨基酸饥饿)对哺乳动物雷帕霉素靶蛋白与脑富集Ras同源蛋白、哺乳动物雷帕霉素靶蛋白调节相关蛋白相互作用及亚细胞定位的影响。方法细节上,将转染后的细胞进行血清饥饿过夜后,再进行氨基酸饥饿1h,然后重新加入氨基酸,在不同时间点观察哺乳动物雷帕霉素靶蛋白的亚细胞定位变化,并通过荧光寿命成像检测荧光寿命的变化。结果解读显示,氨基酸饥饿后,哺乳动物雷帕霉素靶蛋白在胞质中形成点状结构,而脑富集Ras同源蛋白不与这些点状结构共定位;饥饿状态下,哺乳动物雷帕霉素靶蛋白与脑富集Ras同源蛋白在胞质中的相互作用减弱(增强型绿色荧光蛋白寿命升高至2100 ps左右),但在核周区域的相互作用仍维持稳定;哺乳动物雷帕霉素靶蛋白与哺乳动物雷帕霉素靶蛋白调节相关蛋白的相互作用在饥饿状态下仅略有减弱,表现为荧光寿命略有升高,重新加入氨基酸后,点状结构逐渐消失,相互作用恢复至正常水平。
4. Biomarker研究及发现成果
本文虽未聚焦于临床生物标志物的筛选,但发现了核定位的脑富集Ras同源蛋白这一潜在的哺乳动物雷帕霉素靶蛋白通路调控生物标志物,其为研究哺乳动物雷帕霉素靶蛋白通路的核内调控机制提供了新的靶点,同时也为哺乳动物雷帕霉素靶蛋白相关疾病的机制研究提供了新的方向。
该生物标志物的定位逻辑为:通过高灵敏度的多光子时间相关单光子计数荧光成像技术,在活细胞中检测到脑富集Ras同源蛋白的核内信号,随后通过荧光共振能量转移-荧光寿命成像技术验证其与核内哺乳动物雷帕霉素靶蛋白的直接相互作用,验证逻辑遵循“细胞系水平成像验证→亚细胞定位定量分析→相互作用功能验证”的完整链条。
该生物标志物的来源为转染荧光标记脑富集Ras同源蛋白的HEK293、HeLa、CHO活细胞,验证方法包括多光子3D成像、免疫荧光染色、荧光共振能量转移-荧光寿命成像相互作用检测;特异性方面,核内脑富集Ras同源蛋白的荧光信号强度约为胞质的40%(n=3),且与哺乳动物雷帕霉素靶蛋白在核内存在特异性的直接相互作用;敏感性方面,多光子时间相关单光子计数技术能够检测到低丰度的核内蛋白,避免了传统成像技术因灵敏度不足导致的信号丢失。
该生物标志物的功能关联在于,核定位的脑富集Ras同源蛋白与哺乳动物雷帕霉素靶蛋白的相互作用可能参与核内的核糖体生物发生过程(领域共识:哺乳动物雷帕霉素靶蛋白复合物1通路调控核糖体生物发生,而核糖体生物发生主要发生在细胞核内);创新性在于首次在活细胞中证实脑富集Ras同源蛋白的核定位及与核内哺乳动物雷帕霉素靶蛋白的直接相互作用,拓展了对脑富集Ras同源蛋白功能及哺乳动物雷帕霉素靶蛋白通路区域化调控的认知;由于本研究为细胞水平的机制研究,未涉及临床样本检测,因此无特异性、敏感性的临床数据及统计学风险比(HR)等指标。
