1. 领域背景与文献引入
文献英文标题:Genome-wide analysis of protein–protein interactions and involvement of viral proteins in SARS-CoV-2 replication;发表期刊:Cell & Bioscience;影响因子:未明确提供;研究领域:冠状病毒分子生物学、病毒复制机制与抗病毒药物靶点研究。
冠状病毒科β属成员是人类重要的呼吸道病原体,2003年严重急性呼吸综合征冠状病毒(SARS-CoV)、2012年中东呼吸综合征冠状病毒(MERS-CoV)及2019年新型冠状病毒(SARS-CoV-2)的爆发,对全球公共卫生造成重大威胁。领域共识:SARS-CoV-2作为单股正链RNA病毒,其复制依赖于病毒蛋白间的精密相互作用形成复制转录复合物(RTC),解析这些相互作用是阐明病毒复制机制、开发特异性抗病毒药物的核心基础。截至2021年,临床可用的抗SARS-CoV-2药物极为有限,仅瑞德西韦获FDA批准,但仅能缩短患者住院时间,且对重症患者疗效有限;疫苗虽能有效降低感染率,但存在抗体依赖增强(ADE)、免疫持续时间不足及突变株逃逸等问题。现有研究中,酵母双杂交(Y2H)、免疫沉淀结合质谱(IP-MS)是解析病毒蛋白相互作用的主要技术,但Y2H基于酵母细胞环境,可能漏检仅在哺乳动物细胞中发生的相互作用;IP-MS无法区分直接与间接相互作用,且对弱相互作用的检测敏感性不足。针对这一研究空白,本研究采用哺乳动物双杂交系统,对SARS-CoV-2的28个病毒蛋白进行全基因组范围的两两相互作用筛选,旨在构建更精准的病毒蛋白相互作用网络,并解析关键相互作用对病毒复制的调控机制。
2. 文献综述解析
作者对SARS-CoV-2蛋白相互作用领域的现有研究按技术方法(Y2H、IP-MS)与研究对象(病毒-病毒、病毒-宿主相互作用)进行分类评述,明确了现有研究的成果与局限性,为自身研究的创新定位提供了依据。
现有研究已通过Y2H和IP-MS技术发现了部分SARS-CoV-2病毒蛋白间的相互作用,证实了Nsp10与Nsp14、Nsp16等蛋白的保守相互作用在病毒复制中的关键功能。Y2H技术的优势在于能够检测蛋白间的直接相互作用,而IP-MS技术可实现大规模、无偏倚的相互作用筛选,但两类技术均存在明显局限性:Y2H的酵母细胞内环境与哺乳动物细胞差异显著,可能漏检仅在哺乳动物细胞中发生的特异性相互作用;IP-MS无法区分直接相互作用与间接相互作用,且对低丰度、弱结合的蛋白对检测敏感性不足。此外,现有研究尚未完全覆盖SARS-CoV-2所有病毒蛋白的两两相互作用组合,也未深入解析部分新发现相互作用的结构基础及对病毒复制的调控功能。本研究的创新价值在于,首次采用哺乳动物双杂交系统对28个病毒蛋白的784种组合进行系统性筛选,弥补了Y2H与IP-MS技术在细胞环境、相互作用类型区分上的不足,发现了14个未被报道的新相互作用,并聚焦Nsp3.1与N蛋白的相互作用,深入解析了其结构域及对病毒复制的调控作用,为抗病毒药物靶点开发提供了新的候选位点。
3. 研究思路总结与详细解析
本研究的整体研究目标是构建SARS-CoV-2全基因组病毒蛋白相互作用图谱,解析关键相互作用的结构基础及对病毒复制的调控机制;核心科学问题是SARS-CoV-2病毒蛋白间的相互作用网络如何调控病毒复制,尤其是N蛋白与复制转录复合物的关联机制;技术路线遵循“相互作用筛选→验证→结构解析→功能验证”的闭环逻辑,通过多层面实验明确了Nsp3.1与N蛋白相互作用的生物学功能。
3.1 哺乳动物双杂交系统构建与蛋白相互作用筛选
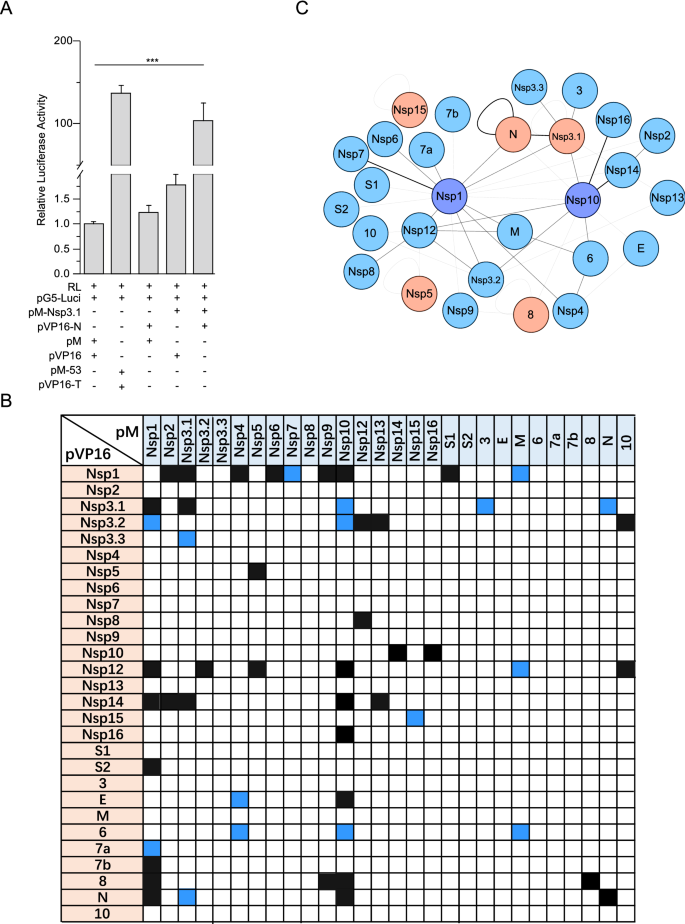
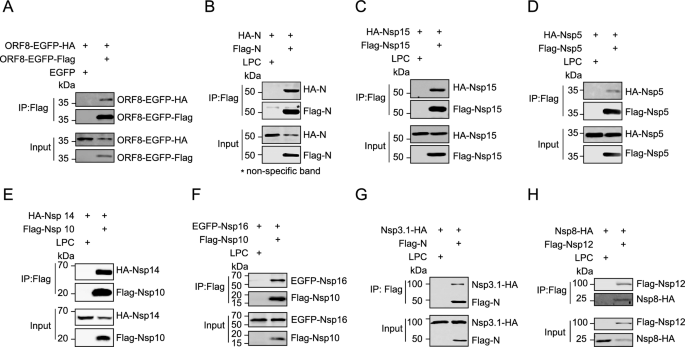
实验目的是全基因组范围筛选SARS-CoV-2病毒蛋白间的两两相互作用,构建完整的病毒蛋白相互作用网络。方法细节为:将SARS-CoV-2的28个病毒蛋白(其中Nsp3按功能域分为Nsp3.1、Nsp3.2、Nsp3.3三个截短体,S蛋白按弗林蛋白酶切割位点分为S1、S2)分别克隆到pM(结合域载体)和pVP16(激活域载体),在HEK293T细胞中进行两两共转染,同时转染pG5-Luci报告质粒和pRL-TK内参质粒,通过双荧光素酶报告系统检测相互作用,每个组合重复至少3次;采用免疫印迹(WB)验证载体中蛋白的表达,并用免疫共沉淀(Co-IP)验证部分阳性相互作用。结果解读:共检测到48个阳性相互作用,其中14个为未被报道的新相互作用;与SARS-CoV的Nsp1不同,SARS-CoV-2的Nsp1具有最多的相互作用伴侣(9个非结构蛋白和7个辅助蛋白),提示其作为病毒蛋白枢纽在复制复合物组装中的核心作用;5个自相互作用(ORF8、N、Nsp15、Nsp5、Nsp3)被确认,5个相互作用(Nsp1/Nsp3.1、Nsp3.1/N、Nsp3.2/Nsp12、Nsp10/Nsp14、Nsp10/Nsp16)为双向阳性;通过Cytoscape软件构建的相互作用网络显示,Nsp1和Nsp10是关键的枢纽蛋白,Co-IP实验进一步验证了包括Nsp3.1-N在内的多个相互作用的真实性。产品关联:文献未提及具体实验产品,领域常规使用双荧光素酶检测试剂盒、免疫沉淀琼脂糖珠、Flag/HA标签抗体等试剂。
3.2 N蛋白与Nsp3.1相互作用的结构域解析
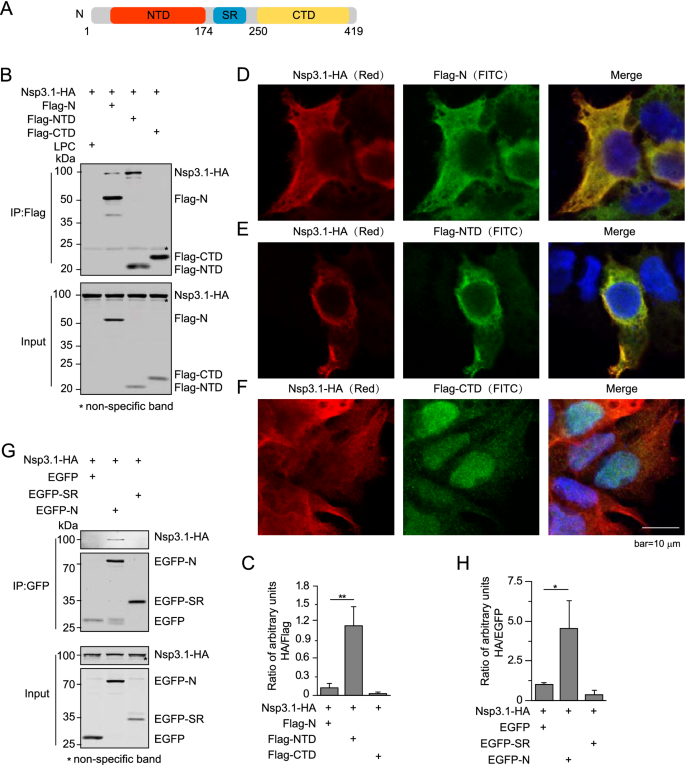
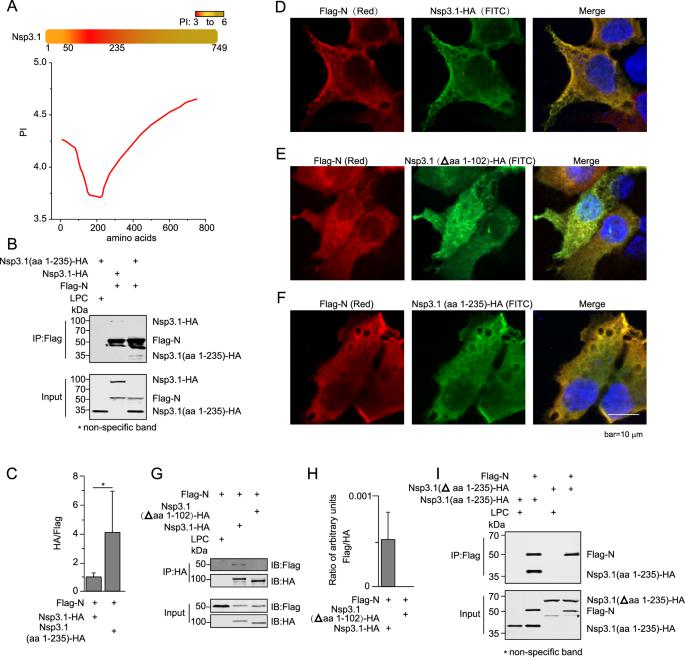
实验目的是确定N蛋白与Nsp3.1相互作用的关键结构域,明确两者结合的分子基础。方法细节为:构建N蛋白的截短体(N端结构域NTD、C端结构域CTD、丝氨酸-精氨酸富集结构域SR)和Nsp3.1的截短体(aa1-235、Δaa1-102、Δaa1-235),在HEK293T细胞中分别与对应蛋白共表达,通过Co-IP检测相互作用能力,通过免疫荧光染色观察蛋白共定位情况;对于难以表达的SR结构域,采用EGFP融合标签增强表达后进行检测。结果解读:N蛋白仅通过NTD结构域与Nsp3.1相互作用,CTD和SR结构域无相互作用能力,且NTD与Nsp3.1的相互作用强度显著高于全长N蛋白,提示N蛋白的其他结构域可能对该相互作用存在负调控;Nsp3.1通过N端aa1-102的酸性区域与N蛋白结合,删除该区域后,两者的相互作用显著减弱,共定位消失;EGFP融合的SR结构域无法与Nsp3.1相互作用,进一步证实SR不参与该结合过程。产品关联:文献未提及具体实验产品,领域常规使用免疫荧光染色试剂盒、激光共聚焦显微镜、蛋白融合标签载体等。
3.3 体外直接相互作用验证与亲和力测定
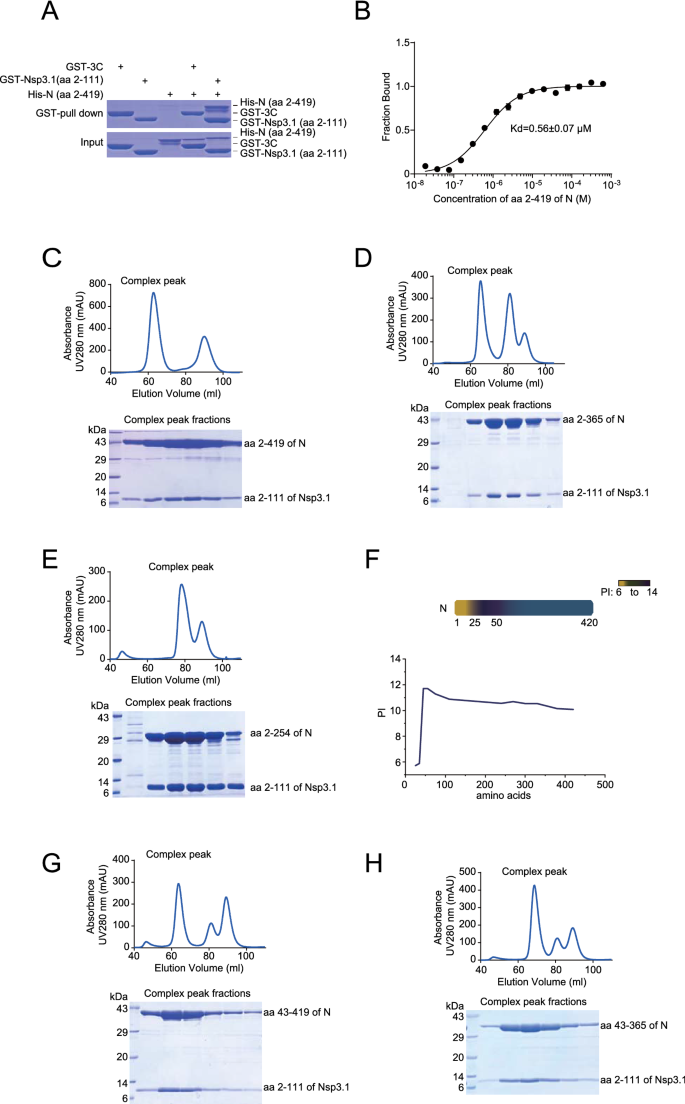
实验目的是在体外蛋白水平验证N与Nsp3.1的直接相互作用,并测定两者的结合亲和力。方法细节为:在大肠杆菌BL21(DE3)中表达GST标签的Nsp3.1截短体(aa2-111)和His标签的N蛋白截短体(aa2-419),通过GST-pull down实验检测直接相互作用;采用微量热泳动(MST)技术测定两者的解离常数(Kd);通过凝胶过滤层析分析两者形成的复合物。结果解读:GST-pull down实验证实Nsp3.1与N蛋白在体外可直接结合;MST检测显示两者的解离常数为0.56±0.07 μM(n=3),表明具有中等强度的结合亲和力;凝胶过滤层析结果显示,两者共表达后可形成稳定的蛋白复合物,且N蛋白的CTD缺失不影响复合物形成。产品关联:文献未提及具体实验产品,领域常规使用原核表达载体、GST亲和树脂、MST检测系统、凝胶过滤层析柱等。
3.4 相互作用对病毒复制的调控作用验证
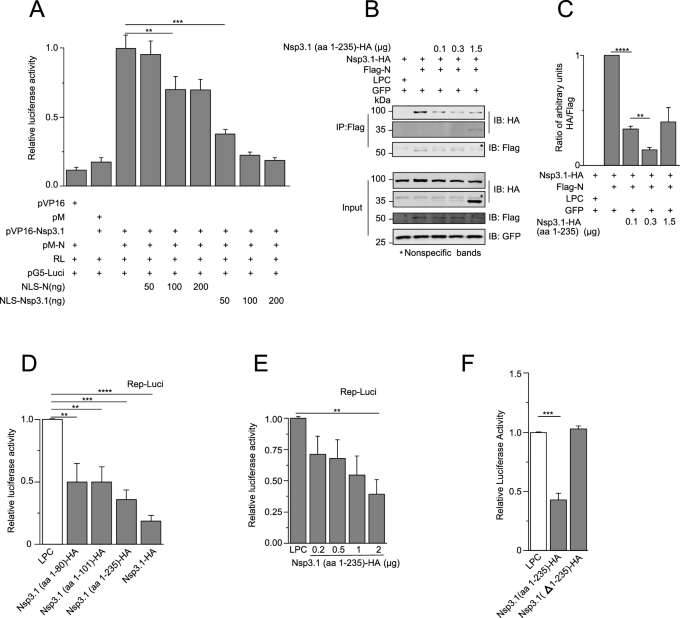
实验目的是明确Nsp3.1与N蛋白的相互作用对SARS-CoV-2复制的调控功能,评估其作为抗病毒药物靶点的潜力。方法细节为:构建S基因替换为荧光素酶的SARS-CoV-2复制子(Rep-Luci),在HEK293T细胞中共转染复制子与Nsp3.1截短体质粒,通过双荧光素酶报告系统检测复制子的活性;构建带有核定位序列(NLS)的N或Nsp3.1质粒,竞争性抑制两者在细胞内的相互作用,检测复制子活性的变化。结果解读:Nsp3.1可显著抑制复制子的荧光素酶活性,其N端aa1-235区域是抑制作用的关键,且抑制效果呈剂量依赖性(P<0.0001,n=3);带有NLS的N或Nsp3.1可竞争性抑制两者的相互作用,导致复制子活性显著降低;Nsp3.1的Δaa1-235截短体失去了对复制子的抑制作用,进一步证实该区域是调控病毒复制的关键位点。产品关联:文献未提及具体实验产品,领域常规使用病毒复制子系统、双荧光素酶检测试剂盒、核定位序列标签载体等。
4. Biomarker研究及发现成果解析
本研究中涉及的Biomarker为抗病毒药物潜在靶点类型,即SARS-CoV-2的Nsp3.1与N蛋白的相互作用,其筛选与验证遵循“全基因组筛选→细胞水平验证→体外蛋白水平验证→功能验证”的完整逻辑链条,为抗病毒药物开发提供了新的候选靶点。
Biomarker定位为病毒蛋白相互作用靶点,筛选与验证逻辑为:首先通过哺乳动物双杂交系统全基因组筛选发现Nsp3.1与N蛋白的相互作用,随后通过细胞水平的Co-IP、免疫荧光共定位实验验证该相互作用的真实性,再通过体外蛋白水平的GST-pull down、MST实验证实其为直接相互作用并测定亲和力,最后利用病毒复制子模型验证该相互作用对病毒复制的调控功能。研究过程中,该Biomarker的来源为SARS-CoV-2的结构蛋白N与非结构蛋白Nsp3.1,验证方法包括细胞内共表达后的Co-IP、免疫荧光共定位,体外蛋白纯化后的相互作用实验,以及病毒复制子的功能验证;特异性方面,N蛋白仅通过NTD结构域与Nsp3.1的N端酸性区域结合,具有明确的结构特异性;敏感性方面,哺乳动物双杂交系统可检测到低表达蛋白间的相互作用,MST实验的检测下限可达纳摩尔级别。核心成果:该相互作用是SARS-CoV-2复制的关键调控节点,抑制该相互作用可显著降低病毒复制子的活性(P<0.0001,n=3);创新性在于首次发现并解析了Nsp3.1与N蛋白的直接相互作用及其结构基础,明确了其对病毒复制的调控功能,为抗病毒药物开发提供了新的特异性靶点;统计学结果显示,MST实验测得的解离常数为0.56±0.07 μM(n=3),双荧光素酶实验中Nsp3.1对复制子的抑制作用具有极显著统计学差异(P<0.0001,n=3)。
