1. 领域背景与文献引入
文献英文标题:Transforming growth factor-β1 blocks the enhancement of tumor necrosis factor cytotoxicity by hyaluronidase Hyal-2 in L929 fibroblasts;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:细胞生物学(细胞凋亡与细胞因子调控)
转化生长因子-β(transforming growth factor-β,TGF-β)家族是一类多功能细胞因子,可调控细胞生长、细胞外基质蛋白合成及免疫细胞功能,在肿瘤发生发展中呈现双向调控作用,早期抑制肿瘤生长,晚期促进肿瘤侵袭转移。透明质酸酶是一类降解细胞外基质中透明质酸的酶类,其中睾丸来源的PH-20已被证实可增强肿瘤坏死因子(tumor necrosis factor,TNF)的细胞毒性,而TGF-β1可阻断PH-20的这一效应。领域共识:恶性肿瘤细胞常同时过表达TGF-β和透明质酸酶,两者的功能互作在肿瘤微环境调控中具有重要意义。当前研究空白在于,溶酶体来源的透明质酸酶Hyal-1和Hyal-2与TGF-β1的功能拮抗关系尚未明确,其调控TNF细胞毒性的分子机制也未被揭示。因此,本研究旨在明确Hyal-1和Hyal-2对TNF细胞毒性的调控作用,以及与TGF-β1的功能互作机制,为细胞因子调控细胞凋亡的研究提供新的分子靶点与理论依据。
2. 文献综述解析
本文献综述部分以透明质酸酶的类型为分类维度,对比了睾丸来源PH-20与溶酶体来源Hyal-1、Hyal-2的功能差异,系统梳理了TGF-β与透明质酸酶在TNF细胞毒性调控中的研究进展。
已有的研究表明,PH-20可通过上调促凋亡蛋白p53和含WW结构域的氧化还原酶(WW domain-containing oxidoreductase,WOX1)、下调抗凋亡的α-抑制剂,从而增强L929细胞对TNF的敏感性;TGF-β1则通过上调抗凋亡蛋白TIAF1、TIF2及新型细胞外基质蛋白,诱导细胞对TNF的抵抗,同时可抑制PH-20介导的ERK激活。这些研究的优势在于明确了PH-20与TGF-β1的功能拮抗关系,建立了初步的调控网络,但局限性在于仅聚焦于PH-20,未涉及溶酶体来源的Hyal-1和Hyal-2,且对具体分子机制的解析不够深入,缺乏对亚细胞定位变化的研究。
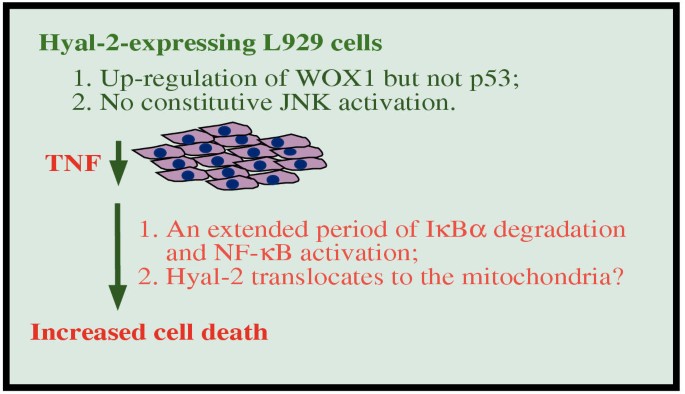
与现有研究相比,本研究首次将研究对象拓展到溶酶体透明质酸酶Hyal-1和Hyal-2,揭示了两者与TGF-β1在TNF细胞毒性调控中的功能拮抗关系,明确了Hyal-2增强TNF细胞毒性的分子机制与PH-20不同,不依赖p53而是通过WOX1、延长的NF-κB激活及线粒体转位实现,填补了溶酶体透明质酸酶在细胞凋亡调控领域的研究空白,为进一步理解细胞因子与细胞外基质降解酶的互作机制提供了新的视角。
3. 研究思路总结与详细解析
本研究的整体框架为“假设-实验验证-机制解析-结论”闭环,研究目标是明确溶酶体透明质酸酶Hyal-1、Hyal-2对TNF细胞毒性的调控作用及与TGF-β1的功能拮抗机制,核心科学问题是Hyal-2增强TNF细胞毒性的具体分子通路,以及TGF-β1阻断该效应的作用方式。研究通过构建稳定表达细胞系、细胞毒性检测、分子表达分析、亚细胞定位观察等实验,逐步解析了Hyal-2与TGF-β1的功能互作网络。
3.1 稳定表达GFP-Hyal-1/2的L929细胞系构建
实验目的是获得过表达溶酶体透明质酸酶Hyal-1和Hyal-2的细胞模型,为后续功能研究提供工具。方法细节为从EST数据库获取小鼠Hyal-1和Hyal-2的cDNA序列,将编码区亚克隆到pEGFP-N1载体构建GFP融合表达载体,通过电转染(250V、960Fd)将载体导入L929细胞,使用G418(200μg/ml)筛选约2周获得稳定转染株,采用免疫印迹(Western blotting)技术,以抗GFP抗体检测融合蛋白的表达。结果解读显示,成功构建了稳定表达GFP-Hyal-1、GFP-Hyal-2及对照GFP的L929细胞系,免疫印迹结果证实了融合蛋白的表达,且稳定表达的Hyal-1和Hyal-2未介导JNK的组成型激活。实验所用关键产品:Clontech的pEGFP-N1载体、G418、抗GFP抗体,Santa Cruz Biotechnology的α-微管蛋白抗体,Pepro-Tech的TNF-α等。
3.2 Hyal-1/2对TNF及抗癌药物细胞毒性的影响
实验目的是明确Hyal-1和Hyal-2对不同凋亡诱导剂的细胞毒性调控作用,筛选出特异性调控的靶点。方法细节为将构建的稳定转染细胞系分别暴露于TNF-α、星形孢菌素、放线菌素D、柔红霉素、喜树碱中16-24小时,采用结晶紫染色法检测细胞死亡程度,每组实验重复8次,结果以均值±标准差表示。结果解读显示,与对照GFP表达细胞相比,Hyal-2表达细胞对TNF的敏感性显著增加60-110%(n=8),Hyal-1表达细胞的敏感性增加20-90%,但两类细胞对其他抗癌药物诱导的细胞死亡无显著差异,提示Hyal-1和Hyal-2对细胞毒性的调控具有TNF特异性。
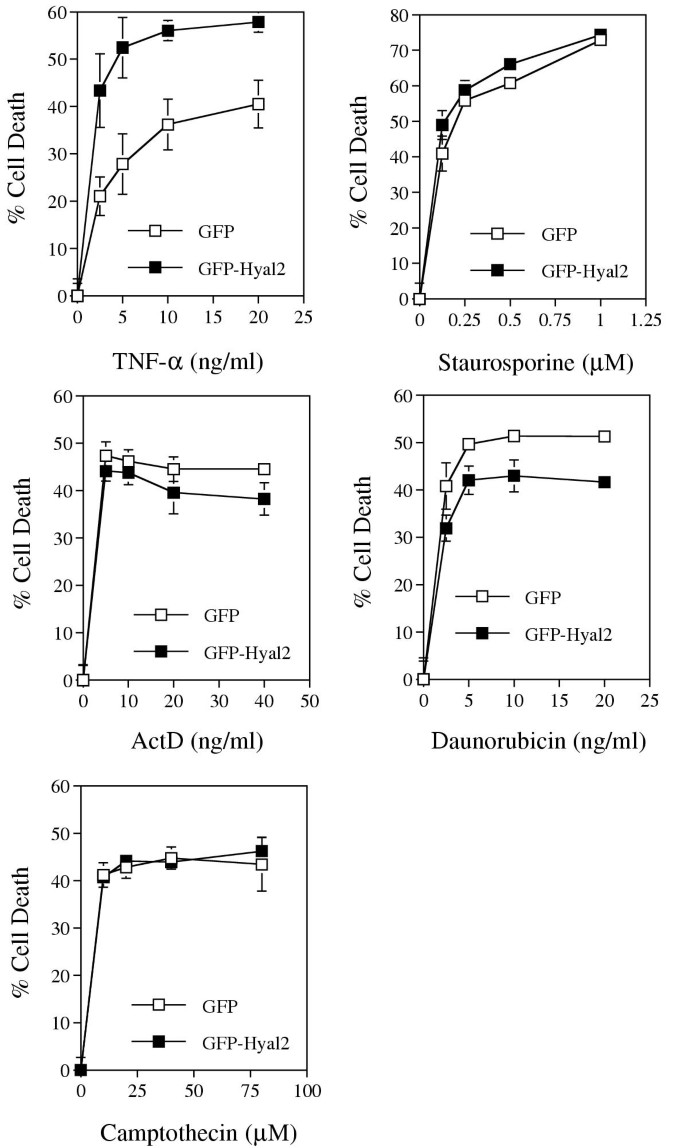
文献未提及具体实验产品,领域常规使用结晶紫染色试剂盒、各类抗癌药物试剂。
3.3 Hyal-1/2对WOX1和p53表达的调控
实验目的是解析Hyal-1和Hyal-2增强TNF细胞毒性的下游分子机制,明确关键调控蛋白。方法细节分为三部分:一是电转染L929细胞GFP-Hyal-1、GFP-Hyal-2或对照载体,培养48小时后采用免疫印迹检测WOX1和p53的表达;二是对稳定转染细胞系进行TNF处理,检测不同时间点WOX1的表达变化;三是将GFP-Hyal-2与WOX1载体共转染L929细胞,48小时后结晶紫染色检测细胞死亡情况。结果解读显示,瞬时表达Hyal-1和Hyal-2均能诱导WOX1的表达,其中46kDa为全长WOX1,31kDa为降解产物,但未检测到p53的表达;稳定表达Hyal-2的细胞组成型表达胞质WOX1,TNF处理后WOX1表达降低,推测是由于TNF介导WOX1从线粒体转位到细胞核;稳定表达Hyal-1的细胞中,TNF处理40分钟后诱导WOX1表达;共转染实验显示,Hyal-2能增强WOX1介导的细胞死亡,而Hyal-1无此效应,提示WOX1是Hyal-2增强TNF细胞毒性的关键下游分子。
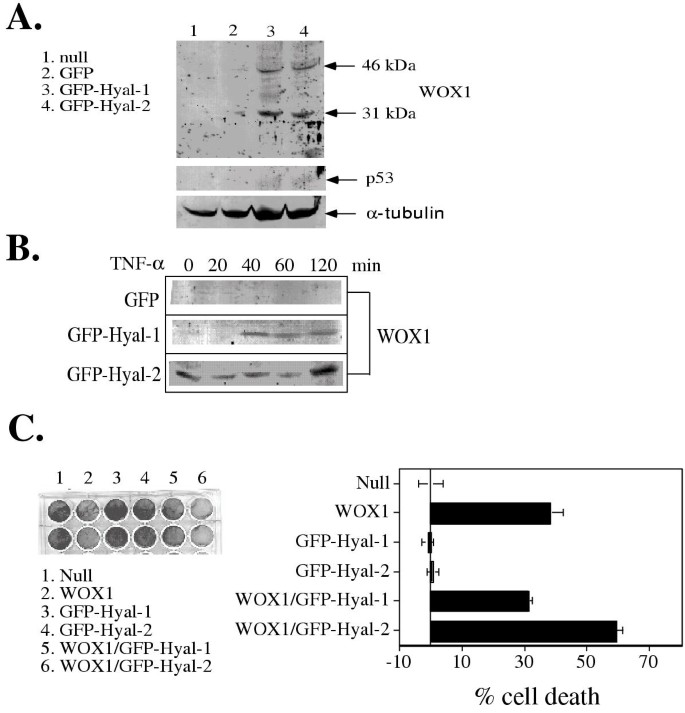
实验所用关键产品:自制的WOX1抗血清,Santa Cruz Biotechnology的p53抗体,结晶紫染色试剂等。
3.4 TNF介导的NF-κB激活分析
实验目的是明确Hyal-2对NF-κB信号通路的调控作用,探索其增强TNF细胞毒性的信号机制。方法细节为将稳定转染细胞系暴露于TNF(50ng/ml)0、20、40、60、120分钟,采用NE-PER核质提取试剂分离胞质和细胞核组分,通过免疫印迹检测胞质中IκBα的降解情况及细胞核中NF-κB p65的定位,以此反映NF-κB的激活状态。结果解读显示,对照细胞和Hyal-1表达细胞在TNF处理20分钟时出现IκBα降解和NF-κB激活,而Hyal-2表达细胞中该过程持续20-60分钟,呈现延长的NF-κB激活状态,提示延长的NF-κB激活可能参与Hyal-2对TNF细胞毒性的增强作用。
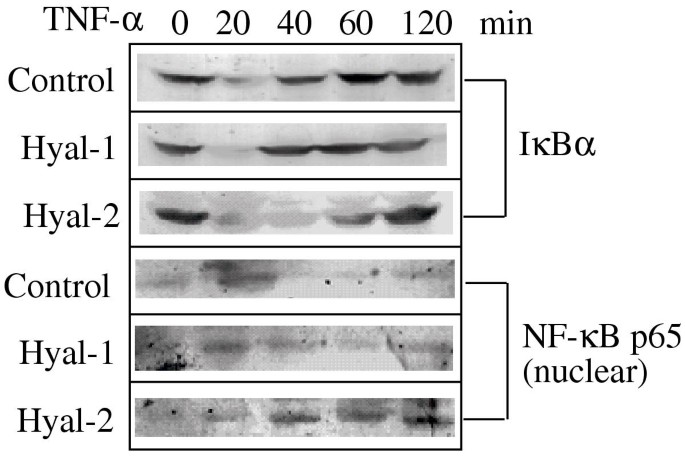
实验所用关键产品:Pierce的NE-PER核质提取试剂,Santa Cruz Biotechnology的IκBα、NF-κB p65抗体。
3.5 Hyal-2在凋亡过程中的亚细胞定位
实验目的是探索Hyal-2参与细胞凋亡的潜在机制,明确其亚细胞定位变化与凋亡的关联。方法细节为将GFP-Hyal-2载体转染到COS7细胞(该细胞体积大,便于荧光显微镜观察),培养24-48小时后用星形孢菌素诱导凋亡,采用Mitotracker Red染色线粒体,DAPI染色细胞核,通过荧光显微镜观察GFP-Hyal-2与线粒体的共定位情况。结果解读显示,正常状态下Hyal-2定位于溶酶体,在星形孢菌素诱导的凋亡过程中,部分Hyal-2从溶酶体转位到线粒体,提示Hyal-2可能通过损伤线粒体参与凋亡调控。
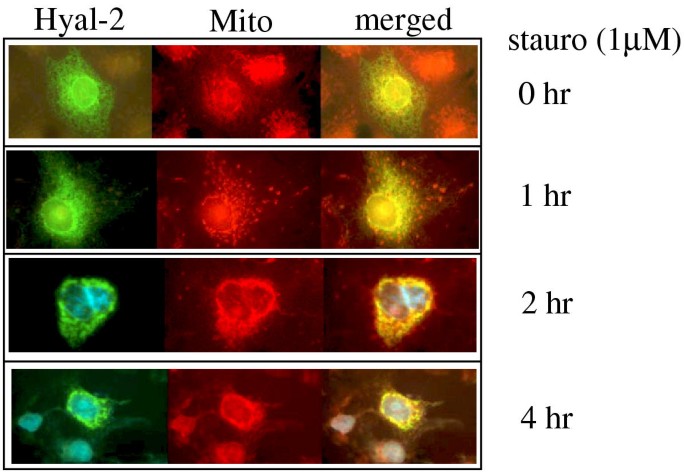
实验所用关键产品:Molecular Probes的LysoTracker、Mitotracker Red,Roche的FuGene 6转染试剂,DAPI染色剂。
3.6 TGF-β1与Hyal-1/2的功能拮抗作用分析
实验目的是明确TGF-β1对Hyal-1和Hyal-2调控细胞生长及TNF细胞毒性的影响,验证两者的功能拮抗关系。方法细节分为两部分:一是将稳定转染细胞系用TGF-β1(2ng/ml)处理24小时,结晶紫染色检测细胞生长情况;二是用TGF-β1预处理细胞2小时后加入TNF,继续培养16-24小时,检测细胞死亡程度。结果解读显示,TGF-β1可促进对照L929细胞的生长约20%(n=8),但Hyal-1和Hyal-2表达细胞的生长被阻断;TGF-β1能抑制Hyal-1和Hyal-2增强的TNF细胞毒性30-50%,对对照细胞的抑制率为50-70%,证实了TGF-β1与Hyal-1、Hyal-2在细胞生长和TNF细胞毒性调控中的功能拮抗关系。
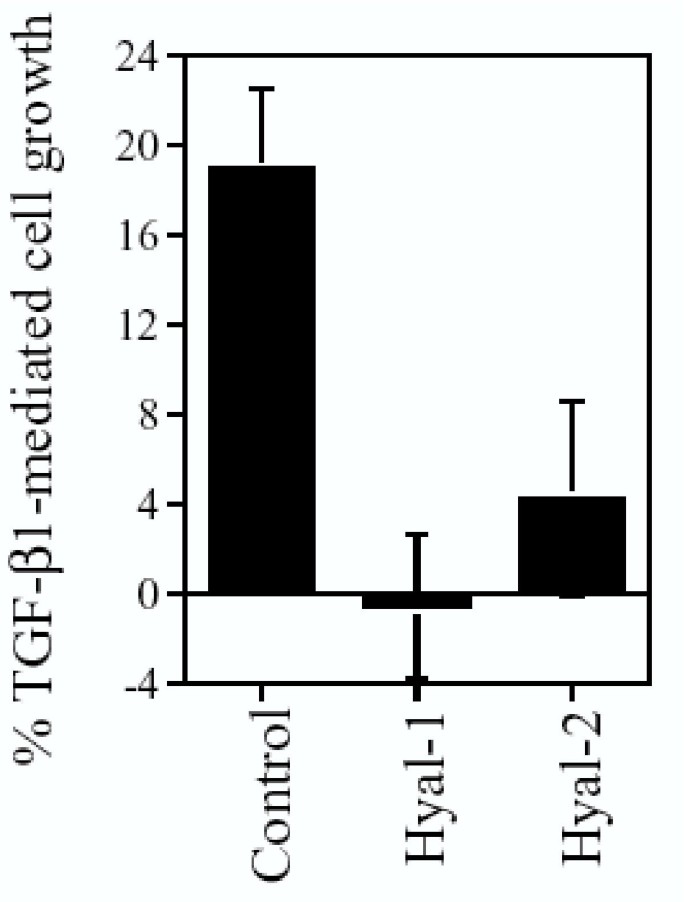
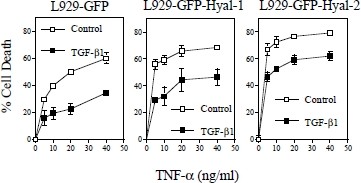
实验所用关键产品:R&D的TGF-β1,结晶紫染色试剂。
4. Biomarker研究及发现成果
本研究中涉及的Biomarker为促凋亡蛋白WOX1,其作为Hyal-2增强TNF细胞毒性的关键分子,通过细胞水平的表达验证与功能实验,明确了其在调控网络中的核心作用。
WOX1属于促凋亡蛋白,本研究中其筛选与验证逻辑为:首先通过瞬时转染实验发现Hyal-1和Hyal-2可诱导WOX1表达,随后通过稳定转染实验证实Hyal-2可组成型表达WOX1,最后通过共转染实验验证Hyal-2可增强WOX1介导的细胞死亡,形成了完整的“表达调控-功能验证”逻辑链条。
WOX1的来源为L929细胞的内源性表达,验证方法包括免疫印迹检测表达水平、共转染实验检测功能活性。特异性方面,仅Hyal-2稳定表达细胞组成型表达WOX1,Hyal-1稳定表达细胞需TNF诱导才能表达WOX1;敏感性方面,Hyal-2增强WOX1介导的细胞死亡,提示WOX1对Hyal-2的调控具有特异性。文献未明确提供ROC曲线、HR值等数据,基于图表趋势推测WOX1的表达水平与Hyal-2增强的TNF细胞毒性呈正相关。
WOX1作为Hyal-2增强TNF细胞毒性的关键下游分子,其功能关联在于介导细胞凋亡,与延长的NF-κB激活、Hyal-2的线粒体转位共同构成Hyal-2调控TNF细胞毒性的核心机制。本研究的创新性在于首次发现溶酶体透明质酸酶Hyal-2通过调控WOX1而非p53来增强TNF细胞毒性,明确了WOX1在该调控网络中的核心作用,为细胞凋亡的分子调控机制提供了新的靶点。