1. 领域背景与文献引入
文献英文标题:Quantitative phosphoproteomics reveals that nestin is a downstream target of dual leucine zipper kinase during retinoic acid-induced neuronal differentiation of Neuro-2a cells;发表期刊:BMC Molecular and Cell Biology;影响因子:未公开;研究领域:神经科学-神经元分化与轴突再生
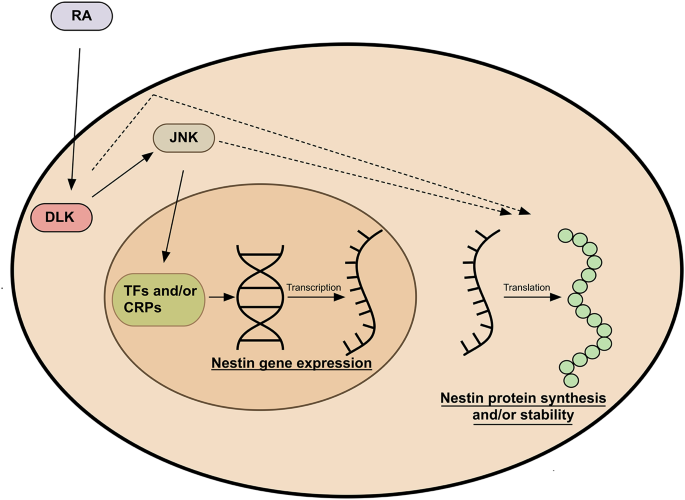
神经元分化是神经系统发育和功能维持的核心过程,新生神经元通过轴突生长、分支形成功能性神经环路,该过程受神经生长因子、维甲酸等多种内外源因子调控。双亮氨酸拉链激酶(DLK)是轴突生长的关键调控因子,现有研究证实其通过激活JNK-c-Jun通路、调控微管稳定蛋白磷酸化、介导损伤信号逆向转运等机制参与神经系统发育与再生,但DLK的下游底物谱仍不完整,尤其是对中间丝蛋白的调控作用尚未被系统解析。领域共识:巢蛋白(nestin)作为神经前体细胞特异性标志物,参与干细胞分化与迁移,但它在DLK信号通路中的功能关联仍属空白。本研究通过定量磷酸化蛋白质组学技术,在维甲酸诱导的Neuro-2a细胞中筛选DLK的下游靶点,首次揭示巢蛋白是DLK的新下游靶点,填补了DLK信号通路在中间丝蛋白调控层面的研究空白。
2. 文献综述解析
作者对领域内现有研究的分类维度为DLK调控轴突生长的机制类型,包括微管动力学调控、转录因子激活与转运、下游基因表达调控三个方向。现有研究支持DLK在神经系统发育和再生中的核心作用,例如小鼠DLK基因敲除会导致皮层神经元轴突生长缺陷与迁移障碍,DLK通过激活JNK-c-Jun通路促进外周神经轴突再生;技术方法上,前期研究多采用基因敲除、免疫印迹、免疫荧光等手段验证DLK的上游调控因子与部分下游靶点,但局限性在于缺乏全局磷酸化水平的系统分析,无法全面鉴定DLK介导的磷酸化底物。本研究的创新价值在于首次应用iTRAQ定量磷酸化蛋白质组学技术,在细胞模型中系统筛选DLK的下游磷酸化靶点,发现巢蛋白与DLK信号通路的功能关联,补充了DLK下游调控网络的中间丝蛋白分支,为进一步解析DLK调控神经元分化的机制提供了新方向。
3. 研究思路总结与详细解析
本研究的整体框架为:构建DLK稳定敲减的Neuro-2a细胞模型,验证DLK对维甲酸诱导轴突生长的调控作用;通过iTRAQ定量磷酸化蛋白质组学筛选差异磷酸化肽段;聚焦巢蛋白验证其表达与磷酸化水平的变化;通过基因敲减与过表达实验明确巢蛋白在DLK介导轴突生长中的功能。研究遵循“模型构建→靶点筛选→功能验证”的闭环逻辑,逐步解析DLK与巢蛋白的调控关系。
3.1 DLK稳定敲减Neuro-2a细胞模型构建与验证
实验目的是建立DLK功能缺失的细胞模型,验证DLK对维甲酸诱导神经元分化的调控作用。方法细节:采用慢病毒载体表达两种靶向DLK的shRNA(shDLK#1、shDLK#2)感染Neuro-2a细胞,经嘌呤霉素筛选获得稳定敲减细胞系;通过免疫印迹检测DLK、磷酸化JNK、磷酸化c-Jun的蛋白水平,利用IncuCyte® S3活细胞分析系统连续72小时监测轴突生长情况。结果解读:免疫印迹结果显示shDLK#2对DLK的敲减效率约75%(n=3,P<0.01),DLK敲减后维甲酸诱导的JNK与c-Jun磷酸化水平显著降低(n=3,P<0.05);轴突生长分析显示,DLK敲减细胞的轴突长度较对照组缩短约40%(n=5,P<0.0001),证实DLK是维甲酸诱导Neuro-2a细胞轴突生长的必需因子。
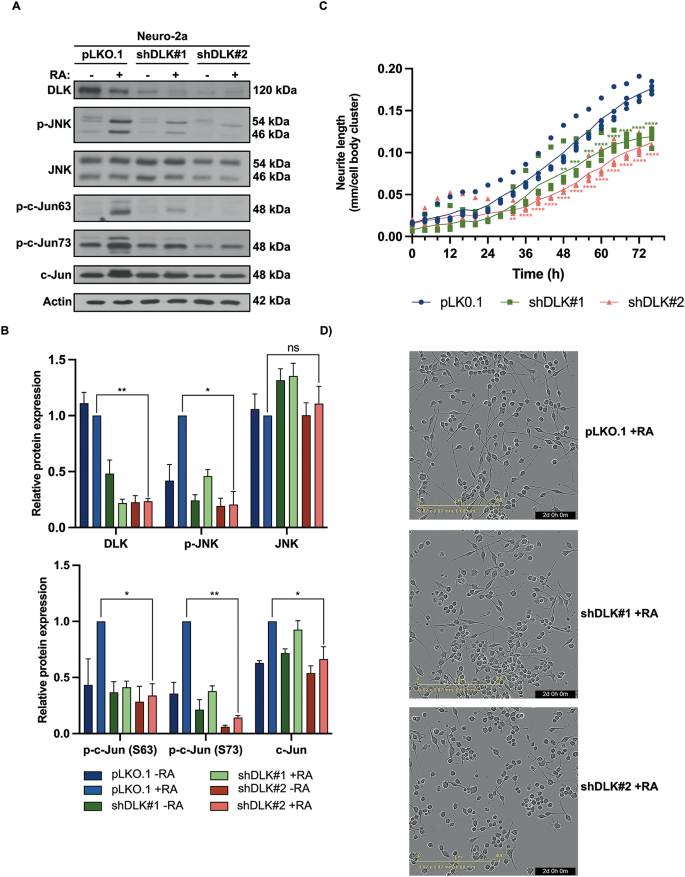
实验所用关键产品:慢病毒载体pLKO.1、IncuCyte® S3 Live-Cell Analysis System(Essen BioScience)、免疫印迹相关抗体(详情见补充材料5)
3.2 定量磷酸化蛋白质组学筛选DLK下游靶点
实验目的是系统鉴定DLK调控的下游磷酸化蛋白质。方法细节:将对照组与DLK敲减组细胞用20μM维甲酸处理24小时,提取总蛋白后采用iTRAQ试剂标记肽段,通过TiO2磁珠富集磷酸化肽段,利用纳米液相色谱-串联质谱(nanoLC-MS/MS)进行检测,借助Proteome Discoverer软件分析差异磷酸化肽段(筛选标准:P<0.05,z score>2)。结果解读:共鉴定到4942个磷酸化肽段,其中32个肽段的丰度在DLK敲减组中发生显著变化,对应27个差异磷酸化蛋白质;STRING互作网络分析显示这些蛋白主要富集于神经系统发育相关通路,其中巢蛋白的两个磷酸化肽段(Ser-894、Ser-1837)丰度降低最为显著(n=2,P<0.05)。
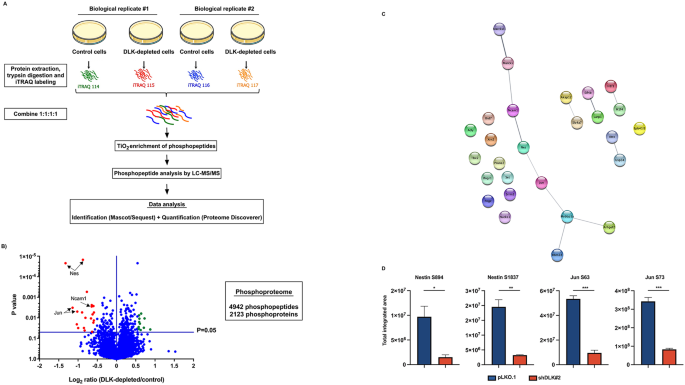
实验所用关键产品:iTRAQ多重标记试剂(SCIEX)、High-Select™ TiO2磷酸化肽段富集试剂盒(Thermo Fisher Scientific)、Orbitrap Fusion质谱仪(Thermo Fisher Scientific)
3.3 巢蛋白表达与磷酸化水平的验证
实验目的是明确DLK敲减对巢蛋白表达及磷酸化的调控机制。方法细节:采用实时定量PCR(RT-qPCR)检测巢蛋白mRNA水平,通过免疫印迹检测巢蛋白总蛋白水平,利用平行反应监测(PRM)质谱技术靶向验证巢蛋白的磷酸化水平。结果解读:RT-qPCR结果显示,对照组细胞经维甲酸处理后巢蛋白mRNA水平升高约2.5倍(n=3,P<0.05),而DLK敲减组的升高幅度仅为对照组的40%且无统计学显著性;免疫印迹结果显示DLK敲减组巢蛋白总蛋白水平较对照组降低约60%(n=3,P<0.0001);PRM结果证实巢蛋白Ser-894与Ser-1837的磷酸化水平显著降低(n=3,P<0.01),且该变化源于巢蛋白总蛋白水平下降而非单纯磷酸化修饰改变。
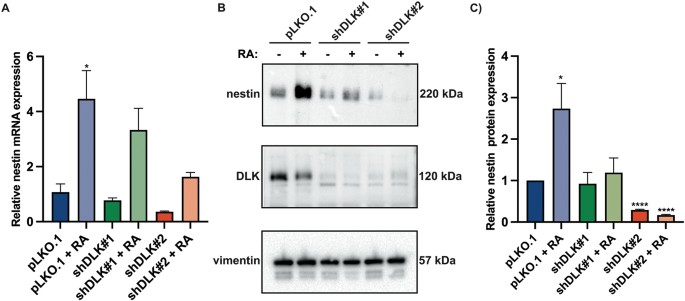
实验所用关键产品:Direct-zol RNA MiniPrep Kit(Zymo Research)、iTaq Universal SYBR Green Supermix(Bio-Rad)、Skyline软件(用于PRM定量分析)
3.4 巢蛋白在DLK介导轴突生长中的功能验证
实验目的是验证巢蛋白是否为DLK调控轴突生长的功能性介质。方法细节:采用siRNA敲减亲本Neuro-2a细胞的巢蛋白,利用IncuCyte系统检测维甲酸诱导的轴突生长情况;在DLK敲减细胞中过表达野生型巢蛋白,观察轴突生长缺陷是否得到恢复。结果解读:四种巢蛋白siRNA的敲减效率达70%-90%(n=3,P<0.01),但敲减巢蛋白后维甲酸诱导的轴突生长未受显著影响(n=5,P>0.05);过表达巢蛋白也未能恢复DLK敲减细胞的轴突生长缺陷(n=3,P>0.05),说明巢蛋白不介导DLK对轴突生长的调控作用。
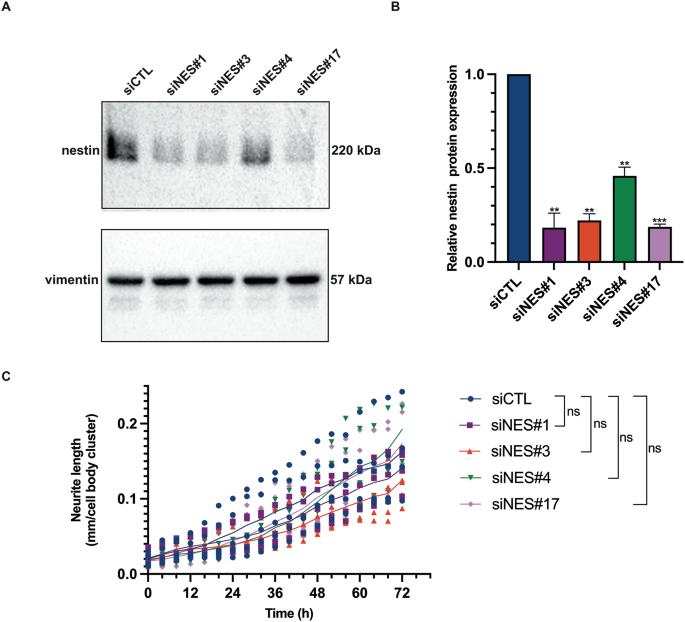
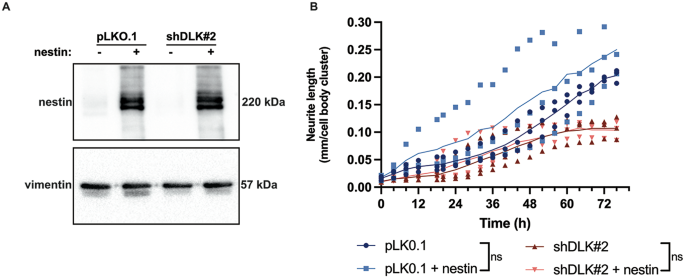
实验所用关键产品:巢蛋白siRNA文库(Dharmacon)、Lipofectamine® RNAiMAX转染试剂(Thermo Fisher Scientific)、野生型巢蛋白表达质粒(OriGene)
4. Biomarker研究及发现成果
Biomarker定位
本研究中涉及的Biomarker为巢蛋白(nestin),属于VI型中间丝蛋白,是神经前体细胞的经典标志物。研究通过“定量磷酸化蛋白质组学筛选→PRM靶向验证→表达水平验证→功能验证”的完整逻辑链条,确认巢蛋白是DLK信号通路的新下游靶点,筛选与验证过程均基于维甲酸诱导的Neuro-2a细胞模型。
研究过程详述
样本来源为维甲酸处理24小时的Neuro-2a细胞,验证方法包括iTRAQ定量磷酸化蛋白质组学、PRM质谱、RT-qPCR、免疫印迹等;特异性方面,DLK敲减后巢蛋白的表达与磷酸化水平特异性降低,而同为中间丝蛋白的波形蛋白(vimentin)水平无显著变化;敏感性方面,PRM检测显示巢蛋白Ser-894与Ser-1837磷酸化肽段的丰度较对照组降低约50%-70%(n=3,P<0.01),RT-qPCR显示mRNA水平降低约60%(n=3,P<0.05)。
核心成果提炼
本研究首次发现DLK通过正向调控巢蛋白的转录与表达水平参与神经元分化过程,且该调控作用不依赖于直接磷酸化修饰;创新性在于将DLK信号通路与中间丝蛋白巢蛋白关联,拓展了DLK下游调控网络的覆盖范围;统计学结果显示,DLK敲减组巢蛋白mRNA水平较对照组降低约60%(n=3,P<0.05),总蛋白水平降低约60%(n=3,P<0.0001)。同时研究明确巢蛋白不介导DLK对轴突生长的调控作用,为后续解析DLK调控神经元分化的具体机制排除了非功能性靶点,为神经发育与再生领域的研究提供了新的参考方向。