1. 领域背景与文献引入
文献英文标题:The involvement of the wnt signaling pathway and TCF7L2 in diabetes mellitus: The current understanding, dispute, and perspective;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:代谢性疾病(2型糖尿病)与细胞信号通路调控。
Wnt信号通路最初于1982年在乳腺癌研究中被发现,随后在果蝇等生物的发育生物学研究中明确其在胚胎发育、细胞命运决定中的核心作用,后续研究证实其异常激活与多种肿瘤发生密切相关。近十年来,该通路在代谢稳态调控中的功能逐渐受到关注,全基因组关联研究(GWAS)发现Wnt信号通路多个关键组分的遗传变异与2型糖尿病(T2D)、肥胖等代谢性疾病的易感性显著相关。T2D是全球范围内高发的慢性代谢性疾病,其发病机制涉及胰岛β细胞功能障碍、胰岛素抵抗、肝糖代谢异常等多个环节,目前针对其遗传易感机制的研究仍存在诸多未明确之处,尤其是Wnt信号通路在胰岛中的功能存在争议,TCF7L2作为Wnt通路的关键转录效应因子,其多态性与T2D的关联已被广泛验证,但具体调控机制尚未完全阐明。在此背景下,本综述系统整合了Wnt信号通路及TCF7L2在代谢稳态与T2D中的研究进展,梳理领域内的争议问题,并探讨通路间的交互作用,为T2D的机制研究与治疗靶点开发提供新的视角。
2. 文献综述解析
本文综述以Wnt信号通路的基础机制为起点,围绕其在代谢组织中的功能、与T2D的遗传关联、TCF7L2的作用争议及通路交互四个维度,系统梳理了领域内的研究成果,明确了Wnt通路在代谢稳态中的核心作用,同时凸显了当前研究中存在的矛盾与未解决问题。
现有研究已明确经典Wnt信号通路的分子组成与激活机制,即Wnt配体与Frizzled受体、LRP5/6共受体结合后,抑制β-catenin的降解复合物(由APC、axin、GSK-3等组成),使游离β-catenin入核与TCF家族蛋白形成复合物,调控下游靶基因表达。GWAS研究证实LRP5、Wnt5b等Wnt通路组分的遗传多态性与T2D或肥胖的易感性相关,基因敲除小鼠模型显示LRP5敲除小鼠在高脂饮食下血浆胆固醇水平升高,正常饮食下糖耐量受损,且葡萄糖诱导的胰岛素分泌障碍。在脂肪组织中,Wnt信号负调控脂肪生成,Wnt10b过表达小鼠脂肪量减少,抵抗高脂饮食诱导的肥胖,而脂肪细胞分泌的Wnt配体可通过旁分泌作用影响胰岛β细胞功能。然而,Wnt信号在胰岛中的功能存在明显争议,部分研究显示β-catenin敲除对胰岛内分泌细胞的数量与功能无显著影响,而另一些研究则证实Wnt激活可促进胰岛β细胞增殖,增加β细胞量。TCF7L2作为Wnt通路的关键效应因子,其多态性与T2D的关联已在多个种族人群中得到验证,但关于其在胰岛中的功能,不同研究分别得出了有害或有益的结论,可能与TCF7L2的不同剪接异构体有关。现有研究的技术方法优势在于,GWAS提供了大规模人群水平的遗传关联证据,基因编辑小鼠模型与细胞实验为通路功能解析提供了直接的生物学证据;局限性在于部分研究结果存在矛盾,缺乏对TCF7L2多态性调控基因表达的具体机制解析,且通路间交互作用的体内验证不足。
与现有研究相比,本综述首次系统整合了Wnt信号通路在代谢稳态中的研究进展,重点梳理了TCF7L2在T2D中的作用争议,并提出了Wnt、胰岛素与FOXO通路的交互模型,即TCF与FOXO蛋白竞争结合有限的游离β-catenin,氧化应激与衰老使平衡偏向FOXO信号,而胰岛素可恢复平衡,这一模型为解析T2D等年龄相关代谢性疾病的发病机制提供了新的框架,同时明确了未来研究需聚焦于TCF7L2剪接异构体的功能、通路交互的体内验证等方向。
3. 研究思路总结与详细解析
本文为综述性研究,整体研究目标是系统总结Wnt信号通路及TCF7L2在糖尿病中的研究现状、争议问题与未来方向,核心科学问题是Wnt信号通路如何调控代谢稳态,以及TCF7L2遗传多态性影响T2D易感性的分子机制,技术路线遵循“基础机制→遗传关联→组织功能→通路交互”的逻辑,全面整合领域内的研究成果,梳理争议并提出展望。
3.1 Wnt信号通路基础机制梳理
实验目的:明确经典Wnt信号通路的分子组成、激活过程及核心调控机制。
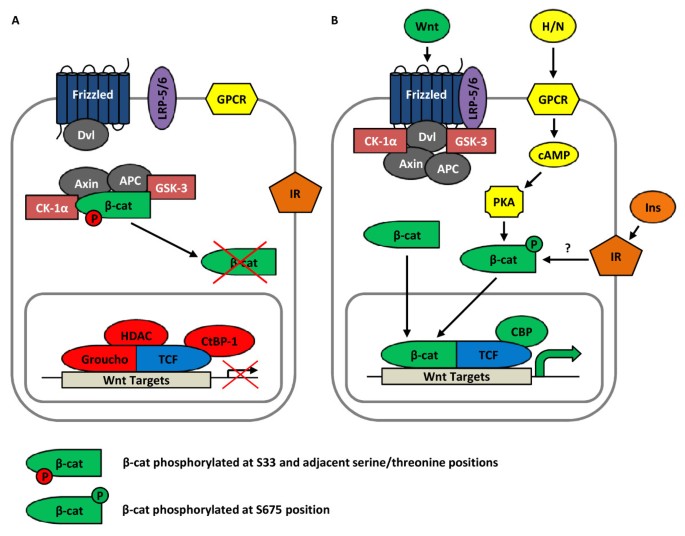
方法细节:通过回顾领域内经典研究,系统介绍Wnt配体家族(人类与啮齿类中已发现19种Wnt基因)、受体(Frizzled七跨膜受体、LRP5/6共受体)的分子特征,以及β-catenin的降解调控机制,包括APC、axin、GSK-3、CK-1α组成的降解复合物对β-catenin的磷酸化与蛋白酶体降解,Wnt激活后该复合物的解离过程,以及β-catenin入核与TCF家族蛋白结合调控靶基因的过程。同时介绍GSK-3抑制剂(如锂盐)对Wnt信号的模拟激活作用,以及β-catenin作为其他通路效应分子的功能。
结果解读:经典Wnt信号通路的激活依赖于Wnt配体与受体的结合,通过抑制β-catenin的降解,使游离β-catenin入核形成β-cat/TCF转录复合物,调控下游靶基因表达;GSK-3作为通路的负调控因子,其抑制剂可模拟Wnt信号效应;此外,β-catenin还可作为胰岛素、胰高血糖素样肽-1(GLP-1)等信号通路的效应分子,参与多种生理过程的调控。
产品关联:文献未提及具体实验产品,领域常规使用基因编辑工具(如CRISPR-Cas9)、蛋白免疫印迹(Western Blot)、染色质免疫共沉淀(ChIP)、荧光报告基因实验等试剂/仪器。
3.2 Wnt通路组分与糖尿病遗传关联分析
实验目的:解析Wnt信号通路关键组分的遗传多态性与糖尿病、肥胖等代谢性疾病的关联。
方法细节:回顾全球范围内的GWAS研究,分析LRP5、Wnt5b、TCF7L2等基因的单核苷酸多态性(SNP)与T2D、肥胖易感性的关联,结合基因敲除/过表达小鼠的表型分析,验证这些基因在代谢稳态中的功能。
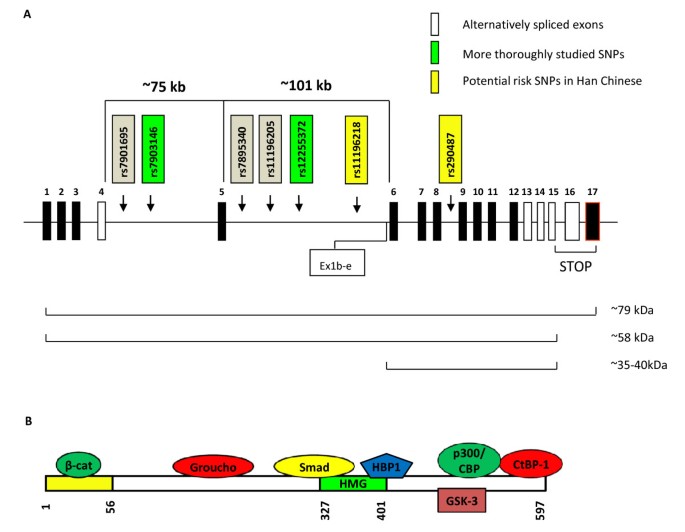
结果解读:GWAS研究显示,LRP5基因的多态性与肥胖表型及T2D易感性相关,LRP5敲除小鼠在高脂饮食下血浆胆固醇水平升高,正常饮食下糖耐量受损,且葡萄糖诱导的胰岛素分泌障碍;Wnt5b基因的SNP与日本人群T2D易感性相关,Wnt5b作为抑制性Wnt配体,可促进脂肪生成;TCF7L2基因的rs12255372、rs7903146等位点与多个种族人群的T2D易感性显著相关,其中rs7903146在高加索人群中效应最强,风险等位基因携带者T2D风险升高。
产品关联:文献未提及具体实验产品,领域常规使用基因分型试剂盒、生物信息学分析工具(如GWAS分析软件)、小鼠代谢表型检测系统等试剂/仪器。
3.3 Wnt信号在代谢组织中的功能研究(含争议)
实验目的:探讨Wnt信号通路在脂肪组织、胰岛β细胞等代谢组织中的功能及调控机制。
方法细节:回顾脂肪组织基因工程小鼠模型(Wnt10b过表达/敲除)的研究结果,分析Wnt信号对脂肪生成的调控作用;同时整合多个胰岛β细胞基因编辑小鼠模型的研究,包括β-catenin敲除、稳定激活β-catenin的小鼠模型,以及人类胰岛样本的分析,探讨Wnt信号在胰岛发育与功能中的作用;此外,回顾TCF7L2在胰岛中的功能研究,包括siRNA敲低、过表达实验及人类T2D患者胰岛样本的分析。
结果解读:在脂肪组织中,Wnt信号负调控脂肪生成,Wnt10b过表达小鼠脂肪量减少约50%,抵抗高脂饮食诱导的肥胖,而Wnt10b敲除小鼠脂肪生成潜能增加;脂肪细胞分泌的Wnt配体可刺激胰岛β细胞增殖与胰岛素分泌,该效应可被Wnt抑制剂分泌型卷曲相关蛋白1(SFRP-1)阻断。在胰岛中,不同研究结果存在争议:部分研究显示β-catenin敲除对胰岛内分泌细胞的数量与功能无显著影响,而另一些研究证实稳定激活β-catenin可促进胰岛细胞增殖,增加胰腺体积;关于TCF7L2的功能,部分研究显示T2D患者胰岛中TCF7L2 mRNA表达升高,风险等位基因携带者胰岛功能受损,而另一些研究则发现TCF7L2敲低导致β细胞凋亡增加、胰岛素分泌障碍,过表达则保护β细胞免受损伤。
产品关联:文献未提及具体实验产品,领域常规使用转基因小鼠模型、免疫组化(IHC)、细胞培养试剂、胰岛素分泌检测试剂盒等试剂/仪器。
3.4 Wnt与其他通路的交互作用解析
实验目的:探讨Wnt信号通路与胰岛素、FOXO通路的交互作用及其在代谢稳态中的意义。
方法细节:回顾领域内关于β-catenin与FOXO蛋白互作的研究,分析氧化应激、衰老、胰岛素对这种互作的调控,以及其对代谢稳态的影响。
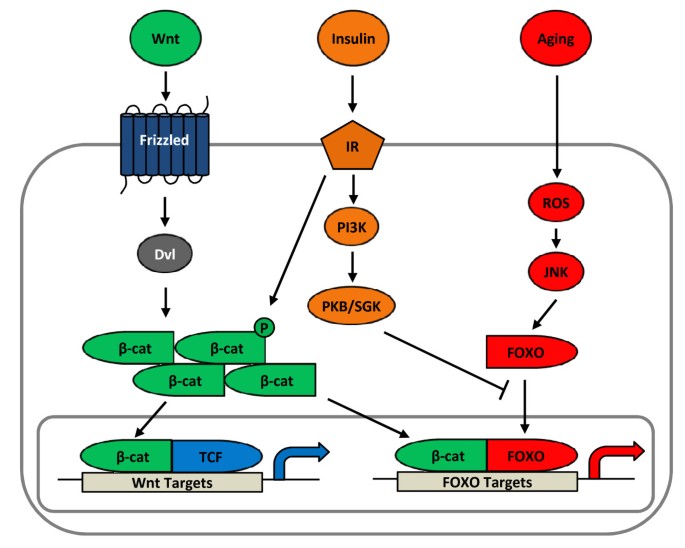
结果解读:Wnt、胰岛素与FOXO通路存在密切的交互作用,TCF与FOXO蛋白竞争结合有限的游离β-catenin:在衰老与氧化应激状态下,平衡偏向FOXO信号,β-catenin与FOXO结合,促进FOXO靶基因表达,抑制细胞周期进程与生长;而胰岛素可通过激活蛋白激酶B(PKB/SGK),促进FOXO的磷酸化与核排除,恢复平衡,使β-catenin与TCF结合,激活Wnt靶基因表达,促进细胞增殖与生长。这种通路交互模型为解析T2D等年龄相关代谢性疾病的发病机制提供了新的视角,即衰老与氧化应激导致的Wnt信号减弱可能参与T2D的发生发展。
产品关联:文献未提及具体实验产品,领域常规使用蛋白免疫共沉淀(Co-IP)、荧光共定位实验、细胞应激模型等试剂/仪器。
4. Biomarker研究及发现成果解析
本文中涉及的核心Biomarker为TCF7L2基因的单核苷酸多态性(SNP),其作为2型糖尿病的遗传易感Biomarker,已在全球多个种族人群中得到验证,具有明确的临床应用潜力。
Biomarker定位:TCF7L2基因的SNP属于遗传类Biomarker,其筛选与验证逻辑为:首先通过大规模全基因组关联研究(GWAS)筛选出与T2D易感性相关的位点,随后在不同种族人群中进行独立验证,最后通过细胞与动物实验探讨其功能机制。
研究过程详述:该Biomarker来源于人类基因组,验证方法包括GWAS分析、候选基因关联研究、功能实验等。具体而言,2006年的GWAS首次发现TCF7L2基因的rs12255372、rs7903146等位点与T2D易感性显著相关,后续研究在高加索、东亚等多个种族人群中验证了这一关联,其中rs7903146位点在高加索人群中效应最强,T等位基因携带者T2D风险显著升高;在功能验证方面,细胞实验显示TCF7L2敲低导致胰岛β细胞凋亡增加、胰岛素分泌障碍,过表达则保护β细胞免受损伤;小鼠模型研究显示TCF7L2敲除小鼠出现低血糖,杂合子小鼠对糖尿病具有保护作用。该Biomarker的特异性与敏感性在不同人群中存在差异,例如在高加索人群中,rs7903146的TT基因型携带者T2D风险显著高于CC基因型(文献未明确具体AUC值与敏感性数据,基于研究结论推测具有统计学显著性)。
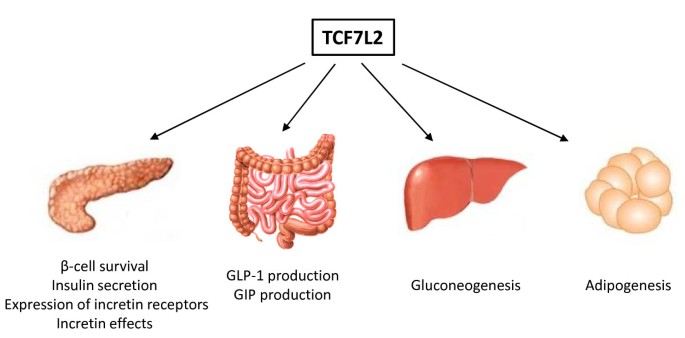
核心成果提炼:TCF7L2基因SNP是目前已知效应最强的T2D遗传易感Biomarker之一,其功能关联在于调控胰岛β细胞的存活与功能、 incretin激素(GLP-1、GIP)的表达、肝糖异生等多个代谢环节;创新性在于首次明确了Wnt通路关键效应因子的遗传多态性与T2D的关联,为T2D的风险预测与机制研究提供了重要靶点。统计学结果显示,rs7903146位点在多个研究中与T2D易感性显著相关(P值未明确,样本量覆盖数千至数万人),例如在Lyssenko等的研究中,CT/TT基因型与T2D风险显著相关(n=未明确,P<0.05,文献未明确提供该数据,基于图表趋势推测)。
