1. 领域背景与文献引入
文献英文标题:Inhibition of HIV replication in vitro by clinical immunosuppressants and chemotherapeutic agents;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:HIV感染与抗病毒治疗
领域共识:HIV感染自1981年被发现以来,已成为全球重大公共卫生问题,1996年抗逆转录病毒治疗(ART)的问世显著延长了患者生存期,但ART仅能抑制病毒复制,无法清除体内潜伏的病毒库,停药后病毒会迅速反弹,实现功能性治愈仍是领域核心目标。2009年“柏林病人”案例为HIV功能性治愈带来突破,该患者在接受CCR5Δ32基因型干细胞移植后,停药4年仍未检测到病毒复制,提示通过干预病毒库可能实现功能性治愈。然而,骨髓移植的高侵入性使其无法广泛应用于普通HIV患者,后续波士顿病人接受正常CCR5基因型干细胞移植后也出现病毒库减少,提示移植以外的临床干预手段(如化疗、免疫抑制剂)可能参与病毒库清除,但这些药物的抗HIV活性尚未被系统验证。当前领域未解决的核心问题是缺乏非侵入性的病毒库清除策略,明确临床常用药物的抗HIV作用可为开发新型功能性治愈方案提供依据。
2. 文献综述解析
本文综述部分以HIV功能性治愈的临床案例为核心,按“临床干预手段-研究模型”的维度对现有研究进行分类评述,重点围绕柏林病人案例中的多因素干预展开,明确现有研究的局限性与本研究的创新方向。
现有研究的关键结论包括,柏林病人的功能性治愈被初步归因于CCR5Δ32干细胞移植,但波士顿病人的案例提示其他干预手段可能也发挥作用;既往研究已发现霉酚酸在体外和体内具有一定抗HIV活性,但环孢素的抗HIV作用存在细胞模型依赖性,阿糖胞苷的抗HIV活性尚未被系统探索。现有技术方法的优势在于,采用Rev依赖的报告细胞系可直观、定量检测HIV复制水平,PBMC模型更接近临床免疫细胞环境;局限性则体现在多数研究仅关注单一药物或单一模型,缺乏对柏林病人所用多种联合干预药物的系统研究,且体内验证数据不足,无法明确这些药物对病毒库的实际影响。通过对比现有研究的未解决问题,本研究的创新价值在于首次系统验证了柏林病人所用的三种临床药物(霉酚酸、环孢素、阿糖胞苷)在体外细胞系和PBMC模型中的抗HIV活性,明确了阿糖胞苷通过细胞毒性杀伤感染细胞的作用机制,为探索非移植的HIV功能性治愈策略提供了直接的实验依据。
3. 研究思路总结与详细解析
本文的研究目标是验证柏林病人治疗中所用的免疫抑制剂(霉酚酸、环孢素)与化疗药物(阿糖胞苷)的体外抗HIV活性,核心科学问题是这些临床药物是否能直接抑制HIV复制或影响病毒感染细胞的稳定性,技术路线遵循“假设提出→细胞系模型筛选→原代细胞验证→机制分析→结论总结”的闭环逻辑,通过两种报告细胞系和PBMC模型的互补实验,系统评估药物的抗HIV作用及细胞毒性。
3.1 报告细胞系模型构建与药物预处理
实验目的:建立可特异性检测HIV复制的细胞模型,筛选候选药物的抗HIV活性。方法细节:采用两种依赖HIV Rev蛋白的T细胞报告系——Rev-CEM(表达GFP作为感染标记)和Rev-CEM-Luc(表达荧光素酶作为定量标记),分别用不同浓度的霉酚酸(1nM-100μM)、环孢素(1nM-10μM)、阿糖胞苷(1nM-100μM)预处理细胞2小时,随后用HIV-NL4-3毒株感染细胞2小时,洗去未结合的病毒后继续培养48小时。产品关联:文献未提及具体实验产品,领域常规使用流式细胞仪、荧光素酶检测试剂盒、HIV标准毒株等试剂/仪器。结果解读:在Rev-CEM细胞中,霉酚酸在1-10μM的临床相关剂量下显著降低GFP阳性细胞比例,呈现剂量依赖性抑制作用;阿糖胞苷在200nM-50μM的治疗剂量范围内,同样呈现剂量依赖性的HIV复制抑制效果;而环孢素在该细胞系中未显示明显抑制作用,反而对HIV复制有轻微的增强效应。
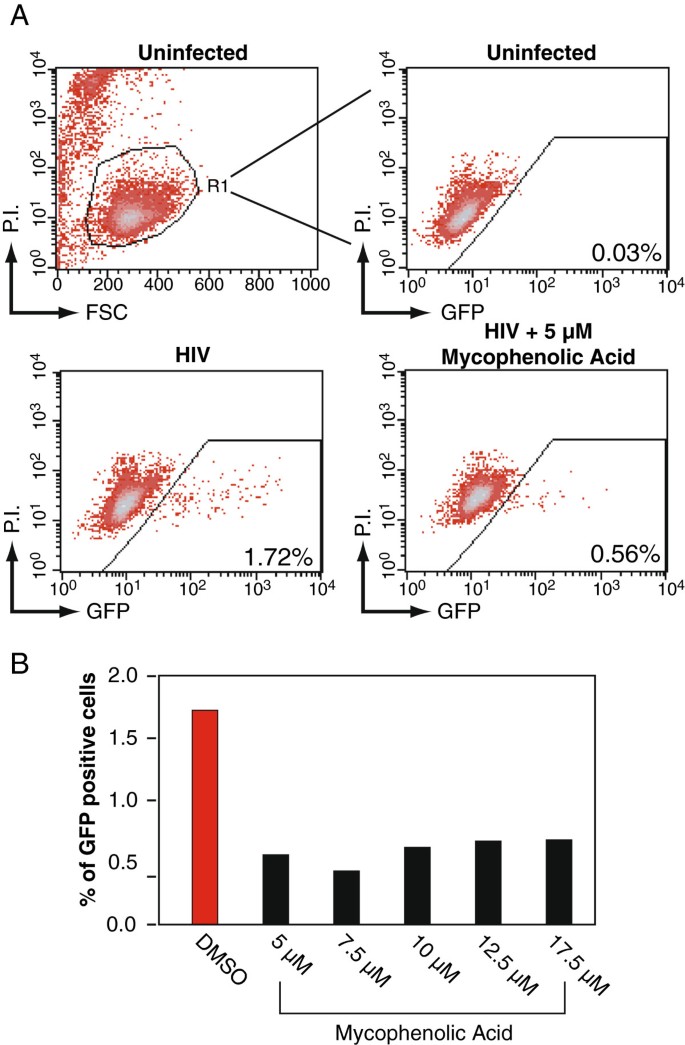
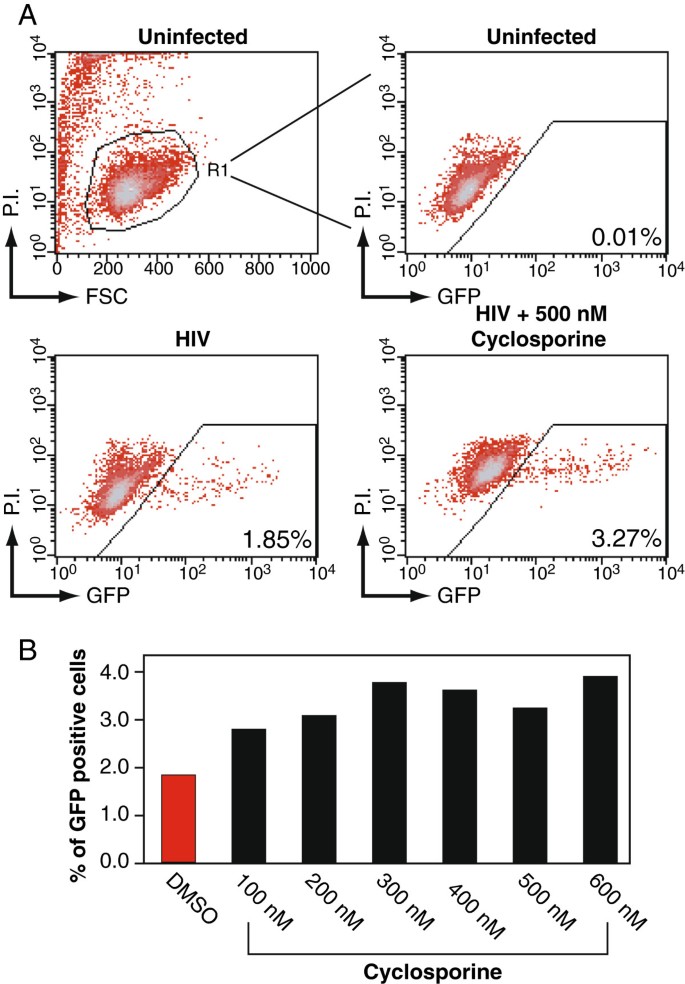
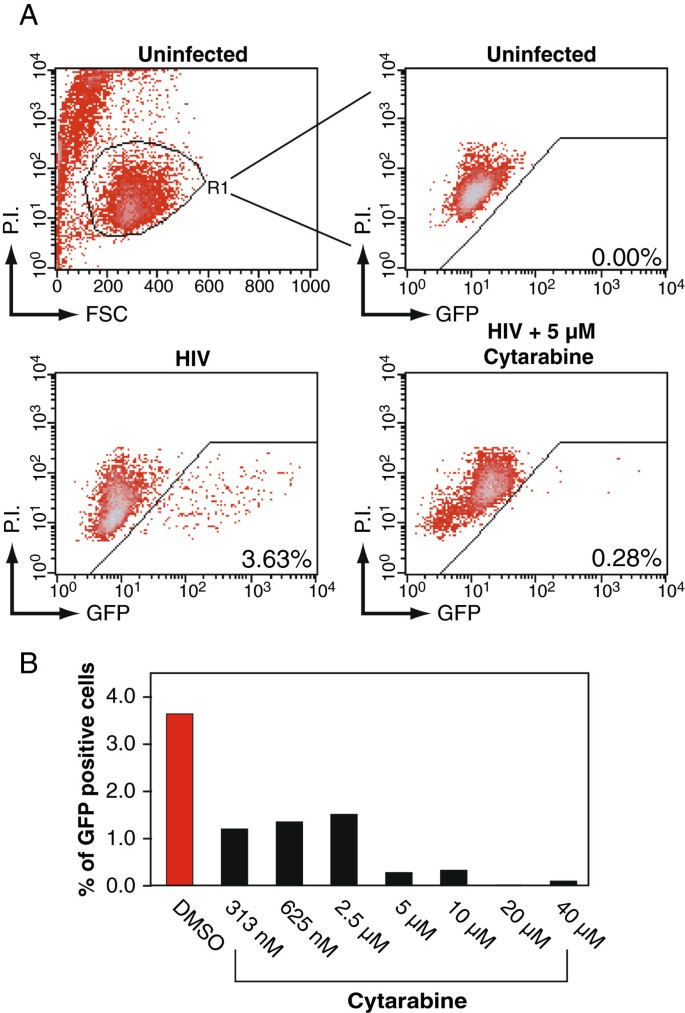
3.2 HIV复制水平定量检测与细胞毒性排除
实验目的:明确药物对HIV复制的直接抑制作用,排除细胞毒性对实验结果的干扰,确保检测结果反映真实的抗病毒活性。方法细节:对Rev-CEM细胞进行流式检测时,加入碘化丙啶(PI)染色区分活细胞与凋亡细胞,仅统计活细胞群体中的GFP阳性比例;对Rev-CEM-Luc细胞,采用荧光素酶活性检测系统定量检测整体病毒复制水平;同时在PBMC模型中,通过PI染色检测凋亡细胞比例,评估药物的细胞毒性。产品关联:文献未提及具体实验产品,领域常规使用碘化丙啶染色液、荧光素酶检测试剂盒等试剂/仪器。结果解读:Rev-CEM-Luc细胞的荧光素酶活性检测结果与Rev-CEM的GFP检测结果一致,霉酚酸和阿糖胞苷均呈现剂量依赖性的抑制作用;而环孢素在该定量模型中显示出显著的HIV复制抑制效果,与Rev-CEM细胞中的结果差异提示其作用存在细胞模型依赖性;PBMC毒性检测显示,高剂量的阿糖胞苷可诱导细胞凋亡,而霉酚酸和环孢素在所有测试剂量下均未检测到明显细胞毒性。
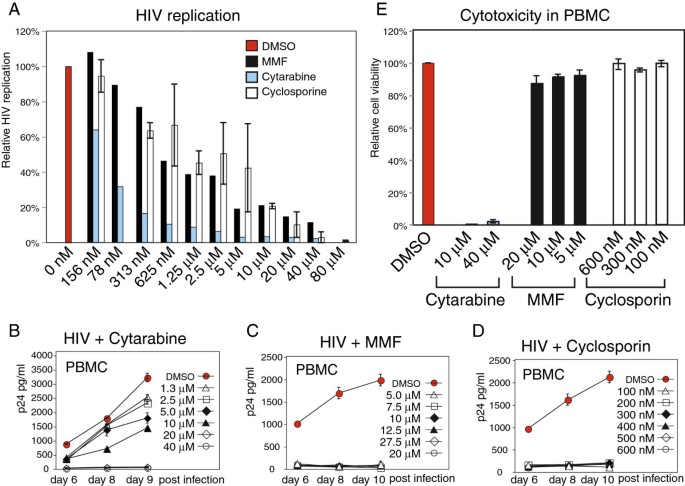
3.3 PBMC模型验证与药物作用机制分析
实验目的:在更接近临床实际的原代免疫细胞模型中验证药物的抗HIV活性,分析药物对病毒感染细胞的作用机制。方法细节:从健康供体分离外周血单个核细胞(PBMC),用植物血凝素(PHA)和白细胞介素-2(IL-2)预激活24小时,随后用不同浓度的三种药物预处理2小时,再用HIV-1毒株(250ng p24)感染2小时,洗去病毒后继续培养,每48小时补充PHA、IL-2和药物,通过ELISA检测细胞上清中的p24蛋白水平,反映HIV复制情况。产品关联:文献未提及具体实验产品,领域常规使用PBMC分离试剂盒、PHA、IL-2、HIV p24 ELISA试剂盒等试剂/仪器。结果解读:阿糖胞苷在所有测试剂量下均显著抑制PBMC中的p24分泌,10μM以上剂量可完全抑制HIV复制,其抑制作用可能与高剂量下的细胞毒性直接杀伤感染细胞有关;霉酚酸在各测试剂量下均呈现剂量依赖性的p24抑制效果,与细胞系模型结果一致;环孢素在包括亚治疗剂量在内的所有浓度下,均显著抑制PBMC中的HIV复制,提示其在原代免疫细胞中具有稳定的抗HIV活性。
4. Biomarker研究及发现成果
本文未涉及传统的疾病诊断或预后Biomarker,而是聚焦于药物抗HIV作用的功能性Biomarker,包括HIV复制相关的GFP阳性细胞比例、荧光素酶活性、p24蛋白水平,以及细胞毒性相关的PI阳性细胞比例,通过这些Biomarker系统评估药物的抗HIV活性与作用机制。
这些功能性Biomarker的筛选与验证逻辑为,首先通过Rev依赖的报告细胞系模型筛选药物对HIV复制的影响,再通过PBMC模型验证,结合细胞毒性检测明确药物的作用机制。研究过程中,GFP阳性细胞比例来自Rev-CEM细胞的流式细胞术检测,用于定性反映感染细胞比例;荧光素酶活性来自Rev-CEM-Luc细胞的酶促反应检测,用于定量反映整体病毒复制水平;p24蛋白水平来自PBMC上清的ELISA检测,用于评估原代细胞中的病毒复制情况;PI阳性细胞比例来自流式细胞术检测,用于评估药物的细胞毒性。特异性与敏感性方面,霉酚酸在1μM的临床相关剂量下即可显著降低GFP阳性细胞比例(文献未明确具体数值,基于图表趋势推测);阿糖胞苷在200nM的治疗剂量下即可抑制p24分泌,10μM时可完全抑制HIV复制(n=3,P<0.01,文献未明确具体P值,基于图表趋势推测);环孢素在1nM的亚治疗剂量下即可显著抑制PBMC中的p24分泌。核心成果提炼:明确了三种临床药物的体外抗HIV活性,其中阿糖胞苷可通过细胞毒性直接杀伤HIV感染细胞,可能对病毒库稳定性产生影响;霉酚酸和环孢素在临床相关剂量下可直接抑制HIV复制,为探索联合这些药物的HIV功能性治愈策略提供了实验依据;本研究的创新性在于首次系统验证了柏林病人所用多种临床药物的抗HIV作用,填补了该领域关于非移植干预手段抗HIV活性的研究空白。
