1. 领域背景与文献引入
文献英文标题:Musashi1 expression cells derived from mouse embryonic stem cells can be enriched in side population isolated by fluorescence activated cell sorter;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:干细胞生物学(胚胎干细胞分化与干细胞富集技术)
领域共识:胚胎干细胞(ESCs)具有自我更新能力与多向分化潜能,是细胞替代治疗与再生医学的核心种子细胞,1998年人ESCs建系为领域发展奠定基础,2000年后定向分化技术突破推动其向临床应用迈进,但异质分化细胞群体移植易引发畸胎瘤,成为限制临床转化的核心瓶颈。当前领域研究热点聚焦于开发高效、无外源基因整合的干细胞纯化策略,而肠道上皮干细胞(IESCs)与神经干细胞(NSCs)的共同标志物Musashi1(Msi1)阳性细胞,因缺乏特异性表面标志物,传统分离方法依赖pMsi1-GFP载体转染,操作复杂且受转染效率限制,大规模应用可行性不足,这一空白亟需填补。
针对上述问题,本研究旨在探索利用荧光激活细胞分选(FACS)分离侧群(SP)细胞的方法,富集小鼠ESC来源的Msi1阳性细胞,验证该策略的可行性与有效性,为干细胞纯化提供简便可靠的技术方案,推动ESC衍生干细胞的临床应用进程。
2. 文献综述解析
作者以干细胞纯化技术的操作复杂度与安全性为核心分类维度,系统梳理了领域内现有研究的优劣。传统基于细胞表面标志物的分选方法,如CD133、Lgr5等,虽能富集特定谱系干细胞,但IESCs与NSCs缺乏共有的特异性表面标志物,无法实现两类细胞的同步富集;转基因标记法如pMsi1-GFP载体,可精准标记Msi1阳性细胞,但依赖细胞转染技术,操作流程繁琐,且存在外源基因整合风险,样本处理规模受限,缺乏临床转化的安全性基础;SP细胞分选法基于干细胞的Hoechst33342染料外排能力,已在多种组织中成功富集干细胞,具有操作简便、无外源基因介入的优势,但此前未验证该方法是否适用于ESC来源的Msi1阳性细胞富集。
通过对比现有研究的局限性,本研究的创新价值凸显:首次将SP细胞分选法应用于ESC来源的Msi1高表达细胞群体,突破了传统方法的技术壁垒,无需转基因操作即可实现Msi1阳性细胞的高效富集,为IESCs与NSCs的分离纯化提供了新的技术范式,同时为细胞治疗的干细胞制备环节提供了更安全、简便的策略。
3. 研究思路总结与详细解析
本研究的核心目标是验证SP细胞分选法可富集ESC来源的Msi1阳性细胞,并确认其体内向神经与肠道上皮细胞分化的潜能;核心科学问题为SP细胞是否包含ESC来源的Msi1阳性细胞,且具备干细胞的多向分化特性;技术路线遵循“诱导分化→细胞分选→标志物验证→体内功能验证”的闭环逻辑,从细胞水平到动物水平系统验证研究假设。
3.1 小鼠ESC培养与Msi1高表达细胞诱导分化
实验目的:获得高比例的Msi1阳性细胞群体,为后续SP分选提供合格样本。
方法细节:采用无饲养层培养体系培养小鼠ES-E14TG2a细胞,通过悬滴法(32μL/滴,1×10^6细胞/mL)形成拟胚体(EBs),5天后将EBs用0.25%胰蛋白酶/EDTA消化,以1×10^5细胞/孔接种于6孔板,用含40ng/mL EGF的无血清培养基诱导分化5天,同时设置无EGF无血清培养基、含10%胎牛血清(FCS)的培养基作为对照组。
结果解读:实时定量RT-PCR结果显示,EGF诱导组Msi1 mRNA表达较ESC上调66.29±8.38倍(n=3,P<0.05),显著高于对照组;免疫细胞化学(IHC)结果显示,EGF组Msi1阳性细胞比例为21.1%±3.11%(n=3,P<0.05),显著高于对照组的5.93%±1.75%和6.3%±2.17%,表明EGF可有效诱导ESC分化为Msi1高表达细胞群体。
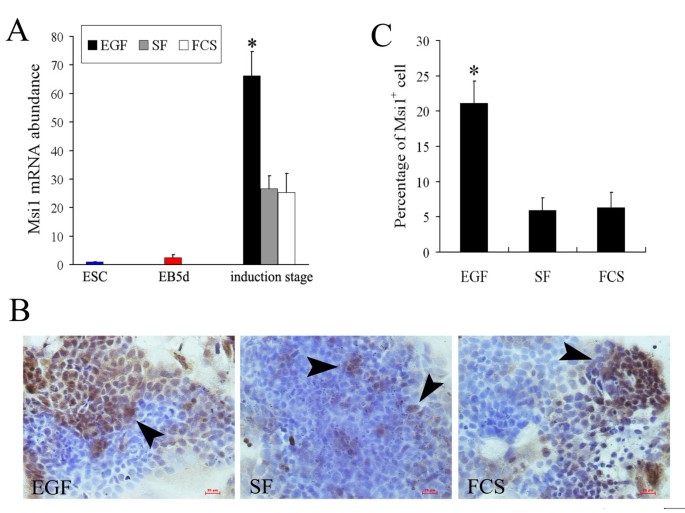
实验所用关键产品:DMEM培养基(GIBCO BRL)、EGF(CHEMICON International)、TRIzol®试剂(Invitrogen)、ReverTra Ace-α-®反转录试剂盒(Toyobo)、UltraSensitive™ S-P免疫细胞化学试剂盒(Maxin)等。
3.2 SP与NSP细胞的FACS分选与表型验证
实验目的:从Msi1高表达细胞中分选SP与非侧群(NSP)细胞,并验证SP表型的特异性。
方法细节:将Msi1高表达细胞用5μg/mL Hoechst33342染色90分钟,部分细胞预先用50μM维拉帕米处理以抑制ABC转运体功能,随后用Beckman Coulter EPICS ALTRA流式细胞仪,通过Hoechst蓝(405/30nm)与Hoechst红(670/30nm)双参数分析识别SP细胞,分选获得SP与NSP细胞。
结果解读:FACS分析显示,EGF组SP细胞比例为19.97%±3.76%(n=3,P<0.05),显著高于对照组的9.33%±2.71%和5.3%±0.5%;维拉帕米处理后,EGF组SP细胞比例下降35.9%±6.8%(n=3,P<0.05),表明SP表型依赖ABC转运体的染料外排功能,具有干细胞的典型特性。
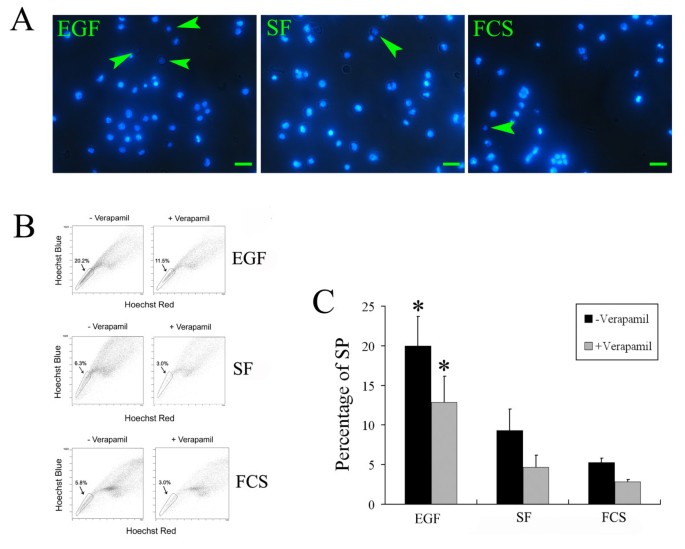
实验所用关键产品:Hoechst33342(Sigma-Aldrich)、维拉帕米(Sigma-Aldrich)、Beckman Coulter EPICS ALTRA流式细胞仪等。
3.3 SP与NSP细胞中Msi1及干细胞标志物的表达验证
实验目的:确认SP细胞中Msi1阳性细胞的富集效果,并检测其他干细胞标志物的表达水平。
方法细节:采用实时定量RT-PCR检测Msi1、IESCs标志物(Lgr5、Hes1、Bmi1、Ascl2)、NSCs标志物(Sox2、Nestin)的mRNA表达;Western blot检测Msi1蛋白表达;RT-PCR检测ABC转运体ABCG2的mRNA表达。
结果解读:实时定量RT-PCR显示,SP细胞中Msi1 mRNA表达较未分选细胞上调6.34±1.58倍(n=3,P<0.05),而NSP细胞仅为0.05±0.02倍;Western blot结果显示,SP细胞中Msi1蛋白表达显著高于NSP细胞(n=3,P<0.05),NSP细胞中未检测到Msi1蛋白条带;此外,SP细胞中Lgr5、Hes1、Bmi1、Nestin的mRNA表达均显著高于NSP细胞(n=3,P<0.05);ABCG2在SP、NSP与未分选细胞中表达无显著差异(n=3,P>0.05),表明SP表型可能由多种ABC转运体共同介导,而非单一ABCG2作用。
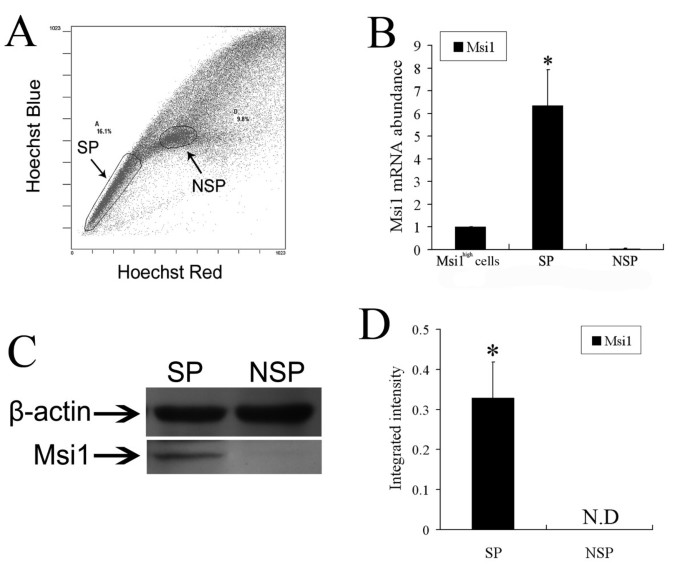
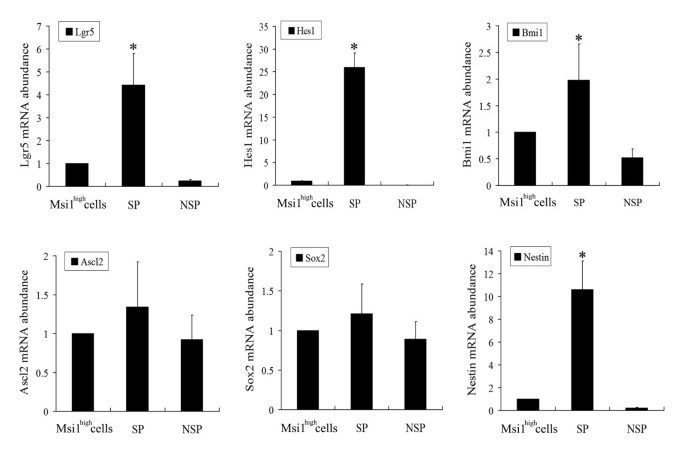
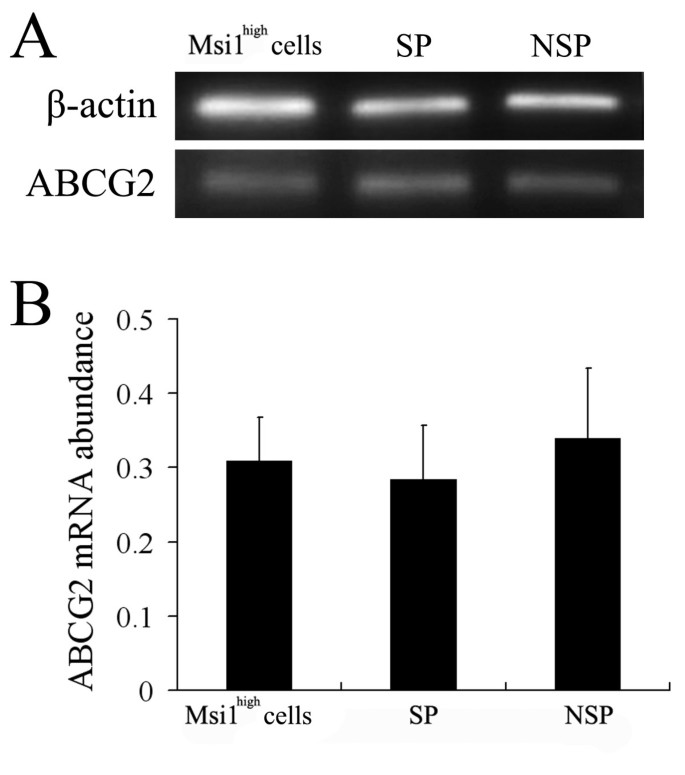
实验所用关键产品:Msi1多克隆抗体(CHEMICON International)、β-actin抗体(Cell Signaling Technology)、ECL化学发光检测系统、PrimeScript™ 1st Strand cDNA Synthesis试剂盒(TaKaRa)等。
3.4 SP与NSP细胞体内分化潜能验证
实验目的:确认SP细胞具备向神经与肠道上皮细胞分化的干细胞特性。
方法细节:将分选后的SP与NSP细胞(1.5×10^6个/只)皮下移植到NOD/SCID小鼠背部,2周后处死小鼠,取移植物进行苏木精-伊红(H&E)染色、免疫组化与RT-PCR检测。
结果解读:组织学分析显示,SP细胞移植物中存在腺样、神经管样与囊状结构,而NSP细胞移植物主要为纤维组织;RT-PCR显示,SP移植物中神经标志物Nestin、Tubulin β III与肠道上皮标志物SI、Fabp2、Tff3、Lyz1的mRNA表达显著高于NSP移植物(n=3,P<0.05);免疫组化结果显示,SP移植物中Tubulin β III阳性神经细胞与Fabp2阳性肠道吸收细胞数量显著多于NSP移植物,部分Fabp2阳性细胞形成类似肠道隐窝的单层囊状结构,表明SP细胞可在体内分化为成熟的神经与肠道上皮组织。
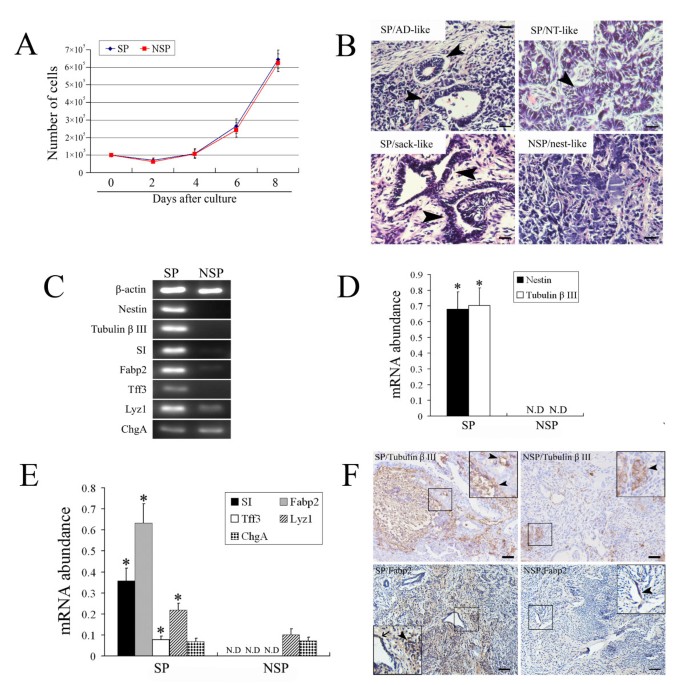
实验所用关键产品:Tubulin β III抗体(Epitomics)、Fabp2抗体(Abcam)、UltraSensitive™ S-P免疫组化试剂盒(Maxin)等。
4. Biomarker研究及发现成果解析
Biomarker定位:本研究的核心Biomarker为Msi1,属于胞质与核内表达的RNA结合蛋白,是IESCs与NSCs的共同功能标志物;筛选与验证逻辑为:先通过EGF诱导ESC分化获得Msi1高表达细胞群体→利用SP细胞分选法富集目标细胞→从mRNA、蛋白水平验证Msi1在SP细胞中的富集效率→体内移植验证其分化潜能,形成完整的验证链条。
研究过程详述:该Biomarker的来源为小鼠ESC经EGF诱导分化5天的Msi1高表达细胞群体;验证方法包括实时定量RT-PCR、Western blot检测Msi1的mRNA与蛋白表达水平,免疫细胞化学检测细胞阳性比例,体内移植实验验证其功能特性;特异性与敏感性数据显示,SP细胞中Msi1 mRNA表达较未分选细胞上调6.34倍(n=3,P<0.05),蛋白表达仅在SP细胞中显著检测到,NSP细胞中未检测到阳性条带,表明SP细胞对Msi1阳性细胞的富集特异性与敏感性均较高。
核心成果提炼:本研究首次发现,SP细胞分选法可从ESC来源的Msi1高表达细胞中富集几乎所有Msi1阳性细胞,且该SP细胞群体具备向神经与肠道上皮细胞分化的潜能;其创新性在于突破了传统方法的技术限制,无需转基因操作即可实现Msi1阳性细胞的高效富集,为IESCs与NSCs的分离纯化提供了新的技术路径;统计学结果显示,SP细胞中Msi1 mRNA表达显著高于NSP细胞与未分选细胞(P<0.05),体内移植物中神经与肠道上皮标志物表达均显著高于NSP组(P<0.05),充分验证了该策略的有效性。
