1. 领域背景与文献引入
文献英文标题:Comparing chemical transfection, electroporation, and lentiviral vector transduction to achieve optimal transfection conditions in the Vero cell line;发表期刊:BMC Molecular and Cell Biology;影响因子:未公开;研究领域:细胞生物学-细胞转染技术优化
细胞转染是将外源核酸导入细胞以研究基因功能、制备重组蛋白及疫苗的核心技术,其发展历经多个关键节点:1973年磷酸钙共沉淀法的建立开启了真核细胞转染的先河,1980年代脂质体转染试剂的问世大幅提升了转染效率与普适性,2000年后病毒载体转染及电穿孔技术的优化进一步拓展了难转染细胞系的研究范围。当前领域研究热点聚焦于高效低毒的非病毒转染试剂开发、针对特定细胞系的个性化转染方案优化,以及转染过程中核酸胞内运输机制的解析。然而,不同细胞系的生理特性差异极大,现有转染方案的效率和毒性表现参差不齐,尤其是Vero细胞系作为世界卫生组织推荐的疫苗生产首选连续细胞系,其标准化高效转染方案的缺失,已成为制约疫苗研发、病毒学研究及基因功能分析的核心瓶颈。
针对Vero细胞系转染方法缺乏系统对比、最优条件不明确的研究空白,本研究通过平行对比化学转染、电穿孔及慢病毒载体转导三种主流方法的转染效率与细胞毒性,筛选出适配Vero细胞系的最优转染策略,为基于Vero细胞的疫苗生产及基础研究提供了标准化的技术支撑,具有重要的应用价值与学术必要性。
2. 文献综述解析
作者以转染方法的技术类型为分类维度,系统梳理了细胞转染领域的现有研究成果,明确不同转染技术的优势、局限性及适用场景,并针对性指出Vero细胞系转染研究的空白。
化学转染是当前应用最广泛的非病毒转染技术,其中阳离子脂质体(如Lipofectamine系列)试剂具有操作简便、细胞毒性较低的优势,已被广泛应用于多种细胞系,但针对Vero细胞的转染效率数据零散且缺乏系统性;阳离子聚合物(如PEI)转染效率较高,但对部分细胞系的毒性较强,可能影响后续实验结果。物理转染中的电穿孔技术依赖电场脉冲在细胞膜上形成微孔,适合转染难转染的悬浮细胞或原代细胞,但其细胞毒性高,且电压、缓冲液等条件的优化过程复杂,不同细胞系的最优参数差异显著。病毒载体转染以慢病毒为代表,具有转染效率高、可实现外源基因长期稳定表达的优势,适用于基因治疗及长期功能研究,但存在生物安全风险,且部分灵长类细胞系(如Vero)中存在天然的病毒限制因子(如TRIM5α蛋白),会显著抑制慢病毒的复制与转染效率。现有研究的局限性在于,缺乏针对Vero细胞系的三种主流转染方法的系统对比研究,不同研究的实验条件不统一,难以直接比较各方法的优劣,导致Vero细胞的转染实验缺乏标准化的参考方案。
本研究的创新点在于首次在统一实验条件下,系统对比了化学转染、电穿孔及慢病毒转导三种方法在Vero细胞系中的转染效率与细胞毒性,明确了最优的化学转染试剂及具体参数,填补了Vero细胞系转染方案标准化的研究空白,为基于Vero细胞的相关研究提供了可靠的技术依据。
3. 研究思路总结与详细解析
本研究的核心目标是筛选并建立Vero细胞系的最优转染方法及条件,核心科学问题是不同转染技术在Vero细胞中的效率差异及潜在机制,技术路线遵循“实验体系建立→多方法条件优化→效率与毒性评估→综合对比分析→结论”的闭环逻辑,通过GFP报告基因系统量化转染效率,结合细胞活力检测评估毒性,最终确定最优转染策略。
3.1 细胞培养与质粒制备
实验目的是建立标准化的Vero细胞培养体系,获得高纯度的转染用重组质粒,为后续转染实验奠定基础。方法细节:Vero细胞购自伊朗国家细胞库,采用含10%热灭活胎牛血清、0.1mg/mL链霉素及100U/mL青霉素的DMEM培养基,在37℃、5%CO2的 humidified培养箱中连续传代培养;携带GFP报告基因与嘌呤霉素筛选标记的pCDH-CMV-MCS-EF1-CopGFP-T2A-Puro质粒,使用Qiagen Miniprep质粒纯化试剂盒提取,通过紫外-可见分光光度计检测质粒浓度与纯度,合格后于-20℃保存备用。结果解读:成功获得状态稳定、增殖活性良好的Vero细胞系,以及纯度与浓度符合转染要求的重组质粒,确保后续实验的可重复性与可靠性。产品关联:实验所用关键产品:Gibco的DMEM培养基、胎牛血清,Qiagen的Miniprep质粒纯化试剂盒。
3.2 化学转染方法的条件优化
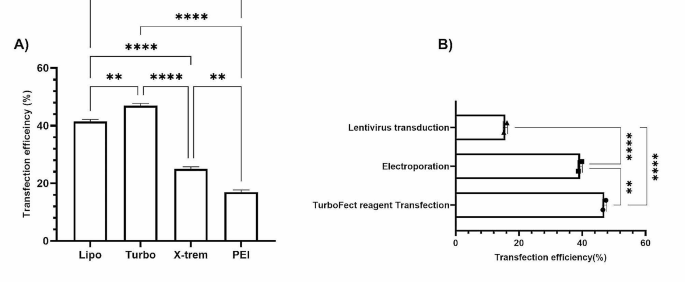
实验目的是筛选适配Vero细胞系的最优化学转染试剂及DNA-试剂比例,平衡转染效率与细胞毒性。方法细节:选取Lipofectamine™2000、TurboFect™、X-tremeGENE™9、PEI MAX®四种商业化化学转染试剂,设置0.5μg、1μg、2μg三种质粒剂量,以及1μL、2μL、4μL三种试剂剂量,共9种DNA-试剂比例组合;将6×10^4个Vero细胞接种于24孔板,贴壁过夜后进行转染,转染复合物在OptiMEM培养基中室温孵育30分钟后加入细胞,4小时后更换含10%胎牛血清的完全培养基;72小时后采用流式细胞术检测GFP阳性细胞比例以评估转染效率,台盼蓝排斥法检测细胞活力,所有实验重复3次。结果解读:TurboFect™在1μg质粒与4μL试剂的比例下表现出最高转染效率,GFP阳性细胞比例为46.5%(n=3,P≤0.05),同时细胞活力保持在94%左右;Lipofectamine™2000的最优条件为1μg质粒与2μL试剂,转染效率为41%(n=3,P≤0.05),细胞活力约93%;X-tremeGENE™9的最优转染效率为24.5%(n=3,P≤0.05),细胞活力约91%;PEI MAX®的最优转染效率为16.5%(n=3,P≤0.05),细胞活力约89%,且其细胞毒性显著高于其他三种试剂。
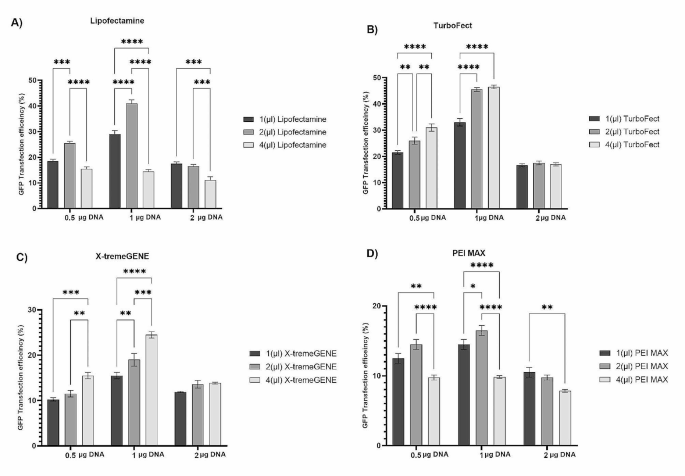
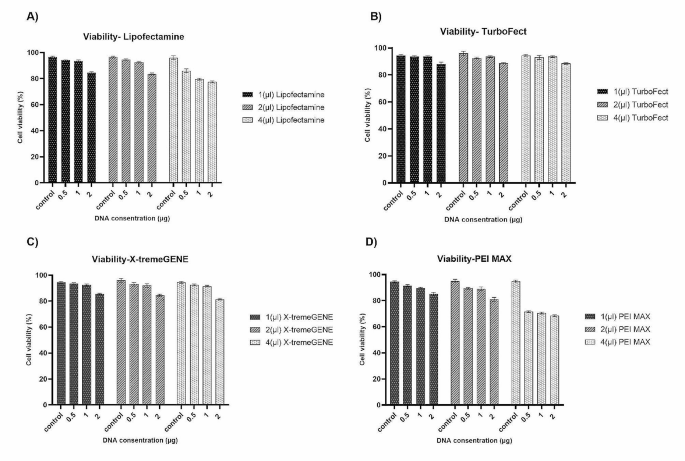
产品关联:实验所用关键产品:Invitrogen的Lipofectamine™2000、TurboFect™,Sigma-Aldrich的X-tremeGENE™9,Polysciences的PEI MAX®,Partec的流式细胞仪。
3.3 电穿孔转染的条件优化
实验目的是筛选电穿孔技术在Vero细胞系中的最优电压与缓冲液条件,提升转染效率并降低细胞毒性。方法细节:设置200V、300V、400V三种电压梯度,以及三种不同成分的电穿孔缓冲液(Ebuffer1含140mM氯化钠与pH7.3的磷酸氢二钠;Ebuffer2含10mM HEPES缓冲盐与272mM蔗糖磷酸缓冲液;Ebuffer3含RPMI1640、10mM磷酸氢二钾、1mM氯化镁与250mM蔗糖,pH7.3);收集对数生长期的Vero细胞,调整浓度为1×10^6个/mL,与5μg质粒混合后加入4mm间隙电穿孔杯,采用Bio-Rad Gene Pulser Xcell电穿孔仪进行方波脉冲(850μF,100Ω,20ms);电穿孔后立即将细胞转移至含12%胎牛血清的完全培养基中培养,72小时后检测GFP阳性细胞比例与细胞活力,所有实验重复3次。结果解读:三种缓冲液在300V电压下均表现出最高转染效率,其中Ebuffer3的转染效率为38.8%(n=3,P≤0.01),但细胞活力仅约67%;400V电压下细胞出现不可逆损伤,死亡率显著升高,转染效率降低;200V电压不足以在细胞膜上形成有效微孔,外源核酸难以进入细胞,转染效率最低。
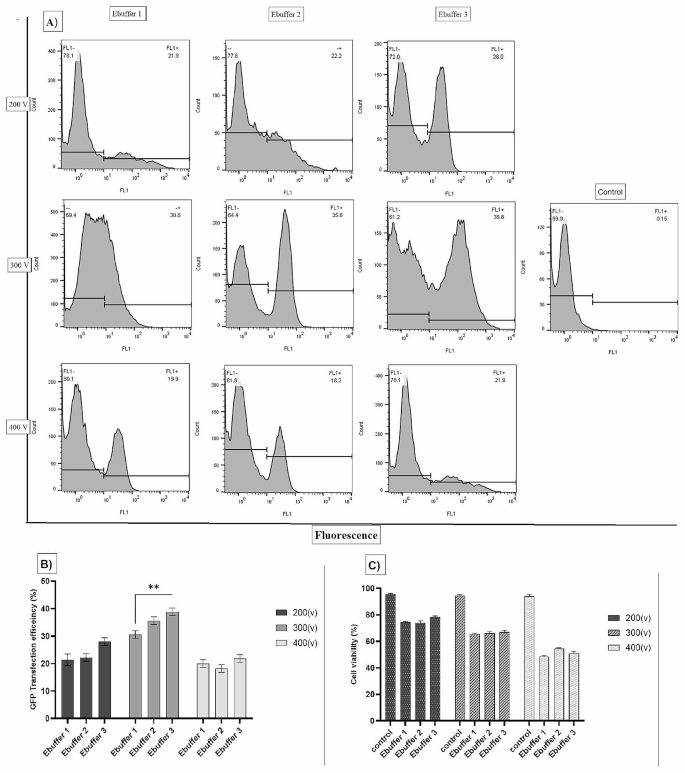
产品关联:实验所用关键产品:Bio-Rad的Gene Pulser Xcell电穿孔仪,Partec的流式细胞仪。
3.4 慢病毒载体转染的效率评估
实验目的是评估HIV-1来源慢病毒载体在Vero细胞系中的转染效率,明确其适用性。方法细节:在HEK293 Lenti-X细胞中包装慢病毒载体,共转染pCDH-CMV-MCS-EF1-CopGFP-T2A-Puro转移质粒、pMD2G包膜质粒(表达VSV-G蛋白)与psPAX2包装质粒(表达Gag-pol与Tat蛋白);转染后48小时与72小时收集细胞上清,经0.22μm滤膜过滤后,通过50,000×g超速离心4小时浓缩病毒颗粒,重悬于高糖DMEM中并于-80℃保存;将6×10^4个Vero细胞接种于24孔板,次日加入含8μg/mL polybrene的不同稀释度(1、4、16、64)病毒液,6小时后更换完全培养基,72小时后检测GFP阳性细胞比例,根据公式计算病毒滴度,所有实验重复3次。结果解读:慢病毒转染的最高效率为15.2%(病毒稀释度为1时,n=3,P≤0.05),病毒滴度为1.9×10^5 TU/mL;转染效率显著低于化学转染与电穿孔,推测其原因是Vero细胞中的TRIM5α蛋白作为天然免疫限制因子,通过泛素连接酶活性抑制慢病毒衣壳的解聚与基因组整合。
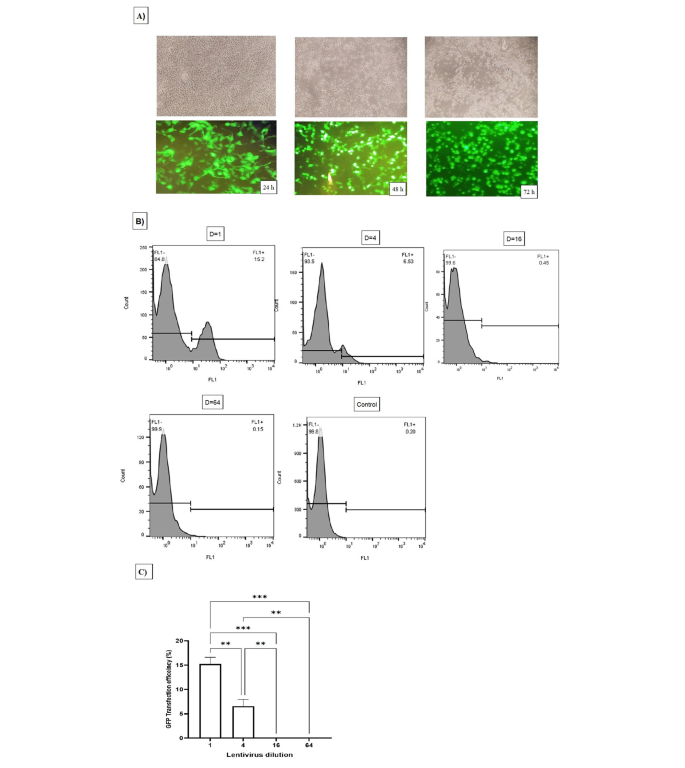
产品关联:实验所用关键产品:Addgene的pMD2G、psPAX2质粒,Sigma-Aldrich的polybrene,Partec的流式细胞仪。
3.5 三种转染方法的综合对比分析
实验目的是系统对比三种转染方法在Vero细胞系中的表现,确定最优转染策略。方法细节:整合三种转染方法的最优条件下的转染效率与细胞活力数据,采用双向ANOVA进行统计学分析,比较组间差异。结果解读:TurboFect™化学转染的效率显著高于电穿孔与慢病毒转导(P≤0.05),同时保持了较高的细胞活力;电穿孔的转染效率仅次于TurboFect™,但细胞毒性过高;慢病毒转导的效率最低,不适用于Vero细胞系的常规转染实验。综合效率与毒性表现,TurboFect™是Vero细胞系的最优转染选择。
4. Biomarker研究及发现成果解析
本研究以绿色荧光蛋白(GFP)为报告型Biomarker,建立了Vero细胞系转染效率的定量评估体系,通过GFP的表达水平精准区分不同转染方法与条件的效率差异,为转染实验的标准化评估提供了可靠工具。
本研究中涉及的Biomarker为重组表达的绿色荧光蛋白(GFP),属于报告型Biomarker,其筛选与验证逻辑为:基于CMV启动子构建携带GFP编码序列的重组质粒→将质粒通过不同转染方法导入Vero细胞→通过流式细胞术定量检测GFP阳性细胞比例,评估转染效率的高低,形成“载体构建→转染导入→定量检测”的完整验证链条。
GFBiomarker来源于pCDH-CMV-MCS-EF1-CopGFP-T2A-Puro重组质粒,其表达由CMV强启动子驱动,仅在成功转染外源质粒的Vero细胞中特异性表达;验证方法采用流式细胞术定量检测GFP阳性细胞的比例,该方法具有高灵敏度与高特异性,可精准量化低至1%左右的阳性细胞比例(文献未明确提供具体敏感性数据,基于图表趋势推测);同时通过荧光显微镜定性观察GFP的表达分布,辅助验证转染效果。
GFP作为报告Biomarker,成功实现了不同转染方法与条件下Vero细胞转染效率的精准量化,明确TurboFect™在1μg质粒与4μL试剂的条件下,转染效率达到46.5%(n=3,P≤0.05),细胞活力保持94%,是Vero细胞系的最优转染方案;其创新性在于首次系统利用GFP报告Biomarker对比三种主流转染方法在Vero细胞中的表现,建立了标准化的转染效率评估体系,为基于Vero细胞的相关研究提供了可靠的技术参考;此外,研究还发现Vero细胞中的TRIM5α蛋白是慢病毒转染效率低的关键限制因子,为后续慢病毒载体的改造提供了方向。
