1. 领域背景与文献引入
文献英文标题:Acetylation of C-terminal lysines modulates protein turnover and stability of Connexin-32;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:细胞生物学与神经生物学交叉领域,聚焦间隙连接蛋白32(Cx32)的翻译后修饰与功能调控。
间隙连接蛋白家族是一类介导细胞间通讯的整合膜蛋白,目前已发现21种同源蛋白,形成的间隙连接通道可允许小分子和离子在细胞间扩散,同时还参与细胞增殖、自噬、迁移等不依赖通道的生理过程。领域发展关键节点可追溯至1984年,Warner等首次证实间隙连接蛋白抗体可阻断两栖类胚胎的细胞间通讯,后续研究逐渐揭示磷酸化、泛素化等翻译后修饰对间隙连接蛋白功能的调控作用,但乙酰化修饰的研究相对滞后。当前研究热点集中于间隙连接蛋白的非通道功能及翻译后修饰的调控机制,未解决的核心问题包括Cx32的乙酰化修饰是否存在、如何调控其蛋白稳定性,以及这些修饰在X连锁腓骨肌萎缩症(CMT1X)中的病理作用。
Cx32主要表达于肝脏、胰腺、胃肠道上皮及中枢和周围神经系统的胶质细胞,其突变是CMT1X的致病原因,然而Cx32 C端结构域的翻译后修饰调控机制尚不明确。本研究针对Cx32 C端赖氨酸的乙酰化修饰展开系统研究,旨在揭示其对蛋白稳定性、泛素化及细胞增殖的调控作用,为CMT1X的发病机制提供新的分子靶点,同时填补间隙连接蛋白乙酰化修饰研究的空白。
2. 文献综述解析
作者以间隙连接蛋白的功能分类(通道依赖、通道非依赖)为核心评述逻辑,系统梳理了间隙连接蛋白家族的研究现状,重点聚焦Cx32的组织分布、疾病关联及翻译后修饰的研究进展,明确了现有研究的局限性与本研究的创新方向。
现有研究已证实间隙连接蛋白介导的细胞间通讯参与多种生理过程,同时其非通道功能在细胞增殖调控中发挥重要作用;Cx32的磷酸化修饰已有报道,但其对蛋白稳定性的调控机制尚未完全阐明,乙酰化修饰的研究更是处于空白状态。既往研究多采用细胞模型结合电生理技术验证通道功能,技术优势在于可直接检测间隙连接的电导特性,但局限性在于对翻译后修饰的调控机制研究不足,尤其是缺乏对Cx32乙酰化修饰的系统分析,且未明确其对非通道功能的调控作用。
通过对比现有研究的空白,本研究的创新点在于首次发现Cx32 C端存在5个赖氨酸乙酰化靶点,揭示了乙酰化修饰通过调控泛素化影响蛋白周转的分子机制,同时证实该修饰参与通道非依赖的细胞增殖调控,为间隙连接蛋白的翻译后修饰研究提供了新的范式,也为CMT1X的发病机制研究提供了新的分子视角。
3. 研究思路总结与详细解析
本研究的整体框架以“乙酰化修饰鉴定-靶点功能验证-生理效应解析”为逻辑闭环,研究目标是明确Cx32 C端赖氨酸乙酰化修饰对其稳定性、泛素化及功能的调控作用,核心科学问题是Cx32乙酰化修饰如何协调蛋白周转与细胞增殖的非通道功能,技术路线涵盖HDAC抑制剂处理、定点突变、免疫印迹、脉冲追踪、电生理及细胞增殖实验等多维度验证。
3.1 HDAC6抑制对Cx32蛋白水平的调控
实验目的:验证Cx32是否存在乙酰化修饰,并明确HDAC6对其蛋白水平的调控作用。方法细节:采用瞬时转染Cx32的神经母细胞瘤细胞系(Neuro2A,N2a),分别用广谱组蛋白去乙酰化酶(HDAC)抑制剂曲古抑菌素A(TSA)和HDAC6特异性抑制剂Tubastatin A(TubA)处理,通过免疫印迹(Western blot)检测Cx32蛋白表达水平,用35-S甲硫氨酸/半胱氨酸脉冲追踪实验检测蛋白半衰期,用细胞表面生物素化实验检测膜定位Cx32的稳定性,同时通过免疫荧光共聚焦成像观察Cx32的细胞内分布。结果解读:TSA处理使Cx32蛋白水平较对照组升高2.5倍(文献未明确样本量,基于图表趋势推测);TubA处理使Cx32水平升高3.7±0.35倍(n=5,P<0.05);35-S脉冲追踪显示,TubA处理后Cx32的半衰期显著延长,1.5小时后蛋白剩余量从对照组的40%升至79%(n=4,P<0.05);细胞表面生物素化实验显示,TubA处理1.5小时后,膜定位Cx32的剩余量为82%±12%(n=3,P<0.05),而对照组仅为48%±5.5%(n=3,P<0.05);免疫荧光成像显示,TubA处理后Cx32在细胞表面和胞质中均出现明显积累。产品关联:实验所用关键产品:抗Cx32抗体(clone 7c6.7c)、抗乙酰化赖氨酸抗体(Cell Signaling Technologies)、抗泛素抗体(Covance)、Lipofectamine LTX转染试剂(Invitrogen)、Zeiss LSM 700共聚焦显微镜。
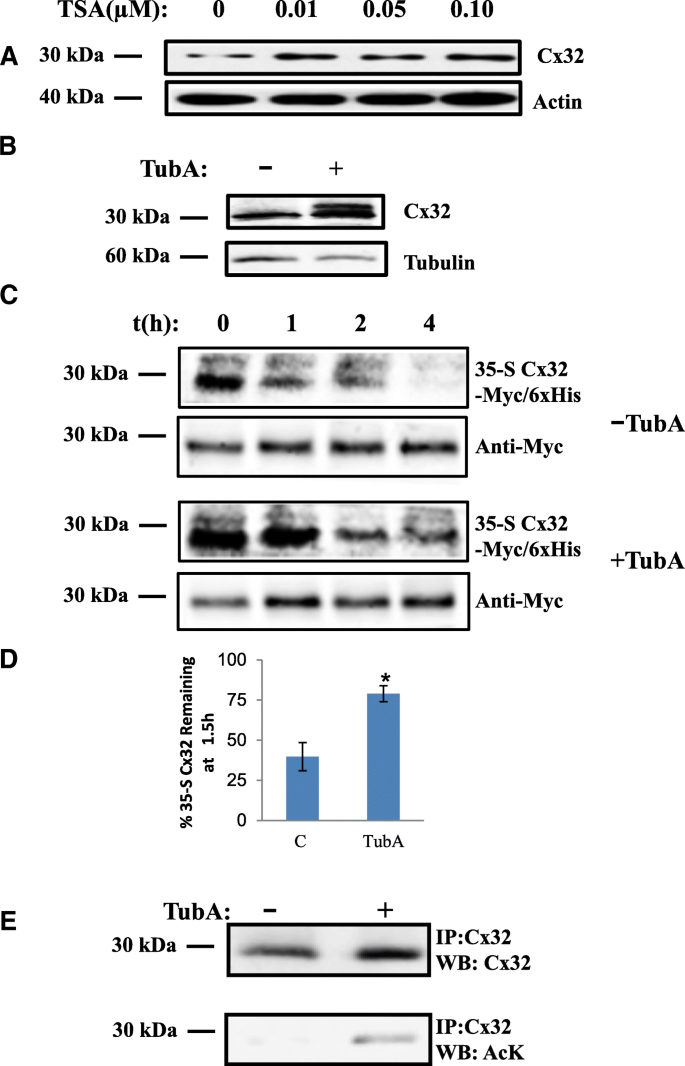
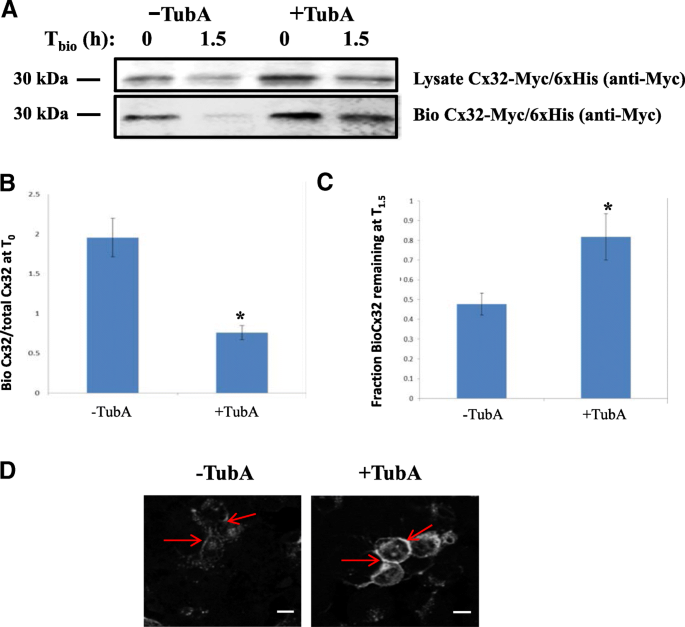
3.2 C端赖氨酸乙酰化靶点的鉴定
实验目的:筛选Cx32上的乙酰化修饰靶点,明确其对HDAC6抑制剂响应的调控作用。方法细节:构建Cx32胞质环和C端结构域的赖氨酸-精氨酸(K→R)点突变体(阻断乙酰化)、赖氨酸-谷氨酰胺(K→Q)点突变体(模拟乙酰化),以及C端5个赖氨酸同时突变的5R(全部K→R)和5Q(全部K→Q)突变体,将这些突变体转染N2a细胞后用TubA处理,通过免疫印迹检测Cx32蛋白水平,通过免疫沉淀结合乙酰化抗体检测乙酰化水平。结果解读:胞质环的K→R突变体对TubA的响应与野生型无显著差异,而C端单个K→R突变体均不同程度降低了TubA诱导的Cx32积累;5R突变体完全不响应TubA处理,蛋白水平无明显变化,而5Q突变体仍能被TubA诱导升高蛋白水平;免疫沉淀实验显示,5R突变体的乙酰化水平不随TubA处理升高,而5Q突变体的乙酰化水平虽低于野生型,但仍能被TubA诱导显著升高。产品关联:实验所用关键产品:Genetailor定点突变试剂盒(Invitrogen)、抗Myc标签抗体(AbCam)、Protein G-琼脂糖珠(Pierce)。
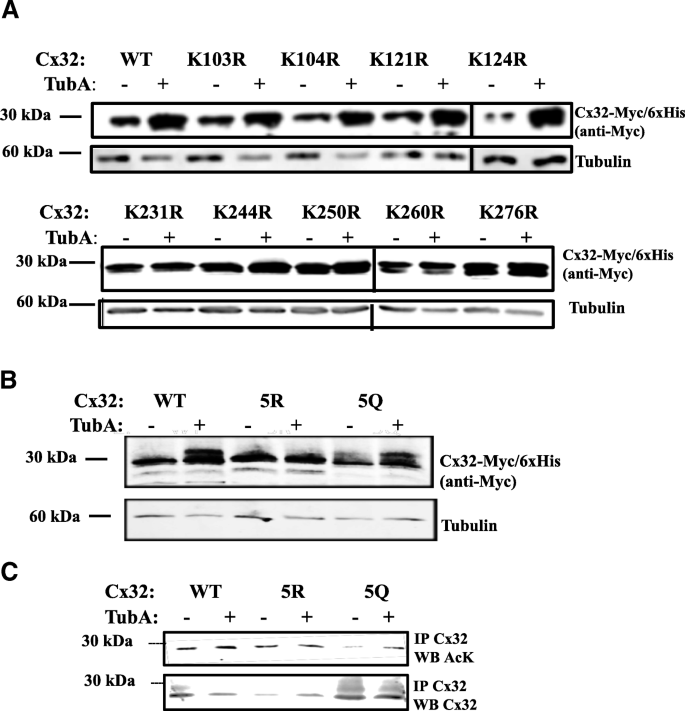
3.3 C端赖氨酸修饰对Cx32泛素化与蛋白周转的调控
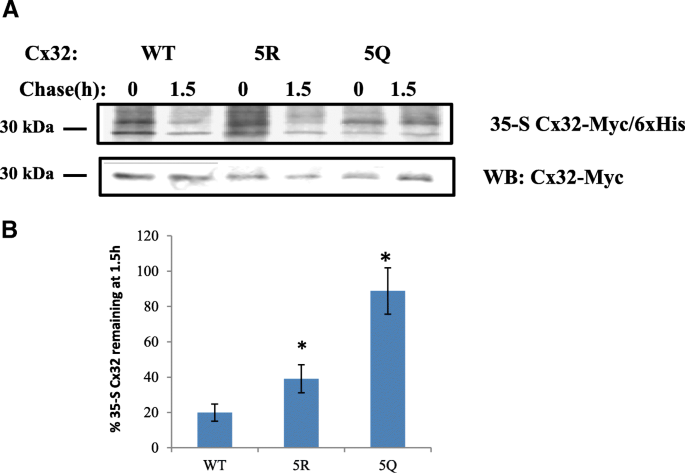
实验目的:验证C端赖氨酸的乙酰化修饰是否调控Cx32的泛素化修饰及蛋白周转速率。方法细节:对转染野生型、5R和5Q突变体的N2a细胞,通过免疫沉淀结合泛素抗体检测Cx32的泛素化水平,通过35-S脉冲追踪实验检测不同突变体的蛋白周转速率。结果解读:5Q突变体的泛素化水平仅为野生型的15%±2%(n=3,P<0.05),5R突变体的泛素化水平为野生型的47%±15%(n=3,P<0.05);35-S脉冲追踪显示,5Q突变体的蛋白周转速率最慢,1.5小时后蛋白剩余量显著高于5R突变体和野生型(n=3,P<0.05),5R突变体的蛋白剩余量也显著高于野生型(n=3,P<0.05)。产品关联:实验所用关键产品:35-S甲硫氨酸/半胱氨酸标记混合物(Perkin Elmer)、HisPur-Co2+琼脂糖珠(Pierce)、Storm磷成像仪(GE Life Sciences)。
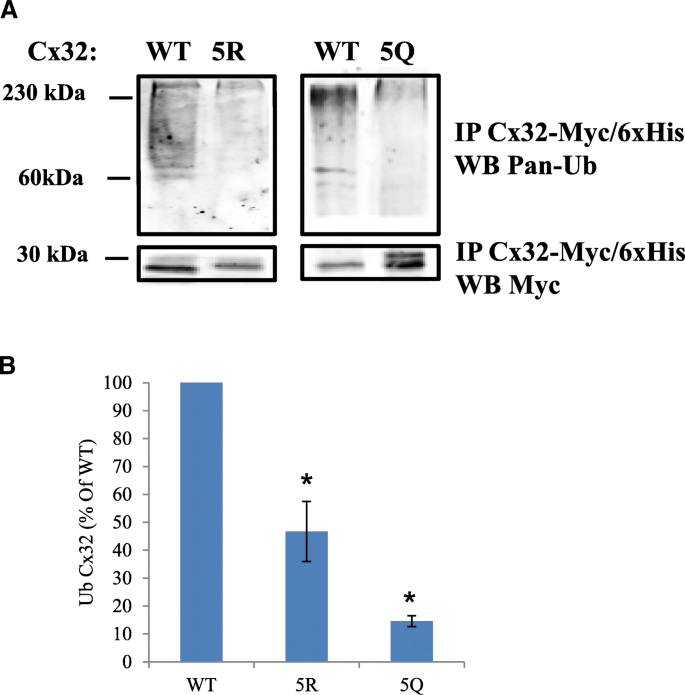
3.4 C端赖氨酸修饰对间隙连接通道功能的影响
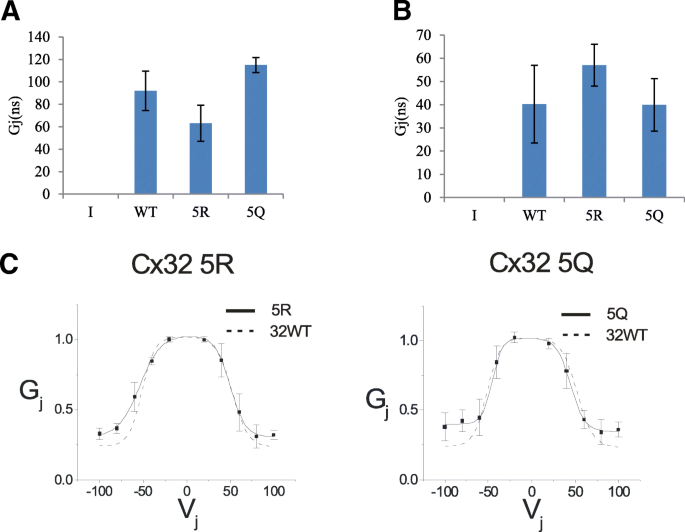
实验目的:验证C端赖氨酸的乙酰化修饰是否影响Cx32介导的间隙连接通道功能。方法细节:对转染野生型、5R和5Q突变体的N2a细胞,采用双细胞膜片钳技术检测跨膜连接电导(Gj)及电压门控特性,通过辛醇处理验证连接的特异性(辛醇可阻断间隙连接通道)。结果解读:5R和5Q突变体的跨膜连接电导与野生型无显著差异,说明突变体仍能形成功能性间隙连接;电压门控曲线分析显示,突变体的门控特性与野生型相似,表明C端赖氨酸的修饰不影响Cx32通道的电压门控功能。产品关联:文献未提及具体膜片钳系统品牌,领域常规使用Axopatch系列膜片钳仪器;辛醇购自Sigma Aldrich。
3.5 C端赖氨酸修饰对细胞增殖的调控作用
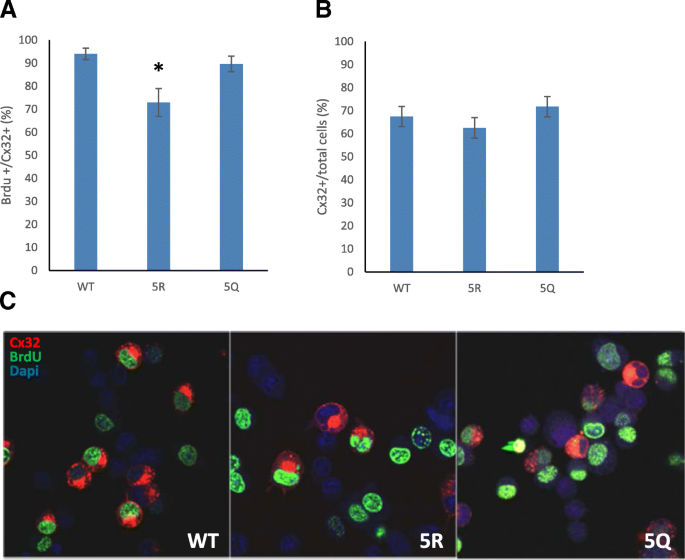
实验目的:明确Cx32的乙酰化修饰是否参与通道非依赖的细胞增殖调控。方法细节:对转染野生型、5R和5Q突变体的N2a细胞,采用BrdU掺入实验检测细胞增殖率,通过免疫荧光共定位检测Cx32阳性细胞中的BrdU阳性率,同时统计Cx32阳性细胞占总细胞的比例以排除突变体的毒性影响。结果解读:5R突变体的BrdU阳性率显著低于野生型(P<0.0026,n=3),而5Q突变体的BrdU阳性率与野生型无显著差异;三组的Cx32阳性细胞占总细胞的比例无显著差异,说明5R突变体的增殖抑制效应并非由蛋白毒性引起。产品关联:实验所用关键产品:BrdU试剂(Molecular Probes)、抗BrdU抗体(LabVision/ThermoFisher)、Alexa-Fluor标记二抗(Molecular Probes)、Metamorph图像分析软件(Molecular Devices)。
4. Biomarker研究及发现成果解析
本研究鉴定的Biomarker为间隙连接蛋白32(Cx32)C端的5个赖氨酸乙酰化修饰位点,属于蛋白翻译后修饰类功能标志物,其调控Cx32的蛋白稳定性与细胞增殖功能,为X连锁腓骨肌萎缩症(CMT1X)的发病机制提供了新的分子靶点。
Biomarker定位:本研究通过“抑制剂筛选-定点突变-功能验证”的逻辑链条筛选并验证了Cx32的乙酰化修饰靶点:首先通过HDAC抑制剂处理证实Cx32存在乙酰化修饰,然后通过逐个突变胞质结构域的赖氨酸,最终确定C端的5个赖氨酸为乙酰化靶点,通过突变体的泛素化、周转及增殖实验验证其功能调控作用。该Biomarker属于蛋白翻译后修饰位点,可反映Cx32的功能状态。
研究过程详述:该Biomarker的研究样本为转染Cx32的N2a细胞总蛋白及膜蛋白,验证方法包括免疫沉淀结合乙酰化抗体的定性检测、突变体的功能学验证(泛素化水平、蛋白周转速率、细胞增殖率);特异性方面,C端赖氨酸的突变仅影响Cx32的稳定性和非通道功能,不影响其通道介导的细胞间通讯,说明该修饰位点具有功能特异性;敏感性方面,HDAC6特异性抑制剂TubA可显著升高野生型Cx32的乙酰化水平,而5R突变体无响应,说明该检测方法可灵敏反映乙酰化状态的变化。
核心成果提炼:该乙酰化修饰位点可通过调控Cx32的泛素化水平影响蛋白周转,进而调控细胞增殖,属于通道非依赖的功能调控机制;创新性在于首次发现Cx32的乙酰化修饰及其对蛋白稳定性和细胞增殖的调控作用,填补了间隙连接蛋白乙酰化修饰研究的空白;统计学结果显示,各实验组的差异均具有统计学意义(P<0.05或P<0.0026),样本量为3-5次独立实验。该成果为CMT1X的发病机制研究提供了新的分子视角,也为间隙连接蛋白的翻译后修饰调控研究提供了新的方向。
