1. 领域背景与文献引入
文献英文标题:A cell behavior screen: identification, sorting, and enrichment of cells based on motility;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:细胞生物学(细胞运动调控与肿瘤细胞异质性)
领域共识:细胞运动是胚胎发育、组织修复、肿瘤侵袭转移等生理病理过程的核心环节,1962年Boyden建立的趋化实验是细胞运动检测的经典方法,后续发展的Transwell实验成为群体水平细胞运动检测的常用技术;1997年激光捕获显微切割技术实现了组织中特定细胞的分离,但无法基于活细胞的行为特征进行分选。当前研究热点聚焦于肿瘤细胞异质性与运动能力的关系,尤其是克隆起源的肿瘤细胞系内存在的运动能力差异,这与肿瘤的侵袭转移密切相关,但现有方法无法有效分离具有不同运动能力的活细胞,限制了对细胞运动调控机制的深入研究。本研究针对这一空白,建立了基于荧光微球吞噬的细胞运动能力定量与分选方法,为解析细胞运动的分子机制提供了新工具。
2. 文献综述解析
作者从细胞运动检测方法的维度对现有研究进行分类,包括群体水平的功能实验、组织水平的细胞分离技术,系统总结了各类方法的优势与局限性,明确了本研究的创新方向。
现有群体水平的细胞运动检测方法以Transwell实验为代表,该方法能有效检测不同细胞系的群体运动差异,但仅能反映群体中高运动能力亚群的特征,需要大量起始细胞,且无法分离具有特定运动能力的单个细胞;组织显微切割技术能从组织样本中分离特定形态的细胞,但只能分析静态的细胞特征,无法基于活细胞的运动行为进行分选。此外,传统的吞噬动力学实验(如胶体金法)可定量细胞运动能力,但无法实现细胞的分选与富集。本研究的创新点在于将荧光微球与吞噬动力学实验结合,首次实现了单个细胞运动能力的定量检测与活细胞的分选,解决了克隆细胞系内运动能力异质性细胞的分离难题,为后续的分子机制研究奠定了基础。
3. 研究思路总结与详细解析
本研究的核心目标是建立一种可定量单个细胞运动能力并能分选不同运动能力活细胞的方法,核心科学问题是如何将细胞运动能力转化为可量化的分选指标,技术路线遵循“方法建立→方法验证→相关性分析→分选与稳定性验证”的闭环逻辑。
3.1 荧光吞噬动力学检测体系的建立与验证
实验目的是建立可定量单个细胞运动能力的可视化检测方法,并验证该方法与传统Transwell实验的一致性。方法细节为:用50μg/ml聚-D-赖氨酸处理培养器皿30分钟,包被1μm直径的绿色荧光微球(Molecular Probes),接种胶质瘤细胞系U118MG、T98G及原代小鼠皮层星形胶质细胞,培养18-24小时后用4%多聚甲醛固定;同时设置Transwell实验作为对照,将细胞接种于包被聚-D-赖氨酸的Transwell小室(BD,孔径8μm),上下室均加入含20%胎牛血清的DMEM培养基,培养6小时后固定并计数穿膜细胞。结果解读:荧光显微镜观察显示,细胞在荧光微球包被的基质上运动时会吞噬微球,留下无荧光的运动轨迹(图1);定量分析显示U118MG细胞的平均清除面积比T98G高2.29倍(n=300,P=0.0012),与Transwell实验结果一致(U118MG细胞穿膜数是T98G的1.33倍,n=60,P=0.0185)(图2);此外,该方法可检测不同细胞外基质(纤连蛋白、IV型胶原、层粘连蛋白)对细胞运动能力的影响,U118MG细胞在IV型胶原上的运动能力显著高于纤连蛋白和层粘连蛋白(P<0.001)。实验所用关键产品:BD的Transwell小室、Molecular Probes的荧光微球(F8815、F8814)、Lipofectamine 2000转染试剂、Alexa 546标记鬼笔环肽、Hoescht 33342染液,Zeiss LSM510共聚焦显微镜。
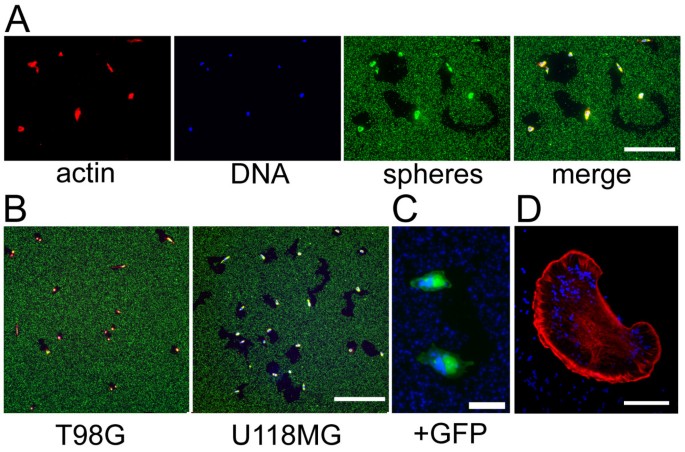
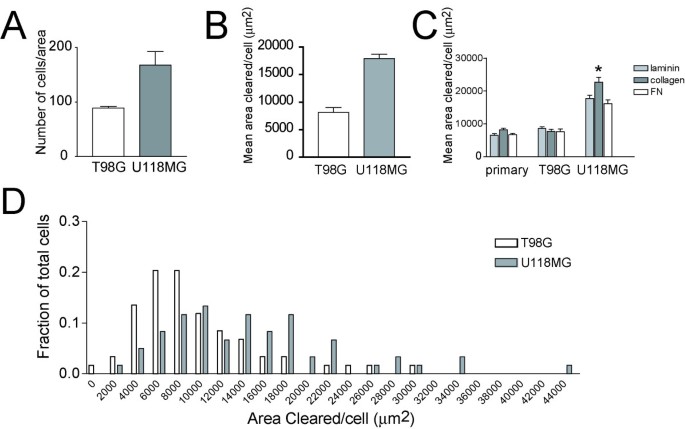
3.2 细胞运动能力与荧光强度的相关性验证
实验目的是验证细胞内吞荧光微球的荧光强度可作为运动能力的替代量化指标。方法细节为:用Roper Inc.的Cascade 650 16位CCD相机采集荧光图像,通过Metamorph成像软件定量单个细胞的清除面积和总荧光强度,确保所有图像的曝光时间一致(25ms)以避免信号饱和。结果解读:定量分析显示单个细胞的荧光强度与清除面积呈线性相关(图3),且克隆起源的U118MG和T98G细胞系内,单个细胞的运动能力存在广泛的异质性,清除面积呈连续分布。实验所用关键产品:Roper Inc.的Cascade 650 CCD相机、Metamorph成像软件。
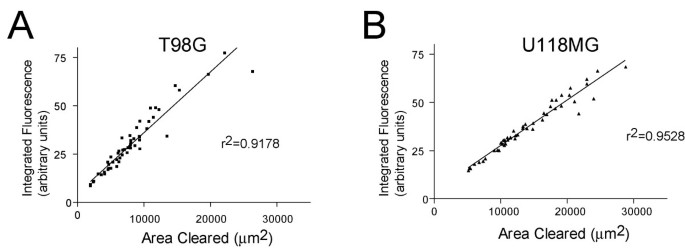
3.3 基于运动能力的细胞流式分选与稳定性验证
实验目的是分离具有不同运动能力的细胞亚群,并验证该亚群的运动能力差异是否可稳定维持。方法细节为:将U118MG细胞接种于荧光微球包被的10cm培养皿,培养20小时后用0.25%胰酶-EDTA消化,通过Beckman Coulter的Epics Elite ESP流式细胞仪根据荧光强度和侧向散射光分选高荧光和低荧光细胞亚群,分选后将细胞重新培养,在1、2、3、5周后用荧光吞噬动力学实验检测运动能力。结果解读:流式分选结果显示细胞荧光强度与侧向散射光(反映细胞内颗粒度,即吞噬的微球数量)呈正相关,与细胞大小无关(图4);分选后的高荧光细胞亚群在培养1-5周后,运动能力仍显著高于低荧光亚群,第1周差异为1.23倍(n>100,P=0.0106),第5周差异为1.18倍(n>100,P=0.0201),表明克隆细胞系内的运动能力差异具有稳定性。实验所用关键产品:Beckman Coulter的Epics Elite ESP流式细胞仪。
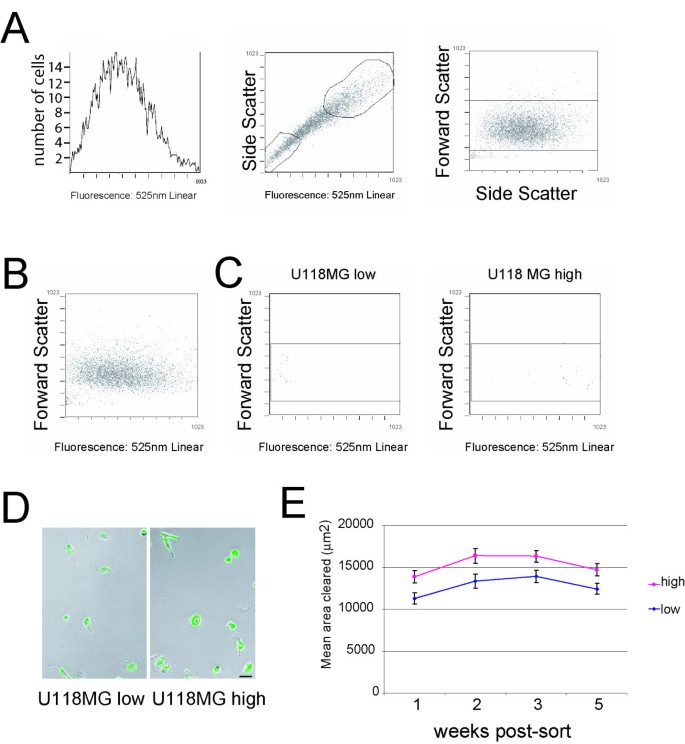
4. Biomarker研究及发现成果解析
本研究中涉及的Biomarker为细胞内吞荧光微球后的荧光强度,作为细胞运动能力的替代表型标志物,其筛选与验证逻辑为“荧光吞噬动力学实验建立相关性→流式分选验证分选可行性→长期培养验证稳定性”。
该Biomarker的来源为体外培养的活细胞,通过荧光吞噬动力学实验产生;验证方法包括荧光显微镜定量分析、流式细胞术分选、长期培养后的运动能力检测;特异性与敏感性数据显示,该标志物能有效区分克隆细胞系内的运动能力异质性,分选后的细胞亚群运动能力差异在5周内仍保持统计学显著性(P<0.05)。核心成果为:首次建立了基于荧光微球吞噬的细胞运动能力分选方法,证明克隆起源的胶质瘤细胞系内存在稳定的运动能力异质性,该方法为分离具有不同运动能力的活细胞提供了新工具,可用于后续筛选调控细胞运动的分子标志物或药物靶点;此外,该方法适用于多种细胞类型与细胞外基质,具有广泛的应用前景。
