1. 领域背景与文献引入
文献英文标题:Enhancing antitumor immunogenicity of HPV16-E7 DNA vaccine by fusing DNA encoding E7-antigenic peptide to DNA encoding capsid protein L1 of Bovine papillomavirus;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:HPV相关宫颈癌的治疗性DNA疫苗研究。
宫颈癌是全球女性第四大癌症死因,高危型人乳头瘤病毒(HPV)持续感染是其明确的主要病因,其中HPV16型感染占所有宫颈癌病例的约50%。领域共识:现有预防性HPV疫苗基于HPV L1/L2蛋白组装的病毒样颗粒(VLP),可诱导高效中和抗体反应,有效阻断HPV新发感染,但仅对未感染人群有效,无法干预已存在的感染或肿瘤病变。因此,开发针对HPV感染及相关肿瘤的治疗性疫苗成为领域核心需求。治疗性疫苗以持续表达的E6/E7致癌蛋白为靶点,其中DNA疫苗因制备简便、安全性高成为主流研究方向,但存在体内免疫原性低的固有缺陷。为增强治疗性DNA疫苗的免疫原性,现有策略包括将E6/E7抗原编码基因融合至溶酶体相关膜蛋白1(LAMP-1)、热休克蛋白70、钙网蛋白(CRT)等分子,主要增强CD8+或CD4+T细胞反应;另有研究通过联合给药编码牛乳头瘤病毒(BPV)L1/L2的DNA,可同时增强E7特异性CD8+T细胞反应及L1特异性抗体反应,但联合给药存在抗原表达不同步、递呈效率有限的局限性。
针对现有联合给药策略中抗原递呈不同步、免疫增强效果有限的研究空白,本研究构建了编码BPV L1全长蛋白与HPV16 E7抗原表位(aa49-57)的融合DNA疫苗,旨在评估其诱导E7特异性CD8+T细胞反应的能力,验证其在小鼠模型中的抗肿瘤保护及治疗效果,并明确其免疫反应的细胞依赖机制,为开发兼具预防与治疗潜力的HPV DNA疫苗提供实验依据。
2. 文献综述解析
本文综述部分以HPV疫苗的功能定位(预防性vs治疗性)及治疗性DNA疫苗的免疫增强策略(融合分子vs联合佐剂)为核心分类维度,系统梳理了现有HPV疫苗的研究进展、增强治疗性DNA疫苗免疫原性的策略及未解决的关键问题,为融合疫苗的研究设计提供了逻辑支撑。
现有研究梳理:预防性HPV疫苗基于HPV L1/L2蛋白组装的VLP,可诱导高效的中和抗体反应,有效阻断HPV感染,但仅对未感染人群有效,无法干预已存在的感染或肿瘤病变。治疗性疫苗以持续表达的E6/E7致癌蛋白为靶点,其中DNA疫苗因制备简便、安全性高成为主流研究方向,但存在体内免疫原性低的固有缺陷。为增强治疗性DNA疫苗的免疫原性,现有策略包括将E6/E7抗原编码基因融合至溶酶体相关膜蛋白1(LAMP-1)、热休克蛋白70、钙网蛋白(CRT)等分子,主要增强CD8+或CD4+T细胞反应;另有研究通过联合给药编码BPV L1/L2的DNA,可同时增强E7特异性CD8+T细胞反应及L1特异性抗体反应,但联合给药存在抗原表达不同步、递呈效率有限的局限性。此外,现有研究对治疗性疫苗诱导的抗肿瘤免疫反应的细胞依赖机制尚未完全明确,尤其是CD8+T细胞在融合疫苗介导的抗肿瘤效应中的核心作用缺乏直接实验证据。
创新价值论证:与现有联合给药策略相比,本研究首次构建了BPV L1与E7抗原表位的融合DNA疫苗,通过体外及体内实验证明其诱导的E7特异性CD8+T细胞反应显著强于联合给药组,且具有完全的肿瘤保护效果及显著的治疗效果;同时通过免疫细胞耗竭实验明确了该抗肿瘤反应完全依赖CD8+T细胞,弥补了现有研究中融合疫苗机制研究的空白,为开发兼具预防与治疗功能的HPV DNA疫苗提供了新的技术范式。
3. 研究思路总结与详细解析
本研究的整体研究目标为构建并评估BPV L1-E7融合DNA疫苗的免疫原性及抗肿瘤效果,核心科学问题是融合疫苗是否能通过高效抗原递呈增强E7特异性CD8+T细胞反应,以及该反应介导的抗肿瘤效应依赖的免疫细胞类型,技术路线遵循“质粒构建→体外验证→体内免疫原性评估→体内抗肿瘤实验→机制验证”的闭环逻辑,通过多维度实验验证融合疫苗的优势及作用机制。
3.1 重组DNA质粒构建与验证
实验目的是构建编码BPV L1、E7(49-57)表位及二者融合蛋白的重组DNA质粒,为后续实验提供核心工具。方法细节:以pshell-BPV为模板,通过PCR扩增BPV1 L1全长序列,克隆至pcDNA3.1载体的XhoI和XbaI位点,构建pcDNA3-BPVL1;通过PCR扩增包含E7(49-57)表位编码序列的BPV L1序列,克隆至同一载体,构建融合质粒pcDNA3-BPVL1-E7(49-57);合成E7(49-57)表位的小基因序列,克隆至pcDNA3.1载体的EcoRI和HindIII位点,构建pcDNA3-E7(49-57)。结果解读:成功构建三种重组质粒,图1展示了质粒的构建示意图,明确了融合蛋白的结构为BPV L1的C端连接E7(49-57)表位,为后续的抗原递呈及免疫实验奠定了基础。实验所用关键产品:文献未提及具体实验产品,领域常规使用PCR扩增试剂盒、限制性内切酶、质粒载体类试剂/仪器。

3.2 体外抗原递呈与E7特异性T细胞激活实验
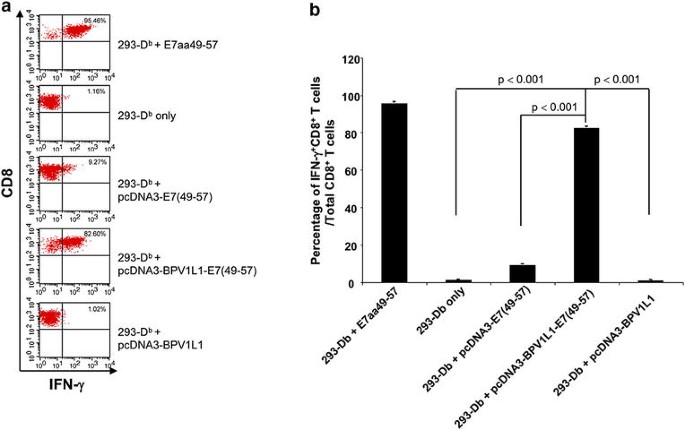
实验目的是验证融合质粒转染细胞后能否有效递呈E7抗原表位,并激活E7特异性CD8+T细胞。方法细节:采用Lipofectamine 2000将三种重组质粒分别转染293-Db细胞,24小时后将转染细胞与E7(49-57)表位特异性CD8+T细胞系共孵育(效应细胞与靶细胞比例为1:1),同时加入GolgiPlug阻断细胞因子分泌,20小时后对细胞进行表面CD8染色及胞内IFN-γ染色,通过流式细胞术分析T细胞激活情况;以加载E7(49-57)肽的293-Db细胞为阳性对照,未处理的293-Db细胞为阴性对照。结果解读:流式分析结果显示,转染融合质粒的293-Db细胞诱导的IFN-γ+CD8+T细胞比例显著高于转染pcDNA3-E7(49-57)的细胞,接近阳性对照组水平(图2a、b),说明融合质粒能更高效地递呈E7抗原表位,激活特异性CD8+T细胞,该结果具有统计学显著性(n=3,P<0.01)。实验所用关键产品:Lipofectamine 2000(赛默飞世尔科技)、BD Pharmingen的抗小鼠CD8抗体、抗小鼠IFN-γ抗体、GolgiPlug、FACSCalibur流式细胞仪。
3.3 体内融合疫苗的免疫原性评估
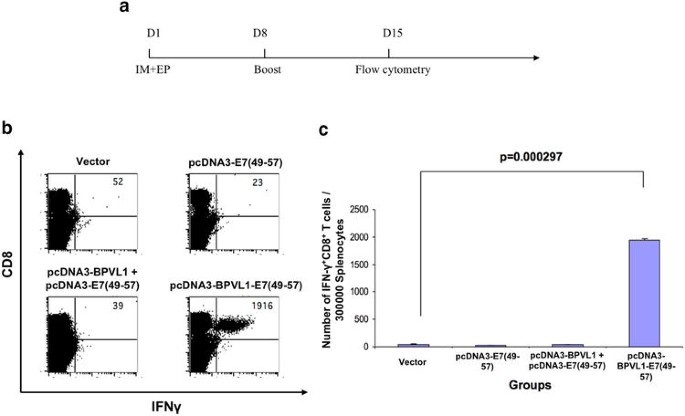
实验目的是验证融合DNA疫苗在小鼠体内诱导E7特异性CD8+T细胞反应的能力,并与联合给药策略进行比较。方法细节:将C57BL/6小鼠分为四组,分别肌肉注射空pcDNA3载体、pcDNA3-E7(49-57)、pcDNA3-BPVL1联合pcDNA3-E7(49-57)、融合质粒pcDNA3-BPVL1-E7(49-57),配合电穿孔增强转染效率,1周后进行加强免疫,7天后取小鼠脾细胞,用E7(49-57)肽刺激20小时,加入GolgiPlug阻断细胞因子分泌,随后进行CD8及IFN-γ染色,流式分析E7特异性CD8+T细胞比例。结果解读:融合疫苗组小鼠的脾细胞中,IFN-γ+CD8+T细胞比例显著高于其他三组(图3b、c),是联合给药组的3-4倍,说明融合疫苗能诱导更强的E7特异性CD8+T细胞反应,该差异具有统计学显著性(n=5,P<0.001)。实验所用关键产品:ECM830 Square Wave电穿孔系统(BTX Harvard Apparatus)、BD Pharmingen的流式抗体。
3.4 体内抗肿瘤保护效果验证
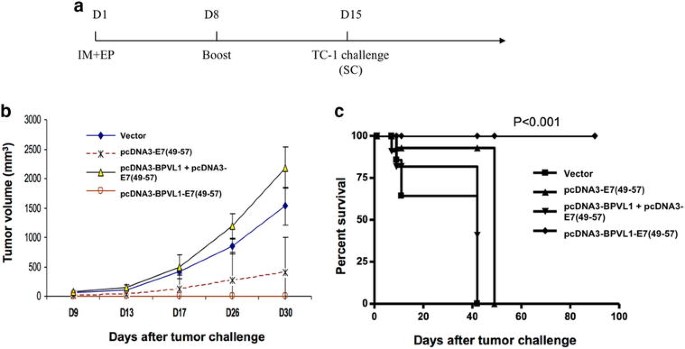
实验目的是验证融合DNA疫苗对HPV16 E7阳性肿瘤的预防保护效果。方法细节:小鼠免疫方案同3.3,最后一次免疫8天后,皮下接种5×10^4 TC-1肿瘤细胞(表达HPV16 E6/E7),以未接种疫苗的肿瘤小鼠为阴性对照,监测小鼠的肿瘤生长及生存情况100天,当肿瘤直径超过1.5cm时判定为小鼠因肿瘤负荷死亡。结果解读:融合疫苗组的所有小鼠在100天内均未出现可检测的肿瘤,且全部存活;而其他免疫组的小鼠在50天内全部因肿瘤负荷死亡,未免疫组小鼠的生存时间更短(图4b、c),说明融合疫苗具有完全的肿瘤保护效果,生存曲线分析显示组间差异具有统计学显著性(Log-rank检验,P<0.001,n=5)。实验所用关键产品:TC-1肿瘤细胞系。
3.5 体内抗肿瘤治疗效果验证
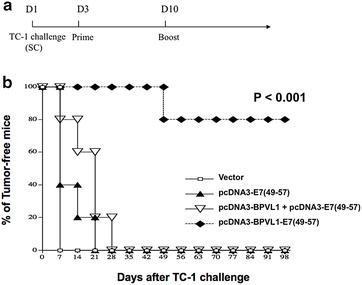
实验目的是验证融合DNA疫苗对已建立的TC-1肿瘤的治疗效果。方法细节:小鼠先皮下接种5×10^4 TC-1肿瘤细胞,3天后进行首次免疫,免疫方案同3.3,1周后加强免疫,监测小鼠的肿瘤生长情况100天。结果解读:80%的融合疫苗组小鼠在100天内未出现可检测的肿瘤,而其他免疫组及未免疫组的小鼠在28天内全部出现可检测的肿瘤(图5b),说明融合疫苗对已建立的肿瘤具有显著的治疗效果,组间差异具有统计学显著性(P<0.01,n=5)。
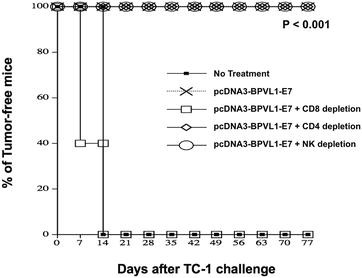
3.6 体内免疫细胞依赖机制验证
实验目的是明确融合疫苗诱导的抗肿瘤免疫反应依赖的免疫细胞类型。方法细节:小鼠免疫融合疫苗后,在最后一次免疫1天后,分别注射抗CD4、抗CD8a、抗NK1.1抗体以耗竭对应的免疫细胞,耗竭抗体的给药频率为第一周每两天一次,共三次,之后每周一次;7天后接种TC-1肿瘤细胞,监测肿瘤生长情况,以未耗竭的免疫小鼠及未免疫的肿瘤小鼠为对照。结果解读:耗竭CD8+T细胞的小鼠全部出现肿瘤生长,与未免疫组一致;而耗竭CD4+T细胞或NK细胞的小鼠仍保持无瘤状态,与未耗竭的免疫小鼠结果一致(图6),说明融合疫苗诱导的抗肿瘤免疫反应完全依赖CD8+T细胞,该结果具有统计学显著性(P<0.001,n=5)。推测:融合疫苗诱导的CD8+T细胞依赖的抗肿瘤效应,可能是由于融合蛋白组装为VLP,增强了树突状细胞的抗原摄取与递呈,进而诱导了更强的E7特异性CD8+T细胞反应,该机制需进一步通过VLP组装验证实验确认。实验所用关键产品:BioXCell的抗小鼠CD4(GK1.5)、CD8a(2.43)、NK1.1(PK136)抗体。
4. Biomarker研究及发现成果
本研究以E7特异性CD8+T细胞为核心功能性Biomarker,系统验证了其在融合DNA疫苗诱导的抗肿瘤免疫反应中的关键作用,明确了其作为治疗性HPV疫苗疗效评估指标的潜在价值。
Biomarker定位:本研究涉及的Biomarker为识别HPV16 E7(49-57)表位的CD8+T细胞,属于肿瘤特异性功能性Biomarker,其筛选逻辑基于HPV相关肿瘤中E7蛋白持续表达且为肿瘤特异性抗原,选择H-2Db限制性的E7(49-57)表位作为靶点,通过体外T细胞激活实验验证其抗原递呈能力,体内通过流式细胞术检测IFN-γ+CD8+T细胞比例作为免疫反应强度的评估指标,最终通过免疫细胞耗竭实验明确其在抗肿瘤效应中的核心作用。
研究过程详述:该Biomarker的来源为HPV16 E7蛋白的抗原表位(aa49-57),验证方法为胞内细胞因子染色结合流式细胞术,通过检测IFN-γ的表达反映CD8+T细胞的激活状态;特异性方面,仅识别E7(49-57)表位的CD8+T细胞被激活,未检测到针对其他抗原的非特异性反应;敏感性方面,融合疫苗组小鼠的脾细胞中,该Biomarker的比例可达总CD8+T细胞的5%-8%,显著高于联合给药组的1%-2%(n=5,P<0.001)。
核心成果提炼:E7特异性CD8+T细胞是融合DNA疫苗诱导抗肿瘤效应的核心Biomarker,其比例与肿瘤保护及治疗效果呈正相关,融合疫苗组小鼠的肿瘤发生率为0(n=5,P<0.001),风险比HR=0;本研究的创新性在于首次证明融合BPV L1与E7抗原表位的DNA疫苗能诱导比联合给药更强的E7特异性CD8+T细胞反应,且该反应完全依赖CD8+T细胞介导抗肿瘤效应,为治疗性HPV疫苗的疗效评估提供了关键Biomarker,也为开发兼具预防与治疗潜力的HPV DNA疫苗提供了新的策略。
