1. 领域背景与文献引入
文献英文标题:Irradiated mesenchymal stem cells support stemness maintenance of hepatocellular carcinoma stem cells through Wnt/β-catenin signaling pathway;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:肝癌肿瘤微环境与放疗抵抗
肝癌是全球发病率较高的恶性肿瘤之一,具有高转移、高复发特性,严重威胁人类健康。肝癌细胞多药耐药基因高表达导致化疗敏感性差,放疗已成为失去手术机会患者的核心治疗手段,但部分患者存在原发性或继发性放疗抵抗,提升肝癌放疗敏感性是当前临床与基础研究的核心需求。领域共识:肿瘤干细胞(CSCs)是肿瘤复发、转移及治疗耐药的核心驱动因素,CD133是已被广泛认可的肝癌CSCs表面标志物。肿瘤微环境中的间充质干细胞(MSCs)参与肿瘤进展与耐药调控,但辐照后的MSCs如何影响肝癌放疗耐药的具体分子机制尚未明确,这一研究空白限制了肝癌放疗抵抗干预策略的开发。本研究针对这一核心问题,旨在探讨辐照处理的MSCs对肝癌CSCs干性的调控作用及分子机制,为肝癌放疗耐药的靶向干预提供新的理论依据。
2. 文献综述解析
本文综述部分围绕肝癌治疗现状、CSCs的核心作用、MSCs在肿瘤微环境中的调控角色三个维度展开,系统梳理了领域内现有研究的进展与不足。现有研究已证实,CSCs是肝癌复发、转移及治疗耐药的关键,CD133+亚群具有典型的干细胞干性特征,包括自我更新、克隆形成及体内成瘤能力;MSCs作为肿瘤微环境的重要组成部分,可通过多种途径促进肿瘤进展与耐药,但针对辐照后MSCs与肝癌CSCs相互作用的研究较为匮乏,且未明确具体的信号通路机制。部分研究虽提及Wnt/β-catenin通路参与CSCs干性维持,但未将其与辐照后的MSCs功能关联起来。本研究的创新价值在于首次建立了辐照后MSCs与肝癌CSCs干性维持的直接关联,并明确了Wnt/β-catenin通路的核心介导作用,填补了辐照后肿瘤微环境细胞调控CSCs机制的研究空白,为肝癌放疗耐药的机制研究提供了新的方向。
3. 研究思路总结与详细解析
本研究的核心目标是明确辐照间充质干细胞(IR-MSCs)对肝癌干细胞(CSCs)干性的调控作用及分子机制,核心科学问题为IR-MSCs是否通过激活Wnt/β-catenin信号通路维持CSCs干性,技术路线遵循“细胞分离→共培养处理→功能验证→通路检测→反向验证”的闭环逻辑,通过多层次实验验证研究假设。
3.1 CD133+肝癌干细胞分离与鉴定
实验目的是从肝癌细胞系中筛选并获得具有干性特征的CD133+细胞亚群。方法细节为将Huh7和PLC肝癌细胞制备为单细胞悬液,采用PE标记的抗CD133抗体染色30分钟后,通过流式细胞术分选CD133+细胞,分别命名为Huh7-CD133和PLC-CD133。结果解读为成功分选出CD133+细胞亚群,为后续干性相关实验提供了研究对象。产品关联:实验所用关键产品:PE-conjugated anti-CD133抗体(文献未提及具体品牌货号,领域常规使用BD、Miltenyi Biotech等品牌的流式抗体)。
3.2 辐照后间充质干细胞(IR-MSCs)制备
实验目的是制备经辐照处理的MSCs,模拟放疗后肿瘤微环境中的MSCs状态。方法细节为将脐带来源的MSCs培养至80%汇合度,使用ELEKTA Synergy直线加速器(Cravoley, UK)以6 Gy剂量辐照,剂量率为350 cGy/min,辐照后恢复培养12小时。结果解读为成功获得IR-MSCs,用于后续与肝癌细胞的共培养实验。产品关联:实验所用关键产品:ELEKTA Synergy Linear Accelerator(Cravoley, UK)。
3.3 IR-MSCs对肝癌细胞CD133+比例的影响
实验目的是检测IR-MSCs是否能诱导肝癌细胞向CSCs表型转化,增加CD133+细胞比例。方法细节为采用Transwell小室(0.4 μm孔径)将Huh7、PLC细胞与MSCs或IR-MSCs共培养7天,通过流式细胞术检测CD133+细胞比例,同时采用反转录-聚合酶链反应(RT-PCR)和蛋白免疫印迹(Western blotting)检测CD133的mRNA及蛋白表达水平。结果解读为与MSCs组相比,IR-MSCs共培养组的CD133+细胞比例显著升高,且CD133的mRNA和蛋白表达水平均显著上调(n=4,P<0.05),提示IR-MSCs可促进肝癌细胞向CSCs表型转化。
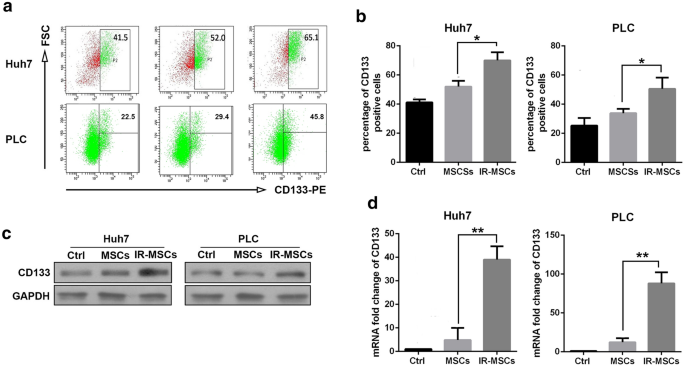
产品关联:实验所用关键产品:Cell Signal Technology的CD133抗体(货号64326)、abcam的GAPDH抗体(货号ab8245)、ABI Prism 7300实时PCR系统。
3.4 IR-MSCs对肝癌干细胞干性的维持作用
实验目的是验证IR-MSCs是否能增强肝癌CSCs的干性特征,包括克隆形成能力和体内成瘤能力。方法细节为将分选得到的Huh7-CD133和PLC-CD133细胞与IR-MSCs共培养7天后,以每孔500个细胞的密度接种于6孔板,培养7天后经结晶紫染色计数克隆形成数;同时将1×10^6个共培养后的细胞皮下注射至裸鼠体内,4周后检测肿瘤体积及重量。结果解读为IR-MSCs共培养组的克隆形成数显著多于对照组(n=4,P<0.01),裸鼠成瘤的体积和重量也显著增加(样本量未明确,P<0.01),表明IR-MSCs可显著增强肝癌CSCs的干性维持能力。
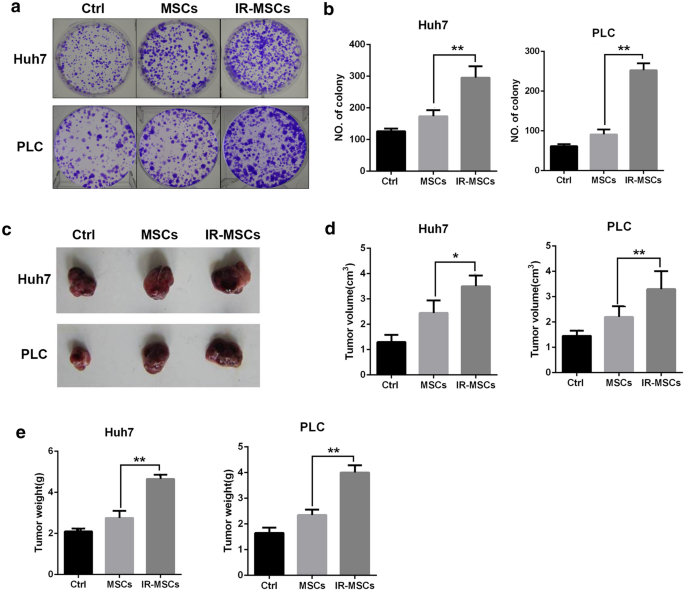
产品关联:文献未提及具体实验产品,领域常规使用结晶紫染色试剂、BALB/c裸鼠动物模型等。
3.5 IR-MSCs对Wnt/β-catenin信号通路的激活作用
实验目的是检测IR-MSCs是否通过激活Wnt/β-catenin信号通路调控CSCs干性。方法细节为采用RT-PCR和蛋白免疫印迹检测共培养后CSCs中Wnt3a和β-catenin的mRNA及蛋白表达水平。结果解读为IR-MSCs组的Wnt3a和β-catenin表达水平显著高于MSCs组(n=4,P<0.05),提示IR-MSCs可激活CSCs中的Wnt/β-catenin信号通路。
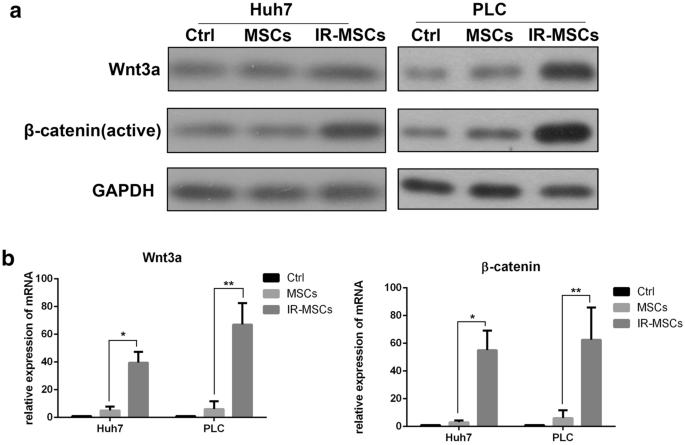
产品关联:实验所用关键产品:abcam的Wnt3a抗体(货号ab28472)、β-catenin抗体(货号ab6302)。
3.6 Wnt通路抑制剂反向验证实验
实验目的是明确IR-MSCs对CSCs干性的维持依赖于Wnt/β-catenin信号通路。方法细节为采用Wnt抑制剂PRI-724(30 nM)预处理Huh7-CD133细胞48小时,再与IR-MSCs共培养,随后检测CD133表达、克隆形成能力及裸鼠成瘤能力。结果解读为PRI-724处理后,IR-MSCs对CSCs干性的促进作用被完全抵消,CD133表达水平、克隆形成数、肿瘤体积及重量均显著降低(n=4,P<0.05),证实Wnt/β-catenin通路是IR-MSCs维持CSCs干性的核心介导通路。
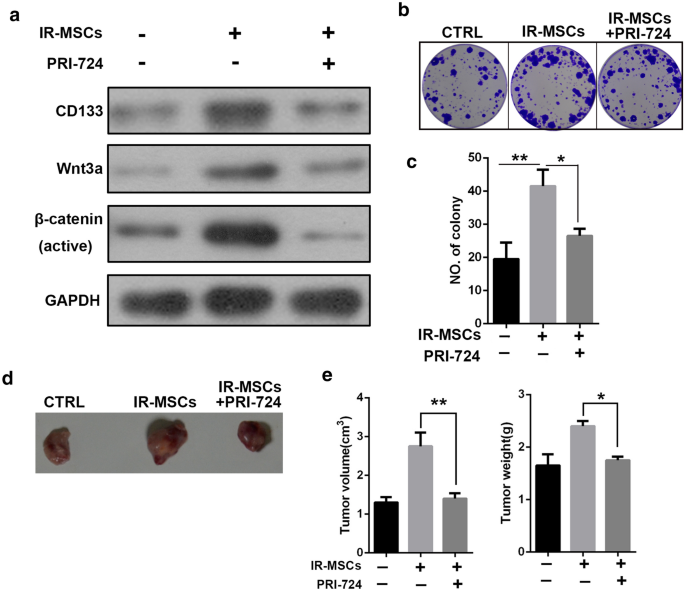
产品关联:实验所用关键产品:Wnt信号通路抑制剂PRI-724。
4. Biomarker研究及发现成果解析
本文聚焦的Biomarker为CD133,属于肝癌干细胞的表面标志物,同时涉及Wnt/β-catenin信号通路中的关键分子Wnt3a和β-catenin,通过多层次实验验证了这些分子在IR-MSCs调控CSCs干性中的核心作用。
Biomarker定位:CD133作为肝癌CSCs的经典表面标志物,筛选逻辑基于领域共识的CSCs标志物特征,通过流式细胞术从肝癌细胞系中分离,再通过克隆形成、裸鼠成瘤等功能实验验证其干性;Wnt3a和β-catenin作为通路关键分子,其表达变化与CSCs干性直接关联,验证逻辑为“表达检测→功能验证→抑制剂反向验证”的完整链条。
研究过程详述:CD133来源于Huh7和PLC肝癌细胞系,验证方法包括流式细胞术检测细胞比例、反转录-聚合酶链反应和蛋白免疫印迹检测表达水平,以及克隆形成和裸鼠成瘤实验验证干性功能;Wnt3a和β-catenin的验证方法为反转录-聚合酶链反应和蛋白免疫印迹检测表达,结合抑制剂实验验证功能关联。文中未明确给出CD133作为CSCs标志物的特异性与敏感性数据,但领域共识认为CD133在肝癌CSCs中具有较高的特异性;Wnt3a和β-catenin的表达水平在IR-MSCs共培养后显著上调(n=4,P<0.05)。
核心成果提炼:本研究的核心成果是揭示了IR-MSCs通过激活Wnt/β-catenin信号通路维持CD133+肝癌CSCs的干性,CD133+细胞的克隆形成能力和体内成瘤能力在IR-MSCs共培养后显著增强(n=4,P<0.01);创新性在于首次建立了辐照后MSCs与肝癌CSCs干性维持的关联,并明确了Wnt/β-catenin通路的核心介导作用,为肝癌放疗耐药的机制研究提供了新的靶点,同时为开发针对肿瘤微环境的放疗增敏策略提供了理论依据。文中未提及CD133作为预后或诊断标志物的风险比等数据,相关临床转化价值仍需进一步研究验证。
