1. 领域背景与文献引入
文献英文标题:Multiple-gene targeting and mismatch tolerance can confound analysis of genome-wide pooled CRISPR screens;发表期刊:Genome Biology;影响因子:2019年影响因子14.028;研究领域:功能基因组学、癌症细胞功能筛选、成簇规律间隔短回文重复序列/CRISPR相关蛋白9(CRISPR/Cas9)技术应用
功能基因组学的核心目标是解析基因型与表型的关联,全基因组功能筛选是基因功能研究的关键手段。早期RNA干扰(RNAi)筛选因脱靶效应显著、基因敲降不完全等局限,难以精准揭示基因功能。CRISPR/Cas9系统的问世革新了功能筛选领域,其高效的基因敲除能力大幅降低了脱靶风险,Project Achilles等大规模项目已完成391个癌细胞系的全基因组CRISPR筛选,为癌症靶点发现提供了海量数据。现有研究已针对拷贝数变异导致的切割毒性偏差开发了CERES校正模型,但尚未系统关注多靶点单引导RNA(sgRNA)(同时靶向多个基因组位点)的非加性遗传效应,以及sgRNA与基因组DNA错配容忍引发的脱靶干扰,这些空白导致CRISPR筛选结果的解读仍存在偏差,亟需深入分析以提高筛选准确性。
针对这一研究空白,本研究依托Project Achilles的大规模CRISPR筛选数据,系统分析了多靶点sgRNA和错配容忍对筛选结果的干扰机制,揭示了遗传相互作用、错配位置、遗传变异等因素对基因必需性评分的影响,为CRISPR筛选的实验设计与结果解读提供了关键指导。
2. 文献综述解析
作者以CRISPR筛选的偏差来源为分类维度,将现有研究分为拷贝数偏差校正、脱靶效应分析、多靶点效应研究三类,系统评述了CRISPR筛选领域的研究进展与未解决问题。
现有研究的关键结论包括:CERES模型通过细胞特异性线性回归校正,有效降低了拷贝数变异导致的切割毒性偏差,提高了基因必需性评分的准确性;CRISPR/Cas9系统的脱靶效应显著低于RNAi,但仍存在序列错配引发的脱靶风险;大规模CRISPR筛选已成功鉴定出大量癌症细胞依赖基因。技术方法优势方面,CERES模型实现了拷贝数偏差的个性化校正,CRISPR筛选的高特异性为基因功能研究提供了更可靠的工具。然而,现有研究存在明显局限性:一是未关注多靶点sgRNA的非加性遗传相互作用,如合成致死效应会导致基因必需性评分被错误估计;二是未系统分析错配位置对脱靶效应的影响,不同位置的错配容忍度差异尚未被充分揭示;三是忽略了细胞系遗传变异(如单核苷酸多态性SNP)对sgRNA靶向效率的干扰,导致部分细胞系的筛选结果出现偏差。
本研究的创新价值在于首次在391个癌细胞系的大规模数据中,全面解析了多靶点sgRNA和错配容忍两类关键偏差的影响机制;通过MYL12A/MYL12B的合成致死例子,证明了非加性遗传相互作用会突破现有加性模型的校正能力;通过SOX9/SOX10的脱靶例子,明确了错配位置对脱靶效应的调控作用;同时揭示了SNP对sgRNA活性的干扰,为CRISPR筛选的结果解读和文库优化提供了可操作的指导方案,填补了领域内的多项研究空白。
3. 研究思路总结与详细解析
本研究以“揭示CRISPR筛选中多靶点与错配容忍的偏差机制”为核心目标,围绕多靶点sgRNA的切割毒性与遗传相互作用、错配容忍的脱靶效应、遗传变异对sgRNA效率的干扰三个核心科学问题,采用生物信息学分析结合实验验证的技术路线,通过分层统计建模、序列比对、siRNA功能验证等方法,系统阐明了三类偏差的影响规律。
3.1 多靶点sgRNA对切割毒性的影响分析
实验目的:明确sgRNA完美匹配靶点数量与sgRNA活性的关联,以及该效应的细胞特异性差异。
方法细节:利用Avana文库的73782条sgRNA(含995条非靶向对照)在391个癌细胞系中的拷贝数校正后log2倍数变化(LFC)数据,采用Jonckheere趋势检验分析靶点数量与LFC的相关性;以靶向4个基因组位点的sgRNA LFC为指标,分析其与细胞系Cas9活性、非靶向对照LFC的相关性。
结果解读:
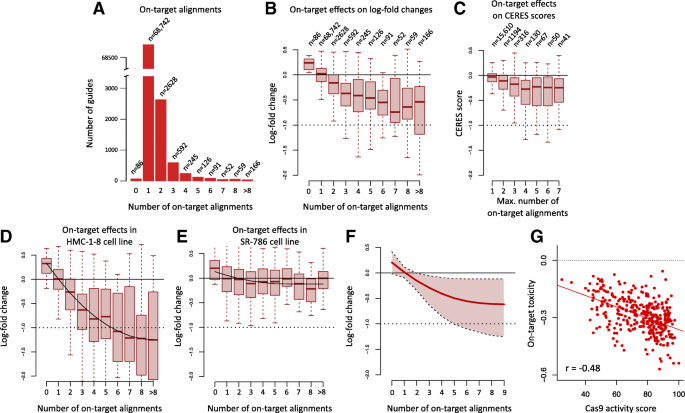
图1显示,随着sgRNA完美匹配靶点数量增加,LFC显著降低(p<2.2×10^-16),提示多靶点导致的切割毒性增强;该效应具有细胞特异性,如乳腺癌细胞系HMC-1-8的多靶点毒性显著高于淋巴瘤细胞系SR-786;Cas9活性越高,多靶点毒性越强(r=-0.48,p<2.2×10^-16),这与CRISPR筛选的竞争性生长特性一致,Cas9活性高的细胞系中,多靶点sgRNA导致的细胞死亡更快,非靶向对照细胞占比增加。
产品关联:文献未提及具体实验产品,领域常规使用CRISPR sgRNA文库、Cas9表达载体、Illumina下一代测序平台等。
3.2 多靶点sgRNA与非加性遗传相互作用的验证
实验目的:验证多靶点sgRNA的非加性遗传效应,尤其是合成致死相互作用对基因必需性评分的干扰。
方法细节:聚焦Avana文库中同时靶向MYL12A和MYL12B的sgRNA,分析其在391个细胞系中的LFC数据,结合MYL9的表达水平,采用线性模型检验基因敲除效应的加性假设;利用细胞特异性切割毒性拟合曲线,校正LFC后进一步分析遗传相互作用的影响。
结果解读:
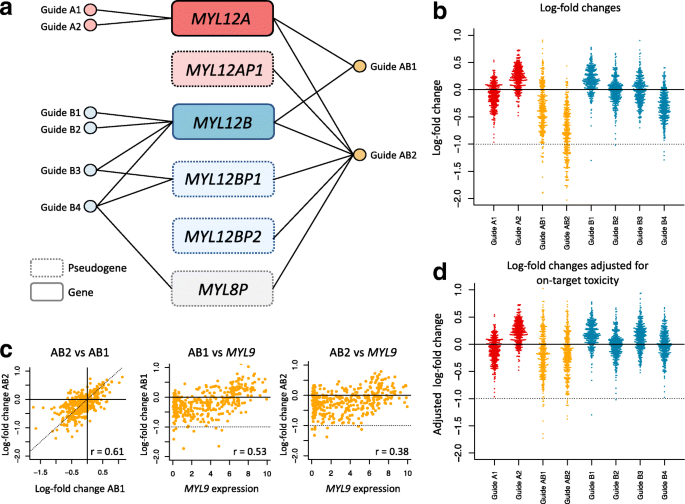
图2显示,单独靶向MYL12A或MYL12B的sgRNA LFC接近0,而同时靶向两者的sgRNA在MYL9低表达的细胞系中LFC显著降低至-1左右(p<2.2×10^-16);线性模型检验证明加性假设不成立(p<2.2×10^-16),提示MYL12A与MYL12B存在合成致死相互作用;校正切割毒性后,该差异仍无法被完全解释,进一步证实了遗传相互作用的独立影响。
产品关联:文献未提及具体实验产品,领域常规使用RNA-seq检测基因表达、R/Python线性统计建模软件等。
3.3 错配容忍对脱靶效应的影响分析
实验目的:明确单错配、双错配的位置与脱靶毒性的关联,以及脱靶效应对基因必需性评分的干扰。
方法细节:分析Avana文库中sgRNA的单错配、双错配数量与LFC的关系;按错配位置(PAM近端1-10位、PAM远端11-20位)分层,采用t检验比较不同位置错配的LFC差异;以SOX9/SOX10为模型,分析脱靶sgRNA对基因必需性评分的影响,并通过siRNA敲降实验验证细胞依赖基因的真实性。
结果解读:
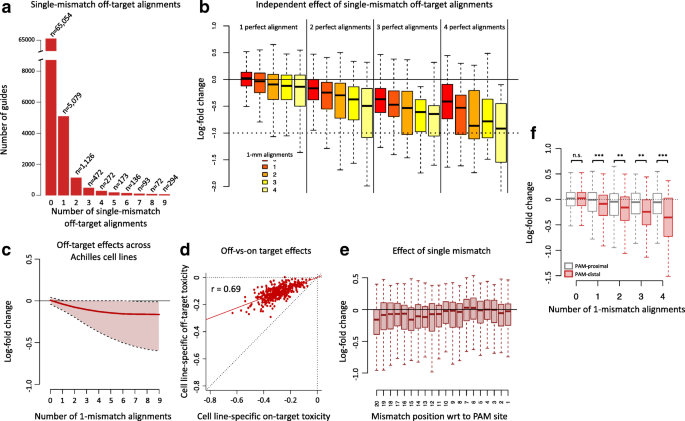
图4显示,PAM远端的单错配导致的脱靶毒性显著高于PAM近端(p<0.001),第20位错配的容忍度最高;
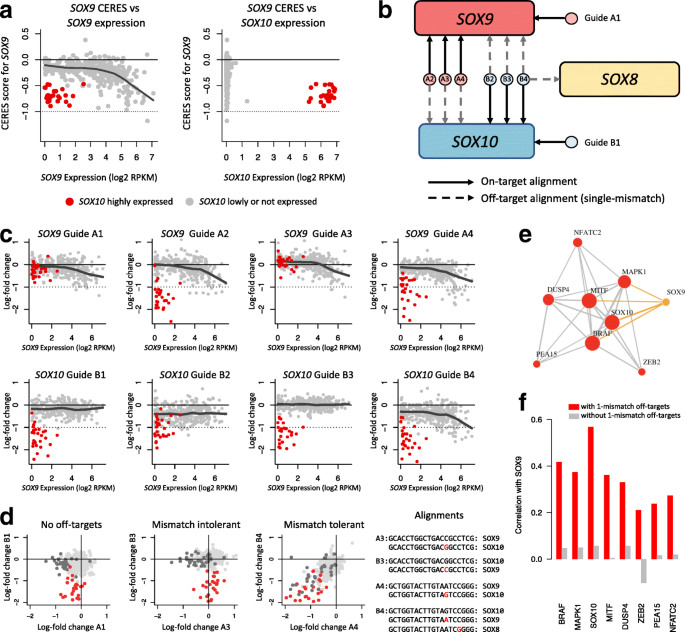
图5显示,SOX9的2条sgRNA因单错配脱靶到SOX10,导致SOX10高表达的黑色素瘤细胞系中SOX9的必需性评分被错误降低;
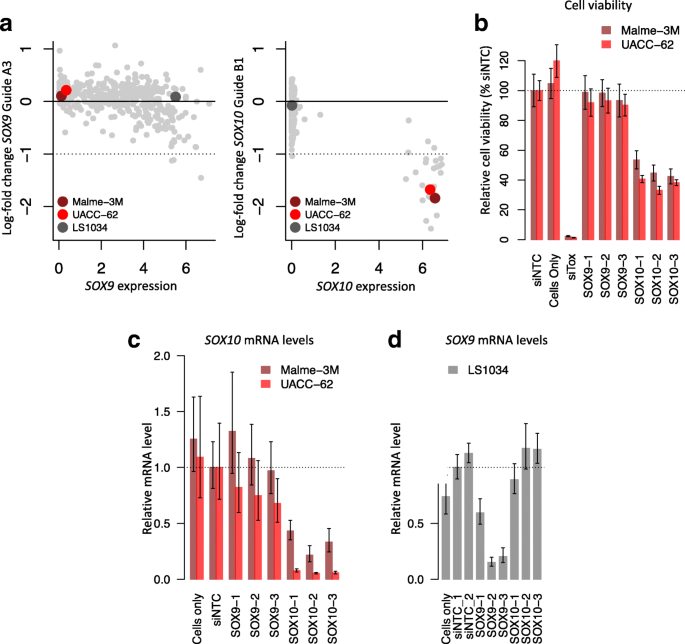
图6的siRNA实验验证,这些细胞系依赖SOX10而非SOX9,证实脱靶效应导致了必需性评分偏差;
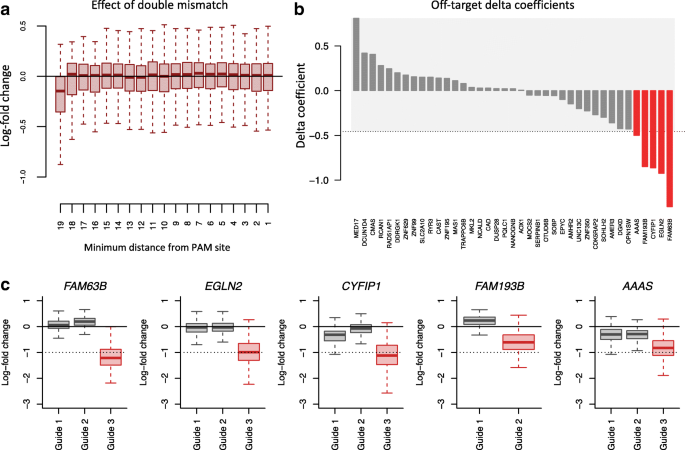
图8显示,PAM远端的双错配也会导致显著的脱靶毒性,部分sgRNA的LFC降低幅度接近必需基因。
产品关联:实验所用关键产品:SOX9 siRNA(货号Hs00165814_m1)、SOX10 siRNA(货号Hs00366918_m1,Life Technologies);CellTiter-Glo细胞活力检测试剂盒(Promega);RNeasy Mini QIAcube RNA提取试剂盒(Qiagen 74116);High Capacity cDNA反转录试剂盒(Applied Biosystems 4368814);TaqMan通用PCR预混液(Applied Biosystems 4304437)。
3.4 细胞系遗传变异对sgRNA效率的影响分析
实验目的:明确protospacer区域SNP对sgRNA靶向效率的干扰机制。
方法细节:利用CCLE的Affymetrix SNP Array 6.0数据,分析363个细胞系中protospacer区域SNP与sgRNA LFC的相关性;以EIF2B3和OAS1为模型,验证SNP对sgRNA活性和基因必需性评分的影响。
结果解读:
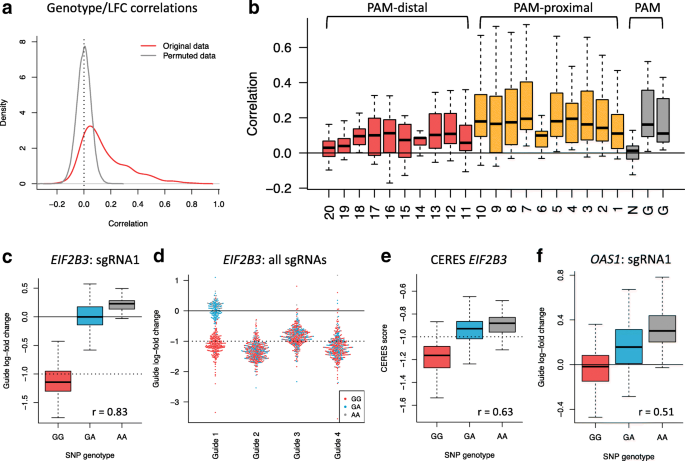
图9显示,EIF2B3的sgRNA中存在SNP rs11556200时,携带次要等位基因的细胞系中sgRNA活性显著降低(LFC从-1变为0),导致基因必需性评分与SNP基因型显著相关(r=0.63,p<2.2×10^-16);OAS1的sgRNA中SNP rs1131454破坏了NGG PAM位点,携带次要等位基因纯合的细胞系中sgRNA完全失活,LFC接近非靶向对照。
产品关联:文献未提及具体实验产品,领域常规使用Affymetrix Genome-Wide Human SNP Array 6.0、qRT-PCR检测平台等。
4. Biomarker研究及发现成果解析
本研究鉴定了三类影响CRISPR筛选准确性的“偏差标志物”,包括多靶点sgRNA、特定位置的错配sgRNA、protospacer区域SNP,系统解析了其筛选逻辑、验证方法与核心功能。
Biomarker定位与筛选逻辑:1)多靶点sgRNA:通过bowtie序列比对,筛选Avana文库中完美匹配靶点数量≥2的sgRNA,共鉴定出3959条多靶点sgRNA,对应2023个基因;2)错配敏感sgRNA:筛选PAM远端(11-20位)存在单错配或双错配的sgRNA,其中单错配sgRNA的脱靶风险显著更高;3)protospacer区域SNP:通过SNP芯片数据与sgRNA序列比对,筛选出protospacer区域存在SNP的sgRNA,共鉴定出473条对应SNP的sgRNA。验证逻辑均为结合391个细胞系的LFC数据,通过统计分析(相关性检验、t检验)验证其对sgRNA活性或基因必需性评分的影响。
研究过程详述:多靶点sgRNA来源于Avana文库的全基因组序列比对,验证方法为统计分析LFC与靶点数量的相关性,结果显示靶点数量与LFC呈显著负相关(p<2.2×10^-16),细胞系Cas9活性可作为该效应的预测指标(r=-0.48);错配敏感sgRNA的验证采用分层分析,PAM远端单错配的sgRNA LFC显著低于PAM近端(p<0.001),SOX9的例子中,2/4的sgRNA因PAM远端错配产生脱靶效应,导致SOX10高表达细胞系的SOX9必需性评分偏差;protospacer区域SNP的验证采用相关性分析,EIF2B3的SNP rs11556200的次要等位基因频率(MAF)=0.249,在携带次要等位基因的细胞系中,sgRNA活性降低约100%(LFC从-1变为0)。
核心成果提炼:三类偏差标志物的核心功能关联为:多靶点sgRNA可通过非加性遗传相互作用(如合成致死)错误升高基因必需性评分,MYL12A/MYL12B的例子中,合成致死效应导致LFC降低幅度超出加性模型预测(p<2.2×10^-16);错配敏感sgRNA可导致脱靶基因的必需性评分被错误关联,SOX9的例子中,去除脱靶sgRNA后,SOX9不再属于BRAF突变黑色素瘤的共必需基因簇;protospacer区域SNP可导致sgRNA活性降低甚至失活,干扰基因必需性评分的准确性。创新性方面,本研究首次系统揭示了多靶点sgRNA的非加性遗传效应,明确了错配位置对脱靶效应的调控规律,以及SNP对CRISPR筛选的干扰机制,为CRISPR筛选的实验设计与结果解读提供了关键依据。
