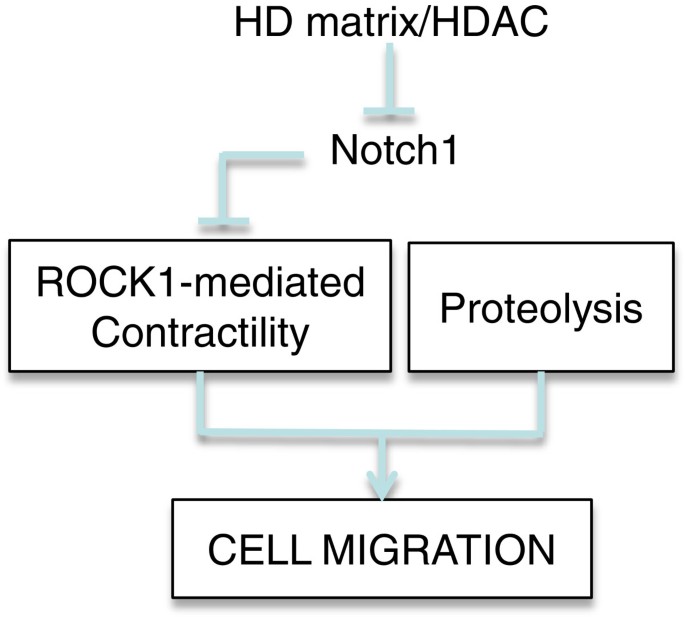
1. 领域背景与文献引入
文献英文标题:Regulation of ROCK1 via Notch1 during breast cancer cell migration into dense matrices;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:肿瘤学(乳腺癌基质微环境与细胞迁移调控)
乳腺癌是全球女性发病率最高的恶性肿瘤,肿瘤基质微环境在其发生、发展及转移过程中发挥关键调控作用。领域共识:乳腺致密组织的高胶原含量是乳腺癌发生的高危因素之一,致密基质可通过机械转导调控肿瘤细胞的基因表达与行为,但基质密度对肿瘤细胞迁移的具体调控机制尚未完全阐明。现有研究表明,肿瘤细胞迁移主要包括间充质样和阿米巴样两种模式,Rho相关卷曲螺旋形成激酶1(ROCK1)是调控阿米巴样迁移的核心分子,其在肿瘤迁移中的蛋白水平调控已被证实,但基质密度对ROCK1的表观遗传调控机制及信号通路介导作用仍不明确。组蛋白去乙酰化酶(HDAC)抑制剂可抑制肿瘤细胞迁移,但下游具体调控通路的研究存在空白。针对上述问题,本研究构建了与体内乳腺致密组织高度相似的3D基质模型,旨在揭示致密基质中HDAC/Notch1通路对ROCK1的调控机制,明确其在乳腺癌细胞迁移中的作用,为乳腺癌抗转移治疗提供新的靶点与策略。
2. 文献综述解析
作者从基质微环境对肿瘤细胞的调控、肿瘤细胞迁移模式的可塑性、ROCK1的多层面调控三个维度对现有研究进行分类评述。
现有研究已证实,乳腺致密组织的高胶原沉积可通过增加基质刚度促进肿瘤细胞增殖、侵袭及转移;肿瘤细胞可根据基质环境在间充质样和阿米巴样迁移模式间转换,ROCK1通过调控细胞收缩在阿米巴样迁移中发挥核心作用;HDAC抑制剂可通过表观遗传修饰调控肿瘤细胞的基因表达与行为,但多数研究仅关注单一分子的调控,未揭示表观遗传与信号通路的关联机制。现有研究的技术优势在于,3D基质模型可模拟体内微环境,活细胞成像技术可实时观察细胞迁移行为,但存在局限性:多数研究仅关注单一迁移模式的调控,未揭示不同模式间的补偿机制;对ROCK1的调控研究多集中在蛋白活性层面,缺乏表观遗传调控的系统分析;未构建与体内乳腺致密组织高度匹配的体外模型,实验结果的体内相关性不足。本研究的创新价值在于,首次构建了胶原含量、结构及力学特性与体内乳腺致密组织高度相似的3D基质模型,揭示了HDAC抑制剂通过Notch1通路间接调控ROCK1的表观遗传机制,明确了致密基质中ROCK1与基质金属蛋白酶(MMP)的补偿迁移机制,填补了基质微环境调控肿瘤细胞迁移的机制空白。
3. 研究思路总结与详细解析
本研究以“致密基质调控乳腺癌细胞迁移的分子机制”为核心科学问题,整体研究框架为:构建模拟体内致密基质的3D模型→观察细胞迁移行为与形态变化→检测ROCK1的表达与活性→探究HDAC抑制剂对ROCK1的调控作用→验证Notch1通路的介导作用→明确致密基质中细胞迁移的调控网络,形成“模型构建→表型观察→分子验证→机制解析”的完整闭环。
3.1 模拟体内致密基质的3D模型构建
实验目的:构建与乳腺致密组织胶原含量、结构及力学特性高度一致的体外高密度(HD)基质模型,为后续细胞迁移研究提供可靠的体外模拟体系。
方法细节:采用离心法浓缩I型鼠尾胶原,通过NH₄OH蒸汽聚合制备胶原含量约20mg/cm³的HD基质,同时制备胶原含量1mg/cm³的低密度(LD)基质作为对照;用Masson三色染色、天狼星红染色定量分析胶原含量,扫描电镜(SEM)观察胶原纤维结构,流变学检测基质刚度。
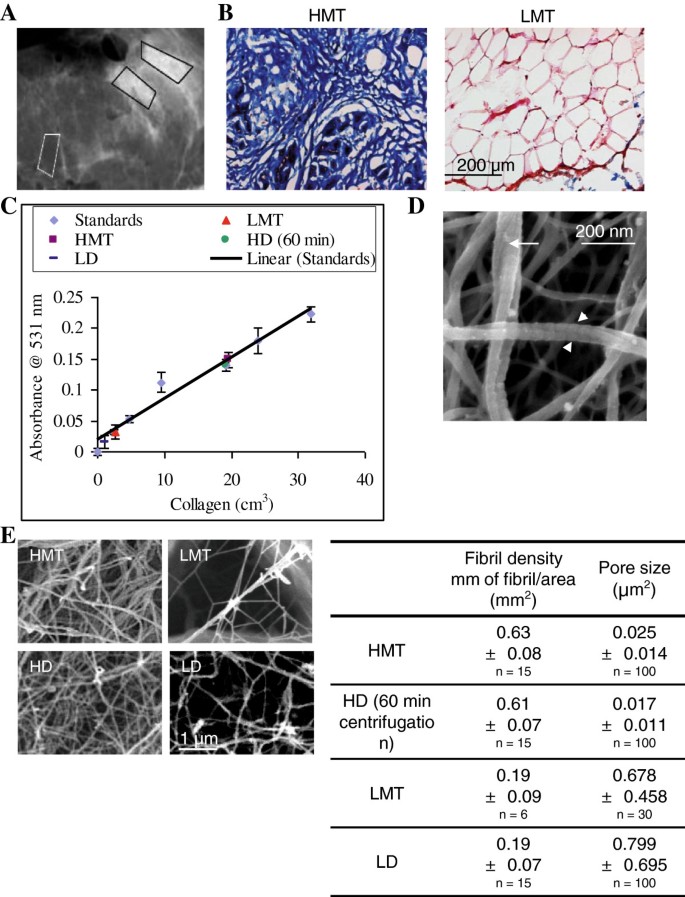
结果解读:天狼星红染色结果显示,HD基质的胶原含量为19.16±0.74mg/cm³,与体内乳腺致密组织的19.59±2.91mg/cm³高度接近(n=3,P<0.01);SEM观察显示HD基质胶原纤维形成致密网络结构,纤维直径约200nm;流变学检测表明HD基质的存储模量显著高于LD基质,刚度约为LD基质的14倍,成功模拟了体内致密基质的力学特性。
产品关联:实验所用关键产品:BD Biosciences的I型鼠尾胶原、Sigma-Aldrich的天狼星红染色剂、Zeiss的场发射扫描电镜、Anton-Paar的Physica MCR 301流变仪。
3.2 乳腺癌细胞迁移行为观察与分析
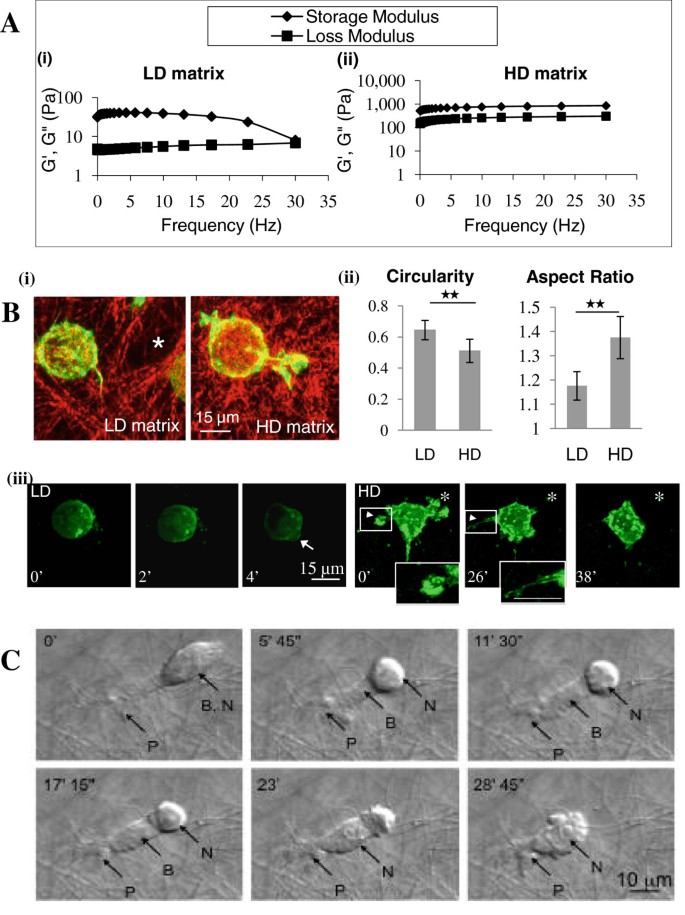
实验目的:对比不同密度基质中乳腺癌细胞的迁移模式、形态变化及迁移效率,明确致密基质对细胞迁移行为的调控作用。
方法细节:将MTLn3大鼠乳腺癌细胞接种于LD和HD基质表面,培养72h后,用活细胞共聚焦显微镜观察细胞形态,微分干涉差(DIC)显微镜实时记录细胞迁移过程;通过ImageJ软件分析细胞的圆形度和纵横比,量化细胞形态;染色后用共聚焦显微镜检测细胞迁移深度。
结果解读:活细胞成像显示,LD基质中细胞呈圆形,迁移过程中形成膜泡出芽;HD基质中细胞通过胞质流动和细胞体收缩完成迁移,细胞核需借助细胞收缩挤过基质纤维;72h后,89%的细胞侵入LD基质(n=4),100%的细胞侵入HD基质(n=2,P<0.05);细胞形态分析显示,HD基质中细胞的圆形度显著降低,纵横比显著升高,呈梭形(n=15,P<0.01)。
产品关联:实验所用关键产品:Olympus的CellR活细胞显微镜、Invitrogen的Alexa Fluor 488鬼笔环肽、ImageJ图像分析软件。
3.3 ROCK1表达与活性的基质依赖性调控验证
实验目的:验证基质密度对ROCK1表达和活性的调控作用,明确ROCK1在致密基质细胞迁移中的功能。
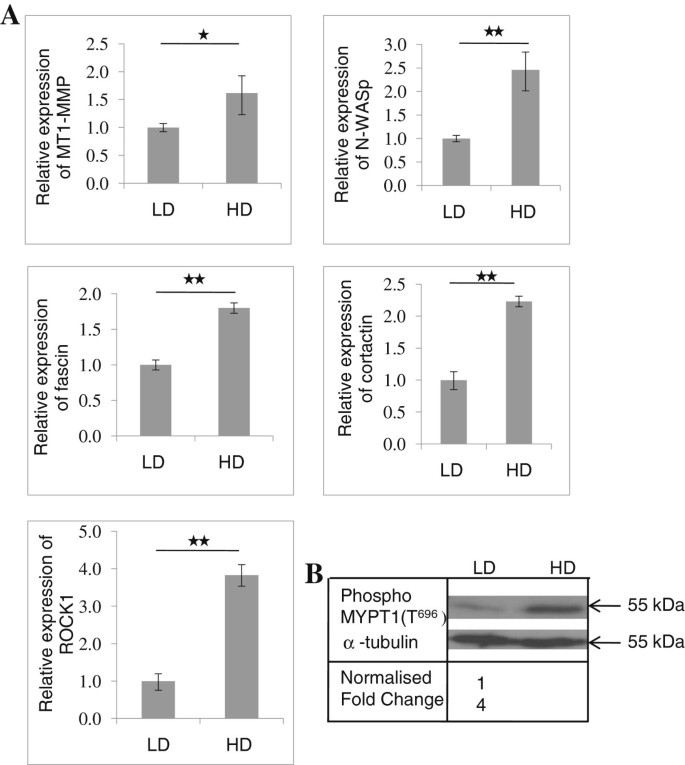
方法细节:提取LD和HD基质中迁移细胞的总RNA和蛋白,采用实时定量聚合酶链式反应(qRT-PCR)检测ROCK1 mRNA表达水平;通过激酶活性实验,以肌球蛋白磷酸酶靶向亚基1(MYPT1)为底物,检测ROCK1的激酶活性;免疫印迹(Western blot)验证ROCK1蛋白表达。
结果解读:实时定量聚合酶链式反应结果显示,HD基质中ROCK1 mRNA表达水平是LD基质的4倍(n=3,P<0.01);激酶活性实验显示,HD基质中ROCK1活性显著升高4倍(n=3,P<0.01);免疫印迹结果进一步证实HD基质中ROCK1蛋白表达显著上调,表明基质密度可显著调控ROCK1的表达和活性。
产品关联:实验所用关键产品:Cell Biolabs的ROCK活性免疫印迹试剂盒、Santa Cruz的ROCK1抗体、Qiagen的RNeasy Mini RNA提取试剂盒。
3.4 HDAC抑制剂对ROCK1的调控作用研究
实验目的:探究HDAC抑制剂对致密基质中ROCK1表达和活性的影响,明确表观遗传调控在细胞迁移中的作用。
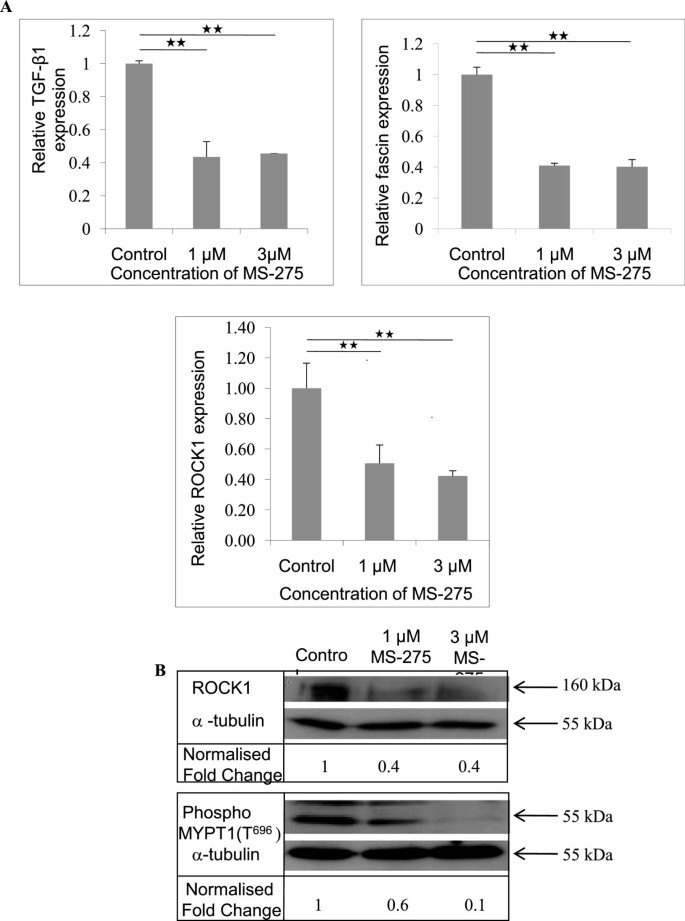
方法细节:用不同浓度的MS-275(HDAC抑制剂,1μM、3μM)处理HD基质中的细胞,培养48h后,提取总RNA和蛋白,用实时定量聚合酶链式反应检测ROCK1 mRNA表达,免疫印迹检测ROCK1蛋白水平,激酶活性实验检测ROCK1活性;同时检测迁移相关基因(TGF-β1、fascin)的表达变化。
结果解读:MS-275处理后,ROCK1 mRNA表达显著下调,1μM和3μM浓度下ROCK1蛋白水平分别降低60%,活性分别抑制40%和90%(n=3,P<0.01);同时,迁移相关基因TGF-β1、fascin的表达也显著下调,表明HDAC抑制剂可通过调控迁移相关基因抑制细胞迁移。
产品关联:实验所用关键产品:Enzo Life Sciences的MS-275、Sigma的RIPA蛋白裂解液、Bio-Rad的蛋白定量试剂盒。
3.5 Notch1通路介导HDAC抑制剂调控ROCK1的机制验证
实验目的:验证Notch1通路在HDAC抑制剂调控ROCK1中的介导作用,明确致密基质中ROCK1的调控网络。
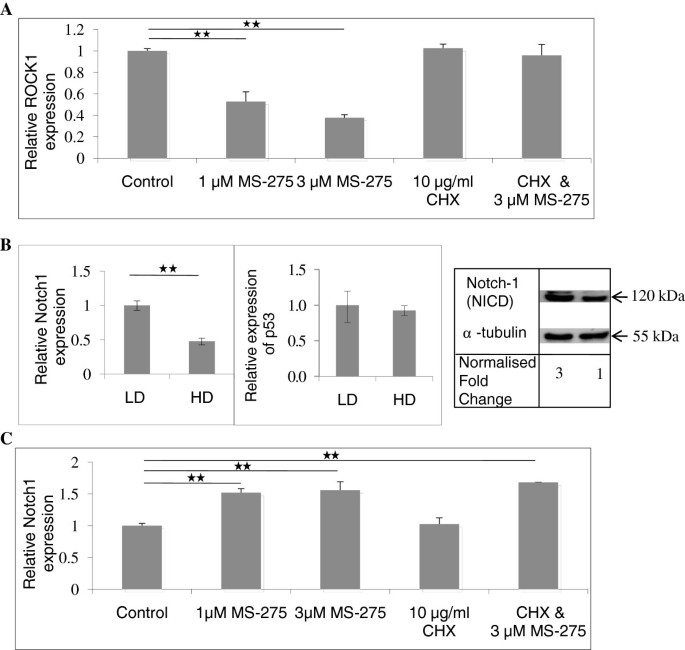
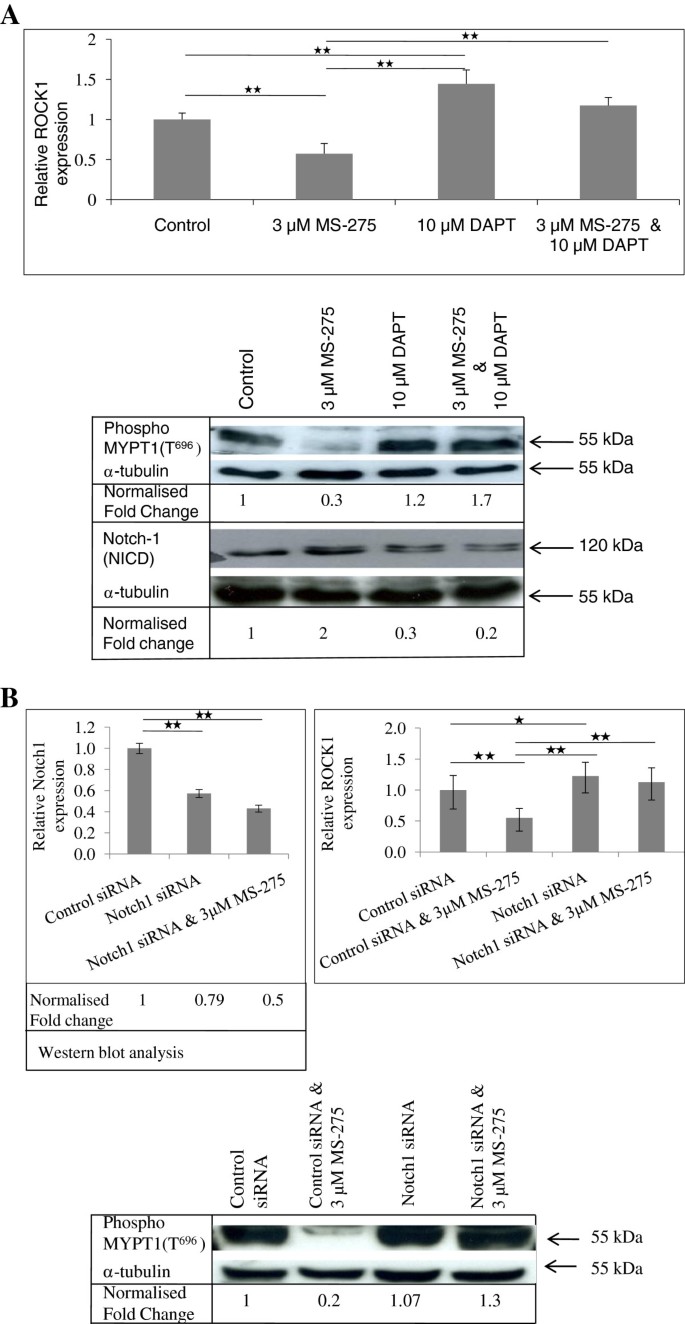
方法细节:用Cycloheximide(CHX,蛋白合成抑制剂)处理细胞,联合MS-275,检测ROCK1表达变化;用实时定量聚合酶链式反应和免疫印迹检测HD基质中Notch1的表达,以及MS-275处理后的变化;用DAPT(Notch1抑制剂)或Notch1 SMART Pool siRNA处理细胞,联合MS-275,检测ROCK1的表达和活性。
结果解读:CHX可逆转MS-275对ROCK1的下调作用,表明HDAC抑制剂对ROCK1的调控依赖新蛋白合成(n=2,P<0.05);HD基质中Notch1的mRNA和蛋白表达显著低于LD基质(n=2,P<0.05),MS-275处理后Notch1表达显著上调;DAPT或Notch1 siRNA可逆转MS-275对ROCK1的抑制作用,ROCK1表达恢复至对照水平(n=3,P<0.01),表明Notch1是HDAC抑制剂调控ROCK1的关键介导分子。
产品关联:实验所用关键产品:Sigma的Cycloheximide、DAPT,Dharmacon的Notch1 SMART Pool siRNA、Santa Cruz的Notch1抗体。
4. Biomarker研究及发现成果解析
本研究中涉及的核心Biomarker为ROCK1,作为致密基质诱导乳腺癌细胞迁移的关键调控分子,其筛选与验证逻辑为:构建3D致密基质模型→观察细胞迁移行为→通过实时定量聚合酶链式反应检测迁移相关基因的差异表达→锁定ROCK1为显著上调的基因→进一步验证其表达、活性及调控通路。
ROCK1的来源为MTLn3大鼠乳腺癌细胞,验证方法包括:实时定量聚合酶链式反应检测mRNA表达、免疫印迹检测蛋白水平、激酶活性实验检测功能活性。特异性方面,HD基质中ROCK1的表达和活性显著高于LD基质(n=3,P<0.01),具有明确的基质密度依赖性;敏感性方面,MS-275处理可显著抑制ROCK1的表达和活性,Notch1通路阻断可完全逆转该抑制作用。核心成果提炼:ROCK1作为致密基质中乳腺癌细胞迁移的关键调控分子,其功能关联为通过调控细胞收缩促进细胞在致密基质中的迁移,且与MMP形成补偿迁移机制(单独抑制ROCK1或MMP对迁移无显著影响,联合抑制可完全阻断迁移,n=3,P<0.01);创新性在于首次揭示了HDAC/Notch1通路对ROCK1的表观遗传调控机制,即致密基质通过HDAC抑制Notch1表达,进而上调ROCK1,促进细胞迁移;本研究为乳腺癌抗转移治疗提供了新的靶点组合(ROCK1+MMP抑制剂),以及表观遗传治疗的新策略(HDAC抑制剂通过Notch1调控ROCK1)。