1. 领域背景与文献引入
文献英文标题:Intracellular mediators of transforming growth factor β superfamily signaling localize to endosomes in chicken embryo and mouse lenses in vivo;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:晶状体发育与转化生长因子β(TGF-β)超家族信号调控
转化生长因子β(TGF-β)超家族是调控胚胎发育、组织稳态及疾病发生的关键信号通路,其中骨形态发生蛋白(BMP)亚家族在晶状体发育中发挥核心作用,从晶状体基板形成到纤维细胞分化的多个阶段均依赖BMP信号的精准调控。领域共识:内体作为细胞内的膜性细胞器,不仅参与受体的内吞降解或循环,还可作为信号转导的平台,招募信号复合物并调控信号传递效率。当前研究热点聚焦于内体在信号通路中的调控机制,但多数研究基于体外细胞系,无法模拟体内组织的复杂微环境,存在的核心问题是:体内组织中TGF-β超家族信号通路组分的亚细胞定位模式是否与体外一致?内体定位的信号分子在体内晶状体发育中的功能机制尚未明确。针对这一研究空白,本研究通过在鸡胚和小鼠晶状体中系统解析TGF-β信号通路多个组分的内体定位,揭示体内与体外信号调控的差异,为内体调控TGF-β信号的体内机制提供直接证据,具有填补体内组织信号定位研究空白的学术价值。
2. 文献综述解析
作者以“体外细胞系研究vs体内组织研究”为核心分类维度,对现有研究进行评述。现有研究的关键结论显示,体外细胞系实验已证实内体参与TGF-β受体的内吞过程,不同内吞通路分别调控Smad信号的激活或受体的降解,例如早期内体富集区(EEA1阳性)可促进Smad2的磷酸化及核转运,而小窝介导的内吞通路则靶向TGF-β受体降解。体外实验的技术优势在于细胞培养体系易操控,可通过基因编辑、药物处理等手段精准解析分子间的互作关系;但局限性也较为明显,体外细胞系无法模拟体内组织的三维结构及细胞间的微环境信号,导致信号分子的亚细胞定位及调控机制可能与体内存在显著差异,且缺乏对体内组织中信号复合物在内体组装及功能的系统研究。
通过对比现有研究的未解决问题,本研究的创新价值凸显:首次在体内晶状体组织中系统检测TGF-β超家族信号通路的多个核心组分(包括激活型Smad、共Smad、抑制型Smad、转录抑制因子、衔接蛋白)的亚细胞定位,明确这些分子在体内定位于内体的模式,同时揭示体内与体外信号分子分布的关键差异,为内体作为信号调控平台的体内功能提供直接证据,弥补了体外研究无法模拟体内微环境的不足。
3. 研究思路总结与详细解析
本研究的整体框架为:以“体内晶状体组织中TGF-β信号通路组分的亚细胞定位及功能调控”为核心,研究目标是明确TGF-β超家族信号分子在体内晶状体细胞中的内体定位模式,核心科学问题是内体定位的信号分子如何参与晶状体发育的信号调控,技术路线遵循“体内样本制备→免疫荧光共定位检测→细胞类型特异性分析→条件敲除模型功能验证→机制推论”的闭环逻辑。
3.1 体内组织样本制备与实验模型构建
实验目的是获取保留亚细胞结构的体内晶状体组织样本,建立BMP信号缺失的功能验证模型,为后续定位分析提供基础。方法细节为选用发育至E7的鸡胚晶状体和出生后3天(P3)的小鼠晶状体作为研究对象,通过将Bmpr1a floxed小鼠与LeCre小鼠交配,构建晶状体特异性Bmpr1a条件敲除(CKO)小鼠模型;将晶状体组织用10%福尔马林固定1-2小时后,包埋于4%琼脂中,使用振动切片机制备100μm厚的组织切片。结果解读显示,成功制备的厚切片可清晰保留细胞的亚细胞结构,Bmpr1a CKO小鼠晶状体呈现明显的发育异常,表现为晶状体体积减小、上皮层变薄,与之前报道的Bmpr1a调控晶状体发育的表型一致。实验所用关键产品:Upstate Biotechnology的磷酸化Smad1抗体、Cell Signaling Technology的磷酸化Smad2/β-微管蛋白抗体、Santa Cruz Biotechnology的Smad4/Smad6/Smad7/SARA/c-Ski/Rab5B/Rab7抗体、Calbiochem的EEA1抗体、BD Transduction Laboratories的EEA1/小窝蛋白1抗体、Molecular Probes的Alexa-Fluor标记二抗/鬼笔环肽/TOTO-1/TOPRO、Vector labs的VectaShield封片剂。
3.2 免疫荧光共定位检测与方法学验证
实验目的是检测TGF-β信号通路组分与内体标记物的共定位关系,同时验证双标实验方法的特异性。方法细节为采用免疫荧光双标技术,针对两种兔源一抗优化实验流程:先孵育第一组一抗及对应的荧光二抗,经福尔马林固定后再孵育第二组一抗及二抗,设置省略第二一抗的阴性对照以排除交叉染色。结果解读显示,共聚焦显微镜观察证实,磷酸化Smad1(pSmad1)、磷酸化Smad2(pSmad2)、Smad4、Smad7、转录抑制因子c-Ski和TGIF、衔接蛋白SARA和C184M均与早期内体标记物EEA1或Rab5B共定位于细胞质囊泡;pSmad1和pSmad2还与晚期内体标记物Rab7共定位,约15-20%的阳性囊泡同时标记Rab7;阴性对照未检测到交叉染色,验证了实验方法的特异性。
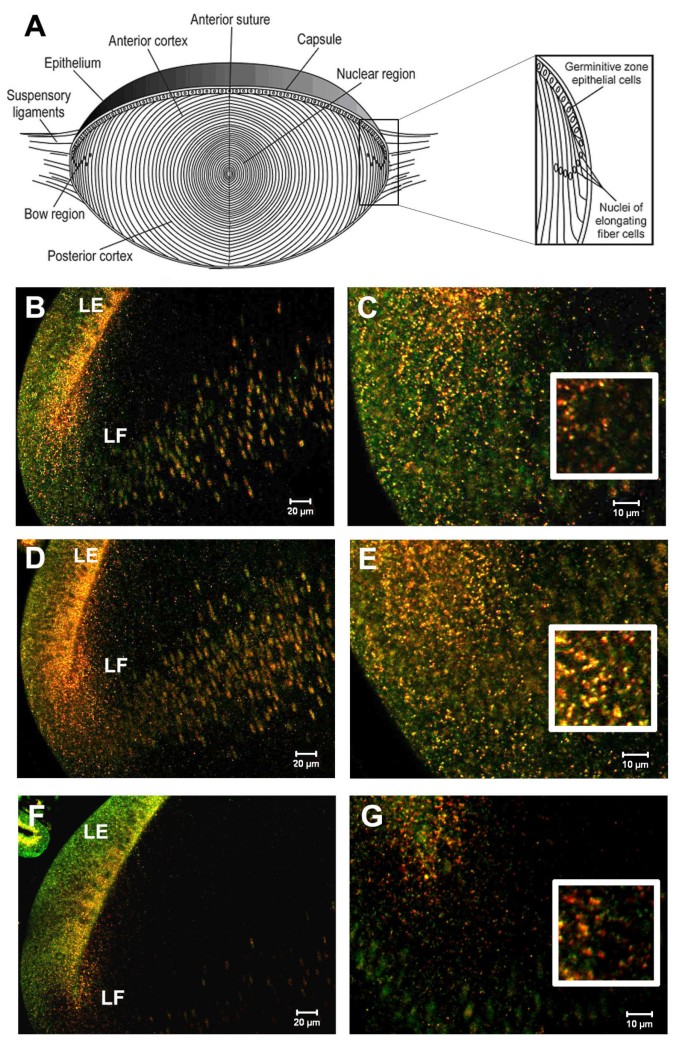
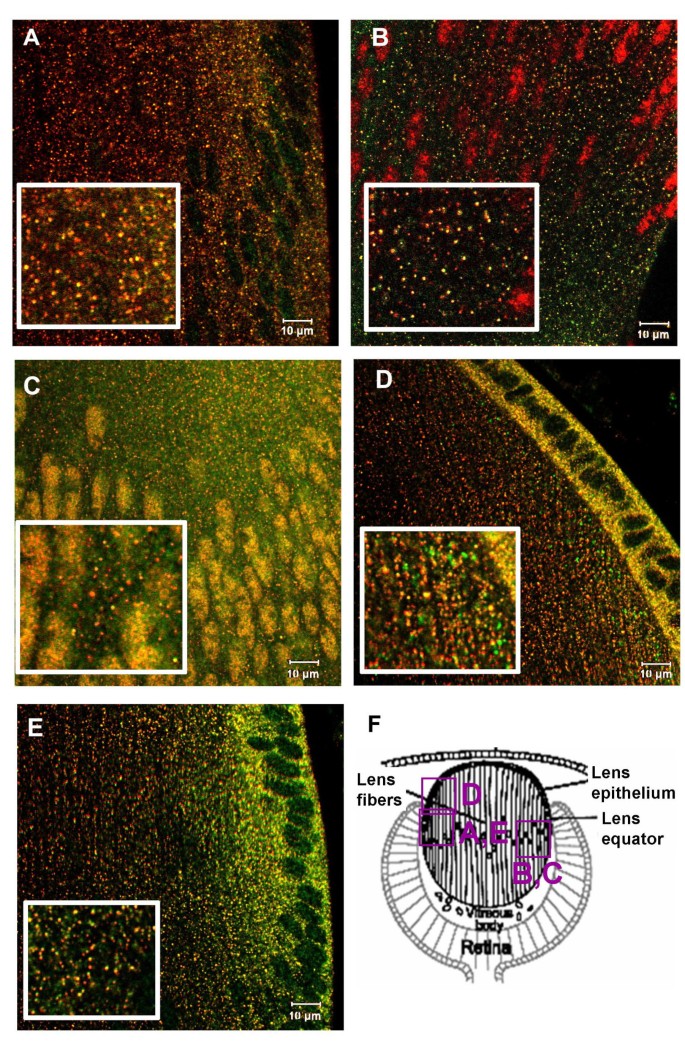
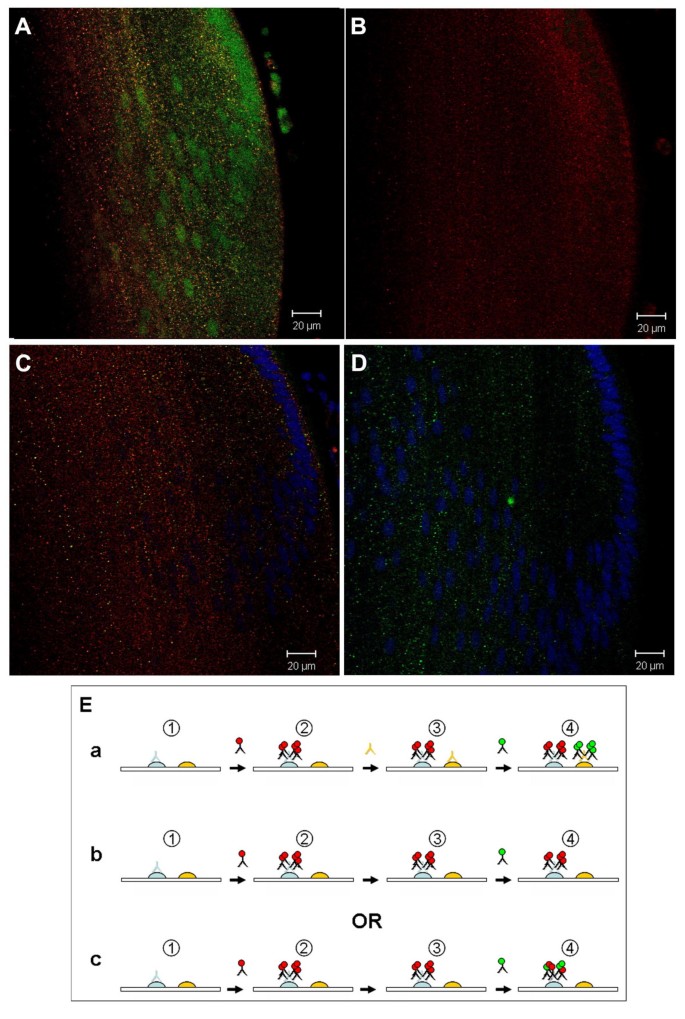
3.3 晶状体细胞类型特异性定位分析
实验目的是比较晶状体上皮细胞与纤维细胞中信号分子的亚细胞分布差异,揭示细胞类型特异性的信号调控机制。方法细节为对晶状体上皮细胞和纤维细胞分别进行免疫荧光染色,观察信号分子在细胞质内体及细胞核的定位模式。结果解读显示,pSmad1、pSmad2、Smad4、Smad7、c-Ski和TGIF在晶状体纤维细胞中同时定位于内体和细胞核,而在晶状体上皮细胞中主要富集于内体,细胞核中几乎无积累;衔接蛋白SARA和C184M在两种细胞类型中均仅定位于内体,未进入细胞核。这一结果提示,晶状体上皮细胞中存在特异性机制,抑制激活的Smad复合物向细胞核转运,与体外细胞系中激活Smad直接入核的模式存在显著差异。
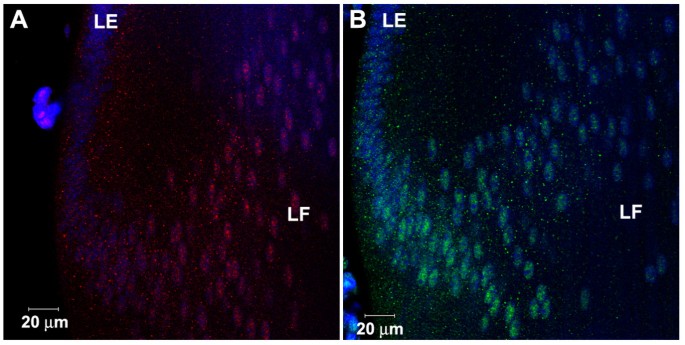
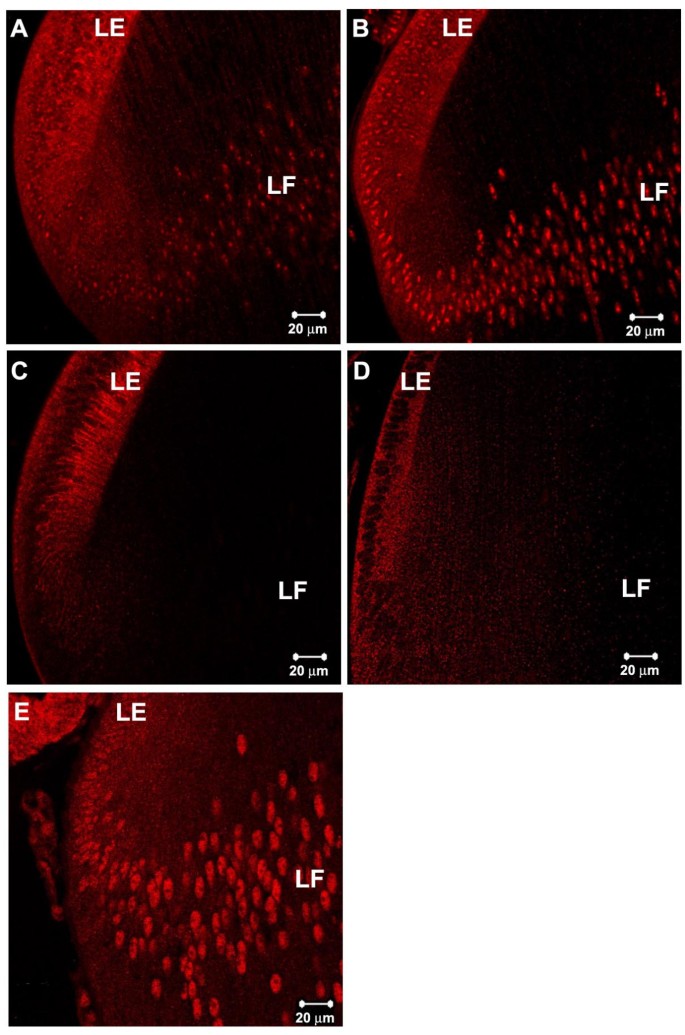
3.4 Bmpr1a条件敲除模型的功能验证
实验目的是验证BMP信号对pSmad1内体及核定位的调控作用,明确内体定位与信号激活的关联。方法细节为对Bmpr1a CKO小鼠晶状体和野生型晶状体进行pSmad1与Rab5B的双标染色,以邻近的睫状上皮作为内参(睫状上皮不表达Cre,Bmpr1a功能正常)。结果解读显示,与野生型晶状体相比,Bmpr1a CKO小鼠晶状体中pSmad1的内体及核定位水平显著降低,而睫状上皮中pSmad1的内体及核定位保持正常,表明Bmpr1a介导的BMP信号是pSmad1内体定位及核转运的关键调控因素,进一步证实内体定位的pSmad1与信号激活状态直接相关。
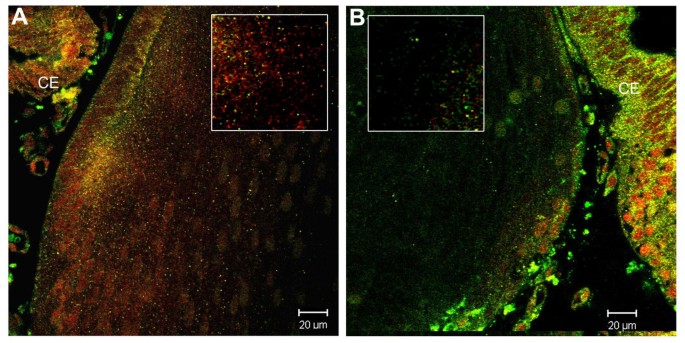
4. Biomarker研究及发现成果解析
Biomarker定位
本研究中涉及的Biomarker为“TGF-β超家族信号通路组分的内体定位模式”,属于细胞功能状态的亚细胞定位标记物,其筛选与验证逻辑为:首先通过体内组织免疫荧光共定位实验,筛选出定位于内体的信号分子;随后进行细胞类型特异性分析,明确不同晶状体细胞中定位模式的差异;最后通过Bmpr1a条件敲除模型验证定位模式与信号激活的功能关联,形成完整的验证链条。
研究过程详述
Biomarker的来源为E7鸡胚和P3小鼠的晶状体组织样本,验证方法为免疫荧光共聚焦显微镜检测,通过与内体标记物(EEA1、Rab5B、Rab7)的共定位分析,明确信号分子的亚细胞定位。特异性与敏感性表现为:激活型Smad(pSmad1、pSmad2)在晶状体纤维细胞中同时定位于内体和细胞核,在上皮细胞中仅定位于内体,具有明确的细胞类型特异性;Smad7在体内晶状体中主要定位于内体,与体外细胞系中Smad7定位于小窝的模式存在显著差异,体现了体内微环境对信号分子定位的调控作用。
核心成果提炼
本研究的核心成果在于首次揭示了体内晶状体中TGF-β超家族信号通路多组分的内体定位模式,证明Bmpr1a介导的BMP信号直接调控pSmad1的内体及核定位,发现体内与体外信号分子分布的关键差异,提示内体作为信号复合物组装平台在体内晶状体发育中发挥重要作用。创新性体现为首次在体内组织中系统解析TGF-β信号通路正负调控因子的内体定位,为内体调控信号转导的体内机制提供新视角,弥补了体外研究无法模拟体内微环境的不足。本研究未提供统计学P值数据,样本量涵盖鸡胚E7晶状体、小鼠P3野生型及Bmpr1a CKO晶状体组织。
