1. 领域背景与文献引入
文献英文标题:Generation of renewable mouse intestinal epithelial cell monolayers and organoids for functional analyses;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:肠道上皮细胞体外模型构建、遗传性肠道疾病(囊性纤维化、肠道肿瘤)功能研究
肠道上皮细胞是肠道生理功能的核心执行者,其体外模型是研究肠道疾病机制、筛选治疗药物的关键工具。领域共识:肠道上皮细胞体外模型的发展经历了三代技术迭代,传统方法包括永生化细胞系、3D类器官培养、多能干细胞定向分化,但均存在明显局限:永生化细胞系遗传不稳定、分化能力有限;3D类器官操作复杂、依赖昂贵生长因子,且实验操作多局限于基底侧;多能干细胞分化模型获得的细胞为胎儿特性,不适合成年肠道疾病研究。当前研究中缺乏一种既能长期扩增原代肠上皮细胞、保持其基因型稳定性,又能灵活适配多种功能分析实验的体外模型,尤其是来自基因工程小鼠模型的原代细胞模型,这极大限制了遗传性肠道疾病的机制研究和药物开发。针对这一空白,本研究采用条件重编程技术,构建了可长期传代的小鼠肠上皮细胞单层模型(IEC monolayers),并验证了其在囊性纤维化和肠道肿瘤功能研究中的应用价值,为遗传性肠道疾病的体外研究提供了新的技术平台。
2. 文献综述解析
本文综述部分按肠道上皮细胞体外模型的技术类型分类,系统评述了现有模型的优势与局限,明确指出当前研究中缺乏可长期保持基因型、适配多种功能分析的原代肠上皮细胞模型的核心问题,为本文的研究创新奠定了基础。
作者首先评述了永生化细胞系的应用,指出其虽能快速增殖、部分可分化为肠上皮细胞类型,但存在遗传不稳定、非整倍体、分化能力不足等问题,难以准确模拟肠道生理;随后介绍了3D类器官模型,强调其能实现正常肠上皮干细胞的扩增与分化,是研究肠干细胞功能的有力工具,但该模型操作复杂、依赖昂贵的生长因子,且实验操作多局限于基底侧,限制了其在功能分析中的应用;最后分析了多能干细胞定向分化模型,指出其获得的肠上皮细胞为胎儿特性,不适合成年肠道疾病的研究,且培养周期长、成本高。
通过对比现有模型的不足,本文的创新点凸显为首次将条件重编程技术应用于小鼠肠上皮细胞培养,成功构建了可长期传代(至少3个月)、保持原基因型的2D单层模型,且该模型可进一步转化为3D类器官和Transwell模型,适配肿胀实验、电生理检测、增殖分析等多种功能实验,填补了基因工程小鼠原代肠上皮细胞长期培养与多维度功能分析的空白,为遗传性肠道疾病的研究提供了更贴近体内生理状态的体外平台。
3. 研究思路总结与详细解析
本文的研究目标是构建可长期传代、保持基因型稳定性的小鼠肠上皮细胞单层模型,验证其功能特性,并将其应用于囊性纤维化和肠道肿瘤的功能研究;核心科学问题为条件重编程技术能否维持小鼠肠上皮细胞的基因型和功能完整性,以及该模型能否替代现有模型进行疾病机制研究与药物筛选;技术路线遵循“模型构建→基因型验证→功能转化→疾病特异性功能分析”的闭环逻辑,实验设计严谨,结果可靠。
3.1 小鼠肠上皮细胞单层模型构建与鉴定
实验目的:构建可长期传代的小鼠肠上皮细胞单层模型,鉴定其上皮细胞特性与基因型稳定性,确保模型的可靠性。
方法细节:从野生型(WT)、囊性纤维化(CFTR∆F508)、肠道肿瘤(ApcMin/+)基因工程小鼠的小肠组织(或肿瘤组织)获取样本,经冷冻保存后,采用胶原酶I和Dispase联合消化,将细胞接种于经辐照的3T3-J2饲养层细胞上,初始培养添加ROCK抑制剂Y-27632及肠干细胞维持所需的生长因子(EGF、Noggin、R-spondin),后续改用F培养基进行长期传代;通过免疫荧光染色检测紧密连接标记物E-钙粘蛋白和ZO-1,流式细胞术检测上皮细胞表面标记物EpCAM,PCR技术检测传代后细胞的基因型稳定性。
结果解读:免疫荧光染色结果显示,IEC monolayers细胞表达E-钙粘蛋白和ZO-1,形成完整的紧密连接结构;流式细胞术检测显示约95%的细胞表达EpCAM,证明培养的细胞为纯上皮细胞群体;PCR结果显示,经过多次传代后,IEC monolayers仍保持原小鼠的基因型,CFTR∆F508来源的细胞携带截短的CFTR基因,ApcMin/+来源的细胞携带突变的Apc基因,基因型未发生改变。
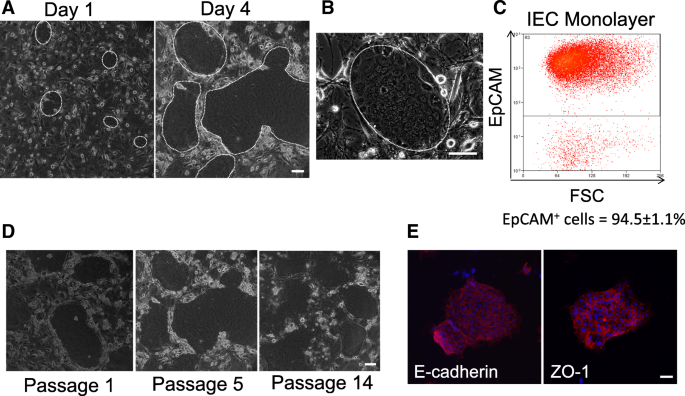
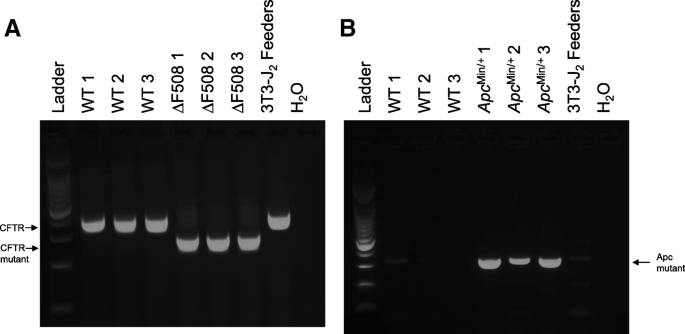
实验所用关键产品:Cell Signaling Technology的E-钙粘蛋白抗体(货号3195)、Biolegend的EpCAM-PE抗体(克隆G8.8)、Sigma-Aldrich的胶原酶I、Corning的Dispase、Enzo Life Sciences的Y-27632等。
3.2 囊性纤维化模型IEC monolayers的功能验证
实验目的:验证CFTR∆F508小鼠来源的IEC monolayers能否保持CFTR功能缺陷的表型,评估其在囊性纤维化功能研究中的应用价值。
方法细节:将WT和CFTR∆F508的IEC monolayers接种于Matrigel中,培养形成3D类器官,进行福斯高林(forskolin)诱导的肿胀实验,同时设置CFTR抑制剂CFTRinh-172预处理组作为对照;将IEC monolayers接种于Transwell小室,添加γ-分泌酶抑制剂DAPT诱导分化,待细胞融合后,采用Ussing小室进行电生理检测,依次添加阿米洛利(抑制ENaC)、福斯高林+IBMX(激活CFTR)、UTP(激活钙激活氯离子通道CaCC)、GlyH-101(抑制氯离子通道),记录跨上皮短路电流(Isc)的变化。
结果解读:3D类器官肿胀实验显示,WT来源的类器官经福斯高林处理后60分钟内,表面积显著增加(n=3,P<0.05),而CFTR∆F508来源的类器官无明显肿胀;经CFTRinh-172预处理的WT类器官,福斯高林诱导的肿胀被完全抑制,证明肿胀反应依赖CFTR功能。Ussing小室电生理检测显示,WT来源的IEC monolayers在福斯高林+IBMX处理后,Isc显著升高(n=2,P<0.001),而CFTR∆F508来源的IEC monolayers无明显变化;UTP诱导的CaCC反应在两组间无统计学差异;GlyH-101对WT组Isc的抑制作用显著高于CFTR∆F508组(n=3,P<0.05),进一步证明CFTR∆F508的IEC monolayers保持了CFTR功能缺陷的表型。
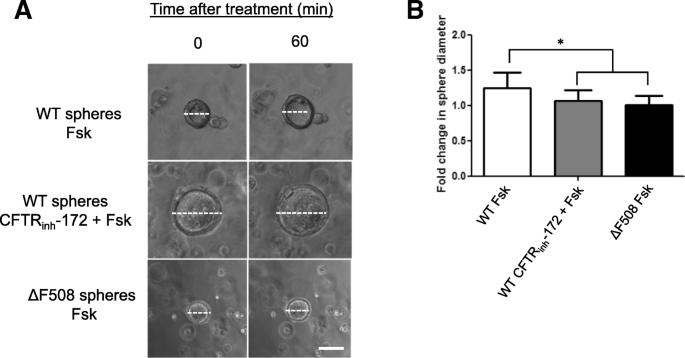
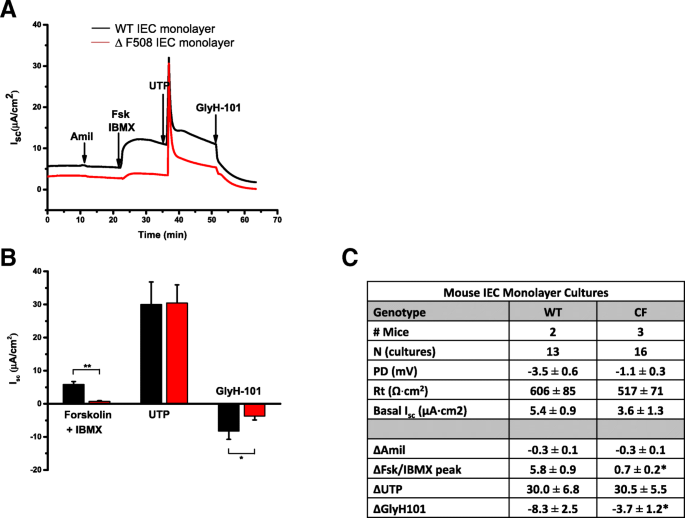
实验所用关键产品:Corning的Matrigel、Sigma-Aldrich的福斯高林、CFTRinh-172、GlyH-101、Stem Cell Technologies的DAPT等。
3.3 肠道肿瘤模型IEC monolayers的功能验证
实验目的:验证ApcMin/+小鼠肿瘤来源的IEC monolayers能否保持肿瘤细胞的高增殖特性,评估其在肠道肿瘤功能研究中的应用价值。
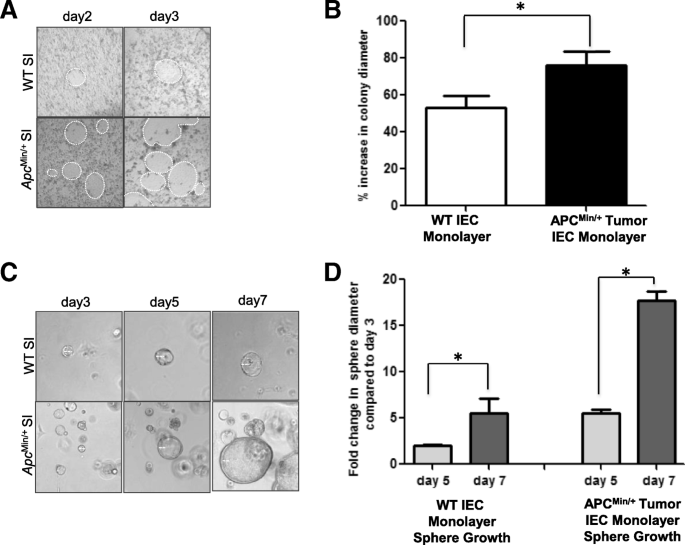
方法细节:将WT和ApcMin/+肿瘤来源的IEC monolayers接种于饲养层细胞上,在第2天和第3天对同一colony进行成像,通过ImageJ软件测量colony直径,计算增殖速率;同时将两种细胞接种于Matrigel中形成3D类器官,在第3、5、7天对类器官进行成像,测量直径并计算生长倍数。
结果解读:饲养层培养实验显示,ApcMin/+肿瘤来源的IEC monolayers colony在第2到3天的直径增长显著高于WT组(n=3,P<0.05);3D类器官培养实验显示,ApcMin/+来源的类器官在第5天和第7天的直径增长倍数显著高于WT组(n=3,P<0.05),证明该模型保持了ApcMin/+肿瘤细胞的高增殖特性,可用于肠道肿瘤的增殖机制研究和药物筛选。
文献未提及具体实验产品,领域常规使用Matrigel、细胞成像分析系统、ImageJ图像分析软件等。
4. Biomarker研究及发现成果
本文涉及的Biomarker为遗传性肠道疾病的致病基因突变,包括囊性纤维化的CFTR∆F508突变和肠道肿瘤的ApcMin/+突变,通过模型构建与功能验证,明确了这些突变在IEC monolayers中的稳定性及对应的功能表型,为疾病的机制研究和药物筛选提供了可靠的体外平台。
Biomarker定位
本文中CFTR∆F508突变是囊性纤维化的致病Biomarker,ApcMin/+突变是家族性腺瘤性息肉病(肠道肿瘤)的致病Biomarker;筛选/验证逻辑为从基因工程小鼠模型获取组织样本→通过条件重编程构建IEC monolayers→PCR技术验证突变的长期稳定性→功能实验验证突变对应的表型特征,形成完整的“基因型-表型”验证链条。
研究过程详述
CFTR∆F508突变的来源为CFTR∆F508纯合子小鼠的小肠组织,验证方法为PCR扩增CFTR基因,检测到截短的基因片段,证明突变在传代过程中保持稳定;功能验证通过3D类器官肿胀实验和Ussing小室电生理检测,结果显示WT组与突变组的功能差异具有统计学显著性(P<0.05、P<0.001),该模型对CFTR功能的检测具有良好的特异性和敏感性。ApcMin/+突变的来源为ApcMin/+小鼠的小肠肿瘤组织,验证方法为PCR扩增Apc基因,检测到突变的基因片段;功能验证通过colony增殖和类器官生长实验,结果显示突变组的增殖速率显著高于WT组(n=3,P<0.05),证明该模型保持了肿瘤细胞的高增殖表型。
核心成果提炼
CFTR∆F508的IEC monolayers保持了CFTR功能缺陷的表型,可用于囊性纤维化治疗药物的筛选与评估,如CFTR矫正剂、增效剂的效果检测;ApcMin/+的IEC monolayers保持了肿瘤细胞的高增殖特性,可用于肠道肿瘤的增殖机制研究,以及抗肿瘤药物的筛选。本文的创新性在于首次建立了可长期保持致病突变基因型与对应功能表型的原代肠上皮细胞模型,为遗传性肠道疾病的体外研究提供了更贴近体内生理状态的平台,弥补了现有模型的不足。
