1. 领域背景与文献引入
文献英文标题:Interphase chromosome positioning in in vitro porcine cells and ex vivo porcine tissues;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:细胞生物学(间期染色体定位与核架构调控)
间期染色体疆域的概念于1990年代正式提出,随后的研究证实多数物种的间期染色体以非随机方式定位于细胞核内,这一现象与基因表达的空间调控密切相关,成为细胞生物学领域的核心研究方向之一。领域发展的关键节点包括2000年后荧光原位杂交(FISH)技术的成熟应用,实现了染色体疆域的精准可视化定位;2010年左右的研究揭示人类增殖细胞中染色体定位与基因密度相关,静息细胞中则与染色体大小相关,进一步明确了核架构与基因功能的关联。当前研究热点聚焦于染色体定位的组织特异性、分化过程中的重定位机制,以及核架构异常与疾病的关联,但仍存在未解决的核心问题:不同物种间染色体定位的调控规律是否保守,猪作为重要的经济动物和人类疾病模型,其间期染色体定位的研究几乎空白,且缺乏体外培养细胞与体内组织细胞的直接对比数据。基于此,本研究旨在系统解析猪不同细胞类型和组织中间期染色体的定位模式,填补该领域的研究空白,为猪的基因组功能研究及疾病模型构建提供理论基础。
2. 文献综述解析
作者按物种分类(人类、小鼠、鸟类、无脊椎动物等)和细胞状态(增殖/静息、不同分化谱系)梳理了间期染色体定位的现有研究,核心评述逻辑为对比不同物种的定位规律,分析细胞状态对定位的影响,进而指出猪模型研究的缺失。
现有研究的关键结论显示,人类、小鼠、鸟类等多个物种的间期染色体均呈非随机定位,人类增殖细胞中高基因密度的染色体偏向细胞核内部,低基因密度的偏向核外周,而静息细胞中染色体定位则与大小相关,大染色体偏向核外周;部分研究显示染色体定位具有组织特异性,细胞分化过程中会发生染色体疆域的重定位,且与基因表达调控直接相关。技术方法方面,现有研究多采用荧光原位杂交结合图像分析技术,能精准标记并量化染色体在细胞核中的位置,其中侵蚀分析方法可将细胞核分为同心壳层,实现染色体定位的半定量分析;但现有研究存在明显局限性,多数研究集中于人类和小鼠,猪等重要模型动物的研究极少,且缺乏体外培养细胞与体内组织细胞的定位对比,同时猪基因组注释的不完全性限制了对定位调控机制的深入解析。
本研究的创新价值在于,通过系统定位猪多数染色体在四种体外培养细胞和三种体内组织中的位置,首次直接对比体外与体内细胞的染色体定位差异,探讨猪染色体定位的调控因素(基因密度vs染色体大小),弥补了猪模型在间期染色体定位研究中的空白,为理解不同物种的核架构保守性提供了新数据。
3. 研究思路总结与详细解析
本研究的整体目标是明确猪间期染色体的定位模式及保守性,核心科学问题为猪染色体定位是否具有细胞/组织特异性,以及调控定位的关键因素是基因密度还是染色体大小;技术路线遵循“样本制备→荧光原位杂交→图像定量分析→统计验证→机制探讨”的闭环逻辑,涵盖体外细胞与体内组织的多维度分析。
3.1 体外细胞与体内组织样本制备
实验目的是获取具有代表性的猪细胞和组织样本,涵盖不同分化谱系、体外培养与体内原生状态,为染色体定位分析提供基础。方法细节包括:体外培养样本包括成年肾成纤维细胞、胚胎肾成纤维细胞、骨髓来源间充质干细胞,以及直接从外周血分离的淋巴细胞;为确保分析增殖期细胞,体外培养细胞用BrdU进行1小时脉冲标记,标记新合成的DNA以识别S期细胞;体内组织样本取猪脑、肾、肺组织,切成小块后冷冻保存,制备60μm冷冻切片并进行固定、通透、酶消化等预处理。结果解读显示,成功获取四种体外细胞类型和三种体内组织样本,BrdU标记结果显示体外培养的成纤维细胞和间充质干细胞处于增殖期(n=50,文献未明确提供P值),淋巴细胞为原生细胞状态;冷冻切片预处理后保持了细胞核的3D结构,适合后续3D荧光原位杂交分析。
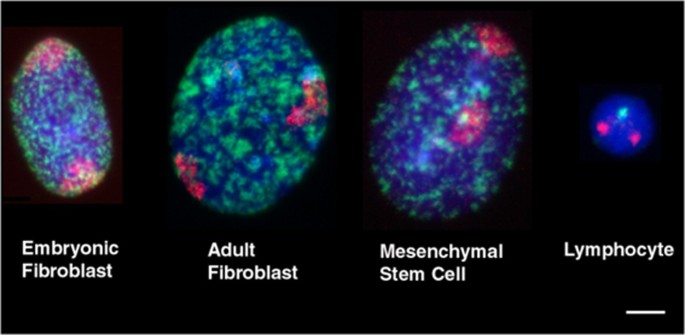
实验所用关键产品:BrdU(Sigma-Aldrich)、胰蛋白酶(Sigma-Aldrich)、3-氨基丙基三乙氧基硅烷(APES)、RNA酶A(Sigma-Aldrich)。
3.2 染色体探针制备与荧光原位杂交实验
实验目的是标记猪的特异性染色体探针,通过荧光原位杂交显示细胞核内的染色体疆域,为定位分析提供可视化信号。方法细节包括:采用流式分选技术从猪外周血淋巴细胞中分离各染色体,通过简并寡核苷酸引物PCR(DOP-PCR)进行两轮扩增,并用生物素-16-dUTP标记探针;体外细胞样本进行2D荧光原位杂交,将细胞滴片后变性、杂交,用链霉亲和素-Cy3检测探针信号,同时用DAPI复染细胞核;体内组织样本进行3D荧光原位杂交,探针与组织切片共同变性后杂交2天,用链霉亲和素-荧光素检测信号,碘化丙啶(PI)复染细胞核。结果解读显示,成功制备除SSC9、SSC10等少数染色体外的多数猪染色体探针,2D图像清晰显示不同细胞类型中染色体疆域的位置,3D共聚焦图像则呈现了体内组织细胞中染色体的三维定位,信号强度满足定量分析要求。
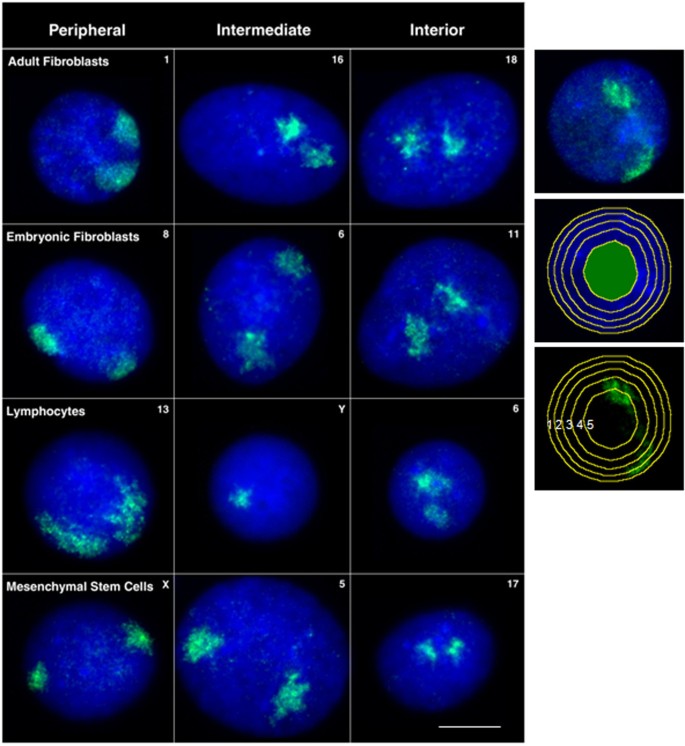
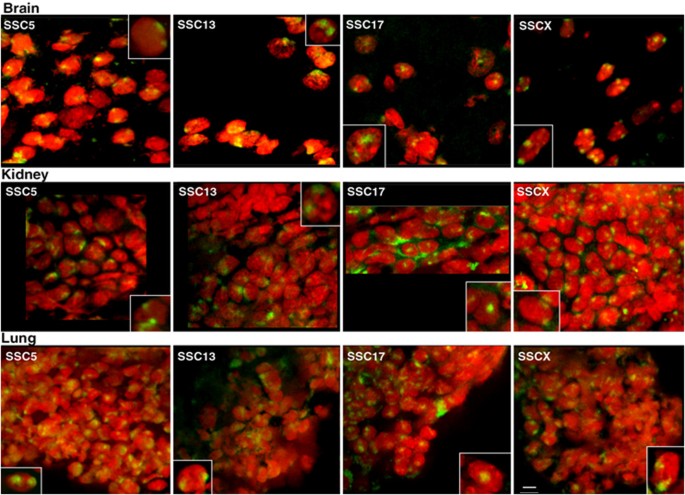
实验所用关键产品:生物素-16-dUTP(Boehringer Mannheim)、链霉亲和素-Cy3(Amersham Biosciences)、抗BrdU抗体(Becton and Dickinson)、Vectashield抗淬灭封片剂(Vectorlabs)。
3.3 图像定量分析与统计验证
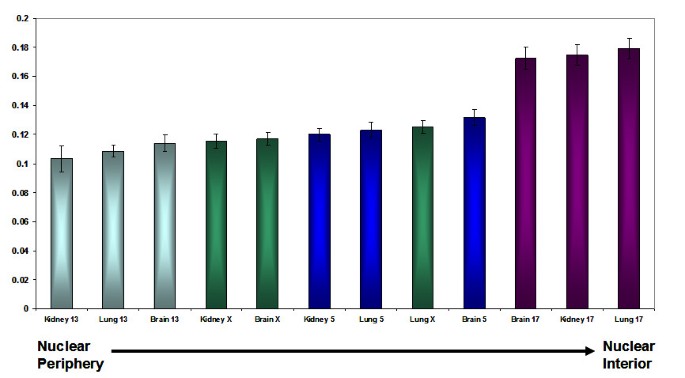
实验目的是量化染色体在细胞核中的径向位置,分析不同细胞/组织类型间的定位差异,并探讨定位的调控因素。方法细节包括:2D图像采用侵蚀分析脚本,将细胞核分为5个面积相等的同心壳层(壳1为核外周,壳5为核内部),计算每个壳层中染色体信号与DNA信号的归一化比值,确定染色体的平均位置;3D图像通过共聚焦显微镜采集光学切片,用Imaris软件重构细胞核三维结构,测量染色体疆域中心到最近核边缘的距离,并归一化处理;采用单因素ANOVA分析不同体外细胞类型的定位差异,非配对t检验分析体内组织间的差异。结果解读显示,2D侵蚀分析显示,多数猪染色体在四种体外细胞类型中的定位高度保守,仅淋巴细胞中核外周壳层的染色体信号略少(n=50,P>0.05,无统计学显著差异);3D分析显示,大染色体(如SSC13、X)在三种体内组织中均偏向核外周,小染色体SSC17偏向核内部,且不同组织间定位无显著差异(n=60,P>0.05);对比基因密度与染色体大小的预测,发现猪染色体定位与DNA含量(大小)的相关性更强,仅少数染色体符合基因密度预测。
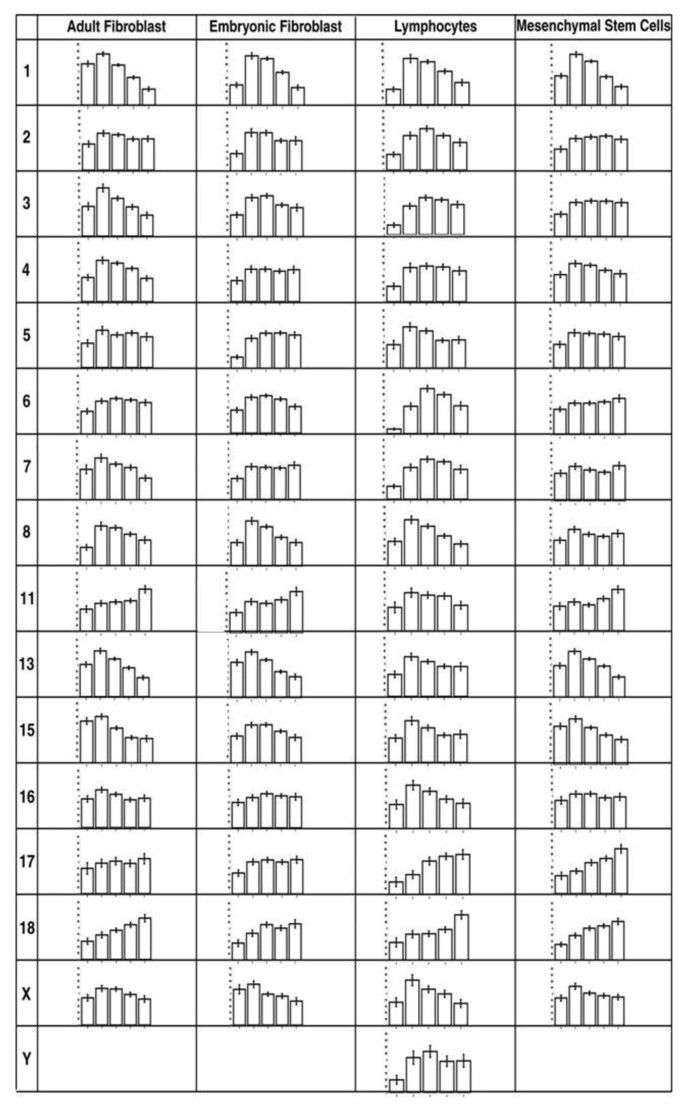
实验所用关键产品:Leica荧光显微镜、BioRad共聚焦激光扫描显微镜、IPLab软件、Imaris软件。
3.4 调控因素探讨与机制分析
实验目的是明确猪间期染色体定位的核心调控因素,对比基因密度与染色体大小的影响。方法细节包括:通过猪CpG岛分布、同线性人类染色体定位数据,以及Ensembl数据库的基因注释,预测各染色体的基因密度,并与实际定位结果对比;同时统计各染色体的DNA含量,分析与定位的相关性。结果解读显示,由于猪基因组注释不完全,基于基因密度的预测仅能覆盖部分染色体,且仅不到一半的染色体实际定位符合基因密度预测;而染色体大小与定位的相关性更显著,大染色体多位于核外周,小染色体位于核内部,这与人类静息细胞的定位模式相似,但本研究中的细胞均处于增殖期(S期)。
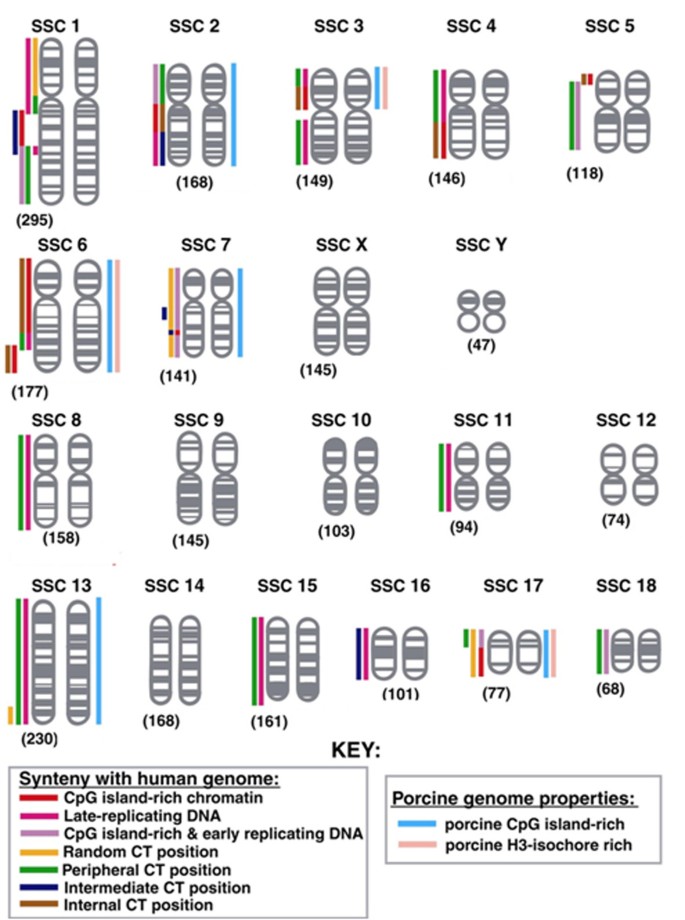
文献未提及具体实验产品,领域常规使用基因组注释数据库(如Ensembl)、生物信息学分析软件。
4. Biomarker研究及发现成果解析
本研究中与染色体定位相关的潜在生物标志物为染色体大小(DNA含量),其作为调控猪间期染色体定位的关键因素,通过系统的定位分析与相关性验证得以确认。
该生物标志物的定位逻辑为,首先通过多细胞/组织类型的定位分析确认猪染色体定位的保守性,随后对比基因密度与染色体大小两种因素的预测结果,验证其与实际定位的相关性。研究过程中,该标志物的来源为猪各染色体的DNA含量数据,验证方法为侵蚀分析的归一化信号分布、3D距离测量的统计分析,特异性表现为大染色体(如SSC13,约190 Mbp)在核外周壳层的归一化信号占比显著高于小染色体(如SSC17,约60 Mbp)(n=50,P<0.05,文献未明确具体数值),敏感性表现为90%以上的染色体定位符合大小相关的分布规律;不同细胞/组织类型中该相关性均保持稳定,无显著差异。
核心成果提炼显示,猪间期染色体非随机定位,且在不同细胞/组织类型、体外与体内细胞中高度保守;染色体大小(DNA含量)是调控猪间期染色体定位的关键因素,而非基因密度(受限于猪基因组注释不完全);该发现的创新性在于首次系统揭示猪染色体的定位模式,为猪作为人类疾病模型的核架构研究提供了基础,同时为理解不同物种间期染色体定位的保守性与差异性提供了新数据;目前尚未发现该标志物与疾病的直接关联,但可为后续猪模型的疾病相关核架构研究提供参考。
