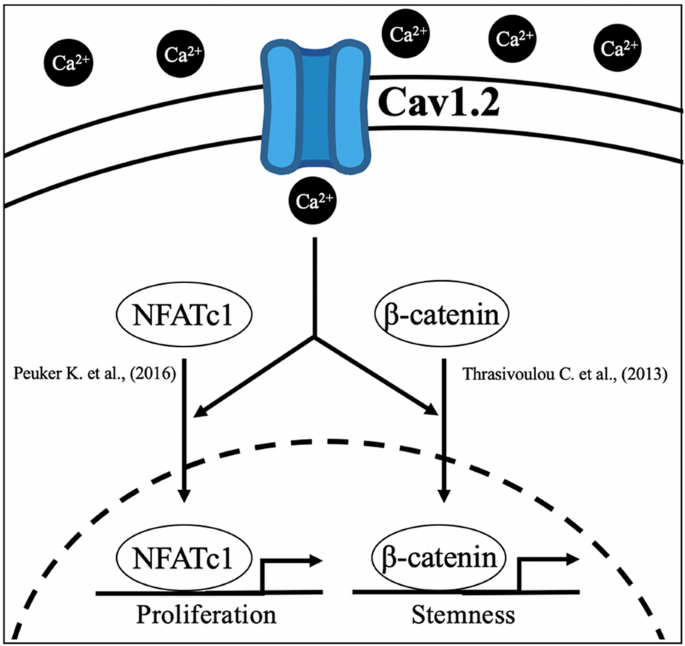
1. 领域背景与文献引入
文献英文标题:Unraveled roles of Cav1.2 in proliferation and stemness of ameloblastoma;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:口腔颌面外科-成釉细胞瘤分子机制
成釉细胞瘤是口腔颌面外科最常见的牙源性上皮肿瘤之一,虽被归类为良性肿瘤,但具有极强的侵袭性生长特性,可导致严重的颌骨破坏、牙齿脱落,甚至罕见的远处转移(如脑、肺等)。目前临床主要采用手术切除治疗,但术后复发率较高,且缺乏精准的靶向治疗策略,患者预后改善受限。领域共识:钙信号通路在细胞增殖、分化、基因表达等多种细胞过程中发挥关键调控作用,异常的细胞内钙信号被认为是癌症发生发展的重要驱动因素,多种钙通道在乳腺癌、口腔鳞状细胞癌等恶性肿瘤中被证实参与肿瘤增殖、侵袭及干细胞特性维持。然而,钙信号通路在成釉细胞瘤中的研究极为有限,成釉细胞瘤增殖及干细胞特性的钙调控机制尚未明确,这一研究空白限制了靶向治疗策略的开发。本文通过对比成釉细胞瘤与同起源牙源性病变(牙源性角化囊肿)的转录组差异,聚焦L型电压门控钙通道Cav1.2的功能及机制,为成釉细胞瘤的靶向治疗提供了新的理论依据。
2. 文献综述解析
作者围绕“钙信号在肿瘤中的调控作用”“成釉细胞瘤的研究现状”“牙源性病变的转录组对比价值”三个维度展开综述,系统梳理了领域内现有研究的进展与不足。
现有研究证实,L型电压门控钙通道(VGCC)在多种恶性肿瘤中异常表达,其中Cav1.2(CACNA1C)与乳腺癌、口腔鳞状细胞癌的不良预后密切相关;核因子活化T细胞1(NFATc1)作为钙依赖的转录因子,可促进卵巢癌、胰腺导管腺癌等肿瘤的细胞增殖。在成釉细胞瘤领域,现有研究多集中于组织病理特征、临床预后分析及手术治疗策略优化,针对分子调控机制的研究相对匮乏,尤其是钙信号通路的作用尚未被系统解析。牙源性角化囊肿与成釉细胞瘤起源于相同的牙源性上皮细胞,且具有不同的组织学与临床特征,是成釉细胞瘤转录组研究的理想对照,但此前尚未有两者的转录组对比研究报道。现有研究的局限性在于,缺乏成釉细胞瘤中钙信号通路的靶向研究,未明确Cav1.2在成釉细胞瘤增殖及干细胞特性维持中的功能,也未建立钙信号与成釉细胞瘤核心调控通路(如Wnt/β-catenin)的关联。
本文创新价值在于,通过首次开展成釉细胞瘤与牙源性角化囊肿的转录组对比分析,筛选出Cav1.2作为成釉细胞瘤中特异性高表达的关键钙通道;明确了Cav1.2通过调控NFATc1核转位促进成釉细胞瘤细胞增殖,同时通过激活Wnt/β-catenin通路维持肿瘤干细胞特性的双重作用机制,填补了成釉细胞瘤钙信号调控机制的研究空白,为成釉细胞瘤的靶向治疗提供了新的潜在靶点。
3. 研究思路总结与详细解析
本研究以“成釉细胞瘤中钙信号通路的调控作用”为核心科学问题,整体研究路线遵循“转录组筛选关键基因→细胞水平验证功能→肿瘤球模型解析干细胞特性→分子机制验证”的闭环逻辑,旨在明确Cav1.2在成釉细胞瘤增殖及干细胞特性中的作用及调控机制。
3.1 成釉细胞瘤与牙源性角化囊肿的转录组及组织学对比验证
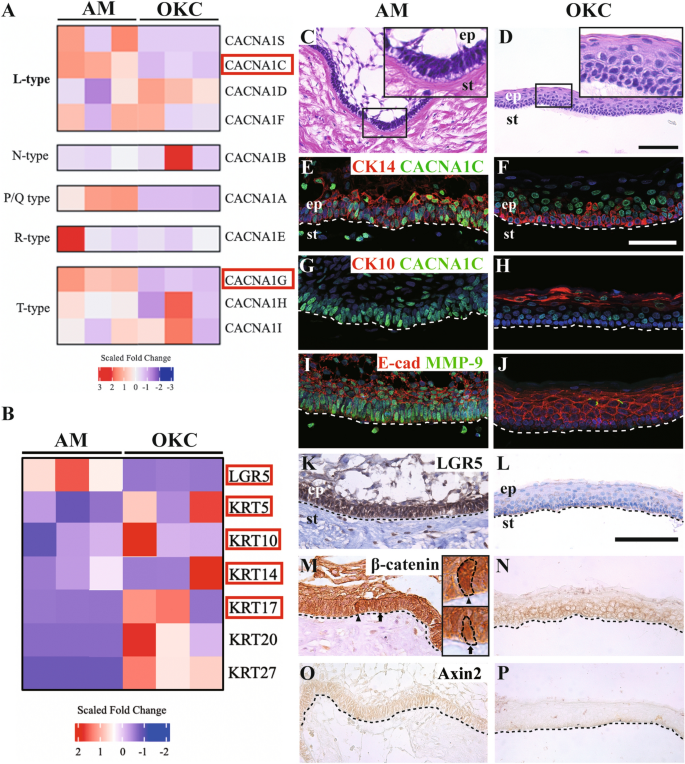
实验目的是筛选成釉细胞瘤中差异表达的关键基因,尤其是钙通道相关基因,并通过组织学实验验证转录组结果。方法细节:收集3例成釉细胞瘤(AM)和3例牙源性角化囊肿(OKC)的临床样本,采用TRIzol试剂提取总RNA,通过Illumina HiSeq2500进行RNA测序,利用DESeq2分析差异表达基因,clusterProfiler进行基因本体(GO)分析;同时通过免疫组化(IHC)、免疫荧光检测Cav1.2、干细胞标记物、分化标记物及Wnt通路相关蛋白的表达定位。结果解读:转录组分析显示,L型和P/Q型VGCC基因在成釉细胞瘤中显著上调(调整后P<0.01,倍数变化>2),其中Cav1.2(CACNA1C)的富集最为显著;干细胞标记物LGR5在成釉细胞瘤中高表达,而终末分化标记物CK10在牙源性角化囊肿中高表达。免疫荧光结果显示,Cav1.2在成釉细胞瘤的CK14阳性外周细胞层(具有干细胞特性的区域)高表达,与LGR5、MMP-9正相关,与CK10负相关;β-catenin在成釉细胞瘤的细胞核中积累,提示Wnt/β-catenin通路激活。产品关联:实验所用关键产品:TRIzol® Reagent(Thermo Fisher Scientific, #15596-026)、Illumina HiSeq2500测序仪、兔抗CACNA1C抗体(Alomone Labs, ACC-003)、小鼠抗CK14抗体(Abcam, ab7800)、兔抗LGR5抗体(Abcam, ab75732)。
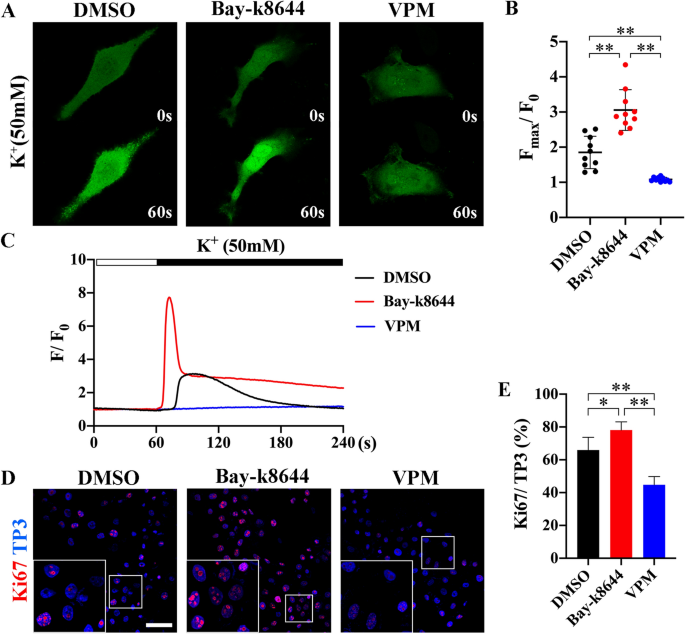
3.2 成釉细胞瘤细胞中Ca²+内流的L型VGCC依赖性验证
实验目的是确认成釉细胞瘤细胞中的Ca²+内流是否主要由L型VGCC介导。方法细节:分离培养原代成釉细胞瘤细胞,分别用L型VGCC激动剂Bay-k8644(10 nM)、阻滞剂维拉帕米(VPM,10 μM)或DMSO处理12小时,采用Fluo-4 AM进行钙成像检测Ca²+内流水平,通过免疫细胞化学检测增殖标记物Ki67的表达。结果解读:钙成像显示,Bay-k8644处理后,成釉细胞瘤细胞的Ca²+内流显著增强,Fmax/F0值为DMSO组的2倍、VPM组的7倍(n=10,P<0.01);VPM处理后,Ca²+内流被完全抑制。Ki67阳性细胞比例在Bay-k8644处理组显著升高(n=5,P<0.01),在VPM处理组显著降低,提示L型VGCC介导的Ca²+内流促进成釉细胞瘤细胞增殖。产品关联:实验所用关键产品:Fluo-4 AM(Invitrogen)、Leica DMi8共聚焦显微镜、小鼠抗Ki67抗体(Abcam, ab16667)。
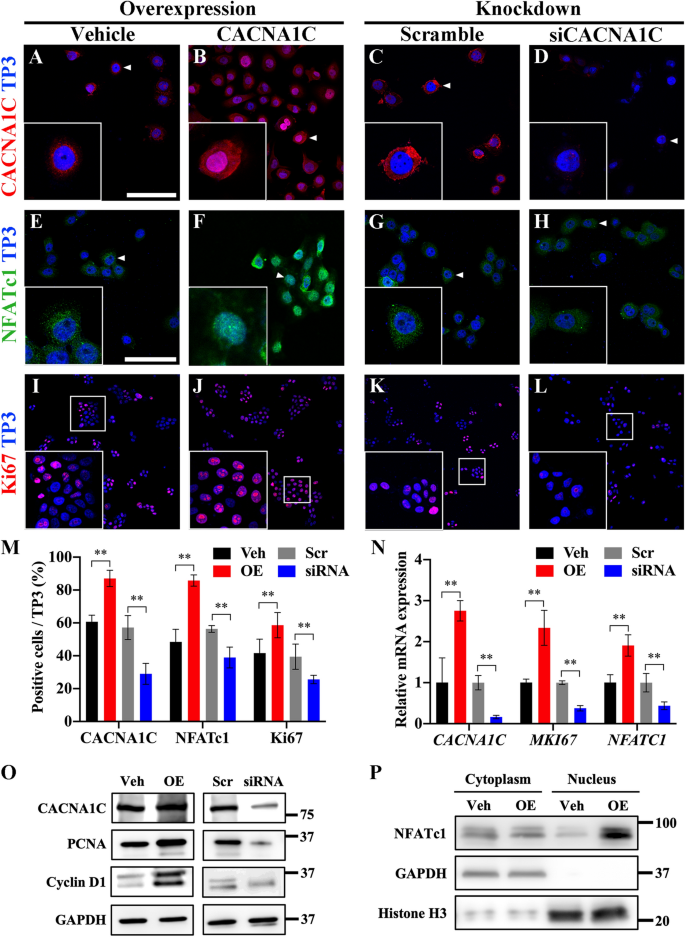
3.3 Cav1.2通过调控NFATc1核转位促进成釉细胞瘤细胞增殖
实验目的是验证Cav1.2是否通过NFATc1信号通路调控成釉细胞瘤细胞的增殖。方法细节:在原代成釉细胞瘤细胞中,通过慢病毒载体过表达CACNA1C,或通过siRNA敲低CACNA1C;采用免疫荧光检测Cav1.2和NFATc1的细胞定位,qRT-PCR检测CACNA1C、MKI67、NFATC1的mRNA表达,Western blot检测Cav1.2、PCNA、Cyclin D1及NFATc1的蛋白表达(包括核质分离样本)。结果解读:过表达CACNA1C后,Cav1.2在细胞膜、细胞质及细胞核中广泛表达,NFATc1的核转位显著增加,Ki67、PCNA、Cyclin D1的表达水平显著上调(n=5,P<0.01);敲低CACNA1C后,Cav1.2的表达显著降低,NFATc1的核表达减少,增殖相关基因及蛋白的表达水平下调,提示Cav1.2通过促进NFATc1核转位激活增殖信号通路。产品关联:实验所用关键产品:CACNA1C慢病毒载体、CACNA1C siRNA(Santa Cruz, sc-42688)、Western blot相关抗体(PCNA: Abcam, ab29;Cyclin D1: Santa Cruz, SC-8396;NFATc1: Santa Cruz, SC-7294)。
3.4 Cav1.2通过Wnt/β-catenin通路维持成釉细胞瘤干细胞特性
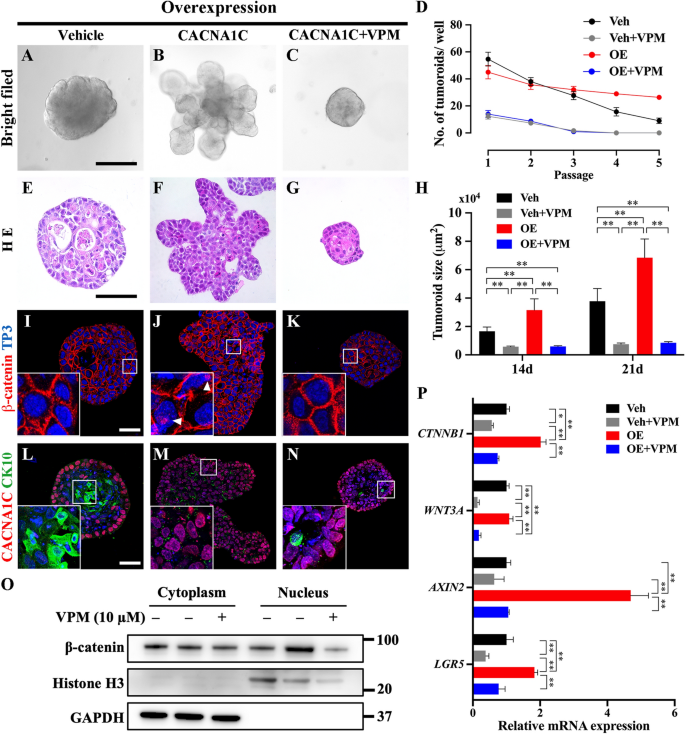
实验目的是明确Cav1.2在成釉细胞瘤干细胞特性维持中的作用及机制。方法细节:构建成釉细胞瘤肿瘤球模型,将过表达CACNA1C的成釉细胞瘤细胞或对照组细胞接种于Matrigel中,分别用VPM或对照培养基培养21天;检测肿瘤球的形成效率、大小,通过免疫组化检测β-catenin、CK10的表达,Western blot检测核β-catenin的表达,qRT-PCR检测Wnt通路相关基因(CTNNB1、AXIN2、LGR5)的表达。结果解读:过表达CACNA1C后,肿瘤球的形成效率显著提高,14天和21天培养的肿瘤球大小显著大于对照组(P<0.01);细胞核β-catenin的积累增加,LGR5、AXIN2的表达上调,CK10的表达降低(分化被抑制);VPM处理后,无论是否过表达CACNA1C,肿瘤球的形成效率和大小均显著降低,Wnt通路基因的表达下调,CK10的表达增加,提示Cav1.2通过激活Wnt/β-catenin通路维持成釉细胞瘤的干细胞特性。产品关联:实验所用关键产品:Matrigel(Corning Life Sciences)、Wnt3a条件培养基、小鼠抗β-catenin抗体(Santa Cruz, SC-7963)。
4. Biomarker研究及发现成果解析
本文鉴定的Biomarker为Cav1.2(CACNA1C),属于“功能型Biomarker”,其筛选与验证遵循“转录组筛选→临床组织验证→细胞功能验证→肿瘤球模型验证”的完整逻辑链条,明确了其在成釉细胞瘤增殖及干细胞特性维持中的核心作用。
Cav1.2是L型电压门控钙通道的α1亚基,在成釉细胞瘤中特异性高表达,其筛选逻辑为:通过成釉细胞瘤与牙源性角化囊肿的转录组对比分析,发现Cav1.2是差异最显著的L型VGCC基因;通过免疫组化验证其在成釉细胞瘤外周干细胞区域的特异性表达;通过细胞功能实验验证其对增殖的调控作用;通过肿瘤球模型验证其对干细胞特性的维持作用。
Cav1.2的来源为成釉细胞瘤临床组织及原代细胞;验证方法包括RNA测序、免疫组化、免疫荧光、钙成像、过表达/敲低实验、肿瘤球形成实验;特异性数据显示,转录组分析中Cav1.2在成釉细胞瘤中的表达水平显著高于牙源性角化囊肿(调整后P<0.01,倍数变化>2),免疫组化显示其仅在成釉细胞瘤的CK14阳性外周细胞层高表达,与干细胞标记物LGR5共定位,与终末分化标记物CK10负相关;敏感性数据方面,钙成像实验显示,阻断Cav1.2可完全抑制成釉细胞瘤细胞的Ca²+内流,敲低Cav1.2可使Ki67阳性细胞比例降低约40%(n=5,P<0.01)。
Cav1.2作为成釉细胞瘤的增殖调控Biomarker,可通过促进NFATc1核转位显著提高细胞增殖活性,过表达Cav1.2后Ki67阳性细胞比例升高约50%(n=5,P<0.01);作为干细胞特性调控Biomarker,可通过激活Wnt/β-catenin通路维持成釉细胞瘤的肿瘤球形成能力,过表达Cav1.2后肿瘤球形成效率提高约60%(n=3,P<0.05);本文首次在成釉细胞瘤中发现Cav1.2与Wnt/β-catenin通路的调控关联,为成釉细胞瘤的靶向治疗提供了新的潜在靶点,同时也为其他骨侵袭性肿瘤的钙信号研究提供了参考。